Los stents farmacoactivos (SFA) han disminuido significativamente la tasa de reestenosis del stent (RS) y la necesidad de nuevo intervencionismo. Recientemente se ha relacionado la presencia de fracturas de stents (FS) con la aparición de RS y/o trombosis de SFA, especialmente con los liberadores de sirolimus (Cypher®)1,2. Sin embargo, es poco conocida la incidencia real de FS, y su diagnóstico sólo por angiografía puede ser difícil.
Se describe la incidencia de FS confirmada con técnicas de imagen intravascular en una población de pacientes evaluados angiográficamente por sospecha de RS. Entre enero de 2007 y junio de 2012, se trataron en nuestro centro 355 lesiones tipo RS, 197 (55%) de stents convencionales y 158 (45%) de SFA. Se utilizó ecografía intracoronaria o tomografía de coherencia óptica en 169 lesiones (48%). La incidencia de FS confirmada con imagen intravascular fue del 3,6% (6/169 lesiones). Las características de las FS se presentan en la tabla.
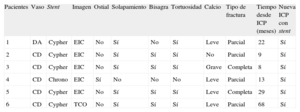
Características de las lesiones con fracturas de stent
| Pacientes | Vaso | Stent | Imagen | Ostial | Solapamiento | Bisagra | Tortuosidad | Calcio | Tipo de fractura | Tiempo desde ICP (meses) | Nueva ICP con stent |
| 1 | DA | Cypher | EIC | No | Sí | No | Sí | Leve | Parcial | 22 | Sí |
| 2 | CD | Cypher | EIC | No | Sí | Sí | Sí | No | Parcial | 9 | Sí |
| 3 | CD | Cypher | EIC | No | Sí | Sí | Sí | Grave | Completa | 8 | Sí |
| 4 | CD | Chrono | EIC | Sí | No | No | No | Leve | Parcial | 13 | Sí |
| 5 | CD | Cypher | EIC | No | Sí | Sí | Sí | Leve | Completa | 29 | Sí |
| 6 | CD | Cypher | TCO | No | Sí | Sí | Sí | Leve | Parcial | 68 | Sí |
CD: coronaria derecha; DA: descendente anterior; EIC: ecografía intracoronaria; ICP: intervención coronaria percutánea; TCO: tomografía de coherencia óptica.
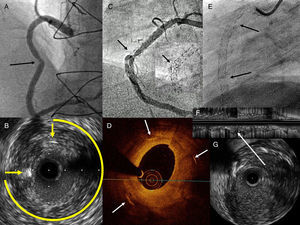
De los 6 casos identificados, la FS era visible radiológicamente sólo en uno. En los restantes se sospechó por la presencia de una RS focal, en una zona tortuosa o con movimiento en bisagra. En algún caso la RS no era angiográficamente importante, pero la ecografía intracoronaria demostró una hiperplasia focal importante y la ausencia de struts en un arco > 270° (figs. A y B). El análisis de la imagen intravascular se realizó cuadro a cuadro para identificar las zonas sospechosas y delimitar la presencia o ausencia de struts (figs. C y D). En los 6 pacientes se realizó nueva intervención coronaria percutánea, con implante de stent en la zona de RS. El seguimiento posterior (clínico y con pruebas no invasivas) no ha mostrado nuevos eventos (mediana, 9 ± 3 meses).
A: reestenosis del stent en coronaria derecha media (flecha). B: imagen de ecografía intracoronaria de A, con abundante hiperplasia concéntrica, sólo dos struts visibles (flechas) y un arco de 270° sin struts. C: imagen radiológica de stents solapados en coronaria derecha, con reestenosis focal en zona angulada e imagen ampliada de distorsión del stent (flecha). D: imagen de tomografía de coherencia óptica de C; abundante hiperplasia concéntrica y sólo tres struts (flechas) muy distantes entre sí. E: imagen radiológica de coronaria derecha; stents desde ostium hasta segmento distal por oclusión crónica; las flechas marcan dos zonas de fractura completa con separación física de los struts. F: imagen longitudinal de ecografía intracoronaria de E; la flecha marca la fractura sin struts. G: imagen transversal de ecografía intracoronaria de E; ausencia de struts.
El diagnóstico de las FS puede ser radiológico (imagen en vacío sin contraste) o con técnicas de imagen intravascular, como la ecografía intracoronaria o la tomografía de coherencia óptica. Se han descrito clasificaciones para ambos métodos, en función de la separación clara de struts o la ausencia de estos en algún segmento coronario3,4. También se han descrito factores que predisponen a su aparición, como la presencia de calcio, la tortuosidad de la arteria y el grado de torsión de esta respecto al ciclo cardiaco.
La incidencia real de FS es poco conocida. Diversos estudios la sitúan entre el 0,84 y el 8,4%, y en muchas ocasiones se descubre al investigar una RS5. Es posible que pase inadvertida si no es radiológicamente muy llamativa o no se estudia el vaso con una técnica de imagen intracoronaria. Los hallazgos intravasculares más comunes son la ausencia de struts en una zona amplia de la circunferencia del vaso y la presencia de abundante hiperplasia en ese mismo segmento6. En ocasiones puede ser difícil diferenciar una FS incompleta de una deformación del stent (curvas pronunciadas, posdilatación de ramas laterales, lesiones calcificadas), que produce separación y asimetría de los struts, pero no que no los haya. Si la fractura es completa, se observa desaparición total de struts en varias imágenes consecutivas (figs. E-G).
Los mecanismos patogénicos de la RS o la trombosis en las FS probablemente tengan relación con la menor cantidad de fármaco dispensada en la zona de fractura y por una mayor agresión mecánica de los struts fracturados, pues ambas producen proliferación de células musculares lisas y endotelización alterada1,5.
Algunos estudios han demostrado que ciertos SFA liberadores de sirolimus (Cypher®) causan más FS debido a su diseño de celda cerrada y por estar fabricados con acero inoxidable, material de menos flexibilidad y conformabilidad que las nuevas aleaciones de cobalto, cromo o platino. La localización en coronaria derecha o en safenas es más frecuente, así como en stents largos, stents solapados y lesiones tortuosas o con zonas de movimiento en bisagra5. En esta serie se revisaron los procedimientos de intervención coronaria percutánea previos en los casos de solapamiento, para descartar una separación real entre stents, y se confirmó la correcta posición de los stents durante la liberación.
Hay varias limitaciones en este registro observacional. El seguimiento angiográfico sólo se ha realizado en pacientes con sospecha de RS por clínica compatible o por isquemia en pruebas no invasivas. Por otro lado, se utilizó ecografía intracoronaria o tomografía de coherencia óptica en la mitad de los casos, por lo que podría haber un número de FS no diagnosticadas aún mayor. Además, el uso de tomografía de coherencia óptica aún es escaso, pero por su mayor resolución de imagen tiene la capacidad de identificar mejor los struts que la ecografía intracoronaria.
En conclusión, el diagnóstico de FS con técnicas de imagen intravascular es muy preciso y superior al diagnóstico exclusivamente por imagen radiológica y tiene implicaciones pronósticas, ya que las FS incrementan el riesgo de RS y trombosis. Algunos SFA liberadores de sirolimus (Cypher®) tienen una incidencia de FS mayor que otros SFA.