El déficit de hierro (DH), con o sin anemia, es una comorbilidad prevalente en la insuficiencia cardiaca crónica que condiciona una peor evolución clínica de esta1,2. No hay datos sobre prevalencia o factores asociados a la aparición de DH en el síndrome coronario agudo (SCA).
Se presenta un análisis descriptivo de pacientes que ingresaron en nuestro centro por SCA. Este análisis forma parte de un registro prospectivo de pacientes con SCA en el que se analizará, una vez completados la inclusión y el seguimiento, la implicación pronóstica de esta comorbilidad en este contexto clínico. Se excluyó a los pacientes que no firmaron consentimiento informado, a los derivados a otro centro durante el ingreso, a los fallecidos los primeros 5 días tras el SCA y a los que sufrieron hemorragias mayores o recibieron tratamiento con derivados sanguíneos o con hierro. Se determinaron parámetros inflamatorios (proteína C reactiva ultrasensible e interleucina 6 [IL-6]) y datos del metabolismo del hierro a los 5 y a los 30 días. Siguiendo el consenso internacional, se determinó DH a partir de ferritina < 100 ng/ml o saturación de transferrina < 20% asociada a ferritina < 800 ng/ml. Tras la inclusión, se recogieron variables demográficas y clínicas potencialmente implicadas en la aparición de DH.
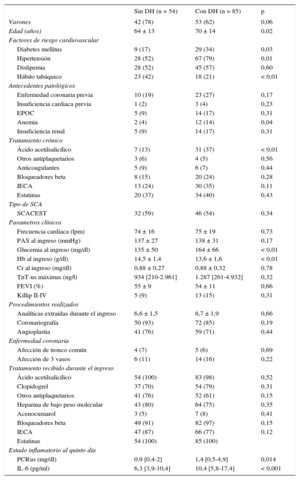
Entre noviembre de 2012 y junio de 2014, se incluyó a 139 pacientes (edad, 67 ± 14 años; el 32% mujeres). De ellos, 85 (61%) presentaban DH y 39 (28%), anemia. Estas tasas disminuyeron al 54 y el 23% entre los 119 pacientes de los que se obtuvo determinación analítica a los 30 días. Los pacientes con DH tenían glucemias más altas, cifras de hemoglobina (Hb) más bajas y mayores concentraciones de proteína C reactiva e IL-6 (p ≤ 0,01) (tabla). No se hallaron diferencias en la proporción de SCA con elevación del segmento ST, la distribución de las lesiones coronarias y el tratamiento recibido durante la hospitalización.
Características clínicas y tratamiento previo al síndrome coronario agudo de pacientes con y sin déficit de hierro
| Sin DH (n = 54) | Con DH (n = 85) | p | |
|---|---|---|---|
| Varones | 42 (78) | 53 (62) | 0,06 |
| Edad (años) | 64 ± 13 | 70 ± 14 | 0,02 |
| Factores de riesgo cardiovascular | |||
| Diabetes mellitus | 9 (17) | 29 (34) | 0,03 |
| Hipertensión | 28 (52) | 67 (79) | 0,01 |
| Dislipemia | 28 (52) | 45 (57) | 0,60 |
| Hábito tabáquico | 23 (42) | 18 (21) | < 0,01 |
| Antecedentes patológicos | |||
| Enfermedad coronaria previa | 10 (19) | 23 (27) | 0,17 |
| Insuficiencia cardiaca previa | 1 (2) | 3 (4) | 0,23 |
| EPOC | 5 (9) | 14 (17) | 0,31 |
| Anemia | 2 (4) | 12 (14) | 0,04 |
| Insuficiencia renal | 5 (9) | 14 (17) | 0,31 |
| Tratamiento crónico | |||
| Ácido acetilsalicílico | 7 (13) | 31 (37) | < 0,01 |
| Otros antiplaquetarios | 3 (6) | 4 (5) | 0,56 |
| Anticoagulantes | 5 (9) | 6 (7) | 0,44 |
| Bloqueadores beta | 8 (15) | 20 (24) | 0,28 |
| IECA | 13 (24) | 30 (35) | 0,11 |
| Estatinas | 20 (37) | 34 (40) | 0,43 |
| Tipo de SCA | |||
| SCACEST | 32 (59) | 46 (54) | 0,34 |
| Parametros clínicos | |||
| Frecuencia cardiaca (lpm) | 74 ± 16 | 75 ± 19 | 0,73 |
| PAS al ingreso (mmHg) | 137 ± 27 | 138 ± 31 | 0,17 |
| Glucemia al ingreso (mg/dl) | 135 ± 50 | 164 ± 66 | < 0,01 |
| Hb al ingreso (g/dl) | 14,5 ± 1,4 | 13,6 ± 1,6 | < 0,01 |
| Cr al ingreso (mg/dl) | 0,88 ± 0,27 | 0,88 ± 0,32 | 0,78 |
| TnT-us máximas (ng/l) | 934 [210-2.961] | 1.287 [261-4.932] | 0,32 |
| FEVI (%) | 55 ± 9 | 54 ± 11 | 0,66 |
| Killip II-IV | 5 (9) | 13 (15) | 0,31 |
| Procedimientos realizados | |||
| Analíticas extraídas durante el ingreso | 6,6 ± 1,5 | 6,7 ± 1,9 | 0,66 |
| Coronariografía | 50 (93) | 72 (85) | 0,19 |
| Angioplastia | 41 (76) | 59 (71) | 0,44 |
| Enfermedad coronaria | |||
| Afección de tronco común | 4 (7) | 5 (6) | 0,69 |
| Afección de 3 vasos | 6 (11) | 14 (16) | 0,22 |
| Tratamiento recibido durante el ingreso | |||
| Ácido acetilsalicílico | 54 (100) | 83 (98) | 0,52 |
| Clopidogrel | 37 (70) | 54 (79) | 0,31 |
| Otros antiplaquetarios | 41 (76) | 52 (61) | 0,15 |
| Heparina de bajo peso molecular | 43 (80) | 64 (75) | 0,35 |
| Acenocumarol | 3 (5) | 7 (8) | 0,41 |
| Bloqueadores beta | 49 (91) | 82 (97) | 0,15 |
| IECA | 47 (87) | 66 (77) | 0,12 |
| Estatinas | 54 (100) | 85 (100) | |
| Estado inflamatorio al quinto día | |||
| PCRus (mg/dl) | 0,9 [0,4-2] | 1,4 [0,5-4,9] | 0,014 |
| IL-6 (pg/ml) | 6,3 [3,9-10,4] | 10,4 [5,8-17,4] | < 0,001 |
Cr: creatinina; DH: déficit de hierro; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; Hb: hemoglobina; IECA: inhibidores de la enzima de conversión de la angiotensina; IL-6: interleucina 6; insuficiencia renal: filtrado glomerular < 60 ml/min/1,73 m2; PAS: presión arterial sistólica; PCRus: proteína C reactiva ultrasensible; SCA: síndrome coronario agudo; SCACEST: síndrome coronario agudo con elevación del segmento ST; TnT-us: troponina T ultrasensible.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
El análisis de regresión logística multivariable mostró que la IL-6 (p = 0,011), la Hb al ingreso (p = 0,001) y el tratamiento previo con ácido acetilsalicílico (p = 0,021) fueron predictores de DH independientes.
El presente estudio demuestra que la prevalencia de DH en el SCA es elevada (61%). Esta alta prevalencia es, además, persistente en más de la mitad de los pacientes al cabo de 30 días del evento coronario. Ambos hallazgos son novedosos y tan solo comparables en el contexto de la cardiopatía isquémica con la serie de Jankowska et al3, en la que se describe una prevalencia de DH del 48% de los pacientes con enfermedad coronaria estable sometidos a cirugía cardiaca. La asociación entre DH y SCA podría tener implicaciones pronósticas en la calidad de vida y la capacidad funcional a largo plazo, todavía por determinar.
El pequeño tamaño muestral y el corto seguimiento no permiten esclarecer el impacto pronóstico que el DH confiere al SCA y, por lo tanto, limita sus implicaciones clínicas a la espera de que se completen la inclusión y el seguimiento de los pacientes de nuestra serie. Tampoco se pueden analizar los mecanismos fisiopatológicos que derivan en un DH en el contexto del SCA. Sin embargo, son llamativos la asociación independiente observada entre DH y el tratamiento crónico con ácido acetilsalicílico, los bajos valores de Hb y con un marcado estado inflamatorio (altas cifras de IL-6 y proteína C reactiva).
Más específicamente, la relación entre DH y estado inflamatorio se ha reconocido en fases evolucionadas de los pacientes con insuficiencia cardiaca crónica4. Por el contrario, en un estudio previo de nuestro grupo se observó que los pacientes con estados inflamatorios más marcados que ingresaban por SCA tenían mayor probabilidad de sufrir anemia durante la hospitalización5. Nuestros datos concuerdan con los de Huang et al6, con una asociación significativa entre una sideremia baja y concentraciones de IL-6 altas en pacientes con SCA con elevación del segmento ST. Como es conocido, la inflamación interviene en el proceso de formación de la placa de aterosclerosis, y el estado inflamatorio se intensifica en el momento en que esta se rompe. Parece plausible, aunque especulativo, que la enfermedad coronaria (y más concretamente su inestabilización) y el DH compartan mecanismos etiopatogénicos comunes relacionados con dicho estado inflamatorio, más allá de una posible asociación propiamente etiopatogénica entre el DH y el SCA.
La asociación entre DH y tratamiento crónico con ácido acetilsalicílico tiene como causa más probable el sangrado digestivo crónico inadvertido. Sin embargo, no queda claro que la posible aparición de DH haga aconsejable modificar la estrategia antiagregante para estos pacientes.
Como conclusión, el DH es una condición prevalente y persistente en el SCA que se asocia a tratamiento antiagregante crónico, anemización y un marcado estado inflamatorio, y sus implicaciones pronósticas están aún por determinar.
FINANCIACIÓNLas investigaciones realizadas en esta publicación tuvieron el apoyo de la Sociedad Catalana de Cardiología con la beca Servier 2012.
CONFLICTO DE INTERESESJ. Comín-Colet fue miembro del comité de dirección de los estudios FAIR-HF y CONFIRM-HF (ambos patrocinados por Vifor Pharma Ltd.). Asimismo, ha recibido honorarios por conferencias de Vifor Pharma Ltd.