Existen pocos estudios que comparen los accesos por la radial izquierda (ARI) y por la radial derecha en intervenciones coronarias percutáneas (ICP) en población general y practicadas por cirujanos con diferentes grados de experiencia en intervencionismo. El objetivo de nuestro estudio es comparar la seguridad y el beneficio clínico con cada acceso en pacientes no seleccionados con síndrome coronario agudo (SCA) y angina estable (AE).
MétodosPara evitar los posibles sesgos de un estudio no aleatorizado, se usó la puntuación de propensión para comparar ambos accesos radiales. Se recogieron datos de 18.716 pares con AE y 46.241 con SCA sometidos a ICP con implante de stent entre 2014 y 2017, en 151 centros terciarios con cardiología intervencionista en Polonia (registro nacional de Polonia [ORPKI]).
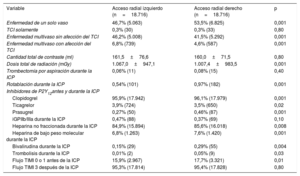
ResultadosNo se encontraron diferencias en cuanto a mortalidad y complicaciones periprocedimiento en AE. El ARI se asoció con mayores dosis de radiación independientemente de la presentación clínica (AE, 1.067,0±947,10 frente a 1.007,4±983,5 mGy; p=0,001; SCA, 1.212,7±1.005,5 frente a 1.053,5±1.029,7 mGy; p=0,001). En los pacientes con SCA, el ARI se asoció con mayor cantidad de contraste (174,2±75,4 frente a 167,2±72,1ml; p=0,001). Además, en los pacientes con SCA y ARI, las complicaciones periprocedimiento como disección coronaria (el 0,16 frente al 0,09%; p=0,008), fenómeno de no reflow (el 0,65 frente al 0,49%; p=0,005) y hemorragia en el sitio de punción (el 0,09 frente al 0,05%; p=0,04) resultaron más frecuentes. No hubo diferencias en la mortalidad entre los 2 grupos (p=0,90).
ConclusionesLos resultados que se presentan podrían estar en relación con una menor experiencia en el ARI. Ambos accesos son seguros en los pacientes con AE, pero el ARI se asoció con una mayor frecuencia de complicaciones periprocedimiento de ICP en el SCA.
Palabras clave
El acceso radial para la intervención coronaria percutánea (ICP) se ha asociado con una reducción de la mortalidad y las complicaciones hemorrágicas en comparación con lo observado con el abordaje por vía femoral1-6. El acceso radial derecho (ARD) se ha adoptado ampliamente como vía de acceso de elección para las intervenciones percutáneas, a pesar de las variaciones anatómicas más marcadas y las dificultades técnicas7,8. En cambio, el acceso radial izquierdo (ARI) tiene el potencial de mejorar la manipulación del catéter debido a la anatomía más favorable, y se considera similar al acceso por vía femoral8-10. No obstante, los cardiólogos intervencionistas optan menos por el ARI8,9.
Escasean los datos de comparación de los resultados clínicos entre el ARI y el ARD para la ICP en poblaciones no seleccionadas (all-comers) y realizada por operadores con diferentes niveles de experiencia. En consecuencia, continúa sin estar claro qué arteria es una opción más favorable para el acceso radial. Sin embargo, cada vez hay más evidencias clínicas de cierta ventaja del ARI frente al ARD por lo que respecta a la duración de la intervención, la dosis de radiación y la tasa de complicaciones cerebrovasculares8,11-14. Por consiguiente, el objetivo de este estudio es comparar la seguridad y los resultados clínicos del ARD con los del ARI durante la ICP en una cohorte no seleccionada de pacientes con angina estable (AE) o síndrome coronario agudo (SCA), utlizando para ello los datos del registro nacional de ICP de Polonia (ORPKI).
MÉTODOSEl ORPKI es un registro nacional de Polonia que recoge los datos de todos los procedimientos de cardiología intervencionista llevados a cabo en este país15-19. Este registro cuenta con el aval de la Asociación de Intervenciones Cardiovasculares de Polonia de la Sociedad Polaca de Cardiología y es gestionado por el Jagiellonian University Medical College de Cracovia20. En la base de datos no se incluye ningún dato personal. Para el presente estudio prospectivo de observación, se evaluaron los datos de 151 centros de cardiología intervencionista de Polonia entre enero de 2014 y diciembre de 2017. Se incluyó en el estudio a un total de 330.450 pacientes consecutivos a los que se practicó una ICP con implante de stents por ARD o ARI.
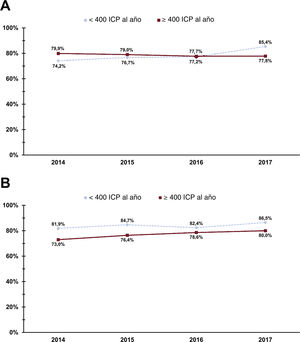
Las intervenciones se llevaron a cabo por ARD o ARI en 255.866 (77,4%) y 74.584 (22,6%) pacientes respectivamente. En la figura 1 se presenta la frecuencia de uso del ARD entre los años 2014 y 2017 en los centros con un volumen de intervenciones por AE o SCA <400 y ≥ 400 ICP al año. Tras un emparejamiento por puntuación de propensión, se incluyó en el análisis a 18.716 pares de pacientes con AE y 46.241 pares de pacientes con SCA sometidos a ICP por ARD o por ARI. En la figura 2 se presenta el diagrama de flujo de los pacientes.
Todas las ICP las realizaron operadores con diferentes grados de experiencia y destreza con la vía radial. Se determinó la experiencia total con el acceso radial de cada operador por separado mediante los números de identificación únicos específicos en el registro. El cálculo se basó en el número total de ICP realizadas por acceso radial entre 2014 y 2017. La vía de acceso vascular para las intervenciones, la elección de la lesión diana y la técnica de tratamiento utilizada se dejaron al criterio del operador. La vía de acceso empleada para cada intervención se determinó por el lugar donde se había obtenido con éxito el acceso vascular. Hubo 1.529 intervenciones (0,46%) en las que no se identificó la vía de acceso. Además, hubo un cambio de la vía de acceso vascular en 159 pacientes con AE (0,17%) y 3.619 pacientes con SCA (1,5%). Todas las intervenciones con una vía de acceso no identificada o con un cambio de la vía de acceso se excluyeron del análisis. Por otra parte, no se recogieron datos relativos a la complejidad y el tipo de lesión.
Todas las intervenciones se llevaron a cabo según estándares locales y la guía de la Sociedad Europea de Cardiología de ICP siempre que fuera pertinente. Se registraron prospectivamente todas las complicaciones intraintervención. La mortalidad periintervención se definió como la muerte por cualquier causa durante la ICP, hasta el traslado del paciente del laboratorio de hemodinámica al servicio de cardiología o la unidad de cuidados intensivos. Las complicaciones hemorrágicas se definieron de manera homogénea en todos los centros como cualquier signo de hemorragia manifiesto y que pudiera motivar alguna actuación (p. ej., sangrado superior al que sería de prever en esas circunstancias clínicas, incluido el observado solo en exploraciones de imagen) que no cumpliera los criterios de hemorragia tipo 3, 4 o 521 pero sí al menos 1 de los siguientes: a) que requiriera la intervención médica, no quirúrgica, de un profesional sanitario; b) que condujera a una hospitalización o un aumento del nivel de asistencia prestado al paciente, o c) que motivara una evaluación. Los médicos locales diagnosticaron los ictus. No se presentaron datos específicos sobre el tipo de ictus o la evolución neurológica. La ausencia de restablecimiento del flujo se definió por el hecho de que no se restableciera una perfusión miocárdica óptima a través de la arteria coronaria sin que hubiera signos angiográficos mecánicos de obstrucción, disección, espasmo o embolia distal en el vaso sanguíneo (flujo de grado Thrombolysis in Myocardial Infarction [TIMI] ≤ 2). La parada cardiaca se diagnosticó por la ausencia de actividad eléctrica organizada en el miocardio, sin una contracción coherente de los ventrículos, causante de una incapacidad del corazón de generar un gasto cardiaco suficiente. Esta definición incluye tanto a los pacientes reanimados como a los que sufrieron parada cardiaca súbita con resultado de muerte. Los eventos adversos se identificaron según el criterio del operador, aplicando las definiciones incluidas en la vigente guía de la Sociedad Europea de Cardiología22. No se realizó ninguna evaluación de seguimiento después de que los pacientes fueran dados de alta del hospital.
Todos los pacientes firmaron un documento de consentimiento informado para cada intervención. El estudio cumplió los principios éticos para la investigación clínica establecidos en la Declaración de Helsinki con sus enmiendas posteriores. No se dispuso de ningún apoyo de financiación para este registro.
Análisis estadísticoCon objeto de superar las posibles repercusiones del diseño no aleatorizado, se calculó una puntuación de propensión mediante un modelo de regresión logística multivariable tomando la vía de acceso (ARD frente a ARI) como variable dependiente. Para reducir los sesgos analíticos, se tomaron como variables el volumen de intervenciones del centro ≥ 400 ICP y todas las características basales disponibles, como sexo, edad, peso, diabetes mellitus, ictus previo, infarto de miocardio previo, ICP previa, cirugía de revascularización coronaria previa, tabaquismo, hipertensión, enfermedad renal crónica, psoriasis, tratamiento periintervención (ácido acetilsalicílico, inhibidores de P2Y12, heparina no fraccionada, heparina de bajo peso molecular), datos clínicos basales, indicación específica para el grupo de SCA (infarto agudo de miocardio con elevación del segmento ST, infarto agudo de miocardio sin elevación del segmento ST, angina inestable), y flujo TIMI basal. Se utilizó un valor de corte del calibrador para obtener un equilibrio satisfactorio asegurando que se estimaran unas diferencias estandarizadas < 10% para todos los factores de confusión. El emparejamiento de los pacientes se realizó en proporción 1:1 y los pacientes no emparejados no se incluyeron en el análisis de los pares emparejados.
Los análisis de la AE y el SCA se realizaron por separado e incluyeron una estadística descriptiva estándar. Las variables cuantitativas se presentan en forma de media±desviación estándar. Las variables cualitativas se describen mediante número y porcentaje. Para la comparación de los grupos antes del emparejamiento, se empleó la prueba de la U de Mann-Whitney (para los datos con distribución no normal) o la prueba de la t de Student (para los datos con distribución normal) en las variables continuas y la prueba exacta de Fisher o la prueba de la χ2 de Pearson en las variables cualitativas (nominales o dicotómicas). La normalidad de la distribución de los datos se determinó con la prueba de Kolmogorov-Smirnov con corrección de Lilliefors. Los pares de pacientes emparejados se compararon con la prueba del orden con signo (signed-rank) de Wilcoxon (para las diferencias en los datos de distribución no normal) o la prueba de la t para datos emparejados (para las diferencias en los datos de distribución normal) en las variables continuas y la prueba de McNemar-Bowker en las variables cualitativas (nominales).
Para los valores de p correspondientes a los resultados periintervención de las ICP tras el emparejamiento por puntuación de propensión, se introdujo un ajuste con el método de control de FDR de Benjamini, Hochberg y Yekutieli. El análisis se llevó a cabo con el criterio de «según tratamiento real». Además, se realizó un análisis de regresión logística multivariado para identificar posibles factores determinantes y predictores independientes del uso de la arteria izquierda o derecha para la ICP. Se utilizó una selección retrógrada en el análisis de regresión logística con un nivel de probabilidad para la inclusión de covariables en el modelo de 0,05. En la elaboración del modelo final se incluyeron todas las variables previas a la intervención (basales). Dado el elevado número de casos, fue posible aplicar un control completo de todos los factores de confusión en la mayor medida posible y reducir al mismo tiempo la posibilidad de un sobreajuste y estimaciones numéricamente inestables.
Los resultados se presentan en forma de odds ratios (OR) con los intervalos de confianza del 95% (IC95%). Dada la gran cantidad de datos y las tasas relativamente bajas de datos no disponibles, no se utilizaron métodos de imputación de los datos. Todos los análisis estadísticos se llevaron a cabo con el programa JMP versión 14.2.0 (SAS Institute Inc., Estados Unidos).
RESULTADOSEn la tabla 1 se presentan los datos clínicos y demográficos basales completos. Todos los datos presentados se calcularon con pares de pacientes emparejados. En la tabla 2, la tabla 3 y la tabla 4, se presenta información detallada sobre las indicaciones angiográficas para la ICP y los tratamientos antiagregante plaquetario y antitrombótico durante la intervención en el total de pacientes incluidos, y aquellos con AE y con SCA por separado.
Características basales antes y después del emparejamiento por puntuación de propensión
| Variable | Acceso radial izquierdo (n=74.584) | Acceso radial derecho (n=255.866) | p |
|---|---|---|---|
| Varones | 50.911 (68,4) | 177.159 (69,8) | 0,001 |
| Peso (kg) | 81,3±16,0 | 81,3±17,6 | 0,03 |
| Edad (años) | 67,4±10,7 | 66,6±10,7 | 0,004 |
| Diabetes mellitus | 18.175 (24,4) | 60.671 (23,7) | 0,002 |
| Ictus previo | 2.358 (3,2) | 7.875 (3,1) | 0,20 |
| IM previo | 24.606 (33,0) | 74.487 (29,1) | 0,001 |
| CABG previa | 7.704 (10,3) | 5.606 (2,2) | 0,001 |
| ICP previa | 28.808 (38,6) | 91.466 (35,8) | 0,001 |
| Tabaquismo | 14.125 (19,0) | 53.667 (21,0) | 0,001 |
| Hipertensión | 53.786 (72,1) | 181.389 (70,9) | 0,001 |
| Enfermedad renal crónica | 3.823 (5,1) | 11.813 (4,6) | 0,001 |
| Enfermedad pulmonar obstructiva crónica | 1.438 (2,5) | 5.281 (2,6) | 0,50 |
| Psoriasis | 319 (0,4) | 1.031 (0,4) | 0,30 |
| Parada cardiaca en la situación inicial | 547 (1,0) | 1.946 (0,9) | 0,40 |
| Datos tras emparejamiento por puntuación de propensión en la angina estable | Acceso radial izquierdo (n=18.716) | Acceso radial derecho (n=18.716) | p |
|---|---|---|---|
| Varones | 13.016 (69,5) | 13.281 (71,0) | 0,10 |
| Peso (kg) | 81,9±15,6 | 81,9±17,0 | 0,70 |
| Edad (años) | 67,3±9,7 | 67,0±9,6 | 0,10 |
| Diabetes mellitus | 4.999 (26,7) | 4.895 (26,2) | 0,20 |
| Ictus previo | 554 (3,0) | 559 (3,0) | 0,90 |
| IM previo | 7.955 (42,5) | 7.996 (42,7) | 0,70 |
| CABG previa | 2.090 (11,2) | 1.930 (10,3) | 0,10 |
| ICP previa | 10.104 (54,0) | 10.334 (55,2) | 0,001 |
| Tabaquismo | 2.895 (15,5) | 2.771 (14,8) | 0,10 |
| Hipertensión | 14.233 (76,1) | 14.285 (76,3) | 0,50 |
| Enfermedad renal crónica | 1.034 (5,5) | 985 (5,3) | 0,30 |
| Enfermedad pulmonar obstructiva crónica | 451 (2,8) | 394 (2,4) | 0,20 |
| Psoriasis | 67 (0,4) | 59 (0,3) | 0,50 |
| Parada cardiaca en la situación inicial | — | — | — |
| Datos tras emparejamiento por puntuación de propensión en el síndrome coronario agudo | Acceso radial izquierdo (n=46.241) | Acceso radial derecho (n=46.241) | p |
|---|---|---|---|
| Varones | 68,2 (31.520) | 68,6 (31.723) | 0,10 |
| Peso (kg) | 81,0±15,9 | 81,0±17,4 | 0,90 |
| Edad (años) | 67,2±11,1 | 67,0±11,0 | 0,10 |
| Diabetes mellitus | 10.791 (23,3) | 10.722 (23,2) | 0,60 |
| Ictus previo | 1.474 (3,2) | 1.459 (3,2) | 0,80 |
| IM previo | 13.178 (28,5) | 12.724 (27,5) | 0,003 |
| CABG previa | 3.007 (6,5) | 2.906 (6,3) | 0,10 |
| ICP previa | 14.894 (32,2) | 14.425 (31,2) | 0,001 |
| Tabaquismo | 9.934 (21,5) | 10.388 (22,5) | 0,10 |
| Hipertensión | 32.990 (71,3) | 32.975 (71,3) | 0,90 |
| Enfermedad renal crónica | 2.221 (4,8) | 2.340 (5,1) | 0,10 |
| Enfermedad pulmonar obstructiva crónica | 798 (2,4) | 943 (2,6) | 0,10 |
| Parada cardiaca en la situación inicial | 494 (1,3) | 501 (1,3) | 0,50 |
CABG: cirugía de revascularización coronaria; ICP: intervención coronaria percutánea; IM: infarto de miocardio.
Los valores expresan n (%) o media ± desviación estándar.
Información detallada de la intervención coronaria percutánea tras el emparejamiento por puntuación de propensión en la angina estable
| Variable | Acceso radial izquierdo (n=18.716) | Acceso radial derecho (n=18.716) | p |
|---|---|---|---|
| Enfermedad de un solo vaso | 46,7% (5.063) | 53,5% (6.825) | 0,001 |
| TCI solamente | 0,3% (30) | 0,3% (33) | 0,80 |
| Enfermedad multivaso sin afección del TCI | 46,2% (5.008) | 41,5% (5.292) | 0,001 |
| Enfermedad multivaso con afección del TCI | 6,8% (739) | 4,6% (587) | 0,001 |
| Cantidad total de contraste (ml) | 161,5±76,6 | 160,0±71,5 | 0,80 |
| Dosis total de radiación (mGy) | 1.067,0±947,1 | 1.007,4±983,5 | 0,001 |
| Trombectomía por aspiración durante la ICP | 0,06% (11) | 0,08% (15) | 0,40 |
| Rotablación durante la ICP | 0,54% (101) | 0,97% (182) | 0,001 |
| Inhibidores de P2Y12antes y durante la ICP | |||
| Clopidogrel | 95,9% (17.942) | 96,1% (17.979) | 0,001 |
| Ticagrelor | 3,9% (724) | 3,5% (650) | 0,02 |
| Prasugrel | 0,27% (50) | 0,46% (87) | 0,001 |
| iGPIIb/IIIa durante la ICP | 0,47% (88) | 0,37% (69) | 0,10 |
| Heparina no fraccionada durante la ICP | 84,9% (15.894) | 85,6% (16.018) | 0,008 |
| Heparina de bajo peso molecular durante la ICP | 6,8% (1.263) | 7,6% (1.420) | 0,001 |
| Bivalirudina durante la ICP | 0,15% (29) | 0,29% (55) | 0,004 |
| Trombolisis durante la ICP | 0,01% (2) | 0,05% (9) | 0,03 |
| Flujo TIMI 0 o 1 antes de la ICP | 15,9% (2.967) | 17,7% (3.321) | 0,01 |
| Flujo TIMI 3 después de la ICP | 95,3% (17.814) | 95,4% (17.828) | 0,80 |
ICP: intervención coronaria percutánea; iGPIIb/IIIa: inhibidores de la glucoproteína IIb/IIIa; TCI: tronco coronario izquierdo; TIMI: Thrombolysis in Myocardial Infarction.
Los valores expresan n (%) o media ± desviación estándar.
Información detallada de la intervención coronaria percutánea tras el emparejamiento por puntuación de propensión en el síndrome coronario agudo
| Variable | Acceso radial izquierdo (n=46.241) | Acceso radial derecho (n=46.241) | p |
|---|---|---|---|
| Enfermedad de un solo vaso | 45,9% (17.539) | 45,9% (18.144) | 0,20 |
| TCI solamente | 0,20% (77) | 0,20% (81) | 0,90 |
| Enfermedad multivaso sin afección del TCI | 47,1% (17.988) | 48,2% (19.082) | 0,001 |
| Enfermedad multivaso con afección del TCI | 6,8% (2.589) | 5,7% (2.243) | 0,001 |
| IAMCEST | 34,2% (15.791) | 31,7% (14.668) | 0,001 |
| IAMSEST | 25,9% (11.991) | 27,5% (12.707) | 0,001 |
| AI | 39,9% (18.459) | 40,8% (18.866) | 0,001 |
| Cantidad total de contraste (ml) | 174,2±75,4 | 167,2±72,1 | 0,001 |
| Dosis total de radiación (mGy) | 1.212,7±1.005,5 | 1.053,5±1.029,7 | 0,001 |
| Trombectomía por aspiración durante la ICP | 5,3% (2.442) | 4,3% (1.964) | 0,001 |
| Rotablación durante la ICP | 0,19% (87) | 0,32% (149) | 0,001 |
| Inhibidores de P2Y12antes y durante la ICP | |||
| Clopidogrel | 93,7% (43.331) | 93,7% (43.447) | 0,01 |
| Ticagrelor | 5,7% (2.618) | 5,5% (2.534) | 0,01 |
| Prasugrel | 0,63% (292) | 0,56% (260) | 0,01 |
| iGPIIb/IIIa durante la ICP | 4,6% (2.104) | 3,5% (1.603) | 0,001 |
| Heparina no fraccionada durante la ICP | 80,6% (37.290) | 81,5% (37.688) | 0,001 |
| Heparina de bajo peso molecular durante la ICP | 7,7% (3.543) | 7,9% (3.644) | 0,06 |
| Bivalirudina durante la ICP | 0,26% (118) | 0,32% (148) | 0,06 |
| Trombolisis durante la ICP | 0,22% (100) | 0,15% (70) | 0,02 |
| Flujo TIMI 0 o 1 antes de la ICP | 38,8% (17.957) | 38,3% (17.730) | 0,10 |
| Flujo TIMI 3 después de la ICP | 94,0% (43.329) | 94,2% (43.454) | 0,10 |
AI: angina inestable; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; ICP: intervención coronaria percutánea; iGPIIb/IIIa: inhibidores de la glucoproteína IIb/IIIa; TCI: tronco coronario izquierdo; TIMI: Thrombolysis in Myocardial Infarction.
Los valores expresan n (%) o media ± desviación estándar.
Información detallada de la intervención coronaria percutánea tras el emparejamiento por puntuación de propensión en el conjunto de todos los pacientes incluidos
| Variable | Acceso radial izquierdo (n=67.462) | Acceso radial derecho (n=67.462) | p |
|---|---|---|---|
| Enfermedad de un solo vaso | 46,4% (23.886) | 47,8% (26.112) | 0,001 |
| TCI solamente | 0,22% (112) | 0,21% (112) | 0,60 |
| Enfermedad multivaso sin afección del TCI | 46,6% (23.975) | 46,5% (25.366) | 0,90 |
| Enfermedad multivaso con afección del TCI | 6,8% (3.487) | 5,4% (2.960) | 0,001 |
| IAMCEST | 24,2% (16.302) | 22,3% (15.057) | 0,001 |
| IAMSEST | 18,6% (12.562) | 19,1% (12.885) | 0,02 |
| AI | 29,1% (19.645) | 28,5% (19.229) | 0,001 |
| AE | 27,6% (18.647) | 29,5% (19.882) | 0,001 |
| Cantidad total de contraste (ml) | 170,9±76,2 | 165,4±72,0 | 0,001 |
| Dosis total de radiación (mGy) | 1.175,6±1.000,2 | 1.039,0±1.009,2 | 0,001 |
| Trombectomía por aspiración durante la ICP | 3,8% (2.547) | 3,0% (2.011) | 0,001 |
| Rotablación durante la ICP | 0,28% (190) | 0,55% (369) | 0,001 |
| Inhibidores de P2Y12antes y durante la ICP | |||
| Clopidogrel | 94,2% (63.576) | 94,7% (63.880) | 0,01 |
| Ticagrelor | 5,2% (3.515) | 4,8% (3.265) | 0,01 |
| Prasugrel | 0,55% (371) | 0,47% (317) | 0,04 |
| iGPIIb/IIIa durante la ICP | 3,4% (2.314) | 2,6% (1.748) | 0,001 |
| Heparina no fraccionada durante la ICP | 80,9% (54.563) | 83,8% (56.529) | 0,001 |
| Heparina de bajo peso molecular durante la ICP | 8,3% (5.616) | 7,8% (5.274) | 0,001 |
| Bivalirudina durante la ICP | 0,23% (155) | 0,30% (204) | 0,001 |
| Trombolisis durante la ICP | 0,15% (103) | 0,11% (75) | 0,03 |
| Flujo TIMI 0 o 1 antes de la ICP | 32,7% (23.875) | 31,9% (77.774) | 0,10 |
| Flujo TIMI 3 después de la ICP | 94,2% (68.758) | 94,8% (232.931) | 0,10 |
AE: angina estable; AI: angina inestable; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; ICP: intervención coronaria percutánea; iGPIIb/IIIa: inhibidores de glucoproteína IIb/IIIa; TCI: tronco coronario izquierdo; TIMI: Thrombolysis in Myocardial Infarction.
Los valores expresan n (%) o media ± desviación estándar.
Tras el emparejamiento por puntuación de propensión, se observaron dosis de radiación superiores en la ICP por ARI tanto en la AE como en el SCA (ARI frente a ARD, 1.067,0±947,1 frente a 1.007,4±983,5 mGy en la AE; p=0,001; 1.212,7±1.005,5 frente a 1.053,5±1.029,7 mGy en el SCA; p=0,001) (tabla 2 y tabla 3). Sin embargo, se observó una cantidad total de contraste superior con el ARI que con el ARD solo en las intervenciones realizadas por SCA (174,2±75,4 frente a 167,2±72,1ml; p=0,001). Además, las dosis de radiación y la cantidad total de contraste utilizado fueron mayores en las ICP por ARI en el total de pacientes incluidos (radiación, 1.175,6±1.000,2 frente a 1.039,0±1.009,2 mGy; p=0,001; cantidad de contraste, 170,9±76,2 frente a 165,4±72,0ml; p=0,001).
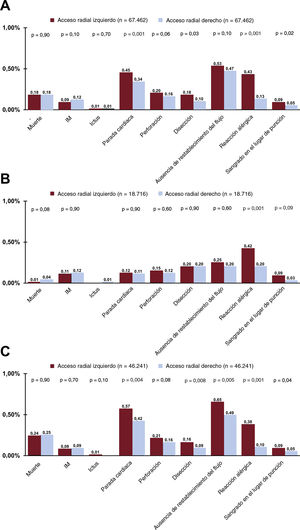
Entre ARI y ARD se observaron similares prevalencias de las complicaciones periintervención de ICP en los pacientes con AE. Sin embargo, las reacciones alérgicas fueron más frecuentes en las intervenciones por ARI que en aquellas por ARD. Además, se observó una tendencia a un aumento del riesgo de complicaciones hemorrágicas en el grupo de ARI. En cambio, hubo una tasa de mortalidad periintervención numéricamente superior, aunque sin significación estadística, asociada con el ARD en las intervenciones por AE (el 0,01 frente al 0,04%; p=0,08) (figura 3). En cambio, en los pacientes con SCA el ARI se asoció con un mayor número de resultados desfavorables, en comparación con el ARD. Los casos de reacción alérgica, parada cardiaca, hemorragia en el lugar de punción, disección de la arteria coronaria y fenómeno de ausencia de restablecimiento del flujo se registraron con más frecuencia en los pacientes con SCA durante las ICP por ARI. Además, hubo una tendencia no significativa a una tasa superior de perforaciones de arterias coronarias en las intervenciones por ARI de pacientes con SCA (p=0,08) (figura 3). No se observaron diferencias de mortalidad entre los 2 grupos en los pacientes con SCA (p=0,90) (figura 3). Por otra parte, los casos de reacción alérgica, parada cardiaca, hemorragia en el lugar de punción y disección de la arteria coronaria se dieron con más frecuencia durante la ICP por ARI en el conjunto de todos los pacientes incluidos. No se apreció ninguna tendencia estadísticamente significativa al aumento del riesgo de perforación arterial coronaria en la ICP por ARI (p=0,06). No hubo diferencias de mortalidad entre los grupos de ARI y ARD en el conjunto de todos los pacientes incluidos (p=0,90). En la figura 3 se presentan los resultados periintervención de ICP en el conjunto de todos los pacientes incluidos y de aquellos con AE y con SCA por separado.
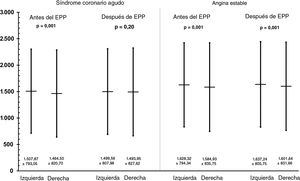
En el análisis multivariante, la cirugía de revascularización coronaria previa fue el más potente factor independiente predictivo de la elección del ARI para la ICP. Además, los cardiólogos intervencionistas de centros grandes con volumen ≥ 400 ICP al año mostraron una mayor probabilidad de elegir la vía de ARI para las intervenciones (tabla 5). Los cardiólogos intervencionistas con similar experiencia en la vía radial realizaron las ICP tanto por ARI como por ARD en los pacientes con SCA. Sin embargo, hubo una proporción ligeramente superior de operadores con experiencia en la vía radial que realizaron las ICP a través del ARI en los pacientes con AE (figura 4).
Factores independientes predictivos del uso de la arteria radial izquierda para la intervención coronaria percutánea
| Variable | OR | IC95% | p |
|---|---|---|---|
| Edad, por cada 10 años | 1,02 | 1,01-1,03 | 0,003 |
| Peso, por cada 10 kg | 0,99 | 0,98-0,99 | 0,003 |
| Sexo femenino | 1,09 | 1,06-1,12 | 0,001 |
| Diabetes mellitus | 0,93 | 0,91-0,96 | 0,001 |
| Infarto de miocardio previo | 1,10 | 1,07-1,14 | 0,001 |
| Intervención coronaria percutánea previa | 0,93 | 0,90-0,96 | 0,001 |
| Cirugía de revascularización coronaria previa | 10,13 | 9,6-10,73 | 0,001 |
| Tabaquismo | 0,96 | 0,93-0,99 | 0,008 |
| Hipertensión | 1,06 | 1,03-1,09 | 0,001 |
| Enfermedades renales crónicas | 0,94 | 0,89-0,99 | 0,04 |
| Enfermedad pulmonar obstructiva crónica | 0,91 | 0,84-0,97 | 0,02 |
| IAMCEST frente a IAMSEST | 1,09 | 1,05-1,13 | 0,001 |
| IAMCEST frente a AE | 1,23 | 1,18-1,28 | 0,001 |
| IAMSEST frente a AI | 0,93 | 0,90-0,97 | 0,001 |
| IAMSEST frente a AE | 1,13 | 1,09-1,18 | 0,001 |
| AI frente a AE | 1,21 | 1,17-1,25 | 0,001 |
| Clase de Killip-Kimball IV frente a I | 0,74 | 0,62-0,88 | 0,001 |
| Clase de Killip-Kimball III frente a I | 2,56 | 2,33-2,80 | 0,001 |
| Clase de Killip-Kimball II frente a I | 2,17 | 2,07-2,27 | 0,001 |
| ≥ 400 ICP en el centro en el año actual | 1,36 | 1,28-1,44 | 0,001 |
| Experiencia del operador de ICP con el acceso radial (2014-2017), por cada 500 intervenciones | 1,02 | 1,01-1.024 | 0,001 |
AE: angina estable; AI: angina inestable; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; IC95%: intervalo de confianza del 95%; ICP: intervención coronaria percutánea; OR: odds ratio.
Un valor de OR > 1 es favorable al empleo de la arteria radial izquierda en vez de la arterial radial derecha para la ICP.
Experiencia de los cardiólogos intervencionistas expresada mediante el número total de intervenciones coronarias percutáneas por acceso radial entre los años 2014 y 2017. Se presentan los datos correspondientes a antes y después del EPP para la angina estable y el síndrome coronario agudo. EPP: emparejamiento por puntuación de propensión.
Los resultados de este estudio ponen de manifiesto que el ARI y el ARD son igual de seguros y eficaces en el contexto de tratamiento de la AE. Sin embargo, se observaron mayores dosis de radiación con las ICP por ARI, con independencia de la presentación clínica. De igual modo, se utilizó una mayor cantidad de contraste en todas las intervenciones por ARI y en el contexto de tratamiento del SCA. En comparación con el ARD, el ARI se asoció con un mayor número de resultados adversos periintervención en el conjunto de todos los pacientes incluidos y en el subgrupo de pacientes con SCA. Los resultados del presente estudio podrían explicarse por la generalmente menor experiencia con el ARI en situaciones de urgencia. Hasta donde nosotros sabemos, el presente estudio es el registro multicéntrico más amplio publicado en el que se ha presentado una perspectiva sobre el ARI y el ARD tanto en la AE como en el SCA en la cardiología clínica contemporánea.
Los estudios anteriores de comparación de ARI y ARD han producido resultados contradictorios. Varios trabajos indicaron una superioridad de la arteria radial izquierda frente a la derecha por lo que respecta a la duración de la intervención, la dosis de radiación y la tasa de complicaciones cerebrovasculares11-14. Sin embargo, en el estudio TALENT23 se observaron unos tiempos de intervención y de fluoroscopia similares con las 2 vías de acceso en las intervenciones coronarias diagnósticas llevadas a cabo por operadores adecuadamente capacitados. Se observaron ligeras reducciones de los tiempos de fluoroscopia con el empleo del ARI en los pacientes de edad avanzada y cuando las intervenciones las realizaban operadores en fase de formación. Sin embargo, otro estudio aleatorizado no confirmó estas observaciones24. Además, en un ensayo aleatorizado previo, en el que se compararon los 2 accesos radiales para realizar coronariografías, se determinó que las características de seguridad eran similares y no se observaron diferencias en la cantidad de contraste utilizado ni en la dosis de radiación aplicada25. Estos resultados fueron coherentes con los del análisis realizado en la subpoblación de pacientes con IAMCEST. No se observaron diferencias entre los 2 tipos de acceso radial por lo que respecta al volumen de contraste utilizado, el tiempo de fluoroscopia, las complicaciones vasculares periintervención y la incidencia de ictus/accidente isquémico transitorio (AIT) o muerte26.
En cambio, los datos de otra cohorte de pacientes con IAMCEST apuntaron a una menor dosis de radiación con el ARI, pero sin diferencias entre las 2 vías de acceso en el volumen de contraste utilizado27. Además, un análisis reciente indica que el ARI se asocia con menos tiempo de fluoroscopia y una menor duración de la intervención en comparación con el ARD para la ICP en pacientes con SCA. Sin embargo, no se observaron diferencias en la cantidad de contraste utilizado28. Otro estudio29 basado en el emparejamiento por puntuación de propensión de 1.100 pacientes, indicó hay asociación entre el ARD y mayores volumen de contraste y tiempo de fluoroscopia. Sin embargo, los resultados clínicos hospitalarios y a los 12 meses fueron similares en los 2 grupos. Por último, en un reciente metanálisis con la inclusión de 3.210 pacientes, no se detectaron diferencias de resultados clínicos entre las 2 vías de acceso radial30. En cambio, con la acumulación de nuevos datos se actualizaron los resultados, y se puso de manifiesto una ventaja del ARI por lo que respecta al tiempo de fluoroscopia y el uso de contraste en comparación con el grupo de ARD, tanto en las intervenciones coronarias diagnósticas como en las de tratamiento. Es de destacar que se propuso que el índice de masa corporal era una posible causa de heterogeneidad de los resultados entre los ensayos31. El metanálisis de datos agrupados más reciente, con un total de 6.450 pacientes, puso de relieve un tiempo de fluoroscopia superior y un mayor uso de contraste en los pacientes en los que se utilizó el ARD. Se observaron unas tasas de complicaciones en la zona de acceso y de ictus similares con las 2 vías de acceso radiales9. Sin embargo, todos estos estudios tenían un tamaño muestral relativamente pequeño, insuficiente para detectar diferencias en los resultados clínicos. Además, los metanálisis mencionados incluyeron estudios sin definiciones unificadas de los objetivos. Por otra parte, los datos procedían de sistemas de asistencia sanitaria diferentes y de distintos países y no eran lo suficientemente homogéneos.
Nuestros resultados contradicen los de la mayoría de los estudios contemporáneos. La mayor dosis de radiación, el mayor volumen de contraste y la tasa superior de complicaciones periintervención podrían estar relacionados con una menor destreza en el uso del ARI. En nuestra base de datos, los cardiólogos intervencionistas optaron por el ARD con una frecuencia más de 3 veces superior a la del ARI. Además, es probable que las intervenciones más complejas se llevaran a cabo por ARI, ya que los factores independientes predictivos de la elección de esta vía de acceso fueron la cirugía de revascularización coronaria previa y el contexto clínico más grave (tasa de enfermedad multivaso con afección del tronco coronario izquierdo más alta y más pacientes con IAMCEST), así como la ICP llevada a cabo en centros de gran volumen (tabla 3, tabla 4 y tabla 5).
Por otro lado, en la mayoría de los estudios previos no se tuvo en cuenta la experiencia total del operador ni el nivel de destreza con la vía radial. En nuestro estudio, las ICP en el contexto del tratamiento del SCA de los grupos de ARI y de ARD fueron realizadas por cardiólogos intervencionistas con igual experiencia. Sin embargo, hubo una proporción ligeramente superior de operadores con experiencia en la vía radial que realizaron las ICP a través del ARI en los pacientes con AE (figura 4). Además, hubo una tasa ligeramente mayor de casos con un flujo TIMI 0 o 1 antes de la ICP en los pacientes con AE del grupo de ARD. Estos factores podrían estar relacionados con una tendencia al aumento de la mortalidad en la AE durante las intervenciones por ARD. Es importante señalar que un estudio reciente ha puesto de manifiesto que la tasa de ictus es superior en las ICP realizadas por operadores con menos experiencia en la vía de acceso radial15. En ese análisis de regresión logística multivariado, el porcentaje de ICP por acceso radial por operador (por cada 1% de aumento, OR = 0,981; IC95%, 0,967-0,997; p=0,02) se consideró un factor independiente predictivo de ictus periintervención15. En cambio, los datos recientes del ensayo ACCOAST muestran ausencia de repercusiones de la vía de acceso radial en el riesgo de ictus32. En nuestro análisis, se observó una tasa baja de ictus periintervención, sin que se apreciaran diferencias entre los grupos. Sin embargo, hay varios factores que podrían tener influencia en los resultados favorables observados en el grupo de ARI. Diversos análisis han mostrado una mayor frecuencia de tortuosidad en la arteria subclavia derecha que en la izquierda7,9,13. La arteria radial izquierda puede facilitar el acceso directo a la aorta ascendente o la arteria mamaria interna izquierda y permitir una aplicación más rápida del dispositivo7,13. Además, se considera que las maniobras realizadas con el catéter al utilizar el ARI son muy similares a las aplicadas por la vía femoral7,13. Estas diferencias podrían explicar en parte algunas de las descripciones de una dosis de radiación y un volumen de contraste superiores en las intervenciones a través del ARD. Sin embargo, aunque la mayor parte de los estudios registraron el tiempo de fluoroscopia, este parámetro tiene una capacidad limitada para estimar la exposición real a la radiación7,9,13 y se considera simplemente un indicador general de la radiación de rayos X producida. En consecuencia, no hay una asociación directa entre la exposición del operador y la absorción en partes concretas del cuerpo, así como encima y debajo de la superficie del delantal9,13. El producto dosis-área o el kerma aéreo son medidas de la exposición a la radiación que tienen una trascendencia clínica mucho mayor12,13,30. Es de destacar que el peso del paciente es también una variable crucial relacionada con la exposición del operador. Lamentablemente, la mayor parte de estos parámetros no se incluyeron en los estudios mencionados. En nuestro estudio, no se observaron diferencias en la masa corporal entre los grupos de ARI y ARD ni en los pacientes con AE o con SCA (tabla 1). Sin embargo, se observó una mayor dosis de radiación en la ICP por ARI, con independencia de la presentación clínica.
En la práctica clínica diaria, la mayoría de los cardiólogos intervencionistas se decantan tradicionalmente por el ARD, principalmente porque el lado derecho del paciente proporciona unas condiciones más apropiadas para la labor del operador y porque los dispositivos de compresión radial están diseñados principalmente para la muñeca derecha7,9,13,30. El impedimento más importante para la adopción generalizada del ARI está en relación con la postura incómoda que es necesaria para abordar el antebrazo izquierdo. Los operadores de baja estatura encuentran especialmente molesto tener que inclinarse sobre los pacientes, en especial si se trata de pacientes obesos. Además, los cardiólogos intervencionistas que realizan las ICP a través del ARI están expuestos a unas dosis de radiación superiores como resultado de esta posición. Este factor podría explicar en parte una mayor dosis de radiación en las ICP por ARI. Los 2 abordajes radiales tienen interés clínico, pero el lado de la punción de la arteria radial podría tener consecuencias importantes en la práctica clínica ordinaria. La ventaja anatómica del ARI podría conducir a una alternativa atractiva para los cardiólogos intervencionistas en formación. Sin embargo, esta vía de acceso podría asociarse también con un aumento del riesgo de complicaciones. Deberán realizarse nuevos estudios con seguimiento a largo plazo para facilitar la identificación del abordaje óptimo para el acceso radial.
LimitacionesLos resultados de este estudio deben interpretarse teniendo en cuenta que tiene varias limitaciones. La más importante es su diseño no aleatorizado, con todos los sesgos intrínsecos que ello implica. No puede descartarse la posibilidad de que haya factores de confusión no medidos que influyan en los resultados. Sin embargo, se utilizó una técnica de emparejamiento por puntuación de propensión para superar esa limitación. No se analizaron las distribuciones detalladas ni los niveles de experiencia en ambos accesos radiales por centros ni en cada cardiólogo intervencionista. En consecuencia, podría haber factores relacionados con el centro o con el operador que hubieran influido en los resultados. No obstante, se presentan los datos correspondientes a la experiencia total con la ICP por vía radial y de centros de gran volumen (≥ 400 ICP al año). Es de destacar que la decisión respecto a la vía de acceso vascular para la intervención y el tratamiento la tomó cada operador según su criterio. Además, no se dispuso de algunos datos clínicos. No registramos los datos relativos a la prevalencia de la tortuosidad de la arteria subclavia ni los de las variaciones anatómicas en los lados derecho o izquierdo. Tampoco se registró el tamaño de las vainas vasculares empleadas durante la ICP ni el uso de dispositivos de cierre, y no se dispuso tampoco de la duración de la intervención ni de datos posteriores al alta hospitalaria. La evaluación de los objetivos a largo plazo podría ser crucial para llevar a cabo una valoración integral de la posible superioridad del ARI o el ARD. Dado que hubo deficiencias en algunos datos clínicos, el emparejamiento por puntuación de propensión podría no haber sido suficiente para descartar la repercusión de factores hipotéticos no medidos. Por tanto, los resultados deben considerarse exploratorios y generadores de hipótesis. A pesar de todas estas limitaciones, los datos presentados reflejan la experiencia de un estudio realizado con un diseño de inclusión de todos los pacientes, sin seleccionar (all-comers). Por consiguiente, los resultados pueden extrapolarse a la población general.
CONCLUSIONESAmbas vías de acceso radiales parecen ser igual de seguras y eficaces en el contexto del tratamiento de la AE. Los pacientes tratados a través de un ARI muestran unas dosis de radiación y una cantidad total de contraste utilizado superiores, con independencia de la forma de presentación clínica. Un aumento de la incidencia de complicaciones periintervención durante la ICP por ARI podría explicarse por la experiencia existente con esta vía de acceso vascular, generalmente inferior.
CONFLICTO DE INTERESESTodos los autores declaran no tener ningún conflicto de intereses.
- –
Aunque el acceso radial para la ICP se ha asociado con una menor mortalidad y una menor frecuencia de complicaciones hemorrágicas en comparación con el acceso femoral, continúa sin estar claro qué arteria es una opción más favorable para el acceso radial.
- –
Son escasos los datos de comparación de los resultados clínicos obtenidos con el ARI y el ARD para la ICP en poblaciones no seleccionadas (all-comers) y realizada por cardiólogos intervencionistas con diferentes niveles de experiencia, y los estudios previos en los que se ha comparado el ARI con el ARD han producido resultados contradictorios.
- –
Sin embargo, cada vez hay más evidencias clínicas de una ventaja del ARI frente al ARD por lo que respecta a la duración de la intervención, la dosis de radiación y la tasa de complicaciones cerebrovasculares.
- –
El presente estudio es el registro multicéntrico más amplio publicado en el que se ha comparado el ARI con el ARD en pacientes con AE y con SCA en la cardiología clínica contemporánea.
- –
El ARI y el ARD son igual de seguros y eficaces en el contexto del tratamiento de la AE pero, a diferencia de lo indicado por la mayoría de los datos recientes, se observó una dosis de radiación superior y un aumento de la incidencia de complicaciones periintervención en las ICP por ARI, con independencia de la forma de presentación clínica.
- –
Además, se utilizó una mayor cantidad de contraste en el conjunto de todas las intervenciones con ARI y en los pacientes con SCA, si bien no hubo diferencias de mortalidad entre las 2 vías de acceso.
- –
Nuestros resultados podrían explicarse por la experiencia con el ARI en situaciones de urgencia, generalmente inferior.