Palabras clave
INTRODUCCIÓN
La fibrosa mitroaórtica es una fina capa de tejido fibroso que separa la porción posterior de la raíz aórtica de la base del velo anterior mitral. Su límite posterior y lateral es la aurícula izquierda, el inferior lo forma el tracto de salida del ventrículo izquierdo y su techo el pericardio1-4. El seudoaneurisma de la fibrosa mitroaórtica (PFMA) o fibrosa intervalvular es una entidad poco frecuente, consistente en una cavidad pulsátil en la unión mitroaórtica, comunicada con el tracto de salida del ventrículo izquierdo. La etiología más frecuente es la endocarditis de la válvula aórtica, sobre todo protésica1-2. Presentamos un caso de PFMA asintomático, desarrollado tardíamente tras una cirugía de reemplazo valvular aórtico y que fue tratado mediante cierre percutáneo.
CASO CLÍNICO
Mujer de 69 años, con hipertensión arterial como único antecedente de interés. Tras presentar un síncope de esfuerzo fue diagnosticada de estenosis aórtica severa degenerativa, con un gradiente pico de 130 mmHg y medio de 81 mmHg. La función ventricular y la válvula mitral eran normales y la coronariografía mostró un árbol coronario normal. Fue intervenida quirúrgicamente con implantación de bioprótesis aórtica «sin soporte» Toronto 23 y el postoperatorio cursó sin complicaciones. Los ecocardiogramas de seguimiento no revelaron ninguna alteración relevante.
Siete años después de la intervención permanecía asintomática; en un ecocardiograma transtorácico (ETT) la bioprótesis aórtica continuaba normofuncionante y se observó un espacio anecoico pulsátil en el plano valvular aórtico, que protruía hacia la aurícula izquierda. Un ecocardiograma transesofágico (ETE) mostró una cavidad pulsátil de 30 x 25 mm en la unión mitroaórtica, con expansión sistólica hacia la aurícula izquierda y colapso diastólico (fig. 1), que comunicaba con el tracto de salida del ventrículo izquierdo (TSVI) a través de un «cuello» de 1 cm. Se realizó una resonancia magnética cardíaca (fig. 2) que confirmó estos hallazgos, estableciéndose el diagnóstico de seudoaneurisma de la fibrosa mitroaórtica. Para prevenir la aparición de complicaciones, y teniendo en cuenta el riesgo de la intervención quirúrgica, se optó por tratamiento percutáneo. El procedimiento se llevó a cabo bajo control de ETE y angiografía (fig. 3), esta última mediante un catéter Pigtail de 6 Fr colocado en TSVI por vía femoral derecha. A través de la arteria braquial izquierda se avanzó una guía Radiofocus de 260 cm (Terumo Corporation, Japón) hasta el interior del PFMA, y con ayuda de un catéter Multipropósito se intercambió por una guía Amplatzer. A través de esta guía, se colocó un dispositivo Amplatzer Muscular VSD Occluder (AGA Medical, Estados Unidos) de 12 mm en el cuello del seudoaneurisma (se eligió un dispositivo cuyo diámetro de cintura fuese ligeramente superior al del cuello). Su posición se comprobó mediante ventriculografía en dos proyecciones (OAD 30° y OAI 45°) y ETE, constatando que no interfería con la función de la bioprótesis aórtica ni la válvula mitral. Tras su liberación, el ETE y la angiografía mostraron ausencia de flujo hacia la cavidad. Un ETE realizado 6 meses después confirmó estos datos y la paciente continúa asintomática tras un año de seguimiento.
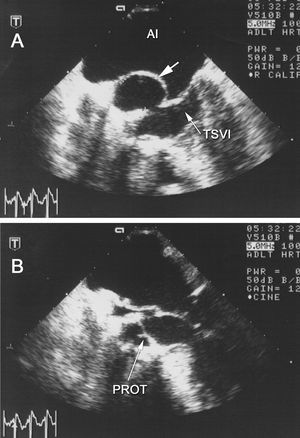
Fig. 1. Ecocardiograma transesofágico; plano transversal en el tracto de salida del ventrículo izquierdo (TSVI). A: imagen en sístole en la que se observa el seudoaneurisma (flecha) protruyendo hacia la aurícula izquierda. Se aprecia el orificio a través del que comunica con el TSVI. B: imagen en diástole que muestra el colapso del seudoaneurisma. En ambas imágenes se aprecia la bioprótesis aórtica (PROT) normofuncionante. AI: aurícula izquierda.
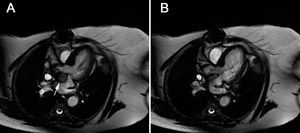
Fig. 2. Resonancia magnética. Corte transversal. Las imágenes en sístole (A) y diástole (B) permiten apreciar el movimiento pulsátil del seudoaneurisma, que se desplaza en sístole hacia la aurícula izquierda (flecha).
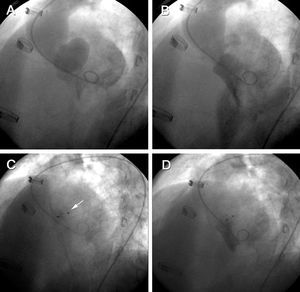
Fig. 3. Ventriculografía izquierda en proyección oblicua anterior izquierda. En la parte superior se observa la expansión del seudoaneurisma en sístole (A) y su colapso en diástole (B). En la parte inferior se puede apreciar el dispositivo Amplatzer (flecha) una vez liberado (C) y la ventriculografía final en la que no se observa paso de contraste hacia la cavidad (D).
DISCUSIÓN
El PFMA suele diagnosticarse en pacientes con antecedentes de reemplazo valvular aórtico por una endocarditis, con más frecuencia protésica, probablemente por la formación de un absceso del anillo que fistuliza hacia el tracto de salida1-4. También se han descrito casos, como el que describimos, tras cirugía valvular aórtica sin datos de endocarditis5. La dehiscencia parcial de una prótesis aórtica puede contribuir a la formación del PFMA3. En ocasiones, como en nuestro caso, se diagnostica de forma tardía, incluso años después de la intervención quirúrgica4-6. Se han descrito casos anecdóticos secundarios a traumatismos torácicos7.
El espectro clínico es variable, desde casos asintomáticos hasta el taponamiento cardíaco por apertura del PFMA hacia la cavidad pericárdica8. Su crecimiento progresivo puede producir angina por compresión de las arterias coronarias6,9,10 e incluso puede llegar a fistulizar hacia la pared anterior del tórax4. Otra manifestación puede ser la insuficiencia cardíaca, al comunicar con la aorta ascendente o la aurícula izquierda, produciendo un cuadro similar al de la insuficiencia aórtica o mitral, respectivamente. Se ha descrito la insuficiencia mitral severa por desplazamiento del velo anterior mitral11. Otra manifestación puede ser el ictus, como consecuencia de la embolización de material trombótico desde el propio PFMA12.
En cuanto al tratamiento del PFMA, se recomienda la cirugía, incluso en los pacientes asintomáticos2, con el objetivo de evitar la aparición de complicaciones. Puede realizarse resección y reparación del defecto4,10, con o sin recambio valvular aórtico5,6,10, o sustitución de la raíz aórtica por un homoinjerto2. Cuando hay afección coronaria puede ser necesario un bypass6,9. Se trata de una cirugía con una morbimortalidad no desdeñable por su complejidad técnica y el antecedente de cirugía previa.
El caso que presentamos es, según nuestra información bibliográfica, la primera descripción de tratamiento percutáneo del PFMA. Al aislar la cavidad respecto del TSVI, creemos que se evita su expansión y, por tanto, sus potenciales complicaciones. Concluimos que es una técnica factible y puede realizarse de forma segura, aporta buenos resultados a medio plazo y puede constituirse en una alternativa al tratamiento quirúrgico.
Correspondencia: Dr. S. Jiménez Valero.
Unidad de Hemodinámica. Hospital de Madrid Montepríncipe.
Avda. Montepríncipe, 25. 28660 Boadilla del Monte. Madrid. España.
Correo electrónico: sjvcardio@yahoo.es