Se consolida la angioplastia con balón de arterias pulmonares (ABAP) en la hipertensión pulmonar tromboembólica crónica (HPTEC) no operable. El procedimiento se ha perfeccionado y han disminuido las complicaciones. Se analizan como objetivo primario los resultados y las complicaciones del primer programa nacional de ABAP.
MétodosEstudio prospectivo, unicéntrico y observacional que incluyó a todos los pacientes con HPTEC no quirúrgica tratados mediante ABAP desde mayo de 2013 hasta febrero de 2017. Se analizaron la mejoría clínica y hemodinámica, el edema de reperfusión y la mortalidad.
ResultadosSe realizaron 156 sesiones de ABAP en 46 pacientes. Se redujeron las resistencias vasculares pulmonares un 44% (10,1 ± 4,9 frente a 5,6 ± 2,2 UW; p < 0,001) y la presión arterial pulmonar media un 23,6% (49,5 ± 12 frente a 37,8 ± 9 mmHg; p < 0,001); el índice cardiaco aumentó un 17,1% (2,3 frente a 2,7 l/min/m2; p = 0,002); las cifras de la fracción aminoterminal del propéptido natriurético cerebral se redujeron el 79,2% (1.233 ± 1.327 frente a 255,5 ± 318 pg/dl; p < 0,001), y la distancia recorrida en la prueba de 6 min de marcha aumentó 74 m (394 frente a 468 m; p = 0,001). Apareció edema de reperfusión en 9 procedimientos (5,8%), y falleció 1 paciente (mortalidad, 2,1%).
ConclusionesEl perfeccionamiento actual de la ABAP en pacientes con HPTEC no operable la convierte en una técnica eficaz y segura que mejora el perfil hemodinámico, la clase funcional y los biomarcadores, con baja incidencia de complicaciones graves y mortalidad periprocedimento.
Palabras clave
La hipertensión pulmonar tromboembólica crónica (HPTEC) produce elevación de las resistencias vasculares pulmonares (RVP) debido a tromboembolias pulmonares de repetición con resolución incompleta que se adhieren a la media de las arterias pulmonares y reemplazan la íntima normal, con lo que se produce obstrucción intravascular. El tratamiento de elección y único potencialmente curativo es la cirugía de tromboendarterectomía pulmonar (TEA)1. La supervivencia a 5 años de los pacientes operados en España es del 86 frente al 65% de los que reciben tratamiento médico2. Aunque los pacientes inoperables reciben medicaciones para la hipertensión arterial pulmonar3, la situación funcional y hemodinámica conseguida no es satisfactoria. La angioplastia con balón de las arterias pulmonares (ABAP) se postula como una alternativa terapéutica prometedora para estos pacientes, pues en las series publicadas se ha conseguido una mejora funcional, hemodinámica y de biomarcadores en pacientes en tratamiento específico para la hipertensión arterial pulmonar4–11.
La complicación más frecuente y principal causa de mortalidad de la ABAP es el edema de reperfusión pulmonar (ERP), que consiste en la aparición de infiltrados pulmonares y caída de la saturación tras la ABAP. En la primera serie de ABAP el ERP apareció en un 61% de los pacientes, 3 precisaron ventilación mecánica y la mortalidad fue del 5,5%, por lo que esta técnica no se aplicó a los pacientes a partir de dicha publicación8. La técnica se ha perfeccionado y han disminuido las complicaciones, con tasas de ERP actuales de un 0,8-53% (según la definición y técnica diagnóstica empleadas), y es grave solo en un 0-10% de los procedimientos4–7,9,10.
Se presenta la primera experiencia consolidada con esta técnica en un centro de referencia para la hipertensión pulmonar en España. El objetivo primario es determinar los resultados clínicos y hemodinámicos de la ABAP en pacientes con HPTEC no operable. El objetivo secundario es determinar qué variables se correlacionan con la aparición de ERP en esta serie, que incorpora las medidas recomendadas para minimizar esta complicación.
MÉTODOSPacientes del estudioEn mayo de 2013 se inició el programa de ABAP. Se consideró candidatos a los pacientes no quirúrgicos en seguimiento en la unidad y a los pacientes remitidos para nueva evaluación a partir de mayo de 2013. La decisión terapéutica se estableció en sesión multidisciplinaria de HPTEC; se valoró como primera opción la TEA. Para los pacientes cuyas comorbilidades, daño distal o negativa a operarse motivaron que se desestimara la TEA, se consideró ABAP si presentaban lesiones susceptibles de tratamiento percutáneo. Los criterios de inclusión en el programa de ABAP fueron: a) pacientes en clase funcional III o IV en tratamiento médico optimizado, y b) pacientes en clase funcional II en tratamiento médico con criterios pronósticos de riesgo intermedio o alto según la guía europea de hipertensión pulmonar3. Los pacientes que no cumplían 1 de estos 2 criterios continuaron con tratamiento médico. Los criterios de exclusión fueron: a) ausencia de lesiones subsidiarias de ABAP; b) pacientes asintomáticos o en clase funcional II sin criterios pronósticos de riesgo intermedio o alto, y c) negativa a firmar el consentimiento informado. El comité ético aprobó el protocolo. Todos los pacientes firmaron el consentimiento informado antes de cada procedimiento.
Tratamiento médico previo a la angioplastia con balón de las arterias pulmonaresTodos los pacientes estaban anticoagulados, recibían oxigenoterapia o diuréticos según necesidades y medicación específica para la hipertensión arterial pulmonar: antagonistas de la endotelina, inhibidores de la fosfodiesterasa 5, prostanoides y riociguat. Los pacientes con criterios pronósticos de alto riesgo (signos o síntomas de insuficiencia cardiaca derecha, síncope, clase IV de la Organización Mundial de la Salud [OMS], índice cardiaco < 2 l/min/m2 o fracción aminoterminal del propéptido natriurético cerebral > 1.400 pg/dl)3 iniciaron epoprostenol por vía intravenosa 48 h antes del primer procedimiento de ABAP, lo mantuvieron durante los primeros 2 procedimientos ingresados y lo suspendieron antes del alta si los criterios pronósticos habían mejorado a riesgo intermedio o bajo4,6.
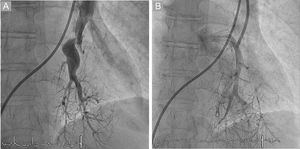
Procedimiento de angioplastia con balón de las arterias pulmonaresSe trataron membranas, bandas, estenosis anulares y terminaciones saculares con paso distal de contraste en fase tardía4,6,7,10. Todos los procedimientos los realizaron 2 hemodinamistas sénior con experiencia en el tratamiento de pacientes con hipertensión pulmonar y con conocimiento del árbol vascular pulmonar; el paciente estaba despierto y sin sedación. Los procedimientos se realizaron según técnica estándar refinada4,7,10,11, limitados a 2-3 ramas segmentarias de un único lóbulo por procedimiento mientras la presión arterial pulmonar media (PAPm) fuera > 35 mmHg4,5,8,11. La terapia incluye el tratamiento de todas las lesiones tratables en todos los lóbulos hasta normalizar los parámetros hemodinámicos y la clase funcional, por lo que consta de varias sesiones, y se suma el beneficio obtenido con los procedimientos sucesivos. Habitualmente se trata solo un lóbulo por sesión para evitar la aparición de ERP, y son necesarios 5 o 6 procedimientos por paciente. La terapia se inicia por uno de los 2 lóbulos inferiores (generalmente el que más daño presente), dado que son los lóbulos con más cantidad de tejido pulmonar. El catéter guía más comúnmente utilizado es el multiusos, seguido del JR 4. Se utilizan guías de angioplastia coronaria de 0,014 pulgadas, poliméricas, con bajo peso en la punta, tipo Pilot 50 o whisper, con las que resulta más fácil cruzar el entramado de membranas. La dilatación se inicia con balones pequeños, seguidos de balones crecientes hasta un tamaño máximo ≤ 80% del tamaño del vaso, para evitar lesiones en la pared del vaso y su potencial rotura. El tamaño de los vasos se estimó visualmente mediante angiografía. La dilatación se consideró eficaz cuando se obtenía mejoría en el flujo distal, aumentaba la captación de contraste del tejido pulmonar distal a la zona tratada y mejoraba el retorno por las venas pulmonares a la aurícula izquierda4,7 (figura 1). La guía de presión se utilizó a partir de septiembre de 2015 en 82 de los 156 procedimientos, con el objetivo de mantener < 35 mmHg la PAPm distal a las zonas tratadas, para evitar la aparición de ERP. Los motivos para finalizar los procedimientos fueron caída de la saturación arterial periférica de oxígeno > 4%, hemoesputo, haber tratado el número límite de ramas segmentarias o riesgo de nefrotoxicidad por contraste4. Los procedimientos se repitieron cada 6-12 semanas hasta tratar todas las lesiones subsidiarias4–7 mientras la PAPm previa a la ABAP fuera > 25 mmHg y las RVP, > 3 UW. Los criterios de interrupción del programa de ABAP fueron: a) ausencia de mejoría de al menos 1 grado en la clase funcional de la OMS o reducción de las RVP > 20% tras 3 procedimientos de ABAP, y b) pacientes frágiles o de edad avanzada incapaces de tolerar los procedimientos por duración e inmovilización prolongada. El criterio de interrupción de la terapia fue propio, basado en la experiencia, tras la observación de que con 3 procedimientos los pacientes experimentaban una mejora clínica y hemodinámica relevante, con una reducción media de las RVP ≥ 35%.
Tratamiento tras el procedimiento de angioplastia de las arterias pulmonaresSe vigiló la aparición de ERP o hemorragia pulmonar a las 48h tras el procedimiento. Se definió como ERP clínico una caída persistente de la saturación arterial periférica de oxígeno tras la ABAP e infiltrados pulmonares en la radiografía de tórax en los lóbulos tratados4. Cuando apareció ERP, se trató según un protocolo previamente establecido7,12. En todos los pacientes con ERP se forzó el balance negativo con diuréticos y se incrementó el aporte de oxígeno. A los pacientes con ERP grave, si con estas medidas no se conseguía oxigenación adecuada, se les implantó un oxigenador extracorpóreo de membrana. Si persistía la mala oxigenación, se agregaba ventilación mecánica7,10,12. Los parámetros hemodinámicos se determinaron antes de cada procedimiento de ABAP y a los 6 meses de finalizar la terapia. Los parámetros bioquímicos, la prueba de 6 min de marcha y la valoración de la clase funcional se determinaron después de la tercera sesión de ABAP, al finalizar la terapia y a los 6 meses. Una vez finalizada la terapia, se redujo progresivamente la medicación específica para la hipertensión arterial pulmonar de los pacientes con criterios pronósticos de bajo riesgo (OMS I-II, ausencia de signos y síntomas de insuficiencia cardiaca derecha, índice cardiaco ≥ 2,5 l/min/m2 y fracción aminoterminal del propéptido natriurético cerebral < 300 pg/dl)3, PAPm < 30 mmHg y RVP < 4 UW.
Análisis de eficacia de resultados terapéuticosSe analizaron los resultados de eficacia de la técnica en toda la población en su conjunto y de manera independiente en los pacientes con al menos 3 procedimientos, y se demostraron un beneficio hemodinámico acumulado de la suma de procedimientos y mejoría funcional y de biomarcadores tras el tercer procedimiento de ABAP.
Análisis estadísticoTodos los análisis se realizaron con el programa estadístico STATA 12.1. Las variables categóricas se presentan como frecuencia absoluta y proporciones; las continuas, como media ± desviación estándar. Se empleó el test de Kolmogorov-Smirnov para estudiar la adecuación de las variables a la distribución normal. Para el estudio comparativo de las variables continuas, se utilizó el test de la t de Student; si no seguían una distribución normal, se empleó la prueba de los rangos con signo de Wilcoxon. Los porcentajes se compararon mediante la prueba de la χ2, la prueba exacta de Fisher o el test de Wilcoxon según correspondiera. Se realizó un análisis multivariable (regresión logística) para identificar las variables asociadas con ERP. Los criterios de inclusión fueron relevancia clínica y plausibilidad biológica. Se utilizaron los criterios de Mickey para excluir las variables con p > 0,20 en el análisis univariable. Se consideró estadísticamente significativo un valor de p < 0,05.
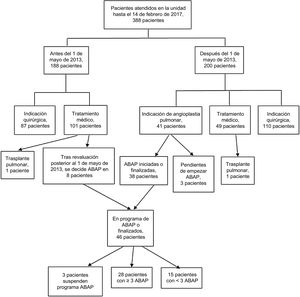
RESULTADOSHasta febrero de 2017 se realizaron 156 sesiones de ABAP en 46 pacientes con HPTEC; se habían realizado al menos 3 procedimientos en 28 de los 46 pacientes. El diagrama de flujo de los pacientes se describe en la figura 2. Desde que se dispone de la terapia de ABAP, los pacientes nuevos a los que se ha indicado cada alternativa terapéutica han sido: TEA a un 55%, ABAP al 20,5% y tratamiento médico al 24,5%. De los 46 pacientes, 16 habían finalizado la terapia de ABAP, con una media de 4,8 (3-9) sesiones/paciente.
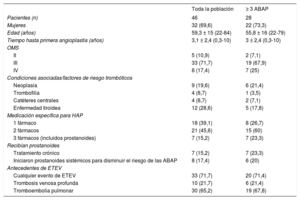
En la tabla 1 se describen las características basales de los 46 pacientes y de los 28 con al menos 3 procedimientos. Para todos los pacientes excepto 3 se desestimó la TEA por localización distal de las lesiones. Estos 3 pacientes presentaban daño al inicio de ramas segmentarias: 1 tenía siringomielia con restricción ventilatoria grave y los otros 2, preferencias personales. En 3 de los 46 pacientes se interrumpió la terapia, 2 por ausencia de mejoría (79 y 78 años) y 1 (82 años) por mala tolerancia a la larga duración de los procedimientos y el confinamiento a silla de ruedas por artrosis grave.
Características basales de la población
| Toda la población | ≥ 3 ABAP | |
|---|---|---|
| Pacientes (n) | 46 | 28 |
| Mujeres | 32 (69,6) | 22 (73,3) |
| Edad (años) | 59,3 ± 15 (22-84) | 55,8 ± 16 (22-79) |
| Tiempo hasta primera angioplastia (años) | 3,1 ± 2,4 (0,3-10) | 3 ± 2,4 (0,3-10) |
| OMS | ||
| II | 5 (10,9) | 2 (7,1) |
| III | 33 (71,7) | 19 (67,9) |
| IV | 8 (17,4) | 7 (25) |
| Condiciones asociadas/factores de riesgo trombóticos | ||
| Neoplasia | 9 (19,6) | 6 (21,4) |
| Trombofilia | 4 (8,7) | 1 (3,5) |
| Catéteres centrales | 4 (8,7) | 2 (7,1) |
| Enfermedad tiroidea | 12 (28,6) | 5 (17,8) |
| Medicación específica para HAP | ||
| 1 fármaco | 18 (39,1) | 8 (26,7) |
| 2 fármacos | 21 (45,6) | 15 (60) |
| 3 fármacos (incluidos prostanoides) | 7 (15,2) | 7 (23,3) |
| Recibían prostanoides | ||
| Tratamiento crónico | 7 (15,2) | 7 (23,3) |
| Iniciaron prostanoides sistémicos para disminuir el riesgo de las ABAP | 8 (17,4) | 6 (20) |
| Antecedentes de ETEV | ||
| Cualquier evento de ETEV | 33 (71,7) | 20 (71,4) |
| Trombosis venosa profunda | 10 (21,7) | 6 (21,4) |
| Tromboembolia pulmonar | 30 (65,2) | 19 (67,8) |
ABAP: angioplastia con balón de arterias pulmonares; ETEV: enfermedad tromboembólica venosa; HAP: hipertensión arterial pulmonar; NYHA: New York Heart Association.
Los valores expresan n (%) o media ± desviación estándar (intervalo).
En la tabla 2 se detalla la información relativa a los procedimientos de ABAP.
Características de los 156 procedimientos de angioplastia con balón de las arterias pulmonares
| N.o de lóbulos tratados por sesión | 1,17 ± 0,3 (1-2) |
| N.o de ramas segmentarias tratadas por sesión | 2,26 ± 0,8 (1-5) |
| N.o de ramas subsegmentarias tratadas por sesión | 3,29 ± 1,6 (1-12) |
| Cantidad de contraste utilizado por sesión (ml) | 308 ± 80 (70-490) |
| N.o de balones utilizados por sesión | 2,43 (1-5) |
| Tamaño de los balones utilizados (mm) | 3,3 (1,2-6) |
| Duración media de los procedimientos (min) | 123 ± 25 (55-205) |
| Tiempo medio de fluoroscopia (min) | 36 ± 11 (4-61) |
| Mediana de exposición a radiación de los pacientes (mGy/cm2) | 86,25 (62,3-129,7) |
Los valores expresan media (intervalo) o media ± desviación estándar (intervalo).
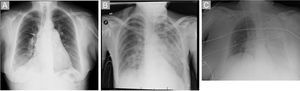
Las complicaciones se muestran en la tabla 3. La mortalidad se detalla por pacientes y el resto de las complicaciones, por procedimiento. El hemoesputo/hemoptisis intraprocedimiento fue la complicación más frecuente. Ninguno evolucionó a ERP, todos se resolvieron revirtiendo la anticoagulación e interrumpiendo el procedimiento. La segunda fue el ERP, 6 aparecieron tras la primera sesión de ABAP y 3 después de la segunda. Siete fueron subclínicos, de grado 2-3 (figura 3A), 1 de grado 4 (figura 3B) y 1 de grado 5 (figura 3C); este necesitó ventilación mecánica y oxigenador extracorpóreo de membrana venoarterial. Falleció a los 8 días por hemorragia cerebral (mortalidad del 2,1% en esta serie). Esta paciente presentaba grave deterioro hemodinámico, clase funcional IV pese a triple terapia específica y la PAPm previa a la ABAP era de 69 mmHg. El ERP ocurrió después del primer procedimiento de ABAP. Un paciente precisó implante de stent recubierto de pericardio tras una perforación por la guía.
Complicaciones de los procedimientos de angioplastia con balón de las arterias pulmonares
| Ausencia de complicaciones | 112 (71,8%) |
| Esputo hemoptoico | 20 (12,8%) |
| Edema de reperfusión | 9 (5,8%) |
| De grado grave | 1 (0,6%) |
| Fallecimiento | 1 (2,1%) |
| Disección por catéter sin pérdida de flujo | 10 (6,4%) |
| Perforación que requiere intervencionismo | 1 (0,6%) |
| Extravasación que no requiere intervencionismo | 2 (1,3%) |
| Disección por guía o balón | 1 (0,6%) |
| Hematoma femoral que requiere transfusión | 1 (0,6%) |
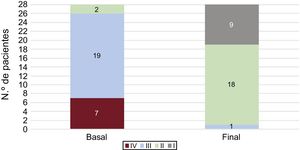
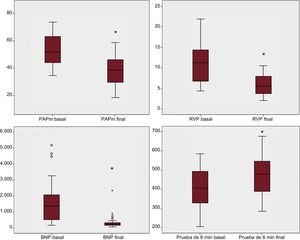
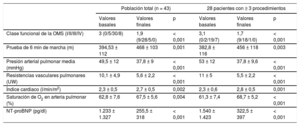
Se muestran los resultados de los 43 pacientes en programa de ABAP con un seguimiento medio de 15,3 ± 9 (1-46) meses y de los 28 pacientes con al menos 3 procedimientos de ABAP (el 61% del total), con un seguimiento medio de 19 ± 9 (5-46) meses. En los 43 pacientes se consiguió una mejoría funcional significativa (prueba de 6 min de marcha y clase funcional de la OMS) en parámetros hemodinámicos y biomarcadores, mejoría que fue más marcada en el grupo de 28 pacientes con al menos 3 procedimientos (tabla 4, figura 4 y figura 5). Los cambios fundamentales en la población total fueron: incremento de 74 m en la distancia recorrida en la prueba de 6 min de marcha, reducción de las RVP del 44% y reducción del 79% de la fracción aminoterminal del propéptido natriurético cerebral. En el grupo de 28 pacientes con al menos 3 procedimientos, la reducción de las RVP fue del 50%. En la tabla 5 se muestra la mejora hemodinámica progresiva con la suma de procedimientos. Una paciente con terapia finalizada persistía con criterios pronósticos de alto riesgo, y actualmente está incluida en lista de espera de trasplante pulmonar.
Modificación de parámetros hemodinámicos, funcionales y de biomarcadores en el seguimiento de la población total y los 28 pacientes con al menos 3 procedimientos
| Población total (n = 43) | 28 pacientes con ≥ 3 procedimientos | |||||
|---|---|---|---|---|---|---|
| Valores basales | Valores finales | p | Valores basales | Valores finales | p | |
| Clase funcional de la OMS (I/II/III/IV) | 3 (0/5/30/8) | 1,9 (9/28/5/0) | < 0,001 | 3,1 (0/2/19/7) | 1,7 (9/18/1/0) | < 0,001 |
| Prueba de 6 min de marcha (m) | 394,53 ± 112 | 468 ± 103 | 0,001 | 382,8 ± 116 | 456 ± 118 | 0,003 |
| Presión arterial pulmonar media (mmHg) | 49,5 ± 12 | 37,8 ± 9 | < 0,001 | 53 ± 12 | 37,8 ± 9,6 | < 0,001 |
| Resistencias vasculares pulmonares (UW) | 10,1 ± 4,9 | 5,6 ± 2,2 | < 0,001 | 11 ± 5 | 5,5 ± 2,2 | < 0,001 |
| Índice cardiaco (l/min/m2) | 2,3 ± 0,5 | 2,7 ± 0,5 | 0,002 | 2,3 ± 0,6 | 2,8 ± 0,5 | 0,001 |
| Saturación de O2 en arteria pulmonar (%) | 62,8 ± 7,6 | 67,5 ± 5,6 | 0,004 | 61,3 ± 7,4 | 68,7 ± 5,2 | < 0,001 |
| NT-proBNP (pg/dl) | 1.233 ± 1.327 | 255,5 ± 318 | < 0,001 | 1.540 ± 1.423 | 322,5 ± 397 | < 0,001 |
NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; OMS: Organización Mundial de la Salud.
Cambios hemodinámicos, de biomarcadores y funcionales en pacientes con al menos 3 procedimientos, mostrados como distribución boxplot. BNP: fracción aminoterminal del propéptido natriurético cerebral; PAPm: presión arterial pulmonar media; RVP: resistencia vascular pulmonar. *Estadísticamente significativo.
Mejora progresiva de parámetros hemodinámicos tras la suma de procedimientos
| Variable | Valores | n | p | |
|---|---|---|---|---|
| Hemodinámica basal frente a hemodinámica antes del segundo procedimiento | PAPm basal (mmHg) | 49,9 ± 12,4 | 36 | < 0,001 |
| PAPm antes del segundo procedimiento (mmHg) | 42,15 ± 9 | 36 | ||
| RVP basal (UW) | 9,5 ± 4,8 | 36 | < 0,001 | |
| RVP antes del segundo procedimiento (UW) | 6,5 ± 2,7 | 36 | ||
| IC basal (l/min/m2) | 2,5 ± 0,8 | 36 | 0,1 | |
| IC antes del segundo procedimiento (l/min/m2) | 2,7 ± 0,6 | 36 | ||
| Hemodinámica basal frente a hemodinámica antes del tercer procedimiento | PAPm basal (mmHg) | 49,9 ± 12 | 37 | < 0,001 |
| PAPm antes del tercer procedimiento (mmHg) | 40,4 ± 10,7 | 37 | ||
| RVP basal (UW) | 10,3 ± 5,1 | 36 | < 0,001 | |
| RVP antes del tercer procedimiento (UW) | 6,5 ± 2,8 | 36 | ||
| IC basal (l/min/m2) | 2,4 ± 0,8 | 36 | 0,1 | |
| IC antes del tercer procedimiento (l/min/m2) | 2,6 ± 0,5 | 36 | ||
| Hemodinámica basal frente a hemodinámica antes del cuarto procedimiento | PAPm basal (mmHg) | 52 ± 11,9 | 31 | < 0,001 |
| PAP antes del cuarto procedimiento (mmHg) | 40,3 ± 12,2 | 31 | ||
| RVP basal (UW) | 11,1 ± 5,2 | 30 | < 0,001 | |
| RVP antes del cuarto procedimiento (UW) | 6,5 ± 3,4 | 30 | ||
| IC basal (l/min/m2) | 2,3 ± 0,6 | 30 | 0,002 | |
| IC antes del cuarto procedimiento (l/min/m2) | 2,6 ± 0,5 | 30 | ||
| Hemodinámica basal frente a hemodinámica final, una vez finalizados todos los procedimientos (16 pacientes) | PAPm basal (mmHg) | 51,3 ± 13,8 | 16 | < 0,001 |
| PAPm final (mmHg) | 33,7 ± 10,2 | 16 | ||
| RVP basal (UW) | 10,1 ± 5,5 | 16 | < 0,001 | |
| RVP final (UW) | 4,6 ± 1,9 | 16 | ||
| IC basal (l/min/m2) | 2,5 ± 0,6 | 16 | 0,08 | |
| IC final (l/min/m2) | 2,8 ± 0,6 | 16 |
IC: índice cardiaco; PAPm: presión arterial pulmonar media; RVP: resistencia vascular pulmonar.
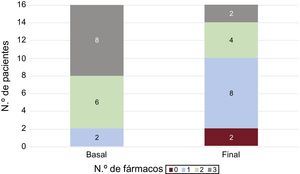
De los 43 pacientes, 16 habían completado la terapia en el momento de enviar este artículo. En 10 de los 16 se redujo la medicación específica para hipertensión pulmonar. A 1 paciente se le retiraron los 3 fármacos; a 2 se les suspendieron 2 fármacos y a 7, 1 fármaco (figura 6). Los pacientes con terapia de ABAP aún no finalizada mantienen la misma medicación.
Factores predictores de aparición de edema de reperfusiónSe eligieron 8 variables que a priori podrían estar implicadas en la aparición de ERP para analizar si había correlación: edad, sexo, PAPm y RVP basales, número de lóbulos y segmentarias tratadas en cada procedimiento, estar recibiendo prostanoides y tratarse del primer procedimiento. En el análisis multivariable, el primer procedimiento de ABAP se correlacionó con la aparición de ERP (odds ratio = 5,92; intervalo de confianza del 95%, 1,09-32,25; p = 0,04). La PAPm previa al procedimiento mostró tendencia a asociarse con ERP sin alcanzar significación estadística (odds ratio = 2,99; intervalo de confianza del 95%, 0,91-9,84; p = 0,072).
DISCUSIÓNEn la presente serie, la terapia de ABAP mejora la capacidad funcional (clase funcional y prueba de 6 min de marcha), el perfil hemodinámico y los biomarcadores en los pacientes con HPTEC inoperable. La tasa de complicaciones graves y la mortalidad son bajas. Además, la mejoría progresiva del perfil de riesgo de los pacientes permite reducir el tratamiento médico específico coadyuvante. Este trabajo aporta, además, información sobre el tratamiento actual de estos pacientes en un centro de referencia de HPTEC.
Población del estudioSe trata de una población gravemente enferma, con uno de los peores perfiles clínico y hemodinámico4,5,9,13. El tiempo de evolución de la enfermedad desde el diagnóstico hasta la primera angioplastia era largo en los intervalos publicados por las series japonesas4,6 y mayor que el de las series europeas9. Predomina el sexo femenino, como se describe en la bibliografía, y el intervalo de edades de los pacientes abarca edades más extremas e incluye a pacientes en la tercera década de la vida (9%) y un número importante de pacientes mayores de 70 años (24%)4,5,9.
Desde la publicación de los resultados de las series japonesas4,6,7 y la recomendación de clase IIb para la ABAP en la guía europea de 20153, numerosos centros en Japón y Europa han iniciado programas de ABAP9,10,12,14. Sin embargo, no hay información sobre cuál es el porcentaje de pacientes con HPTEC a los que se aplica esta terapia en la práctica clínica. Se desconoce tanto en las series japonesas, en las que el número de TEA realizadas es mucho menor que el de ABAP4,7,12, como en las europeas, en las que la ABAP se circunscribe a centros de referencia, con programas establecidos de TEA4,9 y números quirúrgicos superiores a los de la ABAP. Según el registro español de hipertensión pulmonar1, la tasa de TEA en España es del 31,2%, y alcanza el 48% en centros expertos en HPTEC. Desde que se inició la ABAP, se ha indicado esta terapia al 20,5% de los pacientes nuevos. Se puede afirmar así que, actualmente, en nuestro medio y en una unidad de referencia, la ABAP tiene un papel relevante como coadyuvante al tratamiento médico para el 20,5% de los pacientes con HPTEC y el 45,5% de los no candidatos a TEA.
Resultados de la angioplastia con balón de las arterias pulmonaresEl presente trabajo confirma que con la ABAP se obtiene un beneficio clínico, hemodinámico y en los biomarcadores significativo y de magnitud mayor que con el tratamiento médico4,11,15, beneficio que es aún más marcado tras 3 o más procedimientos de ABAP. Analizándose toda la población en su conjunto (al igual que las series publicadas)4–6,9, y de manera más marcada si se analiza a los pacientes con al menos 3 procedimientos, la mejoría hemodinámica y funcional en esta serie se aproxima a la de las series japonesas (reducción de RVP del 45-69%4,6,7 y aumento > 70 m en la distancia recorrida en 6 min)4,6 y supera los resultados de las series europeas (reducción de RVP 26-33% y aumento de solo 33 m en la distancia recorrida en 6 min)5,9. Se ha especulado con razones que expliquen las diferencias de mejora entre las series europeas y japonesas; entre ellas mayor experiencia en ABAP y tratamiento de pacientes con daño proximal en centros japoneses; pacientes que habrían sido operados en centros de referencia europeos y en los que la mejoría hemodinámica tras la ABAP sería mayor, al tratar enfermedad proximal9,13,16. Sin embargo, en la presente serie, los resultados obtenidos se sitúan en los valores de las series japonesas pese a tratarse a pacientes con daño distal en ramas segmentarias y subsegmentarias. Se piensa que la realización de los procedimientos según la técnica estandarizada perfeccionada que se describe en las series japonesas4, la concentración de procedimientos y experiencia en la técnica en un único centro17, ser centro de referencia nacional en hipertensión pulmonar con diagnóstico y tratamiento experto de estos pacientes, un conocimiento detallado del árbol pulmonar con 150 arteriografías pulmonares diagnósticas realizadas antes de iniciar el programa de ABAP, un mayor número de ramas segmentarias y subsegmentarias tratadas por procedimiento respecto a otras series europeas (en esta serie 2,26 ± 0,8 ramas segmentarias y 3,29 ± 1,6 ramas subsegmentarias por sesión frente a 2 vasos/procedimiento en la serie alemana)9 y utilizar balones de mayor tamaño (hasta 6 mm en esta serie frente a 4 mm en la serie alemana)9,16 podrían explicar los resultados obtenidos.
Otro de los beneficios de la terapia de ABAP es la reducción de necesidades de medicación específica4. En la presente serie se se ha reducido la medicación específica en el 62% de los pacientes finalizados, incluidos los prostanoides sistémicos. Esto conlleva importantes implicaciones económicas y mejora en la calidad de vida de los pacientes.
Complicaciones: edema de reperfusión y mortalidadHay que distinguir entre el ERP leve, asintomático o paucisintomático, que solo necesita diuréticos y suplementos de oxígeno, y el ERP grave, que requiere asistencia invasiva. El ERP leve tiene frecuencia moderada en todas las series, y la del ERP grave es mucho menor. En ambos casos, la presente serie se compara favorablemente con lo descrito en la literatura médica, con tasa general de ERP tras el procedimiento del 5,8% y tasa de ventilación mecánica del 2,1% de los pacientes (1 paciente con ERP grave). En series japonesas como la de Mizoguchi et al.4, se produjo ERP en un 60% de los procedimientos, y se precisó ventilación mecánica para el 5,8% de los pacientes, y en la serie de Inami et al.7 la tasa de ERP fue del 38%, con una tasa de ERP grave del 6,4%, y precisaron oxigenador extracorpóreo de membrana el 0,7% de los pacientes. En series europeas, la tasa de ERP tras el procedimiento oscila entre el 1,89 y el 9,5%5, y necesitaron ventilación mecánica 1 paciente (5%)5 y ninguno9. La realización de los procedimientos según una técnica refinada y tratar como máximo 3 ramas segmentarias de un único lóbulo mientras la PAPm fuera > 35 mmHg podrían explicar una tasa de ERP tan baja en la presente serie.
Del mismo modo, la tasa de mortalidad es muy baja, del 2,1%, menor que la de algunas series europeas5,18 (mortalidad del 10% en ambas), similar a la mortalidad del grupo alemán (1,8%) recientemente publicada9 y similar a la de series japonesas recientes, entre el 1,54,7 y el 3,4%6,13,14. En opinión de los autores, una tasa muy baja de ERP y de perforación que necesita de intervencionismo (principales causas de mortalidad), así como un conocimiento preciso del tratamiento adecuado de las complicaciones inherentes a esta técnica19, explicaría la baja mortalidad obtenida.
Variables que se correlacionan con aparición de edema de reperfusión pulmonarDado que el ERP es una de las 2 causas de mortalidad de este procedimiento, se considera importante predecir en quién va a aparecer. El primer procedimiento de ABAP se correlacionó con aparición de ERP, mientras que la PAPm previa al procedimiento mostró tendencia a asociarse con ERP. Según algunos autores, el ERP se inicia por exposición súbita a una presión de perfusión distal elevada, tras dilatar las estenosis que protegen los territorios distales4,7. Esto explicaría que el ERP sea más probable después del primer procedimiento (cuando mayor es la presión pulmonar) y en los procedimientos con PAPm más elevada, como ocurre en la presente serie. De modo similar, en la serie de Feinstein et al.8 el ERP se correlacionó con una PAPm > 35 mmHg, y en la serie de Inami et al.7, el ERP se correlacionó con las RVP, la PAPm y la puntuación PEPSI, que tiene en cuenta el número de ramas tratadas, el cambio en el grado de perfusión de las ramas tratadas y el valor de las RVP.
LimitacionesLos números de esta serie son bajos y el tiempo de seguimiento es corto, por lo que son necesarias series con mayor número de pacientes y tiempos de seguimiento más largos que confirmen que estos resultados se mantienen. Además, aún no se dispone de información respecto a los beneficios en supervivencia con esta técnica debido a la falta de seguimiento a largo plazo. Por último, son necesarios estudios multicéntricos aleatorizados que comparen los resultados de esta terapia con el tratamiento médico en pacientes inoperables.
CONCLUSIONESLa ABAP realizada en un centro experto continúa consolidándose como una herramienta terapéutica eficaz como coadyuvante al tratamiento médico en un porcentaje importante de pacientes con HPTEC no quirúrgica, ya que mejora la capacidad funcional, la hemodinámica y los biomarcadores y disminuye las necesidades de medicación específica para la hipertensión arterial pulmonar. El perfeccionamiento de la técnica ha aumentado mucho el perfil de seguridad de la ABAP, con tasas muy bajas de ERP y de mortalidad en centros expertos, lo que confiere a esta técnica una relación riesgo-beneficio muy favorable para el paciente. El ERP sigue siendo una de las causas de mortalidad de esta técnica. El primer procedimiento de ABAP y una PAPm elevada aumentan la probabilidad de que se produzca un ERP después del procedimiento.
FINANCIACIÓNEstudio financiado por el Instituto de Salud Carlos III, Ministerio de Economía y Competitividad de España, a través del Centro de Investigación Biomédica en Red de Enfermedades Cardiovasculares (CB16/11/00502).
CONFLICTO DE INTERESESNo se declara ninguno.
- –
La ABAP es una opción terapéutica emergente para pacientes con HPTEC no operable. La evidencia disponible a partir de estudios observacionales avala la eficacia de esta técnica en mejorar la hemodinámica y la capacidad de ejercicio de los pacientes con HPTEC. Hay discrepancia en la magnitud de los resultados entre los centros europeos que realizan esta técnica y las series japonesas. Una tasa no despreciable de complicaciones graves inherente a la técnica hace que se recomiende practicarla en centros expertos en esta técnica y en el tratamiento de pacientes con hipertensión pulmonar.
- –
La presente serie describe la experiencia de la primera serie de ABAP en España. Es también la primera serie que describe la experiencia de esta técnica centralizada en un centro de referencia nacional para hipertensión pulmonar. Los resultados obtenidos en eficacia terapéutica y complicaciones posicionan la ABAP como una herramienta terapéutica coadyuvante al tratamiento médico eficaz y con una relación riesgo-beneficio muy favorable también en centros europeos. Además, esta serie aporta información, hasta ahora desconocida, sobre el lugar que ocupa actualmente la ABAP en una unidad de referencia como una de las opciones terapéuticas para los pacientes con HPTEC.