En el año 2012 se presentan, por primera vez de forma conjunta y agrupadas en la misma área de conocimiento, las novedades de tres secciones científicas: insuficiencia cardiaca y trasplante, cardiopatías congénitas y cardiología clínica. Las novedades más relevantes en el área de insuficiencia cardiaca y trasplante están en la publicación de las guías europeas de insuficiencia cardiaca de 2012. En ellas, se considera las nuevas posibilidades de algunos fármacos (eplerenona e ivabradina), la ampliación de los criterios de resincronización y de utilización de la asistencia ventricular, la diálisis peritoneal y las nuevas posibilidades de reparación percutánea de la válvula mitral (MitraClip®). En las cardiopatías congénitas se ha mejorado de manera significativa la supervivencia de los niños con síndrome del corazón izquierdo hipoplásico. Se han revisado indicaciones y se han modificado las técnicas percutáneas y los dispositivos para el tratamiento de la comunicación interauricular ostium secundum y los defectos septales ventriculares. Cada vez son más frecuentes los procedimientos híbridos en el abordaje de defectos cardiacos estructurales congénitos. En el área de cardiología clínica, hay estudios en que la implantación percutánea de prótesis obtendría menor mortalidad que la implantación quirúrgica. También se recomiendan los criterios CHA2DS2-VASc y utilizar los nuevos anticoagulantes orales. Por otro lado, se están desarrollando nuevas técnicas de secuenciación que permiten el análisis de multitud de genes.
Palabras clave
Lo más destacado en el campo de la insuficiencia cardiaca (IC) en Europa es la publicación de la nueva versión 2012 de la guía de práctica clínica sobre diagnóstico y tratamiento de la IC aguda y crónica de la Sociedad Europea de Cardiología1,2. Las principales novedades se exponen en la tabla 1.
Principales novedades de la nueva versión de las guías de práctica clínica para el diagnóstico y el manejo de la insuficiencia cardiaca
| • Presentación de las recomendaciones en tablas que incluyen la referencia que da soporte al grado indicación y el nivel de evidencia |
| • Definición específica y diferenciada para el diagnóstico de la insuficiencia cardiaca con fracción de eyección reducida y la insuficiencia cardiaca con fracción de eyección preservada |
| • Ampliación de la indicación de los antagonistas de los mineralcorticoides (antialdosterónicos) |
| • Nueva indicación para la ivabradina |
| • Más información sobre el papel de la revascularización coronaria |
| • Ampliación de las indicaciones de la terapia de resincronización |
| • Reconocimiento del papel creciente de la asistencia ventricular |
| • Refuerzo de la importancia del manejo holístico del paciente y el papel de los programas multidisciplinarios para el seguimiento de la insuficiencia cardiaca |
Los dos aspectos farmacológicos más relevantes de esta nueva versión son la inclusión por primera vez en la guía de una recomendación específica para el uso de la ivabradina y la mejora del nivel de evidencia otorgado al uso de los antialdosterónicos.
En el caso de la ivabradina, las guías le adjudican un nivel de recomendación IIa con nivel de evidencia B, a partir de los resultados del estudio SHIFT3. Básicamente, en esta versión se incorpora la ivabradina en el algoritmo terapéutico para pacientes ya tratados con diuréticos, si precisan inhibidores de la enzima de conversión de la angiotensina o antagonistas de los receptores de la angiotensina II, bloqueadores beta y antialdosterónicos, siempre que el paciente esté en ritmo sinusal y tenga una frecuencia cardiaca>70lpm. La indicación de este fármaco es, por lo tanto, previa a la consideración de la terapia de resincronización. Es digno de mencionar que el punto de corte para el inicio de este tratamiento según estas guías es 70lpm, que claramente contrasta con el punto de corte ligeramente superior (75lpm) establecido por la Agencia Europea del Medicamento.
En la línea del SHIFT, diversos de sus subestudios recientemente publicados han añadido datos interesantes a los ya conocidos. En primer lugar, uno de los subestudios publicados en Journal of the American College of Cardiology demuestra que el beneficio de la ivabradina está más relacionado con la frecuencia cardiaca basal que con la dosis de bloqueadores beta recibida por el paciente4. La frecuencia basal del paciente candidato a tratamiento con ivabradina parece ser un factor crucial: en uno de los subestudios publicados en 2011, se observó que, en la cohorte de pacientes del SHIFT con frecuencia cardiaca basal ≥75lpm, el tratamiento con ivabradina mostró mejoras en objetivos «duros» importantes, como la mortalidad por cualquier causa y la mortalidad cardiovascular, lo que subraya que el beneficio de este fármaco es más notable cuanto mayor es la frecuencia cardiaca basal5.
Los resultados del estudio EMPHASIS6 han supuesto para los antialdosterónicos (antagonistas de los receptores mineralcorticoideos, como se los denomina en esta nueva versión de las guías) recibir un grado de recomendación I con nivel de evidencia A para pacientes con IC y fracción de eyección del ventrículo izquierdo (FEVI) ≤35% y síntomas. A la evidencia ya existente procedente de estudios previos como el RALES7 y el EPHESUS8 (tras infarto agudo de miocardio), los resultados del EMPHASIS añaden un papel prioritario como tratamiento farmacológico escalonado después de la introducción de los bloqueadores beta y antes de la ivabradina en el algoritmo terapéutico recomendado en esta versión de las guías1.
Respecto a las guías anteriores, esta nueva versión presenta pocos cambios en la indicación de la implantación de desfibrilador automático implantable. Se recomienda implantar desfibrilador automático implantable en prevención primaria para pacientes en clase funcional II-IV con FEVI ≤35%, pero se exige, a diferencia de las guías previas, que el paciente lleve al menos 3 meses con el tratamiento optimizado. En cuanto a la terapia de resincronización, hay que destacar la incorporación de pacientes con IC leve al grupo de candidatos a esta terapia a partir de nuevos estudios recogidos en esta última versión de las guías, que incluyeron a pacientes en clase funcional II de la New York Heart Association (NYHA). A la hora de establecer una recomendación exacta y un nivel de evidencia determinado, en esta versión se da mucho peso a la clase funcional del paciente y a la presencia o ausencia de bloqueo de rama izquierda. En todos los casos se exige un QRS ancho (a partir de 120ms hasta 150ms, según el subgrupo de pacientes) y la presencia de disfunción grave del ventrículo izquierdo (FEVI ≤35% en NYHA III-IV y FEVI ≤30% en NYHA II). En presencia de bloqueo de rama izquierda, las recomendaciones son de clase I; con otras morfologías de QRS, pasan a ser IIa1.
En el campo de la cirugía cardiaca y los procedimientos valvulares percutáneos, se refuerza el papel de la revascularización quirúrgica para alterar el curso natural de la enfermedad en pacientes con enfermedad del tronco común o de tres vasos. En este sentido, la revascularización quirúrgica en pacientes con disfunción sistólica, angina y enfermedad de dos o tres vasos (que incluyan la arteria descendente anterior) con calidad óptima para cirugía recibe un grado de recomendación I con nivel de evidencia B. Una novedad destacada de las guías de 2012 es que por primera vez se plantea la opción de la implantación percutánea de una prótesis valvular aórtica en pacientes con alto riesgo quirúrgico, y se abre la puerta a la reparación valvular percutánea edge to edge (también denominada técnica de Alfieri percutánea) en pacientes con indicación de reparación valvular pero considerados inoperables o con un riesgo quirúrgico inaceptablemente alto. En estas guías no se recomiendan asociar la restauración quirúrgica del ventrículo izquierdo a la revascularización coronaria ni el uso de dispositivos externos de contención en pacientes con dilatación del ventrículo izquierdo1.
Así pues, esta nueva versión aporta nuevas luces a muchos aspectos del manejo de la IC, deja abiertas varias controversias y destaca numerosos temas en que se requiere mayor nivel de evidencia para poder emitir recomendaciones específicas. A pesar de todos los aspectos controvertidos y la falta de información en muchos campos, son una herramienta muy útil para guiar el manejo diario de los pacientes con IC.
NOVEDADES EN INSUFICIENCIA CARDIACA AVANZADA Y TRASPLANTELas guías europeas de IC de 2012 reconocen al trasplante cardiaco como el tratamiento de referencia para determinados pacientes, pero se limitan a enumerar sus indicaciones y contraindicaciones, sin cambios sustanciales1. También destacan el protagonismo creciente del soporte circulatorio mecánico debido al aumento del número de enfermos con IC avanzada, la escasez de órganos y los avances tecnológicos en los dispositivos de asistencia ventricular, y aciertan al clarificar los siguientes aspectos:
- •
Nomenclatura de la asistencia ventricular según su función (puente a la decisión, puente a la candidatura, puente al trasplante, puente a la recuperación y terapia de destino).
- •
Criterios de posible implante de un dispositivo de asistencia ventricular (según fracción de eyección, consumo de oxígeno, criterios clínicos y hemodinámicos).
- •
Grados de recomendación y niveles de evidencia del uso asistencia ventricular.
Asimismo, resaltan la necesidad de aplicar el soporte mecánico circulatorio antes de que el paciente sufra disfunción ventricular derecha o fallo multiorgánico, ya que se relaciona claramente con mejor supervivencia. El elevado coste y las complicaciones inherentes al uso de los dispositivos de asistencia ventricular condicionan un uso muy limitado, por lo que el manejo de los pacientes con IC avanzada sintomáticos a pesar de tratamiento óptimo sigue siendo un desafío para los profesionales encargados de su cuidado.
Por otro lado, las terapias de sustitución renal continuas emergen como una alternativa factible al manejo exclusivamente farmacológico9. La hemofiltración venovenosa continua se usa generalmente en situaciones agudas de sobrecarga de volumen en pacientes oligúricos10,11, pero como terapia de mantenimiento implica dificultades logísticas y costes elevados y los resultados son moderados. La diálisis peritoneal (DP) consiste en introducir una solución osmótica en la cavidad abdominal, y el peritoneo es la membrana que elimina tanto el exceso de fluido como los productos de desecho. Dos trabajos sobre DP publicados recientemente comunican resultados alentadores. En el estudio de Koch et al12, 118 pacientes con IC grave refractaria e insuficiencia renal se sometieron a DP. Se observaron supervivencias a los 3, a los 6 y a los 12 meses del 77% (intervalo de confianza del 95% [IC95%], 70-85%), el 71% (IC95%, 62-79%) y el 55% (IC95%, 45-64%) respectivamente.
Núñez et al13 analizaron la eficacia de la DP en pacientes con IC que cumplían los siguientes criterios: NYHA III-IV, síntomas congestivos a pesar de terapia óptima con diuréticos de asa, dos ingresos por IC aguda en los últimos meses y disfunción renal (filtrado glomerular<60ml/min/1,73m2). Los objetivos fueron: calidad de vida, test de 6 min de marcha, clase funcional de la NYHA y concentraciones de péptido natriurético cerebral, fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP) y Ca-125 séricos a las 6 y las 24 semanas y días de hospitalización en los 6 meses siguientes. De 57 pacientes preseleccionados, se asignó a 25 a DP, y se obtuvo mejoría en todos los parámetros excepto los marcadores séricos.
Estos estudios refuerzan los resultados comunicados previamente, en los que se subraya una supervivencia del 82% al año y del 56% a los 2 años y disminución de los días de hospitalización tras iniciar la DP14.
Por otro lado, y dentro de los avances en el tratamiento de la IC avanzada, destaca la modulación de la contractilidad cardiaca. Esta terapia consiste en la aplicación de impulsos eléctricos durante el periodo refractario ventricular absoluto del ciclo contráctil cardiaco, con lo que se consigue aumentar la fuerza de la contracción muscular cardiaca (dP/dt). El dispositivo se activa, independientemente de la presencia de asincronía, tras tres latidos en ritmo sinusal, lo que implica que no es útil en fibrilación auricular (FA) ni en presencia de ectopia ventricular frecuente.
Estudios preclínicos indican que la contractilidad cardiaca puede normalizar la fosforilación de proteínas clave y la expresión de genes que codifican proteínas implicadas en la regulación del ciclo del calcio y en la contracción15.
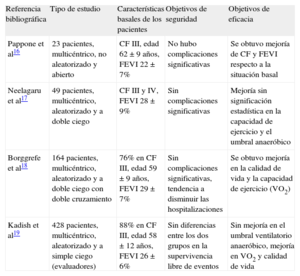
El dispositivo tiene la marca de conformidad europea (CE) y está pendiente de aprobación por la Food and Drug Administration. Hasta la fecha, se han realizado varios ensayos en pacientes con disfunción ventricular grave, en clase funcional avanzada, con QRS estrecho y terapia óptima para la IC (incluido el implante de desfibrilador) que demuestran que los pacientes que reciben terapia con contractilidad cardiaca presentan mejoras en la capacidad de ejercicio y la calidad de vida respecto al grupo de pacientes que no reciben dicho tratamiento (tabla 2)16–19.
Principales estudios en humanos con terapia de modulación de la contracción cardiaca
| Referencia bibliográfica | Tipo de estudio | Características basales de los pacientes | Objetivos de seguridad | Objetivos de eficacia |
| Pappone et al16 | 23 pacientes, multicéntrico, no aleatorizado y abierto | CF III, edad 62±9 años, FEVI 22±7% | No hubo complicaciones significativas | Se obtuvo mejoría de CF y FEVI respecto a la situación basal |
| Neelagaru et al17 | 49 pacientes, multicéntrico, aleatorizado y a doble ciego | CF III y IV, FEVI 28±9% | Sin complicaciones significativas | Mejoría sin significación estadística en la capacidad de ejercicio y el umbral anaeróbico |
| Borggrefe et al18 | 164 pacientes, multicéntrico, aleatorizado y a doble ciego con doble cruzamiento | 76% en CF III, edad 59±9 años, FEVI 29±7% | Sin complicaciones significativas, tendencia a disminuir las hospitalizaciones | Se obtuvo mejoría en la calidad de vida y la capacidad de ejercicio (VO2) |
| Kadish et al19 | 428 pacientes, multicéntrico, aleatorizado y a simple ciego (evaluadores) | 88% en CF III, edad 58±12 años, FEVI 26±6% | Sin diferencias entre los dos grupos en la supervivencia libre de eventos | Sin mejoría en el umbral ventilatorio anaeróbico, mejoría en VO2 y calidad de vida |
CF: clase funcional; FEVI: fracción de eyección del ventrículo izquierdo; VO2: consumo de oxígeno.
Durante los últimos años, ninguna cardiopatía congénita ha sufrido cambios tan relevantes en el diagnóstico, el manejo y los resultados como el síndrome del corazón izquierdo hipoplásico. En esta última década, la supervivencia a 5 años, incluidos los tres procedimientos quirúrgicos paliativos (estadios I, II y III de Norwood), ha aumentado de un 50 a un 69%, aunque hay gran variabilidad en los resultados dependiendo del centro. En los últimos meses ha aparecido gran cantidad de artículos que tratan distintos aspectos de esta enfermedad.
Preestadio I. Diagnóstico y manejo prenatal. El diagnóstico prenatal del síndrome del corazón izquierdo hipoplásico suele conllevar un alto porcentaje de interrupción voluntaria del embarazo, muchas veces condicionada por el desconocimiento actual del pronóstico real del síndrome del corazón izquierdo hipoplásico entre los profesionales que informan a los padres. Hilton-Kamm et al20, mediante cuestionarios realizados a 841 progenitores que habían tenido fetos con cardiopatía congénita grave, analizan cómo el asesoramiento de los profesionales respecto al tratamiento y el pronóstico del síndrome del corazón izquierdo hipoplásico puede condicionar su decisión.
Estadio I. Consiste en la reconstrucción del arco aórtico utilizando el tronco de la arteria pulmonar, preservando un flujo coronario retrogrado adecuado a través de la aorta ascendente hipoplásica, la creación de un defecto interauricular no restrictivo y la preservación del flujo pulmonar a través de un conducto de Gore-Tex desde la arteria subclavia, fístula de Blalock-Taussing o desde el ventrículo derecho a las arterias pulmonares (shunt de Sano). Las ventajas y los inconvenientes de una u otra forma de establecer el flujo pulmonar han sido objeto de controversia en los últimos años. Menon et al21 demuestran mediante estudios histopatológicos (muestras obtenidas de autopsias o de pacientes trasplantados) la presencia de un área de fibrosis significativa en la zona de la ventriculotomía derecha donde se implantó el conducto en la conexión tipo Sano, y que corresponde además a la zona de depleción de la deformación miocárdica, anteriormente evidenciada por ecocardiografía en el seguimiento de cada uno de los pacientes. Por otro lado, Kolcz et al22 describen que el shunt de Sano asegura una distribución más equilibrada del flujo en ambas ramas pulmonares y mejora el desarrollo de la arteria pulmonar izquierda. Por último, Frommelt et al23 no observan ninguna diferencia en el tamaño y la función del ventrículo derecho ni en la incidencia de insuficiencia tricuspídea entre la fístula de Blalock-Taussing y el shunt de Sano a los 14 meses de edad. Tabbutt et al24 describen los factores de riesgo de mayor morbimortalidad hospitalaria después del estadio I de Norwood en un estudio que incluyó a 549 pacientes provenientes de 15 centros. El largo tiempo de parada cardiocirculatoria con hipotermia profunda, la necesidad de mantener el tórax abierto después de la cirugía, el bajo peso, las alteraciones genéticas asociadas, la necesidad de oxigenador de membrana extracorpóreo postoperatorio y los hospitales y los cirujanos con menor volumen de pacientes son los factores asociados a mayor morbimortalidad postoperatoria. Sin embargo, la realización de una fístula de Blalock-Taussing o un shunt de Sano no tuvo relevancia en la evolución postoperatoria. El procedimiento híbrido (implantación de stent en el ductus arterioso y realización de bibanding de ambas arterias pulmonares por acceso quirúrgico sin circulación extracorpórea) es la alternativa de elección en algunos centros en los últimos años. A pesar de las expectativas generadas, no parece haber ventajas significativas en cuanto a la supervivencia total de estos pacientes después del estadio II, como exponen Photiadis et al25.
Estadio II. Consiste en la anastomosis de la cava superior con las arterias pulmonares (procedimiento de Glenn), eliminando el shunt previo. Menon et al26 analizan los riesgos de morbimortalidad en una población de 162 pacientes aportados por 31 hospitales de Estados Unidos. El bajo peso para la edad, el sexo femenino y la atresia aórtica con atresia mitral son las circunstancias asociadas a mayor incidencia de mortalidad y complicaciones.
Estadio III. Consiste en la anastomosis de la cava inferior con las arterias pulmonares (procedimiento de Fontan). Una adecuada función del ventrículo derecho sistémico es fundamental para la buena evolución postoperatoria de los pacientes sometidos a cirugía de Fontan; la resincronización se está incorporando con éxito para pacientes con ventrículo único, incluido el síndrome del corazón izquierdo hipoplásico, para optimizar la contractilidad miocárdica antes del Fontan, como describen Enomoto et al27.
Procedimientos percutáneos e híbridos en cardiopatías congénitasEl cierre percutáneo de la comunicación interauricular ostium secundum con dispositivo Amplatzer® es un procedimiento seguro y bien establecido, aunque no exento de complicaciones precoces y a largo plazo. La peor de todas es la perforación de la pared auricular por la erosión del dispositivo. En una reciente revisión de casos de perforaciones realizada por St. Jude Medical, el 88% de los casos tenía una deficiencia del borde aórtico (borde anterosuperior en la ecocardiografía) y la erosión que condicionaba la perforación se producía a este nivel. Según estos datos, el fabricante ha modificado recientemente las recomendaciones respecto a las contraindicaciones de su utilización28, que afectan fundamentalmente a la evaluación del borde aórtico por ecocardiografía. Mallula et al29 revisan de forma sistemática todos los cortes secuenciales posibles por ecocardiografía transesofágica y ecocardiografía intracardiaca requeridos para el estudio de la comunicación interauricular ostium secundum, y postulan que hay una correlación muy buena en las imágenes obtenidas por ecocardiografía transesofágica y ecocardiografía intracardiaca en el estudio de todos los bordes y en especial del aórtico. Concluyen que sólo la deficiencia del borde aórtico en múltiples cortes secuenciales, ya sea por ecocardiografía transesofágica o por ecocardiografía intracardiaca, contraindicaría el cierre percutáneo de la comunicación interauricular por considerarla de alto riesgo.
El tratamiento percutáneo de los defectos del tabique interventricular perimembranosos y musculares con diversos dispositivos específicos se ha tratado en numerosas publicaciones en los últimos años. Koneti et al30 describen una nueva técnica de cierre percutáneo de defecto del tabique interventricular por acceso retrógrado y el uso off-label del nuevo dispositivo Amplatzer® Duct Occluder II (ADO II). Se trata de un estudio prospectivo que incluyó a 13 niños con diversos defectos del tabique interventricular, seleccionados por tratarse de defectos aislados, hemodinámicamente significativos y<6,5mm por ecocardiografía, ya que el diámetro máximo disponible del cilindro central del Amplatzer® Duct Occluder II es de 6mm. El dispositivo se liberó con éxito en 11 pacientes, y los autores concluyen que se trata de una técnica sencilla y que reduce significativamente los tiempos de fluoroscopia.
El abordaje percutáneo de la obstrucción del tracto de salida ventricular izquierdo en pacientes sintomáticos con miocardiopatía hipertrófica obstructiva (ablación septal con alcohol), que ha constituido desde hace tiempo una alternativa terapéutica en pacientes adultos, no es técnicamente realizable en niños. Sreeram et al31 publican un estudio con los resultados preliminares del tratamiento percutáneo de reducción septal por ablación con radiofrecuencia (ARF) en 32 pacientes de edad pediátrica (2,9 a 17,5 años) con esta enfermedad. La mayoría de los pacientes mostraron una inmediata reducción del gradiente en tracto de salida ventricular izquierdo (78,5±26,2mmHg antes de la ARF frente a 36,1±16,5mmHg después). Los autores concluyen que la ARF es una alternativa terapéutica para los pacientes pediátricos sintomáticos con obstrucción del tracto de salida ventricular izquierdo. Los beneficios de este procedimiento incluyen la facilidad de su aplicación, el uso de un equipo de ablación estándar, la repetibilidad y el acortamiento de la estancia hospitalaria. El procedimiento es mucho más seguro que la ablación septal con alcohol, y la capacidad para identificar el fascículo de His y la posibilidad de preservar la conducción auriculoventricular son también beneficios potenciales de esta técnica.
El abordaje híbrido es uno de los retos actuales del tratamiento de los defectos cardiacos estructurales congénitos, para el que un verdadero trabajo de equipo entre cirujanos y cardiólogos hace posible la mejor estrategia terapéutica para cada situación. Li et al32 revisan su experiencia de 5 años en el abordaje híbrido con buenos resultados en 30 pacientes con atresia pulmonar con septo íntegro. Describen su algoritmo terapéutico para un subconjunto de esta población, que tiene indicación de descompresión del tracto de salida del ventrículo derecho. Su estrategia consiste en un abordaje por esternotomía media, seguido de perforación del tracto de salida del ventrículo derecho con aguja guiada por ecografía pasando una guía hasta la arteria pulmonar y posterior realización de una valvuloplastia pulmonar. En la mayoría de los casos, efectúan a continuación una fístula de Blalock-Taussing modificada tras ligar el ductus. Los autores concluyen que este abordaje híbrido es seguro y eficaz, con ventajas teóricas sobre el tratamiento convencional quirúrgico o percutáneo de esta afección.
Un estudio multicéntrico33 revisa la experiencia de 11 centros de Alemania, Austria y Suiza sobre la factibilidad, la eficacia y los resultados de procedimientos híbridos para cierre de defectos interventriculares, en los que se minimizó el tiempo de circulación extracorpórea o se realizaron completamente sin bomba. En este estudio se seleccionó a 26 pacientes de corta edad o con anomalías complejas, incluidos defectos tras infarto de miocardio, todos con muy alto riesgo quirúrgico. En 20 pacientes se utilizó un acceso periventricular y en 6, los dispositivos oclusores se colocaron con visualización directa como parte de una compleja cirugía cardiaca. En 23 de los procedimientos, la colocación del dispositivo se realizó correctamente (88,5%). Los autores concluyen que el cierre periventricular e intraoperatorio de defectos interventriculares con dispositivos oclusores es tan eficaz como un parche quirúrgico y evita el aumento de morbilidad de la reparación quirúrgica convencional en un subgrupo de pacientes de alto riesgo.
ACTUALIZACIÓN EN VALVULOPATÍASEn el año 2011, las novedades se centraron en el tratamiento percutáneo de las valvulopatías. El estudio más relevante en este campo es la rama del estudio PARTNER, en la que se demostró que, al año, el implante de la prótesis Edwards-SAPIEN® es no inferior al reemplazo quirúrgico en pacientes de alto riesgo quirúrgico con estenosis aortica grave34. Las tasas de mortalidad por cualquier causa fueron del 3,4% en las prótesis percutáneas y del 6,5% en la cirugía, a los 30 días (p=0,07), y del 24 frente al 26,8% al año (p=0,44). Las tasas de ictus fueron 3,8% para las prótesis percutáneas y el 2,1% para la cirugía, a los 30 días (p=0,20), y del 5,1 frente al 2,4% al año (p=0,07). Respecto a los síntomas, que mejoraron claramente en ambos grupos de pacientes, no se observaron diferencias significativas, aunque la estancia hospitalaria fue menor con las prótesis percutáneas.
Respecto a la fisiopatología de la estenosis aortica, cabe destacar un trabajo que demuestra con tomografía por emisión de positrones la presencia de inflamación en las válvulas estenóticas frente a las válvulas de controles sanos; es especialmente interesante que esta inflamación está aumentada en válvulas con estenosis leve y moderada, pero no grave, lo que puede abrir caminos hacia tratamientos que eviten la progresión de la estenosis aortica en estadios precoces35. Un pequeño estudio multicéntrico nacional ha demostrado que el uso del acceso axilar en pacientes seleccionados para las prótesis percutáneas, con CoreValve® y contraindicación para el acceso femoral, es seguro y eficaz y proporciona excelentes resultados en cuanto a éxito del implante y mortalidad intrahospitalaria y a los 30 días36. Otro estudio reseñable es el análisis retrospectivo de pacientes con válvula bicúspide, en el que se aprecia que la incidencia de disección en un seguimiento de 16 años es bajo (3,1 casos/10.000 pacientes-año), pero significativamente superior al de la población general (riesgo relativo [RR]=8,4; IC95%, 2,1-33,5; p=0,003)37.
Con respecto a la válvula mitral, se ha publicado el estudio EVEREST II, que distribuyó aleatoriamente a 279 pacientes con regurgitación mitral de grados 3 o 4 a reparación percutánea con MitraClip® o cirugía convencional. Tras 12 meses de seguimiento, el MitraClip® fue menos efectivo en reducir la regurgitación mitral que la cirugía (el 55 y el 73%; p=0,007), aunque el procedimiento percutáneo se asoció con mayor seguridad al mes de seguimiento (el 15% de eventos adversos graves frente al 48%; p<0,001) y a una mejora similar en la evolución clínica38.
El estudio de Gertz et al se centra en una observación común en clínica y pone en evidencia que la ablación de la FA que condicionó la aparición de regurgitación mitral funcional, mejora con la restauración a ritmo sinusal39.
La enfermedad tricuspídea es compleja de manejar, ya que, especialmente en nuestro medio, afecta a pacientes con cirugías previas, lo que eleva su riesgo quirúrgico cuando empiezan a estar sintomáticos. Por ello, la experiencia inicial con el implante percutáneo de la prótesis pulmonar Melody® sobre la válvula tricúspide en 14 casos abre una nueva posibilidad terapéutica40.
También se ha publicado que la tomografía computarizada puede ser una técnica excelente para descartar lesiones coronarias antes de la cirugía valvular y hace innecesario realizar un estudio invasivo si el estudio es de buena calidad y el resultado es negativo41.
NOVEDADES EN ELECTROCARDIOGRAFÍAEn 2011 se publicó un trabajo con 506 pacientes consecutivos que presentaban dolor torácico atendidos en 55 centros sanitarios periféricos sin cardiólogos y evaluados mediante un sistema de transmisión de electrocardiograma (ECG) transtelefónico analizado de manera centralizada que sirvió para clasificar a los pacientes en dos grupos: A, pacientes sin anormalidades electrocardiográficas (n=445), y B, pacientes con anormalidades que indican etiología cardiaca del dolor torácico (n=61). La presencia de factores de riesgo se evaluó mediante análisis multivariable, que demostró una elevada especificidad (99,6%). El seguimiento de los 506 pacientes confirmó el origen no cardiaco del dolor torácico en 432 pacientes (97%) del grupo A y el origen cardiaco en 59 (97%) del grupo B42.
Para evaluar las alteraciones del ECG y el riesgo coronario, se realizó un estudio con 2.192 adultos sin enfermedad cardiovascular previa. Se analizaron las alteraciones basales del ECG y tras 4 años de seguimiento, según los códigos de Minnesota. El objetivo principal fue la incidencia de una combinación de eventos coronarios (EC). Al inicio del estudio, el 13% tenía alteraciones menores del ECG y el 23%, alteraciones mayores. Durante el seguimiento, 351 participantes sufrieron EC. Las alteraciones basales del ECG se asociaron con un aumento del riesgo de EC, lo que permitió reclasificar el riesgo coronario de los pacientes. Así, se reclasificó a riesgo alto a 176 pacientes considerados de riesgo intermedio. Tras 4 años de seguimiento, 208 participantes tenían nuevas alteraciones del ECG y 416, alteraciones persistentes; en ambos casos se asociaron con un aumento del riesgo de EC. Este estudio aporta evidencia de que las alteraciones del ECG pueden mejorar la predicción del riesgo coronario de los pacientes ancianos43.
Fibrilación auricularLas guías europeas de FA de 2010 recomendaban la utilización de los criterios CHA2DS2-VASc para predecir el riesgo de embolia en los pacientes con FA no valvular y la utilización de los nuevos anticoagulantes orales (ACO) que estaban mostrando resultados similares o mejores que la warfarina en la prevención del ictus. Dos nuevos estudios publicados en el último año, aunque parcialmente comunicados previamente, aportan nueva información sobre estos fármacos. El estudio ARISTOTLE incluyó a 18.201 pacientes (CHADS2 próximo a 2). Los resultados mostraron que apixabán 5 mg/12 h fue superior a la warfarina en la prevención de ictus y tromboembolia sistémica ([RR]=0,79; IC95%, 0,66-0,95; p<0,001), produjo menos hemorragias graves (RR=0,69; IC95%, 0,60-0,80; p<0,001) y redujo la mortalidad por cualquier causa (RR=0,89; IC95%, 0,80-0,99; p<0,001)44.
El estudio ROCKET incluyó a 14.264 pacientes con una media de riesgo CHADS2=3. En el análisis por protocolo, rivaroxabán (20mg/24h) se demostró no inferior a la warfarina en la prevención de eventos embólicos y la incidencia de hemorragias graves o clínicamente relevantes. El rivaroxabán redujo la incidencia de hemorragia intracraneal (el 0,5 frente al 0,7%; p=0,02) y hemorragia mortal (el 0,2 frente al 0,5%; p=0,003) en comparación con la warfarina. Los dos estudios, junto con el RE-LY y los subestudios publicados, forman una sólida evidencia sobre los beneficios de los nuevos ACO45.
En los últimos meses, varios grupos han publicado datos que avalan la utilidad de la escala CHA2DS2-VASc. La mayoría ha confirmado que sigue habiendo una diferencia significativa entre las recomendaciones de anticoagulación de las guías y la práctica clínica habitual y que los controles de anticoagulación con razón internacional normalizada demuestran la dificultad de mantener a los pacientes en control adecuado46–48. Una de las críticas de los nuevos ACO es la reversibilidad de su acción, y ya hay trabajos que comienzan a aportar soluciones al respecto49.
La Sociedad Europea de Cardiología ha publicado en 2012 la actualización de las guías de FA, que incorporan la revisión de estos últimos trabajos y recomiendan el uso de los criterios CHA2DS2-VASc y los nuevos ACO dabigatrán, rivaroxabán y apixabán antes que warfarina50.
NOVEDADES EN ATENCIÓN PRIMARIACabe destacar un estudio prospectivo desarrollado en 102 centros de atención primaria (AP) españoles que valora el cumplimiento terapéutico con inhibidores del sistema renina-angiotensina en hipertensión no controlada sobre 808 pacientes de alto riesgo vascular. La tasa media de dosis tomadas fue del 87,9%. Fueron cumplidores en general el 73,3%; de una toma diaria, el 52,8%, y en horario correcto, el 46,5%. El cumplimiento se asoció a menor número de fármacos prescritos y no ser diabético51.
Como AP tiene reducido acceso al ecocardiografía en España, los péptidos natriuréticos pueden ser una alternativa para el diagnóstico de IC. En un estudio realizado en AP, se determinó el punto de corte del NT-proBNP en pacientes con sospecha de IC, a los que se realizó un ecocardiograma y un cardiólogo valoró. Se incluyó a 220 pacientes (el 65,5% mujeres) con una mediana de edad de 74 años. El diagnóstico de IC se confirmó en 52 pacientes (23,6%). Los valores de NT-proBNP fueron de 715 y 77,5 pg/ml en pacientes con y sin IC respectivamente. El mejor punto de corte fue 280 pg/ml (área bajo la curva receiver operating characteristic=0,94), cifra inferior a la propuesta en las guías National Institute for Health and Clinical Excellence. La utilización del NT-proBNP en la consulta habría evitado el 67% de los ecocardiogramas solicitados, por lo que podría considerarse coste-efectiva52.
La enfermedad arterial periférica se considera como un equivalente de riesgo de cardiopatía isquémica, por lo que se recomienda detectar las formas subclínicas mediante el índice tobillo-brazo. Un estudio nacional analizó la prevalencia de la enfermedad arterial periférica y los factores de riesgo asociados sobre una muestra poblacional aleatoria de 2.833 sujetos. La prevalencia de enfermedad arterial periférica (índice tobillo-brazo<0,9) fue del 3,7% (el 5,0% en varones y el 2,6% en mujeres; p=0,001). Las recomendaciones actuales de cribado no detectaron al 29,6% de los casos asintomáticos. El uso del índice tobillo-brazo aumentó en un 32,7% los casos de riesgo coronario alto53.
Hay aún múltiples lagunas sobre la eficacia del control glucémico en la prevención de eventos cardiovasculares. El estudio ORIGIN analizó la eficacia de la intervención precoz en el control glucémico para la prevención de eventos cardiovasculares. Se incluyó a 12.537 pacientes prediabéticos o con diabetes mellitus tipo 2 y alto riesgo cardiovascular para evaluar el efecto de la insulina glargina frente al tratamiento antidiabético estándar y de ácidos omega-3 frente a placebo en la prevención de eventos cardiovasculares. Tras un seguimiento de 6,2 años, los resultados mostraron un efecto neutro entre el grupo de insulina glargina y el de tratamiento estándar para el objetivo principal y para cada uno de los componentes. Se observó menor incidencia de nuevos casos de diabetes mellitus tipo 2 (odds ratio=0,80; IC95%, 0,64-1; p=0,05). El incremento de peso y la incidencia de hipoglucemias fue superior en la rama de insulina glargina, sin que hubiera diferencias en la incidencia de cáncer. Los resultados para los ácidos omega-3 fueron igualmente neutros. Los resultados del estudio ORIGIN, en concordancia con otros estudios, respaldan la tesis de que la intervención multifactorial es la estrategia más eficiente54.
El tratamiento anticoagulante de la FA es una tarea compartida entre AP y los diferentes especialistas. El estudio Val-FAAP se diseñó para conocer las características de los pacientes con FA atendidos en AP. Se incluyó en un muestreo secuencial nacional a 119.526 individuos. La prevalencia de FA estimada fue del 6,1% (n=3.287), asociada a mayor edad, hipertensión arterial y ser varón (p<0,01). La FA permanente fue la forma clínica más frecuente (45,3%) y se asoció a edad y enfermedad renal y cardiaca. El 66% de los pacientes con FA presentaban un CHADS2≥2 y, sin embargo, un tercio de ellos no recibían tratamiento anticoagulante. Simultáneamente, un 48,8% de los pacientes con CHADS2=0 recibían tratamiento. Los datos de este estudio muestran que la FA es una entidad frecuente en AP. Es importante incrementar la información y la formación para mejorar la estratificación y el correcto manejo terapéutico de estos pacientes55.
NOVEDADES EN ENFERMEDADES FAMILIARESEn 2012 cabe destacar un artículo que ha supuesto un cambio importante en el conocimiento de la fisiopatología de la miocardiopatía arritmogénica del ventrículo derecho, que deja abierta una nueva vía para la investigación de herramientas diagnósticas y el futuro desarrollo de agentes terapéuticos. El grupo de Asimaki et al,56 que ya describió una técnica inmunohistoquímica con una altas sensibilidad y especificidad para el diagnóstico de miocardiopatía arritmogénica a partir de muestras de miocardio, ha conseguido, por un hallazgo inesperado, desarrollar una teoría fisiopatológica en esta enfermedad genética. Para ello realizó una serie de experimentos con muestras de tejido y suero de pacientes con miocardiopatía arritmogénica, sarcoidosis y miocarditis de células gigantes. Los autores encontraron ciertos paralelismos entre estos dos tipos de miocarditis (altamente arritmógena) con la miocardiopatía arritmogénica propiamente dicha. Demostraron el efecto de diferentes mediadores inflamatorios, como la interleucina-17, el factor de necrosis tumoral alfa y la interleucina-6 en la translocación de la placoglobina (proteína principal relacionada con la patogenia de la miocardiopatía arritmogénica) desde el desmosoma al citoplasma. Estos factores inflamatorios estaban elevados en muestras de suero de los casos con miocardiopatía arritmogénica56.
Desde el punto de vista del pronóstico, cabe destacar un estudio sobre el riesgo de arritmias ventriculares malignas en pacientes con miocardiopatía dilatada con mutaciones en el gen de lamina a/c. La presencia de una disfunción sistólica moderada o grave (FEVI<45%), la taquicardia ventricular no sostenida, el sexo masculino y la existencia de una mutación que produzca una terminación prematura o un cambio importante en la pauta de lectura fueron marcadores independientes de eventos arrítmicos. La presencia de dos factores se asoció con una tasa de eventos muy elevada, por lo que se justificaría la implantación de un desfibrilador. Este trabajo es un ejemplo del valor de la genética, tanto en el diagnóstico etiológico de la miocardiopatía dilatada como en la estratificación del riesgo de muerte súbita. En este estudio, el 18% de los pacientes tuvo un evento arrítmico mayor antes de los 4 años de seguimiento. Es importante destacar que sólo el 37% tenía FEVI <45% (media, 55%). De haberse aplicado las recomendaciones actuales (guías de ACC/AHA/ESC) para la implantación de un desfibrilador en pacientes con FEVI <35% y NYHA II-III, en este grupo se habría identificado únicamente al 36% de los pacientes que sufrieron un evento arrítmico mayor. Se abre una nueva era en que la genética permitirá identificar subgrupos de pacientes de alto riesgo arrítmico que se benefician de tratamientos invasivos precoces57.
Un avance tecnológico importante del año 2012 es la aparición en el ámbito clínico de la ultrasecuenciación masiva conocida como next generation sequencing. Hasta ahora, con la técnica de secuenciación empleada, el método Sanger, considerada la de referencia, sólo era posible analizar fragmentos de ADN muy cortos, habitualmente de un solo exón. El estudio de un único gen suponía realizar decenas de análisis, lo que lo convertía en un proceso lento y muy costoso. Con la técnica de next generation sequencing, es posible realizar de una sola vez un análisis de centenares de genes, o incluso de todo el genoma de cada paciente, con unos costes asumibles. A pesar de que esta mejora facilita en extremo el proceso de secuenciación, la identificación de múltiples variantes genéticas de significado incierto en un mismo paciente crea todavía muchos problemas de interpretación. Actualmente, la interpretación correcta de los resultados es la clave de la utilidad de esta potentísima herramienta diagnóstica. El descubrimiento de nuevos genes llevará aparejado necesariamente el desarrollo de modelos animales y estudios funcionales para determinar la causalidad y el papel de las nuevas proteínas estructurales o funcionales en la aparición de las enfermedades cardiacas hereditarias. Estos y otros aspectos relacionados con esta nueva técnica se recogen y se analizan en detalle en la revisión de Ware et al58.
CONFLICTO DE INTERESESNinguno.