INTRODUCCIÓN: Distintas variables han sido identificadas como predictoras de reestenosis angiográfica intra- stent, pero poco se conoce sobre predictores de reestenosis clínica, un aspecto más funcional de la reestenosis coronaria.
OBJETIVO: Conocer de forma práctica si los predictores descritos de reestenosis angiográfica predicen y en qué grado la reestenosis clínica.
PACIENTES Y MÉTODOS: Doscientos dieciséis pacientes consecutivos (271 stents en 256 lesiones) con éxito del procedimiento al alta hospitalaria fueron seguidos durante 17,6 ± 10 meses mediante revisiones periódicas. Reestenosis clínica del stent se definió como la presencia de síntomas o signos de isquemia junto a una reestenosis angiográfica >= 50%.
RESULTADOS: Treinta y tres lesiones (13%), revascularizadas con 34 stents, presentaron reestenosis clínica: 29 casos asociados a angina inestable, tres a infarto agudo de miocardio y uno a la muerte del paciente. El análisis multivariado identificó como predictores independientes el diámetro del vaso menor de 3 mm (p < 0,001; OR 4,5), las lesiones reestenóticas (p = 0,01; OR 2,9) y la estenosis residual visible (> 0%) tras el implante (p = 0,02; OR 2,5). Estas tres variables explicaron el 73% de reestenosis clínica y en presencia de alguna de ellas la reestenosis fue del 22%, frente al 4% en su ausencia. El implante en la arteria descendente anterior, de localización ostial, en pacientes diabéticos y el número o longitud total de stents por lesión, no demostraron una asociación independiente significativa como predictores de reestenosis clínica.
CONCLUSIÓN: La mayoría de reestenosis clínica tras el implante de stents intracoronarios puede ser predicha por el carácter reestenótico de la lesión, el diámetro del vaso < 3 mm y la persistencia de estenosis residual visible, al final del procedimiento
Palabras clave
Stent
Reestenosis
Factores de riesgo
Isquemia
INTRODUCCIÓN
El implante de stents intracoronarios ha permitido reducir las tasas de reestenosis respecto a la angioplastia con balón, aun cuando persisten tasas de reestenosis angiográfica intra- stent entre el 20 y el 30%. Una de las estrategias encaminadas a la mejora de estas tasas ha sido la identificación de predictores de reestenosis. Aunque han sido múltiples las variables asociadas con mayores tasas de reestenosis angiográfica, sólo algunas han sido identificadas de forma más constante en los distintos estudios publicados. Entre éstas estarían la diabetes mellitus, el menor diámetro de referencia del vaso, el carácter reestenótico de la lesión, la localización ostial, el número y longitud total de stents implantados por lesión, el implante en la arteria descendente anterior y la presencia de una mayor estenosis residual 1-6. Estudios con ultrasonidos intracoronarios han identificado una elevada relación entre el área de la placa y el área total del vaso antes del procedimiento y una menor dimensión de la luz alcanzada tras el procedimiento como los principales predictores de reestenosis 5,6.
Aunque la definición angiográfica de reestenosis coronaria evalúa su aspecto anatómico y más objetivo, la definición clínica considera su aspecto funcional y el impacto de la misma en términos de síntomas y signos de isquemia, los cuales representan el primer objetivo de tratamiento. La reestenosis clínica presenta tasas inferiores a la angiográfica; de hecho, aproximadamente sólo entre la mitad y dos tercios de los pacientes con reestenosis angiográfica se someten a nuevos procedimientos de revascularización por la presencia de síntomas 7,8. La reestenosis angiográfica intra- stent puede conducir a revascularizaciones innecesarias 9, máxime si tenemos en cuenta los estudios que demuestran un aumento en el diámetro luminal mínimo intra- stent a partir de los 6-12 meses tras el implante 10,11. Sin embargo, frente a los numerosos estudios que han evaluado predictores de reestenosis angiográfica, pocos lo han hecho respecto a la reestenosis clínica 3,12.
El objetivo de este trabajo ha sido, partiendo de los predictores descritos de reestenosis angiográfica, conocer cuáles de estas variables predicen mejor la reestenosis clínica del stent, de forma que su conocimiento pueda tener una aplicación a la práctica clínica e intervencionista habitual. PACIENTES Y MÉTODOS
Población de estudio
Desde mayo de 1995 a mayo de 1997, un total de 300 stents consecutivos fueron implantados en 278 lesiones de 234 pacientes. Todas las características demográficas, clínicas, angiográficas y del procedimiento fueron recogidas en el momento del implante del stent. Fueron susceptibles de un seguimiento a largo plazo aquellos pacientes con éxito del implante, tanto angiográfico (adecuada expansión angiográfica del stent en la lesión diana con estenosis residual menor del 30% valorada de forma visual) como clínico (ausencia de episodios mayores intrahospitalarios: muerte, infarto de miocardio o necesidad de un nuevo procedimiento de revascularización). En 218 pacientes (93%) se consideró realizar seguimiento a largo plazo. Dos pacientes (0,8%) fueron perdidos en el seguimiento, con lo que un total de 216 pacientes, con 271 stents implantados en 256 lesiones, fueron seguidos durante una media de 17,6 ± 10 meses.
Procedimiento de implante de stents
Se siguieron un total de 271 stents implantados (27,7% Palmaz-Schatz, Johnson & Johnson; 23,6% NIR, SciMed; 21,7% Multilink, ACS; 13,1% Wiktor, Medtronic; 10,5% Gianturco-Roubin, Cook; 2,2% Be-stent, Medtronic; 1,1% Wall-stent, Schneider). El procedimiento de implante fue guiado por el análisis visual de los angiogramas. La indicación del implante fue electiva en el 67%, por resultado subóptimo tras una angioplastia con balón en el 20% y por amenaza u oclusión aguda en el 13%. Previo a la expansión del stent se realizó una dilatación convencional con balón de la lesión y, tras la liberación del stent, la expansión completa de éste se alcanzó con el inflado del balón a altas presiones (15,58 ± 2,25 atm). Tras la inserción del introductor femoral se administró un bolo de 10.000 U de heparina, con posteriores bolos de 5.000 U para mantener un tiempo activado de coagulación por encima de 300 s. Tras finalizar el procedimiento, no se administró más heparina y el introductor fue retirado a las 6-8 h. Todos los pacientes recibieron tratamiento antiagregante plaquetario con aspirina (200 mg cada día) y ticlopidina (250 mg cada 12 h). La aspirina fue iniciada al menos 24 h antes del procedimiento y se continuó indefinidamente. La ticlopidina se administró inmediatamente tras finalizar el procedimiento y se mantuvo durante 4 semanas.
Episodios y seguimiento clínico
Tras el procedimiento de implante, los pacientes fueron contactados mediante visitas periódicas a la consulta hospitalaria, que constaron de entrevista, exploración física y electrocardiograma. Así mismo, a todos los pacientes se les realizó una entrevista telefónica en la fecha final de seguimiento. Ante la sospecha de reestenosis por la presencia de síntomas o signos sugestivos, se realizó una coronariografía diagnóstica. La reestenosis clínica del stent fue definida como la presencia de síntomas o signos indicativos de isquemia, junto a una estenosis angiográfica mayor del 50% en el segmento coronario con el stent implantado.
Factores de riesgo para reestenosis
Seleccionamos posibles factores de riesgo para reestenosis según la experiencia previa en predictores de reestenosis angiográfica intra- stent, los cuales fueron evaluados en forma de variables aplicables a la práctica habitual. Las variables incluidas en el análisis fueron la presencia de diabetes mellitus, el carácter reestenótico de la lesión tras una angioplastia previa, un diámetro de referencia del vaso menor de 3 mm medido en el máximo diámetro, la localización ostial de la lesión, el implante en la arteria descendente anterior, el número y la longitud total de stents implantados en la lesión y la existencia de estenosis residual angiográfica estimada de forma visual al final del procedimiento de implante del stent.
Análisis estadístico
Se estudió la asociación entre los posibles factores de riesgo y la reestenosis clínica del stent durante el seguimiento sobre la base de un análisis por lesión. En el análisis univariado, para variables categóricas se utilizó el método de Kaplan-Meier y la prueba de rango logarítmico, y para variables continuas el test de la t de Student. La identificación de asociaciones independientes se realizó mediante el análisis multivariado de Cox, incluyéndose en el modelo todas las variables con el fin de evitar la exclusión de posibles confusores. Se aceptó como significación estadística todos los valores de p < 0,05. Para el análisis estadístico se utilizó el programa SPSS (versión 7.5, bSPSS Inc.). RESULTADOS
En la tabla 1 se exponen las características basales de la población estudiada. Tras el alta hospitalaria, un total de 33 lesiones (12,9%), revascularizadas con 34 stents (12,5%), presentaron reestenosis clínica. En 3 casos (9%), la reestenosis se asoció a infarto agudo de miocardio no fatal y en un solo caso (3%) se asoció a la muerte del paciente en la espera de un nuevo procedimiento de revascularización. En el resto de casos (88%), la reestenosis se asoció a angina inestable en sus distintas formas de presentación.
En la tabla 2 se expone el resultado del análisis estadístico de posibles predictores de reestenosis clínica en nuestra población. En el análisis univariado, el implante en la arteria descendente anterior, en vasos de diámetro menor de 3 mm, en lesiones reestenóticas y en el ostium coronario se asoció de forma significativa a mayores tasas de reestenosis clínica. El análisis multivariado identificó como predictores independientes de reestenosis clínica el carácter reestenótico de la lesión, la localización en un vaso menor de 3 mm y la existencia de estenosis residual visible tras el implante. La arteria descendente anterior no alcanzó una significación independiente debido a que la mayoría de los implantes en vasos de diámetro menor de 3 mm ocurrieron en esta arteria (el 75% frente al 15%). La localización ostial perdió la significación en el análisis multivariado debido a una mayor incidencia de estenosis residual en esta localización respecto al resto de segmentos coronarios (el 33 frente al 18%), pero mantuvo una significación marginal como predictor independiente. La diabetes mellitus no se asoció a mayores tasas de reestenosis clínica en ninguno de los análisis, al igual que el número de stents por lesión. La longitud total de stent recubriendo la lesión tampoco fue un predictor significativo, si bien en el análisis multivariado se hizo patente una tendencia no significativa a mayores tasas.
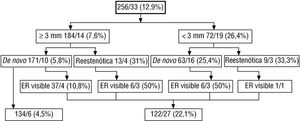
En la figura 1 se observan los casos y la reestenosis clínica atendiendo a la presencia de las tres variables identificadas como predictores independientes. Estas tres variables explicaron 27 de los 33 casos de reestenosis, un 72%. El implante en vasos menores de 3 mm conllevó una incidencia de reestenosis clínica del 26%, que fue del 33% cuando se trataba de una lesión reestenótica. La existencia de estenosis residual tras el implante del stent supuso un aumento de la incidencia hasta el 50% cuando se sumó a alguna de las variables anteriores y del 11% en ausencia de dichas características. La incidencia total en presencia de una o más de estas tres variables fue del 22%, frente al 4% en ausencia de todas ellas.
Fig. 1. En cada grupo de lesiones se expresan: lesiones totales/lesiones con reestenosis clínica (porcentaje de reestenosis en el grupo).
Las 33 lesiones con reestenosis clínica se correspondieron con 28 pacientes (13%), es decir, 5 pacientes presentaron reestenosis de dos lesiones distintas. De los 40 pacientes en que se implantaron stents en dos o más lesiones distintas, ocho presentaron reestenosis de alguna lesión, de los cuales en cinco (60%) la reestenosis ocurrió en dos lesiones distintas. Es decir, en pacientes con dos o más lesiones revascularizadas con stents, la reestenosis de una de las lesiones se asoció a un riesgo del 60% para la aparición de otra reestenosis a distancia. DISCUSIÓN
En nuestra población de stents intracoronarios, tres cuartas partes de la reestenosis clínica ocurrida pudo ser predicha por la presencia de tres variables: el carácter reestenótico de la lesión, el implante en vasos menores de 3 mm y la presencia de estenosis residual visible al final del procedimiento. En ausencia de estas variables, la incidencia de reestenosis fue del 4%, frente al 22% en presencia de alguna de ellas. Otras variables identificadas como predictores de reestenosis angiográfica en trabajos previos, como la longitud del segmento con stent, la diabetes mellitus, la localización en la descendente anterior o en el del ostium coronario, no alcanzaron significación independiente como predictores de reestenosis clínica del stent.
Kastrati et al 3 estudiaron predictores de revascularización de la lesión diana guiada por síntomas en 1.349 pacientes, identificando la diabetes mellitus, el implante de múltiples stents y un menor diámetro mínimo luminal. Previamente, Klugherz et al 12 publicaron un seguimiento de 3 años en 65 pacientes con stents Palmaz-Schatz, identificando la presencia de una elevada clase de angina, un pequeño diámetro del balón usado en la expansión y un mayor número de stents implantados como predictores de episodios clínicos en el seguimiento.
En nuestro estudio, el tamaño del vaso definido por un diámetro de referencia menor de 3 mm fue un predictor independiente de reestenosis clínica a largo plazo. Otros trabajos han establecido una relación inversa entre el diámetro de referencia del vaso y la reestenosis angiográfica 1,5,13. Dado que la elección del tamaño del balón usado en la expansión del stent depende del tamaño del vaso, Klugherz et al, identificando el tamaño del balón como predictor de reestenosis clínica, también estarían expresando la idea de que un menor diámetro de referencia del vaso se asocia a una mayor incidencia de episodios clínicos.
Así mismo, la estenosis residual alcanzó significación independiente como variable dicotómica, definida por la presencia de estenosis residual (> 0%) visual, al final del procedimiento. Esta misma variable había sido identificada por Ellis et al 2 como predictora de reestenosis angiográfica en 206 pacientes consecutivos con stents de Palmaz-Schatz. El diámetro mínimo luminal es una variable relacionada con la estenosis residual final, que también ha sido identificada como predictora de reestenosis angiográfica 3,5. Sin embargo, de los hallazgos de Serruys et al 14 en un metaanálisis se concluye que el tamaño del vaso y la estenosis residual aportan más información como predictores de reestenosis que el diámetro mínimo luminal. De hecho, la inclusión de esta última variable en estudios como el de Kastrati et al pudo hacer perder su significación independiente al diámetro de referencia del vaso, por cuanto estaría agrupando la influencia del tamaño del vaso y la estenosis residual. Por otro lado, atendiendo a los resultados de nuestro estudio, la definición más correcta de implante óptimo de un stent sería aquel resultado sin estenosis residual visible (<= 0%), frente a otras definiciones que sitúan el umbral en el 20-30%.
En concordancia con nuestros resultados, Mittal et al 2 identificaron el carácter reestenótico de la lesión como predictor independiente de reestenosis clínica y angiográfica, tras ajustar por otras variables predictoras. Otros autores también han encontrado una asociación independiente con mayores tasas de revascularización de la lesión diana 15 y reestenosis angiográfica 1,3,16. Por el contrario, algunos autores 4,17 han comunicado reestenosis similares para lesiones de novo y reestenóticas. Ante estos resultados discordantes, nuestro estudio encuentra un valor independiente para el implante de stents en lesiones reestenóticas.
El beneficio del uso de stents respecto a la angioplastia con balón resulta más evidente en la arteria descendente anterior, pero también se han publicado tasas más elevadas de reestenosis angiográfica en esta arteria que en el resto de coronarias 3,18. En nuestro estudio, el análisis univariado halló una mayor incidencia de reestenosis clínica en esta arteria coronaria que en el resto, pero que fue debida a una mayor prevalencia de diámetros menores de 3 mm en esta arteria que en otras. Este hecho nos lleva a sugerir que el valor atribuido en otros trabajos pudiera ser ocasionado por la intercurrencia de otras variables con un verdadero valor predictivo. La diabetes mellitus también ha sido identificada como predictora de reestenosis angiográfica por distintos autores 4,19, asociándola a un mayor grado de hiperplasia intimal en respuesta a la agresión del stent; sin embargo, en nuestro trabajo no alcanzó significación como predictora de reestenosis clínica. La localización ostial ha sido una variable poco estudiada con anterioridad; en nuestro trabajo no alcanzó una significación independiente debido en parte a la mayor dificultad para obtener la menor estenosis residual posible en esta localización, pero sí manifestó una tendencia hacia mayores tasas de reestenosis clínica.
Distintos estudios han identificado el implante de múltiples stents como un predictor significativo de reestenosis angiográfica 1,3 e incluso episodios clínicos 12, mientras que otros trabajos han preconizado que la longitud total de stents implantados aporta más información y es un predictor superior tras comparar ambas variables 5. Sin embargo, la importancia de estas dos variables pudiera ser secundaria al uso de anticoagulación oral en dichos trabajos, ya que estudios más recientes, con ticlopidina y aspirina y dilatación a altas presiones, no han demostrado estos peores resultados. Así, Kornowski et al 20 no encuentran diferencias ni a corto ni a largo plazo entre la implantación de tres o más stents respecto a la de uno o dos stents, y Ponde et al 21 encuentran similares resultados tras el implante de dos o más stents, que los publicados para un único stent. En nuestro trabajo, el número de stents no alcanzó ningún grado de significación, mientras que la longitud total del stent recubriendo la lesión se asoció a una tendencia no significativa hacia más reestenosis, tras el ajuste del análisis multivariado.
El análisis realizado en nuestro trabajo y el resto de los citados fue realizado sobre la base de una independencia entre las distintas lesiones, es decir, "por lesión". Sin embargo, Kastrati et al 22 investigaron la posibilidad de una dependencia en el riesgo de reestenosis entre las distintas lesiones intervenidas en un mismo paciente, de forma que en pacientes con intervención por multilesión, el riesgo de reestenosis de una lesión es 2,5 veces superior cuando alguna otra de las intervenidas desarrolló reestenosis, e independientemente de la presencia de otros factores de riesgo de reestenosis. Nuestro trabajo parece apoyar esta idea, al encontrar que, de los 8 pacientes con stents mutilesión y reestenosis clínica de una de las lesiones, más de la mitad presentaron reestenosis de otra lesión distinta durante la evolución posterior, si bien este hallazgo no tuvo carácter independiente al no ser corregido por el resto de variables predictoras de reestenosis. CONCLUSIÓN
En conclusión, el diámetro del vaso menor de 3 mm, las lesiones reestenóticas y la estenosis residual visible tras el implante del stent permiten predecir la mayoría de reestenosis clínica tras el implante de stents en una población no seleccionada. Desde un punto de vista práctico, los pacientes con una o más de estas características deben ser seguidos más estrechamente y, dado que se trata de la única variable modificable, la optimización del implante de stents debe conllevar la ausencia de estenosis residual visible al final del procedimiento.
El implante de stents intracoronarios ha permitido reducir las tasas de reestenosis respecto a la angioplastia con balón, aun cuando persisten tasas de reestenosis angiográfica intra- stent entre el 20 y el 30%. Una de las estrategias encaminadas a la mejora de estas tasas ha sido la identificación de predictores de reestenosis. Aunque han sido múltiples las variables asociadas con mayores tasas de reestenosis angiográfica, sólo algunas han sido identificadas de forma más constante en los distintos estudios publicados. Entre éstas estarían la diabetes mellitus, el menor diámetro de referencia del vaso, el carácter reestenótico de la lesión, la localización ostial, el número y longitud total de stents implantados por lesión, el implante en la arteria descendente anterior y la presencia de una mayor estenosis residual 1-6. Estudios con ultrasonidos intracoronarios han identificado una elevada relación entre el área de la placa y el área total del vaso antes del procedimiento y una menor dimensión de la luz alcanzada tras el procedimiento como los principales predictores de reestenosis 5,6.
Aunque la definición angiográfica de reestenosis coronaria evalúa su aspecto anatómico y más objetivo, la definición clínica considera su aspecto funcional y el impacto de la misma en términos de síntomas y signos de isquemia, los cuales representan el primer objetivo de tratamiento. La reestenosis clínica presenta tasas inferiores a la angiográfica; de hecho, aproximadamente sólo entre la mitad y dos tercios de los pacientes con reestenosis angiográfica se someten a nuevos procedimientos de revascularización por la presencia de síntomas 7,8. La reestenosis angiográfica intra- stent puede conducir a revascularizaciones innecesarias 9, máxime si tenemos en cuenta los estudios que demuestran un aumento en el diámetro luminal mínimo intra- stent a partir de los 6-12 meses tras el implante 10,11. Sin embargo, frente a los numerosos estudios que han evaluado predictores de reestenosis angiográfica, pocos lo han hecho respecto a la reestenosis clínica 3,12.
El objetivo de este trabajo ha sido, partiendo de los predictores descritos de reestenosis angiográfica, conocer cuáles de estas variables predicen mejor la reestenosis clínica del stent, de forma que su conocimiento pueda tener una aplicación a la práctica clínica e intervencionista habitual. PACIENTES Y MÉTODOS
Población de estudio
Desde mayo de 1995 a mayo de 1997, un total de 300 stents consecutivos fueron implantados en 278 lesiones de 234 pacientes. Todas las características demográficas, clínicas, angiográficas y del procedimiento fueron recogidas en el momento del implante del stent. Fueron susceptibles de un seguimiento a largo plazo aquellos pacientes con éxito del implante, tanto angiográfico (adecuada expansión angiográfica del stent en la lesión diana con estenosis residual menor del 30% valorada de forma visual) como clínico (ausencia de episodios mayores intrahospitalarios: muerte, infarto de miocardio o necesidad de un nuevo procedimiento de revascularización). En 218 pacientes (93%) se consideró realizar seguimiento a largo plazo. Dos pacientes (0,8%) fueron perdidos en el seguimiento, con lo que un total de 216 pacientes, con 271 stents implantados en 256 lesiones, fueron seguidos durante una media de 17,6 ± 10 meses.
Procedimiento de implante de stents
Se siguieron un total de 271 stents implantados (27,7% Palmaz-Schatz, Johnson & Johnson; 23,6% NIR, SciMed; 21,7% Multilink, ACS; 13,1% Wiktor, Medtronic; 10,5% Gianturco-Roubin, Cook; 2,2% Be-stent, Medtronic; 1,1% Wall-stent, Schneider). El procedimiento de implante fue guiado por el análisis visual de los angiogramas. La indicación del implante fue electiva en el 67%, por resultado subóptimo tras una angioplastia con balón en el 20% y por amenaza u oclusión aguda en el 13%. Previo a la expansión del stent se realizó una dilatación convencional con balón de la lesión y, tras la liberación del stent, la expansión completa de éste se alcanzó con el inflado del balón a altas presiones (15,58 ± 2,25 atm). Tras la inserción del introductor femoral se administró un bolo de 10.000 U de heparina, con posteriores bolos de 5.000 U para mantener un tiempo activado de coagulación por encima de 300 s. Tras finalizar el procedimiento, no se administró más heparina y el introductor fue retirado a las 6-8 h. Todos los pacientes recibieron tratamiento antiagregante plaquetario con aspirina (200 mg cada día) y ticlopidina (250 mg cada 12 h). La aspirina fue iniciada al menos 24 h antes del procedimiento y se continuó indefinidamente. La ticlopidina se administró inmediatamente tras finalizar el procedimiento y se mantuvo durante 4 semanas.
Episodios y seguimiento clínico
Tras el procedimiento de implante, los pacientes fueron contactados mediante visitas periódicas a la consulta hospitalaria, que constaron de entrevista, exploración física y electrocardiograma. Así mismo, a todos los pacientes se les realizó una entrevista telefónica en la fecha final de seguimiento. Ante la sospecha de reestenosis por la presencia de síntomas o signos sugestivos, se realizó una coronariografía diagnóstica. La reestenosis clínica del stent fue definida como la presencia de síntomas o signos indicativos de isquemia, junto a una estenosis angiográfica mayor del 50% en el segmento coronario con el stent implantado.
Factores de riesgo para reestenosis
Seleccionamos posibles factores de riesgo para reestenosis según la experiencia previa en predictores de reestenosis angiográfica intra- stent, los cuales fueron evaluados en forma de variables aplicables a la práctica habitual. Las variables incluidas en el análisis fueron la presencia de diabetes mellitus, el carácter reestenótico de la lesión tras una angioplastia previa, un diámetro de referencia del vaso menor de 3 mm medido en el máximo diámetro, la localización ostial de la lesión, el implante en la arteria descendente anterior, el número y la longitud total de stents implantados en la lesión y la existencia de estenosis residual angiográfica estimada de forma visual al final del procedimiento de implante del stent.
Análisis estadístico
Se estudió la asociación entre los posibles factores de riesgo y la reestenosis clínica del stent durante el seguimiento sobre la base de un análisis por lesión. En el análisis univariado, para variables categóricas se utilizó el método de Kaplan-Meier y la prueba de rango logarítmico, y para variables continuas el test de la t de Student. La identificación de asociaciones independientes se realizó mediante el análisis multivariado de Cox, incluyéndose en el modelo todas las variables con el fin de evitar la exclusión de posibles confusores. Se aceptó como significación estadística todos los valores de p < 0,05. Para el análisis estadístico se utilizó el programa SPSS (versión 7.5, bSPSS Inc.). RESULTADOS
En la tabla 1 se exponen las características basales de la población estudiada. Tras el alta hospitalaria, un total de 33 lesiones (12,9%), revascularizadas con 34 stents (12,5%), presentaron reestenosis clínica. En 3 casos (9%), la reestenosis se asoció a infarto agudo de miocardio no fatal y en un solo caso (3%) se asoció a la muerte del paciente en la espera de un nuevo procedimiento de revascularización. En el resto de casos (88%), la reestenosis se asoció a angina inestable en sus distintas formas de presentación.
En la tabla 2 se expone el resultado del análisis estadístico de posibles predictores de reestenosis clínica en nuestra población. En el análisis univariado, el implante en la arteria descendente anterior, en vasos de diámetro menor de 3 mm, en lesiones reestenóticas y en el ostium coronario se asoció de forma significativa a mayores tasas de reestenosis clínica. El análisis multivariado identificó como predictores independientes de reestenosis clínica el carácter reestenótico de la lesión, la localización en un vaso menor de 3 mm y la existencia de estenosis residual visible tras el implante. La arteria descendente anterior no alcanzó una significación independiente debido a que la mayoría de los implantes en vasos de diámetro menor de 3 mm ocurrieron en esta arteria (el 75% frente al 15%). La localización ostial perdió la significación en el análisis multivariado debido a una mayor incidencia de estenosis residual en esta localización respecto al resto de segmentos coronarios (el 33 frente al 18%), pero mantuvo una significación marginal como predictor independiente. La diabetes mellitus no se asoció a mayores tasas de reestenosis clínica en ninguno de los análisis, al igual que el número de stents por lesión. La longitud total de stent recubriendo la lesión tampoco fue un predictor significativo, si bien en el análisis multivariado se hizo patente una tendencia no significativa a mayores tasas.
En la figura 1 se observan los casos y la reestenosis clínica atendiendo a la presencia de las tres variables identificadas como predictores independientes. Estas tres variables explicaron 27 de los 33 casos de reestenosis, un 72%. El implante en vasos menores de 3 mm conllevó una incidencia de reestenosis clínica del 26%, que fue del 33% cuando se trataba de una lesión reestenótica. La existencia de estenosis residual tras el implante del stent supuso un aumento de la incidencia hasta el 50% cuando se sumó a alguna de las variables anteriores y del 11% en ausencia de dichas características. La incidencia total en presencia de una o más de estas tres variables fue del 22%, frente al 4% en ausencia de todas ellas.
Fig. 1. En cada grupo de lesiones se expresan: lesiones totales/lesiones con reestenosis clínica (porcentaje de reestenosis en el grupo).
Las 33 lesiones con reestenosis clínica se correspondieron con 28 pacientes (13%), es decir, 5 pacientes presentaron reestenosis de dos lesiones distintas. De los 40 pacientes en que se implantaron stents en dos o más lesiones distintas, ocho presentaron reestenosis de alguna lesión, de los cuales en cinco (60%) la reestenosis ocurrió en dos lesiones distintas. Es decir, en pacientes con dos o más lesiones revascularizadas con stents, la reestenosis de una de las lesiones se asoció a un riesgo del 60% para la aparición de otra reestenosis a distancia. DISCUSIÓN
En nuestra población de stents intracoronarios, tres cuartas partes de la reestenosis clínica ocurrida pudo ser predicha por la presencia de tres variables: el carácter reestenótico de la lesión, el implante en vasos menores de 3 mm y la presencia de estenosis residual visible al final del procedimiento. En ausencia de estas variables, la incidencia de reestenosis fue del 4%, frente al 22% en presencia de alguna de ellas. Otras variables identificadas como predictores de reestenosis angiográfica en trabajos previos, como la longitud del segmento con stent, la diabetes mellitus, la localización en la descendente anterior o en el del ostium coronario, no alcanzaron significación independiente como predictores de reestenosis clínica del stent.
Kastrati et al 3 estudiaron predictores de revascularización de la lesión diana guiada por síntomas en 1.349 pacientes, identificando la diabetes mellitus, el implante de múltiples stents y un menor diámetro mínimo luminal. Previamente, Klugherz et al 12 publicaron un seguimiento de 3 años en 65 pacientes con stents Palmaz-Schatz, identificando la presencia de una elevada clase de angina, un pequeño diámetro del balón usado en la expansión y un mayor número de stents implantados como predictores de episodios clínicos en el seguimiento.
En nuestro estudio, el tamaño del vaso definido por un diámetro de referencia menor de 3 mm fue un predictor independiente de reestenosis clínica a largo plazo. Otros trabajos han establecido una relación inversa entre el diámetro de referencia del vaso y la reestenosis angiográfica 1,5,13. Dado que la elección del tamaño del balón usado en la expansión del stent depende del tamaño del vaso, Klugherz et al, identificando el tamaño del balón como predictor de reestenosis clínica, también estarían expresando la idea de que un menor diámetro de referencia del vaso se asocia a una mayor incidencia de episodios clínicos.
Así mismo, la estenosis residual alcanzó significación independiente como variable dicotómica, definida por la presencia de estenosis residual (> 0%) visual, al final del procedimiento. Esta misma variable había sido identificada por Ellis et al 2 como predictora de reestenosis angiográfica en 206 pacientes consecutivos con stents de Palmaz-Schatz. El diámetro mínimo luminal es una variable relacionada con la estenosis residual final, que también ha sido identificada como predictora de reestenosis angiográfica 3,5. Sin embargo, de los hallazgos de Serruys et al 14 en un metaanálisis se concluye que el tamaño del vaso y la estenosis residual aportan más información como predictores de reestenosis que el diámetro mínimo luminal. De hecho, la inclusión de esta última variable en estudios como el de Kastrati et al pudo hacer perder su significación independiente al diámetro de referencia del vaso, por cuanto estaría agrupando la influencia del tamaño del vaso y la estenosis residual. Por otro lado, atendiendo a los resultados de nuestro estudio, la definición más correcta de implante óptimo de un stent sería aquel resultado sin estenosis residual visible (<= 0%), frente a otras definiciones que sitúan el umbral en el 20-30%.
En concordancia con nuestros resultados, Mittal et al 2 identificaron el carácter reestenótico de la lesión como predictor independiente de reestenosis clínica y angiográfica, tras ajustar por otras variables predictoras. Otros autores también han encontrado una asociación independiente con mayores tasas de revascularización de la lesión diana 15 y reestenosis angiográfica 1,3,16. Por el contrario, algunos autores 4,17 han comunicado reestenosis similares para lesiones de novo y reestenóticas. Ante estos resultados discordantes, nuestro estudio encuentra un valor independiente para el implante de stents en lesiones reestenóticas.
El beneficio del uso de stents respecto a la angioplastia con balón resulta más evidente en la arteria descendente anterior, pero también se han publicado tasas más elevadas de reestenosis angiográfica en esta arteria que en el resto de coronarias 3,18. En nuestro estudio, el análisis univariado halló una mayor incidencia de reestenosis clínica en esta arteria coronaria que en el resto, pero que fue debida a una mayor prevalencia de diámetros menores de 3 mm en esta arteria que en otras. Este hecho nos lleva a sugerir que el valor atribuido en otros trabajos pudiera ser ocasionado por la intercurrencia de otras variables con un verdadero valor predictivo. La diabetes mellitus también ha sido identificada como predictora de reestenosis angiográfica por distintos autores 4,19, asociándola a un mayor grado de hiperplasia intimal en respuesta a la agresión del stent; sin embargo, en nuestro trabajo no alcanzó significación como predictora de reestenosis clínica. La localización ostial ha sido una variable poco estudiada con anterioridad; en nuestro trabajo no alcanzó una significación independiente debido en parte a la mayor dificultad para obtener la menor estenosis residual posible en esta localización, pero sí manifestó una tendencia hacia mayores tasas de reestenosis clínica.
Distintos estudios han identificado el implante de múltiples stents como un predictor significativo de reestenosis angiográfica 1,3 e incluso episodios clínicos 12, mientras que otros trabajos han preconizado que la longitud total de stents implantados aporta más información y es un predictor superior tras comparar ambas variables 5. Sin embargo, la importancia de estas dos variables pudiera ser secundaria al uso de anticoagulación oral en dichos trabajos, ya que estudios más recientes, con ticlopidina y aspirina y dilatación a altas presiones, no han demostrado estos peores resultados. Así, Kornowski et al 20 no encuentran diferencias ni a corto ni a largo plazo entre la implantación de tres o más stents respecto a la de uno o dos stents, y Ponde et al 21 encuentran similares resultados tras el implante de dos o más stents, que los publicados para un único stent. En nuestro trabajo, el número de stents no alcanzó ningún grado de significación, mientras que la longitud total del stent recubriendo la lesión se asoció a una tendencia no significativa hacia más reestenosis, tras el ajuste del análisis multivariado.
El análisis realizado en nuestro trabajo y el resto de los citados fue realizado sobre la base de una independencia entre las distintas lesiones, es decir, "por lesión". Sin embargo, Kastrati et al 22 investigaron la posibilidad de una dependencia en el riesgo de reestenosis entre las distintas lesiones intervenidas en un mismo paciente, de forma que en pacientes con intervención por multilesión, el riesgo de reestenosis de una lesión es 2,5 veces superior cuando alguna otra de las intervenidas desarrolló reestenosis, e independientemente de la presencia de otros factores de riesgo de reestenosis. Nuestro trabajo parece apoyar esta idea, al encontrar que, de los 8 pacientes con stents mutilesión y reestenosis clínica de una de las lesiones, más de la mitad presentaron reestenosis de otra lesión distinta durante la evolución posterior, si bien este hallazgo no tuvo carácter independiente al no ser corregido por el resto de variables predictoras de reestenosis. CONCLUSIÓN
En conclusión, el diámetro del vaso menor de 3 mm, las lesiones reestenóticas y la estenosis residual visible tras el implante del stent permiten predecir la mayoría de reestenosis clínica tras el implante de stents en una población no seleccionada. Desde un punto de vista práctico, los pacientes con una o más de estas características deben ser seguidos más estrechamente y, dado que se trata de la única variable modificable, la optimización del implante de stents debe conllevar la ausencia de estenosis residual visible al final del procedimiento.
Bibliografía
[1]
Restenosis after placement of Palmaz-Schatz stents in native coronary arteries. Initial results of a multicenter experience. Circulation 1992; 86: 1836-1844.
[2]
Comparison of outcome after stenting for de novo versus restenotic narrowings in native coronary arteries. Am J Cardiol 1997; 80: 711-715.
[3]
Predictive factors of restenosis after coronary stent placement. J Am Coll Cardiol 1997; 30: 1428-1436.
[4]
Predictors of restenosis after coronary stent implantation. J Am Coll Cardiol 1998; 31: 1291-1298.
[5]
Angiographic and intravascular ultrasound predictors of in-stent restenosis. J Am Coll Cardiol 1998; 32: 1630-1635.
[6]
Intravascular ultrasound predictors of angiographic restenosis in lesions treated with Palmaz-Schatz stents. J Am Coll Cardiol 1998; 31: 43-49.
[7]
A comparison of balloon-expandable-stent implantation with balloon angioplasty in patients with coronary artery disease. N Engl J Med 1994; 331: 489-495.
[8]
A randomized comparison of coronary-stent placement and balloon angioplasty in the treatment of coronary artery disease. N Engl J Med 1994; 331: 496-501.
[9]
BENESTENT-II trial: subgroup analysis of patients assigned either to angiographic and clinical follow-up or clinical follow-up alone. Circulation 1997; 96 (Supl 1): 653.
[10]
Three-year follow-up after implantation of metallic coronary-artery stents. N Engl J Med 1996; 334: 561-566.
[11]
Remodeling of in-stent neointima, wich became thinner and transparent over 3 years: serial angiographic and angioscopic follow-up. Circulation 1998; 97: 2003-2006.
[12]
Three-year clinical follow-up after Palmaz-Schatz Stenting. J Am Coll Cardiol 1996; 27: 1185-1191.
[13]
Vessel size and long-term outcome after coronary stent placement. Circulation 1998; 98: 1875-1880.
[14]
Periprocedural quantitative coronary angiography following Palmaz-Schatz stent implantation predicts restenosis rate at 6 months: result of a meta-analysis of Benestent-I, Benestent-II and Music [resumen]. J Am Coll Cardiol 1998; 31 (Supl A): 64.
[15]
Clinical and angiographic predictors of target lesion revascularization after stent placemente in native coronary lesions. Circulation 1997: 96 (Supl 1): 2637.
[16]
Effect of prior coronary restenosis on the risk of subsequent restenosis after stent placement or directional atherectomy. Am J Cardiol 1994; 73: 1147-1153.
[17]
Prior restenois does not increase the risk of restenosis following coronary stenting: an analysis from the Stent Anticoagulation Regimen Study (STARS) Trial. Circulation 1997: 96 (Supl 1): 594.
[18]
The clinical and angiographic evolution of dilated lesions in the proximal segment of the anterior descending coronary artery: stent versus balloon. Rev Esp Cardiol 1999; 52: 181-188.
[19]
Diabetes Mellitus and the Clinical and Angiographic Outcome after Coronary Stent Placement. J Am Coll Cardiol 1998; 32: 1866-1873.
[20]
Procedural results and late clinical outcomes after placement of three or more stents in single coronary lesions. Circulation 1998; 97: 1355-1361.
[21]
Multiple stent implantation in single coronary arteries: acute results and six-month angiographic follow-up. Cathet Cardiovasc Diagn 1997; 42: 158-165.
[22]
Interlesion dependence of the risk for restenosis in patients with coronary stent placement in multiple lesions. Circulation 1998; 97: 2396-2401.