Palabras clave
La trombosis de una válvula protésica (TVP) es una complicación que puede comprometer seriamente la vida del paciente. El recurso terapéutico tradicional ha sido la reoperación, con trombectomía o sustitución de la válvula afectada. La tasa de mortalidad de este procedimiento es importante; series selectas1-5 la cifran en un 15%, pero alguna otra comunicación6 la eleva hasta el 38%, que tal vez está más en consonancia con la realidad.
La trombólisis constituye una clara alternativa al tratamiento quirúrgico. Se ha referido una tasa de éxito en torno al 80%, pero el procedimiento tiene el inconveniente de producir complicaciones embólicas (20%) y hemorragias mayores (5%) que conducen a una mortalidad aproximada del 6%7-17. Por otra parte, en los casos de TVP sin obstrucción, cuya incidencia aumenta por el empleo creciente de la ecocardiografía transesofágica (ETE), pueden ser prácticas apropiadas la perfusión intravenosa de heparina o la simple optimización del tratamiento antitrombótico (OTAT), entendiendo como tal la restitución del INR (razón normalizada internacionalmente) al rango terapéutico y la adición de una pequeña dosis (80-100 mg) de aspirina18.
En el momento actual no está bien definida la modalidad terapéutica más adecuada para estos pacientes, especialmente para los que presentan un cuadro obstructivo grave. El objeto de este estudio es revisar la experiencia de dos hospitales terciarios en el manejo de esta complicación, tratando de responder a la pregunta clave: ¿cuál es el tratamiento inicial más apropiado?
PACIENTES Y MÉTODO
A través de los registros del laboratorio de ecocardiografía, servicio de medicina intensiva y servicio de cirugía cardiovascular de ambos hospitales se identificaron 47 pacientes que habían sido diagnosticados de TVP durante el período 1991-1998.
Mediante un formulario diseñado al efecto se recogieron datos demográficos, variables clínicas, especialmente en lo que respecta a la forma de presentación, técnicas utilizadas en el diagnóstico, modalidad de tratamiento aplicado, evolución hospitalaria de todos los pacientes y evolución tardía de aquellos en los que constaban datos de seguimiento en la historia clínica. La gravedad del cuadro clínico de presentación fue evaluada subjetivamente en una escala de 0 a 4 (0 = asintomático; 1 = poco sintomático; 2 = sintomático estable; 3 = grave; 4 = muy grave). La información adquirida fue incorporada a la hoja de cálculo del programa estadístico GraphPad Prism (versión 2.0, GraphPad Software, San Diego, Ca) para su procesamiento y posterior análisis. Las diferencias entre datos cuantitativos se evaluaron con el test de la t de Student, apareado o no según el caso. Las diferencias porcentuales se analizaron con el test exacto de Fisher. La curva de supervivencia se construyó con el método de Kaplan-Meier.
RESULTADOS
Características de los pacientes
La edad media del grupo era de 55 ± 12 años (rango, 10-75 años) y el 70% eran mujeres. Ningún enfermo tenía prótesis en posición tricuspídea. Todas, pues, eran izquierdas: doble (mitral y aórtica) en 10 casos, mitral en 30 y aórtica en siete. Sólo el 17% de los enfermos (5 prótesis aórticas y 3 mitrales) estaban en ritmo sinusal.
El episodio de TVP se diagnosticó a los 8 ± 6 años (rango, 25 días-19 años) de la operación original. En 41 de los 47 casos había una determinación del INR al ingreso, encontrándose valores subterapéuticos (INR entre 2 y 2,4) en 3 casos y anticoagulación ineficaz (INR < 2) en más de la mitad (23/41) en los que pudo analizarse este dato. En 7 casos había antecedentes recientes de tratamiento anticoagulante irregular, debido a hemorragia digestiva (n = 3), hemorragia cerebral intraparenquimatosa (n = 1), hematoma subdural (n = 1) o intervención quirúrgica no cardíaca (n = 2).
Prótesis valvulares involucradas
En un solo caso la trombosis afectaba a dos prótesis. En el resto, la afección era de una sola prótesis. En la tabla 1 se recogen el tipo y la localización de las prótesis afectadas por la trombosis.
Presentación clínica
En 2 enfermos asintomáticos (grupo I) el diagnóstico se hizo por el hallazgo de trombo protésico en el curso de un ETE, realizado para la valoración de una fuga periprotésica pequeña en un caso y previo a choque eléctrico de un aleteo auricular en el otro. En 10 casos (grupo II) hubo un episodio de embolismo sistémico como causa fundamental de la exploración ecocardiográfica. En 31 casos (grupo III) los síntomas eran derivados de obstrucción protésica. Por último, en 4 casos (grupo IV), a la sintomatología de obstrucción protésica se añadía embolismo reciente. En la tabla 2 se resume la agrupación por síntomas de los 47 pacientes.
Diagnóstico
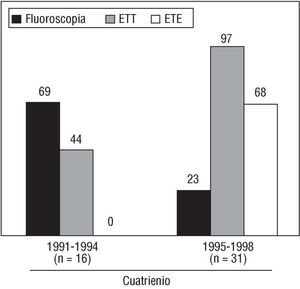
Al tratarse de una serie extendida a lo largo de 8 años, las técnicas diagnósticas utilizadas fueron variables. Así, en un hospital carente durante años de facilidades para la realización de ecocardiografía se utilizó exclusivamente la cinefluoroscopia con intensificador de imágenes para el diagnóstico de sus 9 primeros casos; en un caso adicional fue imposible realizar ecografía por problemas logísticos y, asimismo, se empleó únicamente la fluoroscopia. En el resto de la serie (n = 37) se utilizó el ecocardiograma transtorácico (ETT), acompañado de ETE en 21 casos y de fluoroscopia en siete. En la figura 1 se aprecia cómo se dobló el número de diagnósticos en el segundo cuatrienio; aunque no se puede excluir un aumento de la población expuesta al riesgo, lo lógico es atribuir este incremento a la mejora del equipamiento ecocardiográfico y, sobre todo, a la introducción del ETE en ambos hospitales. La fluoroscopia, que ejerció un papel diagnóstico importante en el primer cuatrienio fue, desafortunadamente, mucho menos utilizada en el segundo.
Fig. 1. Tasa de utilización de las tres técnicas consideradas, según el cuatrienio en el que se efectuó el diagnóstico. En el segundo cuatrienio se dobló el número de diagnósticos, muy probablemente debido al empleo del ETE que no se había podido utilizar en el primero. Desafortunadamente, el uso de la fluoroscopia declinó sobremanera en el segundo cuatrienio. ETE: ecocardiograma transesofágico; ETT: ecocardiograma transtorácico.
En la tabla 3 se consignan los hallazgos diagnósticos obtenidos en cada grupo. La alta incidencia de material trombótico en los grupos I y II se explica porque, al no existir obstrucción protésica, su presencia era requisito imprescindible para el diagnóstico; algo similar sucede en cuanto a la alta incidencia de anomalías en el movimiento del oclusor protésico en el grupo III, ya que fue imperativo diagnóstico en los 10 casos que fueron evaluados exclusivamente por fluoroscopia.
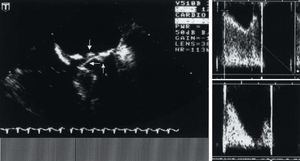
Los 25 casos (26 prótesis) de los grupos III y IV que fueron explorados con ultrasonidos constituyen un subgrupo que permite establecer comparaciones entre el potencial diagnóstico del ETT y del ETE. Se puede ver (tabla 4) que el ETE fue significativamente superior al ETT en la detección de material trombótico, pero no en la visualización de anomalías en el desplazamiento del oclusor protésico (fig. 2).
Fig. 2. Imagen transesofágica en diástole (panel de la izquierda) de una prótesis mitral de doble disco con obstrucción trombótica. La apertura de ambos discos es muy pobre, de apenas 30o (flecha horizontal y flecha apuntando hacia arriba), lo que impide que se produzca la típica imagen de lentes verticales y paralelas cuando el ángulo de apertura es normal (alrededor de 85o). En la cara auricular de la prótesis, independiente del anillo protésico, se aprecia una imagen esferoidal, con densidad ultrasónica media, muy sugestiva de trombo (flecha apuntando hacia abajo). En el panel de la derecha se presenta la velocimetría Doppler mitral del paciente, antes (arriba) y a las 24 h del tratamiento con t-PA. Son muy evidentes los cambios (disminución de la velocidad máxima e incremento en la pendiente de desaceleración diastólica) inducidos por el tratamiento trombolítico. El tiempo de hemipresión pasó de 246 ms a 108 ms y el enfermo, que tenía disnea grado IV, quedó asintomático.
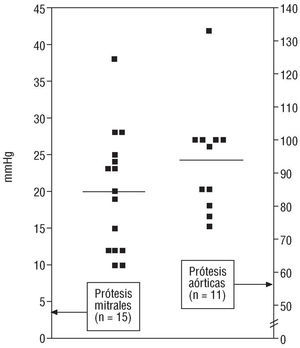
En la figura 3 se aprecia la distribución del gradiente diastólico medio de las 15 prótesis mitrales de los grupos III y IV que fueron exploradas con Doppler. En los 2 casos con obstrucción intermitente, el gradiente variaba considerablemente y se tomó como referencia el de mayor cuantía. En la misma figura está la distribución de los gradientes transvalvulares máximos de las 11 prótesis aórticas con obstrucción. Como en la circunstancia anterior, se anotó el gradiente mayor en el único caso con dificultad intermitente del oclusor. La magnitud de todos los gradientes parecía ofrecer pocas dudas sobre su significado patológico.
Fig. 3. Distribución del gradiente diastólico medio en 15 prótesis mitrales con trombosis obstructiva (izquierda) y del gradiente sistólico máximo en 11 prótesis aórticas con el mismo problema. La raya horizontal indica el valor medio de los respectivos gradientes.
Tratamiento inicial realizado
Grupo I. En un paciente se aplicó OTAT. El otro fue tratado con una perfusión i.v. de heparina no fracciona da durante 72 h. Este último caso fue seguido con ETE, constatándose la desaparición del material trombótico.
Grupo II. En 7 casos el tratamiento consistió en perfusión de heparina durante un período de tiempo que osciló entre 72 h y 10 días. Una enferma falleció por embolismo cerebral repetitivo durante la hospitalización. Dos casos fueron tratados únicamente con OTAT. Otro, finalmente, fue intervenido, realizándose una trombectomía; la operación, en este caso, vino justificada por la magnitud y exagerada movilidad del trombo, que hacía temer un accidente embólico. En los 4 casos en que se hizo seguimiento con ETE (tres de tratamiento con heparina y uno con tratamiento antitrombótico oral) se comprobó la desaparición del trombo.
Grupos III y IV. Dos pacientes (una prótesis aórtica y otra mitral) fueron tratados con heparina. En el primero, que había rehusado la trombólisis, el gradiente transaórtico se redujo desde 133 hasta 85 mmHg; la enferma, que estaba en situación clínica aceptable, rechazó también la propuesta de intervención. En el caso de la prótesis mitral hubo una mejoría franca de la situación clínica y normalización en el movimiento del oclusor vigilado por fluoroscopia.
El tratamiento inicial de los 33 pacientes restantes consistió en trombólisis para 19 y cirugía para 14. La trombólisis se realizó en 6 prótesis aórticas y 13 mitrales, mientras que la cirugía directa se planeó en 3 prótesis aórticas y 10 mitrales, así como en el único caso que tenía doble trombosis mitroaórtica. Al analizar diversas variables (edad, gravedad del cuadro clínico, antecedente reciente de embolismo cerebral, imagen de trombo en el eco y cuatrienio en que se presentó el acontecimiento) sólo se encontraron diferencias entre el grupo de trombólisis y el de cirugía en lo que respecta a la gravedad del cuadro clínico: índice de gravedad de 3,3 ± 0,6 en el grupo sometido a trombólisis, frente a 2,1 ± 0,9 en el de cirugía (p < 0,0001). Se apreció también una tendencia a que la edad fuese superior en los pacientes del grupo de trombólisis (56 ± 10 años frente a 48 ± 14 años en el grupo de cirugía; p = 0,06).
Tratamiento trombolítico
El fibrinolítico usado fue t-PA, salvo en 3 casos en que se empleó estreptocinasa. Las dosis de t-PA fueron distintas según el hospital; en uno se empleó una dosis fija de 100 mg; en el otro, las dosis fueron mayores: 143 ± 8 mg (rango, 100-200 mg). Todos los enfermos sobrevivieron. No hubo ninguna hemorragia mayor y sí 4 leves (una epixtasis y tres en la zona de punción venosa). Ocurrieron 4 episodios embólicos, todos cerebrales, uno de los cuales dejó secuelas hemipléjicas.
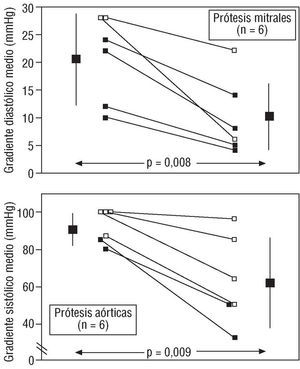
El resultado del tratamiento, en cuanto a la sintomatología, fue considerado como excelente o de franca mejoría en 15 de los 19 casos; de mejoría parcial en tres y de ausencia de mejoría en uno. Los 7 casos con prótesis mitral y exclusiva monitorización fluoroscópica fueron dados de alta en buena situación clínica (n = 6) o mejoría parcial (n = 1). Los 12 pacientes restantes (6 prótesis mitrales y 6 aórticas) tenían seguimiento de la evolución del gradiente (fig. 3). Como se puede apreciar (fig. 4), el gradiente se redujo de forma manifiesta en nueve de los 12 casos, de forma ligera en dos y no hubo modificación en uno. Seis enfermos fueron operados antes del alta: un caso por la nula reducción del gradiente; cuatro (3 prótesis aórticas, una de las cuales además tenía material trombótico subprotésico, y una mitral) porque, a pesar de la reducción, persistían con un gradiente elevado; uno, finalmente, porque, a pesar de la gran mejoría y la dramática reducción del gradiente, seguía con movimiento anómalo de una de las lentes; en la operación se encontró un pequeño trombo que dificultaba el movimiento.
Fig. 4. Evolución del gradiente tras tratamiento trombolítico en 6 prótesis mitrales (panel superior) y 6 prótesis a& oacute;rticas. Los cuadros vacíos corresponden a los enfermos que fueron operados antes del alta hospitalaria. El marcador con barra corresponde al valor medio del gradiente y la desviación estándar.
En cuatro de los 5 casos operados por persistencia manifiesta del gradiente se encontró material trombótico, con pannus asociado en 2 casos. Una prótesis aórtica, sin embargo, pareció normal, sin trombo ni excrecencia fibrosa. Este caso, con un gradiente pico de 100 mmHg, inmodificado a las 48 h de la trombólisis, a pesar de la desaparición de la imagen de un pequeño trombo, se operó a los 5 días del último control con Doppler. La normalidad intraoperatoria de la prótesis significa que se trataba de un falso positivo por desproporción prótesis-paciente o, más probable, al tratarse de una prótesis de doble disco, que se hubiese registrado alta velocidad espúrea proveniente del orificio central que delimitan ambos discos. Una explicación alternativa es que el problema obstructivo se hubiese resuelto en el tiempo que medió entre el último control y la operación.
Tratamiento quirúrgico como elección inicial
En cinco de los 14 casos con TVP obstructiva en los que se optó de entrada por la cirugía se daba una razón en la historia clínica. En 2 enfermos porque tenían prótesis mitrales biológicas en las que al proceso trombótico se añadían signos degenerativos de las valvas; en uno porque había tenido una hemorragia cerebelosa reciente; en dos, por último, porque el trombo era «muy grande», en uno de ellos con la circunstancia añadida de hemorragia vaginal activa. En los 9 casos restantes no figuraba ninguna razón específica de por qué se había optado por la cirugía directa en vez de por el tratamiento trombolítico.
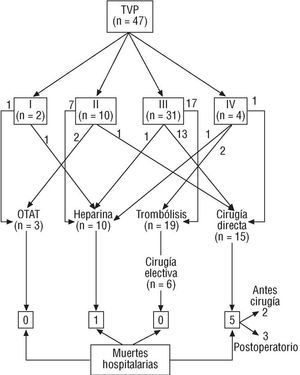
De los 14 pacientes con intención de cirugía como tratamiento primario, 5 fallecieron: dos antes de poder ser operados (uno en la inducción anestésica a las 12 h del ingreso; el otro, por parada cardíaca irrecuperable a las 72 h del ingreso, cuando se encontraba en una situación clínica que parecía estable), y tres en el postoperatorio. Como en el grupo de trombólisis no falleció ningún paciente, si bien seis, como hemos visto, precisaron la intervención antes de abandonar el hospital, la diferencia de mortalidad con la cirugía fue significativa (p = 0,008) al hacer un análisis según intención de tratar. En la figura 5, a modo de resumen, se presenta un diagrama de flujo con el tratamiento aplicado y la mortalidad hospitalaria en cada grupo.
Fig. 5. Diagrama de flujo en el que se pormenoriza el tratamiento aplicado en cada grupo y el número de muertes hospitalarias observadas. OTAT: optimización del tratamiento antitrombótico; TVP: trombosis valvular protésica.
Evolución tardía
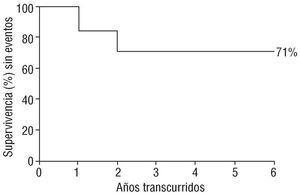
Como hemos visto, 6 pacientes (uno del grupo II, sometido a perfusión de heparina no fraccionada, y 5 del grupo de cirugía directa) fallecieron durante su estancia hospitalaria. Los 41 enfermos restantes fueron dados de alta en buena situación clínica, a excepción de una enferma que quedó con hemiplejía residual manifiesta tras embolismo en el curso de la trombólisis. Hubo seguimiento tardío del 71% (29/41) de los pacientes dados de alta. Tres fallecieron de causa no cardíaca (enfermedad pulmonar obstructiva crónica, cáncer de colon y cáncer de mama, respectivamente) (fig. 6). En los otros 26 enfermos ha habido un total de 7 acontecimientos tromboembólicos en la evolución: 2 recidivas de TVP obstructiva, con fallecimiento en un caso, 4 episodios embólicos aislados y un embolismo recurrente. La recidiva de un acontecimiento obstructivo ocurrió en 2 pacientes cuyo episodio primario había sido tratado con trombólisis en un caso y mediante cirugía directa en el otro. En esta ocasión, ambos fueron sometidos a trombólisis; en el primero, precisamente el que falleció, porque era la única alternativa terapéutica viable, al padecer el enfermo una insuficiencia respiratoria restrictiva muy severa que ya había condicionado 19 meses antes la elección terapéutica del episodio primario; en el otro, la trombólisis, que resultó efectiva, fue elegida por no volver a realizar una intervención quirúrgica, cuando aún no habían transcurrido 6 meses de la anterior. De los 5 enfermos con embolismo, cuatro pertenecían al grupo II y uno al grupo III; este último había sido sometido 21 meses antes a tratamiento trombolítico efectivo. En conjunto, algo más de la cuarta parte de los pacientes seguidos tuvieron un accidente tromboembólico posterior; en la figura 6 se presenta la curva de supervivencia sin episodio tromboembólico para estos 26 pacientes, apreciándose que todos los accidentes ocurrieron en los dos primeros años del acontecimiento índice.
Fig. 6. Curva de supervivencia sin evento trombótico en 26 pacientes que fueron seguidos a largo plazo después del alta hospitalaria. Casi un 30% de los pacientes se vieron afectados por un nuevo accidente tromboembólico en los 2 años que siguieron al acontecimiento índice.
DISCUSIÓN
La TVP, si bien rara, es una complicación temible, razón por la cual el cardiólogo debe estar bien familiarizado con ella. El proceso ocurre fundamentalmente en las válvulas mecánicas, pero tampoco las biológicas, como en dos de nuestros casos, están exentas del problema19. La presentación clínica es muy variable, pudiendo ir desde un completo silencio hasta un cuadro muy grave por obstrucción aguda de la prótesis. Nuestro material, siguiendo la clasificación de Lengyel et al20, ha sido ordenado en 4 grupos: ausencia de síntomas (I), presencia de embolismo (II), síntomas derivados de obstrucción protésica (III) y asociación de embolismo a los síntomas obstructivos (IV).
El problema de la trombosis no obstructiva
El signo princeps del diagnóstico es la visualización de una imagen sugestiva de trombo en el interior o en los aledaños de la prótesis afectada por el proceso. Ciertamente no puede ser de otro modo para los pacientes de los grupos I y II que no tienen los otros dos signos capitales derivados de la trombosis protésica: las anomalías en el movimiento del oclusor y el gradiente patológico.
No se conoce a ciencia cierta la sensibilidad del ecocardiograma para detectar trombosis protésica. Evidentemente, dependerá de la habilidad y experiencia del explorador, pero aun siendo éstas grandes, los trombos pequeños, que pueden ser clave en la disfunción protésica, son de difícil detección, especialmente si asientan en la cara ventricular de una prótesis mitral. En este sentido, cuanto más grande es el trombo y más se extiende fuera del entorno protésico, más fácil es su visualización. Sí queda clara, como en otras circunstancias clínico-ecocardiográficas, la superioridad del ETE sobre el ETT20,21, como se refleja en nuestra serie (tabla 4). Esto es lo que ha hecho, y nuestra experiencia lo refleja claramente (fig. 1), que el diagnóstico de TVP se haya incrementado claramente, a expensas de enfermos de los grupos I y II, por el uso creciente del ETE.
Esta nueva situación nos lleva a formular algunas preguntas: ¿es útil para el paciente que ha sufrido un episodio de embolismo, y no tiene gradiente patológico en el ETT, ser sometido a las molestias de un ETE?; si se descubre un trombo en la exploración ecocardiográfica, ¿se debe realizar tratamiento trombolítico, perfusión prolongada de heparina, o simplemente aplicar OTAT? Nuestro estudio no da respuesta a estos interrogantes, pero lo cierto es que con cualquier tipo de terapia, transcurrido un tiempo prudencial, hemos visto desaparecer la imagen de material trombótico. En un estudio no aleatorizado se afirma que la trombólisis es superior al tratamiento con heparina23, pero es necesaria, a nuestro juicio, una mayor experiencia antes de recomendar con firmeza el tratamiento al que se deben someter los enfermos con TVP no obstructiva.
Laffort el al24 han ido más allá en la investigación del problema tromboembólico explorando de forma sistemática con ETE, a los 9 días y 5 meses de la operación, a un número muy considerable de pacientes con prótesis, divididos en 2 grupos: uno con anticoagulación oral y otro con la adición de 200 mg diarios de aspirina. Las enseñanzas fundamentales de este estudio son dos: a) que la prevalencia de imagen de trombo (9,1%), y sobre todo de hebras (strands [47%]) es muy elevada, y b) que si bien la aspirina reduce los episodios embólicos, tanto mayores (0,9 frente a 4,1% en el grupo sin aspirina) como menores (7,5 frente a 20,8% en el grupo sin aspirina), esta ventaja se ve empañada por la mayor incidencia de hemorragia gastrointestinal (7 frente a 0% en los que no tomaban aspirina). Los mismos autores reconocen que una dosis de aspirina menor (80-100 mg) podría ser tan eficaz como la usada por ellos (200 mg), pero menos gastrotóxica.
El problema diagnóstico de las prótesis obstructivas
En los casos de los grupos III y IV, lo primordial es la obstrucción protésica y, por tanto, la existencia de un gradiente patológico. La conceptuación de un gradiente protésico como patológico, especialmente si estamos tratando de una prótesis aórtica, no es un problema sencillo. En primer lugar, la velocidad de la que deriva el gradiente puede cambiar enormemente con las variaciones del flujo, en especial si la prótesis es de pequeño tamaño, de forma que, con flujos elevados, las velocidades y gradientes pueden alcanzar cifras que normalmente se consideran expresión de estenosis protésica25. Se ha propuesto, para obviar este problema, la utilización del cociente entre la velocidad a través de la prótesis y la del tracto de salida, índice que sería independiente del flujo e identificaría mejor la disfunción protésica estenótica que el gradiente aislado26,27. Este cociente, si bien es independiente de las variaciones del flujo, está relacionado, obviamente, con el diámetro del tracto de salida; por eso, las comparaciones interindividuales, si el índice no se ha corregido por el citado factor anatómico, han de hacerse con cuidado. Su utilidad reside sobre todo en el seguimiento longitudinal de un paciente dado, en el cual se supone que las dimensiones del tracto de salida no varían a lo largo del tiempo. El otro problema interpretativo de la velocidad derivada del Doppler y, en consecuencia, del gradiente transprotésico, es la existencia de velocidades elevadas en el orificio central tuneliforme de las prótesis de doble disco27,28. Esta alta velocidad del orificio central es muy superior a la de los orificios laterales y no refleja la velocidad media global ni el gradiente de presión neto a través de todo el orificio funcional de la válvula. Este problema de velocidades espúreas en las prótesis de doble disco es más pronunciado en las válvulas aórticas que en las mitrales; además, en estas últimas es más fácil mediante ETE identificar y obtener velocidades selectivas del orificio central y de los laterales28.
Si el gradiente se acompaña de imagen trombótica y anomalías en el movimiento del oclusor protésico, el diagnóstico es definitivo. Ya hemos visto, sin embargo, las limitaciones que tiene la ecografía en la detección de la trombosis. En lo referente a la restricción del movimiento de las lentes protésicas, se trata de un signo subjetivo en el que la experiencia del explorador tiene gran importancia. Interesa, además, resaltar la superioridad de la fluoroscopia sobre el ETT para detectar trastorno en el movimiento del mecanismo oclusor29. Por ello, es desafortunado el hecho de que en nuestra práctica hayamos ido abandonando progresivamente la cinefluoroscopia a favor de la ecografía (fig. 1). Ambas técnicas, por sus distintas propiedades y su carácter no invasivo, son complementarias30 y deberían ser practicadas en todo paciente con sospecha de TVP antes de la realización, llegado el caso, de un ETE.
Si una vez hechas las anteriores consideraciones sobre el gradiente concluimos que éste es patológico pero se trata del único dato diagnóstico disponible, surgen dudas razonables sobre la naturaleza del problema obstructivo: ¿se trata de una obstrucción trombótica, que debería ser sometida a trombólisis, de un sobrecrecimiento de tejido fibroso anular (pannus) que sólo tiene tratamiento quirúrgico o, simplemente, de una prótesis de pequeño tamaño que, especialmente a nivel aórtico, puede originar un gradiente muy sustancial?31. El problema de la desproporción (mismatch) prótesis-paciente no produce un cuadro clínico agudo32 y, en todo caso, no hay restricción en el movimiento de las lentes protésicas; de aquí la importancia de examinar con fluoroscopia al paciente.
Más compleja es la distinción entre TP y pannus, teniendo en cuenta, además, la frecuente coexistencia de ambos fenómenos29, como sucedió en dos de nuestros pacientes. Ambas patologías pueden producir cualquiera de los signos que venimos considerando: imagen de masa, anomalías en el movimiento de la prótesis y gradiente patológico. En un estudio paralelo hemos examinado este problema, mediante la comparación de 12 pacientes en los que la obstrucción protésica, comprobada en el acto operatorio, era debida exclusivamente a pannus, con 25 de los enfermos de esta serie33. Las principales características clínicas diferenciales de ambos procesos fueron la antigüedad de la prótesis, siempre mayor de 5 años en el pannus y muy variable, como hemos visto, en la TVP; cuadro clínico crónico en el pannus, frente a agudo o subagudo en la TVP; mayor incidencia de embolismo previo, anticoagulación deficiente e imagen evidente de masa en las TVP. Barbetseas et al34 han referido unos hallazgos diferenciales muy parecidos a los nuestros, añadiendo el dato de que una masa de mayor superficie y, sobre todo, con una menor densidad ultrasónica es muy sugerente de trombosis como causa fundamental de la obstrucción protésica. De todas formas, todos estos datos clínicos son meramente orientativos y la distinción, desde el punto de vista individual, resulta siempre incierta.
Tratamiento de la TVP obstructiva: ¿trombólisis o cirugía?
Es una disyuntiva en discusión, pero parece que la terapia médica va ganado adeptos20. No existe, que sepamos, ningún estudio aleatorizado que compare estas dos modalidades terapéuticas. La información disponible procede de estudios observacionales35,36 similares al presente. Aun así, algunas consideraciones son pertinentes.
La primera es que, como refleja nuestra experiencia, la mortalidad de la trombólisis parece ser menor que la de la cirugía; en nuestro caso esta ventaja podría haber sido aún más contundente, si se tiene en cuenta que los pacientes sometidos a trombólisis tenían un índice de gravedad superior al de los operados. Otra ventaja de la trombólisis es su rapidez de aplicación; no está claro el tiempo que tarda el trombolítico en desocluir, aunque sea parcialmente, una prótesis trombosada, pero es probable que sea menor del que se consigue con la cirugía, cuya puesta en marcha necesita un despliegue logístico considerable. Esto, junto con un riesgo con claridad inferior al de la operación, hace especialmente atractivo el tratamiento trombolítico para los pacientes en situación crítica37.
El embolismo sistémico (10-20%) es la complicación más frecuente del tratamiento trombolítico13-17. En nuestra serie, la incidencia (4/19) fue similar a la citada pero, afortunadamente, salvo en un caso, fueron episodios menores que no dejaron secuela. Se ha considerado, a este respecto, que la visualización de un trombo grande (> 5 mm), sobre todo si es auricular y móvil, constituye una contraindicación para la trombólisis debido al mayor riesgo emb&oac ute;lico15,38; sin embargo, este criterio no es tenido en cuenta por otros autores, que atribuyen el embolismo más a la velocidad de perfusión del fármaco que al tamaño o la movilidad del trombo17.
Las hemorragias mayores no constituyen un problema frecuente; de todas formas es buena práctica, que nosotros no hemos seguido sistemáticamente, realizar una TAC craneal a todo paciente con embolismo cerebral reciente para descartar un área sobreañadida de hemorragia que podría agravarse con la trombólisis.
No está claro tampoco el agente trombolítico que se debe utilizar. Probablemente sean la estrepto y urocinasa con los que más experiencia se tiene20. Nosotros hemos utilizado con mucha mayor frecuencia el t-PA, al que se le ha atribuido un mayor riesgo embólico que a los otros dos agentes20, precisamente por su mayor rapidez y contundencia fibrinolíticas. Recientemente, sin embargo, se ha demostrado la efectividad y seguridad del t-PA16, que tiene la ventaja, caso de que hubiese que recurrir a la cirugía urgente por fracaso de la trombólisis, de un menor efecto lítico sistémico. Tampoco está bien definida la pauta de administración: infusión continua de la dosis total, dosis total en bolo, bolo pequeño seguido de infusión, o doble bolo. En cuanto a la duración del tratamiento, parece que por encima de las 24 h no se produce beneficio añadido y habría que recurrir, en caso de fracaso parcial o completo, a nuevas dosis del mismo agente utilizado u otro distinto36.
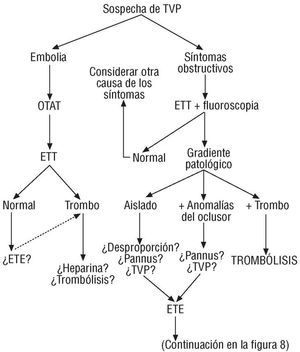
La estreptocinasa tiene la ventaja de un considerable menor precio. Un estudio reciente17, en el que la mayoría de los enfermos fueron tratados con este agente, propone una pauta original de tratamiento. Consiste en administrar el fármaco en infusión lenta (60.000 a 100.000 U/h), sin dosis de carga previa, durante una sesión de 15-24 h. Al término de la misma se reexamina con ETE al paciente y, si persiste el problema trombooclusivo, se administra una nueva infusión de 1.500.000 U. Si después de estas dos sesiones continúa el problema, se administran 100 mg de t-PA (10 mg en bolo, seguidos de una perfusión con la dosis restante durante unas 5 h). Con esta pauta repetitiva lenta y en dosis discretas, los autores sostienen que se incrementa el éxito de la trombólisis, desde un 53% tras la primera sesión hasta un 88% tras dos o más sesiones, al tiempo que se minimiza considerablemente el riesgo embólico. En nuestra opinión, esta pauta lenta puede ser apropiada para los pacientes con TVP subaguda o crónica, pero no parece aconsejable para los enfermos críticos que necesitan una desobstrucción rápida, aun a costa de aumentar el riesgo de embolia. Con todo lo que antecede hemos elaborado un algoritmo de actuación (figs. 7 y 8) que puede ser de utilidad en el manejo de estos pacientes.
Fig. 7. Algoritmo propuesto para el tratamiento de los pacientes con sospecha de TVP. Abreviaturas como en las figuras anteriores.
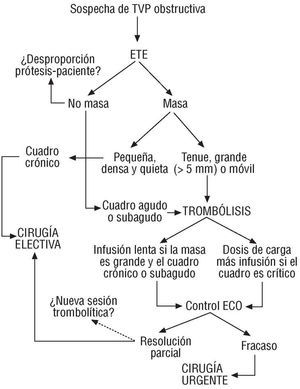
Fig. 8. Continuación del algoritmo.
Es evidente que el resultado de la trombólisis debe ser seguido muy de cerca mediante ecocardiografía que verifique la normalización de la disfunción protésica. Se han propuesto exploraciones repetidas con ETE39, pero probablemente baste con el ETT-Doppler en la mayoría de las ocasiones40. Es corriente referir el resultado de la terapia trombolítica en términos de éxito o fracaso; nosotros pensamos, y tenemos buenos ejemplos de ello, que hay resultados subóptimos, en el sentido de que baja el gradiente pero aún queda lejos de la normalidad. Es posible que estos casos puedan beneficiarse de una segunda tanda trombolítica, pero nosotros hemos optado por la intervención quirúrgica como forma de resolver definitivamente el problema, en parte guiados por el hecho de que puede haber un pannus subyacente que constituya un nido favorecedor de retrombosis41. Creemos también que, aun cuando el resultado de la trombólisis sea subóptimo, producto de una resolución incompleta del proceso trombótico o de pannus concomitante, el tratamiento proporciona beneficio clínico en los pacientes críticos, pues permite afrontar la operación en un entorno de menor riesgo.
Seguimiento del paciente
El enfermo que ha padecido un episodio de TVP tiene un riesgo elevado de sufrir un nuevo accidente tromboembólico. En nuestra serie, algo más de la cuarta parte de los 26 pacientes seguidos a largo plazo tuvieron embolismo o recurrencia de TVP. Es evidente, pues, que el tratamiento antitrombótico debe ser vigilado con un rigor especial, manteniendo un INR que no baje de 2,5 y añadiendo entre 80 y 100 mg diarios de aspirina18,20. No una dosis mayor, puesto que en ese caso, como hemos comentado previamente, el riesgo de hemorragia excede al de tromboembolismo24. Además, si el tratamiento, facultativo u obligado, ha sido la sustitución valvular, cabe plantearse en ese momento la inserción de una prótesis menos trombogénica. Si el paciente tiene la edad adecuada para ello, una buena alternativa puede ser una de las nuevas prótesis de pericardio, cuya durabilidad, a tenor de la información más reciente42,43, parece excelente.
Limitaciones del estudio
Este trabajo adolece de ser retrospectivo. Además, el largo período transcurrido desde el primero hasta el último enfermo hizo que las pautas diagnósticas y terapéuticas fuesen cambiantes a lo largo del tiempo y, en consecuencia, poco homogéneas. En realidad, sólo un trabajo prospectivo y aleatorizado, multicéntrico por fuerza, ya que la complicación motivo de discusión es, afortunadamente, muy poco frecuente6, podría dar respuesta cumplida a muchas de las preguntas aquí enunciadas. La imprecisión de muchos de los informes quirúrgicos revisados impide saber con exactitud la frecuencia de pannus sobreañadido al proceso trombótico. Por último, la información referente a la evolución tardía de los pacientes debe ser tomada con cautela, puesto que sólo fueron seguidos el 71% de los mismos. Aun con estas reservas, y hasta donde llega nuestro conocimiento, este trabajo constituye la mayor aportación cuantitativa que se haya hecho en lengua hispana sobre el problema de la TVP.
Implicaciones clínicas
El principal hallazgo de este estudio retrospectivo es que, al menos en nuestro medio, la trombólisis constituye una alternativa mejor que la cirugía para enfrentarse al grave problema de la TVP obstructiva. Aun en el caso frecuente de que el resultado de la trombólisis sea subóptimo, permite operar al paciente en mejores condiciones clínicas y, por tanto, con un menor riesgo. En cuanto a la TVP no obstructiva, no queda claro todavía si una evaluación y tratamiento agresivos constituyen una pauta mejor que la simple exploración con ETT y la OTAT. En todo caso, el paciente que ha sufrido una TVP sigue teniendo un alto riesgo de recidiva tromboembólica que obliga a mantener de forma continuada una cuidosa terapia antitrombótica.
Correspondencia: Dr. J. Azpitarte. Servicio de Cardiología. Hospital Universitario Virgen de las Nieves. Avda. de las Fuerzas Armadas, 2. 18014 Granada. Correo electrónico: jazpitarte@eresmas.com Recibido el 19 de diciembre de 2000. Aceptado para su publicación el 24 de mayo de 2001.