Palabras clave
INTRODUCCIÓN
En este artículo se analizan los avances y las novedades publicados durante el período de julio de 2004 a julio de 2005 en el campo de la cardiología pediátrica y las cardiopatías congénitas.
Se hace referencia a los nuevos métodos de diagnóstico en cuanto a técnicas de imagen, tanto de la ecocardiografía tridimensional (3D), como de la resonancia magnética (RM) y del Doppler tisular.
También se comentan algunos avances en el campo del intervencionismo fetal respecto a las indicaciones y técnicas empleadas.
Se revisan las novedades en cardiología intervencionista en cuanto a los nuevos dispositivos para el cierre de las comunicaciones interventriculares y de comunicaciones vasculares anómalas, y también las últimas publicaciones respecto al tratamiento quirúrgico en las cardiopatías congénitas.
AVANCES EN TÉCNICAS DE IMAGEN
La introducción de una nueva tecnología, o incluso la utilización de un nuevo método basado en técnicas ya existentes, conlleva la demostración de su utilidad y, a la vez, de las mejoras o ventajas que comporta.
Ecocardiografía Doppler
En el campo de la ecocardiografía Doppler, la aparición del Doppler tisular, la ecocardiografía 3D, etc., ha dado lugar a la publicación de una serie de artículos que ha puesto de manifiesto tanto su utilidad como sus posibles indicaciones y ventajas en comparación con la ecocardiografía bidimensional (2D)-Doppler convencional. En cualquier caso, no debemos olvidar que la disponibilidad de estas nuevas tecnologías no abarca todos los laboratorios de ecocardiografía, por lo que en la práctica clínica resultan especialmente interesantes los trabajos en los que se intenta obtener el máximo rendimiento de la aplicación de técnicas sistemáticas.
El ventrículo derecho (VD) tiene un papel muy especial dentro del mundo de las cardiopatías congénitas, especialmente cuando actúa como ventrículo sistémico o cuando ha sido sometido a agresiones quirúrgicas que pueden alterar su funcionalismo. Es, pues, importante disponer de una metodología que permita detectar y cuantificar alteraciones, tanto de su función sistólica como diastólica. Ello no es una tarea fácil, dada la especial geometría de esta cavidad. Ciertamente, a diferencia de lo que ocurre con el ventrículo izquierdo (VI), no es posible calcular la fracción de eyección del VD (FEVD) a partir de la aplicación de una fórmula matemática sencilla, basada en diámetros obtenidos por ecocardiografía en modo M o 2D. La RM ha demostrado ser la técnica más fiable para el estudio del VD, pero su práctica, especialmente en niños (¿sedación?, disponibilidad, traslado, coste, etc.) puede presentar ciertas dificultades, por lo que resultan de especial interés los estudios en los que se compara la información obtenida con dicha técnica con la obtenida a través de la aplicación de la ecocardiografía 2D-Doppler, el Doppler tisular, la ecocardiografía 3D, etc.
En cuanto a la ecocardiografía en modo M y 2D podemos mencionar el trabajo de Li et al1, donde se evaluó el acortamiento longitudinal del ventrículo sistémico (morfológicamente derecho) medido a través del desplazamiento del anillo tricuspídeo, en pacientes que se habían sometido a una intervención de Mustard, y se correlacionó con el consumo máximo de oxígeno con ejercicio. Se observó que, en comparación con un grupo control, el desplazamiento longitudinal estaba reducido, tanto en situación basal como después de la administración de dobutamina; asimismo, el análisis multivariable demostró que dicho acortamiento era el único predictor independiente de la capacidad de ejercicio. Los autores concluyeron que dicho índice debe ser considerado en la valoración periódica de este tipo de pacientes.
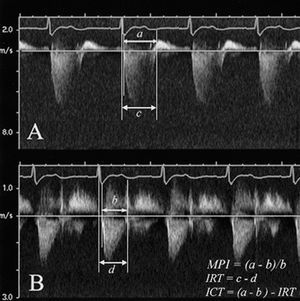
Salehian et al2, considerando el cálculo de la FEVD por RM como el patrón de referencia para la valoración de la función ventricular derecha, llevaron a cabo un estudio retrospectivo en 29 pacientes con un ventrículo sistémico morfológicamente derecho (11 con transposición corregida de los grandes vasos y 18 con transposición de los grandes vasos tras corrección fisiológica por la técnica de Mustard o de Senning), a los cuales, tras practicar un ecocardiograma 2D-Doppler determinaron el «índice de función miocárdica del VD o índice Tei» (RVMPI, Right Ventricular Myocardial Performance Index) (fig. 1); observaron que había una fuerte correlación negativa entre el RVMPI y la FEVD medida por RM (r = -0,82; p < 0,01) y que la FEVD podía ser estimada mediante la fórmula: 65% - (45,2 x RVMPI), llegando a la conclusión de que el MPI podía ser utilizado en pacientes con ventrículo sistémico, morfológicamente derecho, para valorar su función sistólica. Sin duda son necesarios nuevos estudios de tipo prospectivo, y con un mayor número de pacientes, que confirmen dicho hallazgo.
Fig. 1. Cálculo del RVMPI (Right Ventricular Myocardial Performance Index). A: Registro por ecocardiografía Doppler continua de la regurgitación tricuspídea (válvula auriculoventricular sistémica) en un paciente con D-Transposición de los grandes vasos que había sido sometido a una corrección fisiológica tipo Mustard. B: el mismo paciente que en A. Registro por ecocardiografría Doppler pulsado del flujo a través del tracto de salida ventricular derecho. a: corresponde al intervalo entre el inicio y el cese de la insuficiencia tricuspídea. b: corresponde al tiempo de eyección del ventrículo sistémico morfológicamente derecho. ICT: tiempo de contracción isovolumétrica; IRT: tiempo de relajación isovolumétrica. Tomada de Salehian et al2.
Otra técnica de más reciente introducción y que empieza a demostrar su papel en la valoración funcional del VD de los pacientes con una cardiopatía congénita (CC) es el Doppler tisular, ya sea de forma aislada o en combinación con la ecocardiografía 2D-Doppler convencional. Así, por ejemplo, Harada et al3 observaron que en niños con una tetralogía de Fallot corregida quirúrgicamente, las velocidades tisulares, tanto sistólicas (S'), como diastólicas (E', A'), medidas en el anillo tricuspídeo y en comparación con un grupo control, eran menores. Asimismo, observaron que había un menor incremento de las velocidades tisulares sistólicas con el ejercicio, lo que era más evidente en presencia de una insuficiencia pulmonar severa. El cambio en el pico sistólico de velocidad tisular con el ejercicio mostraba una buena correlación con el dP/dt ventricular derecho obtenido a partir de la curva del registro por Doppler continuo de la insuficiencia tricuspídea. Concluyeron que en pacientes con una tetralogía de Fallot corregida, esta técnica podía ser útil para valorar el efecto del ejercicio sobre el ventrículo derecho; así, un incremento insuficiente de las velocidades tisulares sistólicas durante el esfuerzo podía ser expresión de una alteración del funcionalismo ventricular derecho y de la repercusión de la insuficiencia pulmonar sobre él.
En el campo de la ecocardiografía 3D, nuevos artículos han aportado información sobre la utilidad de dicha técnica en el estudio de las CC, y especialmente de los defectos septales4. Ciertamente, en el estudio de las comunicaciones interauriculares (CIA), y dado que la ecocardiografía 3D permite una mejor visualización y cuantificación del área del defecto5, parece que puede ser especialmente útil para valorar las posibilidades de cierre percutáneo o, una vez indicado éste, para facilitar la colocación del dispositivo oclusor6,7. Más aún, su capacidad para proporcionar una imagen casi real del dispositivo puede facilitar la valoración de su correcta o incorrecta implantación y/o de una posible deformación que éste pueda causar sobre las estructuras vecinas como, por ejemplo, la aorta.
La detección prenatal (a poder ser dentro de las primeras 20-22 semanas de gestación) de una posible CC, a través de la ecocardiografía fetal, es un reto importante, pero muchas veces difícil de realizar. La introducción de innovaciones tecnológicas que mejoren la calidad de las imágenes fetales es un elemento fundamental. La ecocardiografía 3D utilizando información obtenida a partir del Doppler tisular (no se dispone de señal electrocardiográfica), para sincronizar la reconstrucción de la imagen tridimensional en relación con el ciclo cardíaco, parece que puede proporcionar imágenes dinámicas 3D de alta calidad8.
Resonancia magnética
Otra técnica que ya ha demostrado su utilidad en el terreno de las de las CC es, sin duda, la RM con todas sus posibilidades: secuencias spin-echo, secuencias gradient-echo, secuencias gradient-echo ultrarrápidas, mapa de velocidades del flujo por análisis de fase, etc., de tal modo que, especialmente en adultos y sobre todo en pacientes con una CC compleja operada, se ha convertido en una exploración de gran ayuda y a veces fundamental.
Como hemos citado previamente, en la valoración morfológica y funcional del VD, la RM se considera el patrón de referencia con que comparar cualquier nueva técnica o metodología. A ello hay que añadir la publicación, en pacientes con una CC, de nuevos estudios en los que se valora la información obtenida a través de la inyección de contraste paramagnético, gadolinio-DTPA, y el estudio por RM de las zonas con realce tardío en las paredes del VD. Babu-Narayan SV et al9 estudiaron a 36 pacientes con una transposición completa de los grandes vasos y cirugía de redirección auricular, y observaron que en 22 había realce tardío con gadolinio en las paredes del ventrículo sistémico, morfológicamente derecho, y que la extensión de dicha captación se correlacionaba con la edad, la disfunción ventricular, algunos parámetros electrofisiológicos y ciertos eventos clínicos, como arritmias y/o síncope. Así pues, y como ya ha sido puesto de manifiesto en otras cardiopatías, como la miocardiopatía hipertrófica, la RM con inyección de gadolinio y valoración de las zonas con realce tardío podría también tener un valor pronóstico en este tipo de pacientes.
Tomografía computarizada con multidetector
La indicación de la práctica de una tomografía computarizada (TC) con multidetector puede estar en relación con el tipo de anomalía cardíaca o con la presencia de contraindicación a la práctica de una RM, como ocurre en pacientes portadores de un marcapasos o de un desfibrilador automático implantable. En el primer caso, la TC con multidetector ha demostrado ser especialmente útil en el estudio de las enfermedades coronarias10,11, si bien en niños pequeños, la frecuencia cardíaca elevada puede dificultar la obtención de imágenes de buena calidad. Cuando se utiliza en lugar de la RM, es necesario comprobar que la información obtenida es superponible a ésta, tanto en el ámbito anatómico, como funcional12, a la vez que recordar la dosis de irradiación que dicha técnica comporta, lo que debe limitar su indicación.
En general, los trabajos de correlación entre TC y RM han mostrado una buena concordancia entre la información obtenida por ambos métodos, pero cabe citar el trabajo de Hager et al13, en el que se comparan los diámetros de la aorta torácica en pacientes adultos con una coartación aórtica (la mayoría de ellos tras corrección quirúrgica) obtenidos por TC helicoidal y RM. Los autores observaron una tendencia hacia unas cifras ligeramente inferiores (como media) en las mediciones obtenidas por RM (1,2 mm), pero en casos concretos la diferencia alcanzó los 9 mm. Lógicamente, ello es importante y debe tenerse en cuenta en la valoración periódica de este tipo de pacientes a través de técnicas de imagen.
CARDIOLOGÍA FETAL
Intervencionismo cardíaco fetal
Junto con el avance en el diagnóstico de las CC intrauterinas, cabe resaltar los avances en intervencionismo fetal como un método para modificar la historia natural de la cardiopatía y prevenir el hidrops.
En este aspecto, es interesante el trabajo de Tworetzky y Marshall14, donde se comentan diversos aspectos de esta técnica y se proporciona una idea de la dificultad para llevarla a cabo: acceso al feto, anestesia materna, equipamiento necesario, así como de sus posibles complicaciones. El acceso al feto puede realizarse por vía percutánea, guiada por ecocardiografía, a través de la pared abdominal materna, el útero, el feto y el corazón fetal, o a través de una laparotomía materna, exponiendo el útero y desde allí, por vía percutánea, acceder al feto.
El intervencionismo fetal en la actualidad queda limitado a las cardiopatías siguientes (Huhta et al15):
- Síndrome de hipoplasia de cavidades izquierdas (SHCI) con foramen oval (FO) atrésico o restrictivo.
- Estenosis aórtica crítica.
- Estenosis pulmonar crítica con FO restrictivo.
En el SHCI con cierre precoz o restricción del FO se produce un aumento de la presión vascular pulmonar fetal que condiciona un mal pronóstico en el nacimiento. En estos casos se puede intentar una apertura o dilatación del FO (septostomía con balón) intrauterino; Marshall et al16 lo intentaron en 7 fetos, lográndolo en 6, pero hubo una muerte fetal posprocedimiento y 4 muertes neonatales. Los autores concluyen que, aunque la septostomía se puede realizar con seguridad para la madre, los resultados todavía no son óptimos y es necesario mejorar los aspectos técnicos para lograr la descompresión de la aurícula izquierda.
En la estenosis aórtica crítica diagnosticada en la época fetal, la valvuloplastia aórtica serviría para mejorar el flujo en el VI y promover su crecimiento. Los criterios de selección para realizarla serían: válvula aórtica estenótica, pero permeable; VI adecuado; válvula mitral normal; flujo retrógrado en el arco aórtico y shunt izquierda derecha en el FO (Huhta et al15). Tworetzky et al17 realizaron una dilatación aórtica a 20 fetos de 24 afectados de estenosis aórtica crítica (21-29 semanas de gestación) y consiguieron una dilatación efectiva en 14, demostrando en el seguimiento una clara diferencia en el tamaño del VI entre los fetos en los que no se logró abrir la válvula (con detención del crecimiento) y los casos en los que la valvuloplastia fue efectiva. Para que la valvuloplastia sea efectiva será necesaria una posición fetal adecuada que favorezca la punción (con o sin laparoscopia).
Otra indicación para la práctica de una valvuloplastia podría ser la estenosis pulmonar crítica cuando se acompaña de FO restrictivo. En estos casos, el aumento de la presión auricular derecha condiciona la aparición de hidrops, lo cual podría evitarse con una valvuloplastia pulmonar.
En conclusión, el intervensionismo cardíaco fetal está en vías de desarrollo y para que avance es necesario que mejore la tecnología (Huhta et al15):
- Láser: la perforación del septo auricular con láser cuando es muscular y no es posible la dilatación con balón. Se ha realizado en animales, pero no se ha probado en humanos.
- Catéteres más pequeños que permitan actuar en edades de gestación más tempranas.
- Endoscopia: visualizar directamente la válvula puede ayudar a valorar si es permeable o no.
Recomendaciones tras el diagnóstico de cardiopatía fetal
Cuando se diagnostica una CC fetal, el cardiólogo prenatal requiere habilidad para dar la información y debe basarse no sólo en el pronóstico de la cardiopatía, sino también en la edad gestacional, los potenciales cambios, las malformaciones asociadas y los resultados conocidos del tratamiento. El consejo efectivo es tan importante como llegar al diagnóstico correcto; en este sentido es interesante el trabajo de Allan y Huggon18, en el que realiza una escala de valoración de las CC según su pronóstico y evolución (tabla 1), con una puntuación de 1 la menos severa, entre 3 y 6 las que pueden ser reparadas aunque con dificultad hacia una anatomía normal, y del 7 al 10 las más complejas (generalmente univentriculares). Es una tabla orientativa que pretende ayudar al facultativo a dar la mejor opción de pronóstico y tratamiento.
AVANCES EN DIAGNÓSTICO Y TRATAMIENTO MÉDICO
El diagnóstico de una miocarditis puede ser difícil, dado que por ecocardiografía lo único que apreciamos es una dilatación del VI con una disminución de la fracción de eyección, lo mismo que podemos observar en una miocardiopatía dilatada (MD) En este aspecto es interesante el artículo de Soongswang et al19, en el que se valora el uso de las troponinas cardíacas T (cTnT) como un indicador no invasivo para el diagnóstico de miocarditis en el niño. Se clasifica a los pacientes en 3 grupos: uno con sospecha clínica de miocarditis, otro con el diagnóstico de MD y un tercero con CC tipo comunicación interventricular (CIV), en fase de insuficiencia cardíaca congestiva (ICC), con un total de 43 casos; los autores demuestran que los valores de cTnT eran significativamente más altos en los casos de miocarditis aguda, con un punto de corte para el diagnóstico de 0,052 ng/ml.
Por otro lado, también parece interesante un estudio realizado por Cohen et al20 que valoran si la determinación de los valores plasmáticos de propéptido natriurético cerebral aminoterminal (N-BNP) permite diferenciar entre una ICC y una neumopatía en lactantes con dificultad respiratoria aguda que acuden a urgencias, así como si dichos valores son útiles para valorar el efecto del tratamiento en lactantes con esta enfermedad. En este estudio se analizan los valores en 17 lactantes con ICC y se comparan con los 18 que ingresan por neumopatía y 13 controles, detectando que en los primeros los valores de N-BNP fueron significativamente más altos (mediana 18,452 pg/ml; límites 5,736-99,700) que en los niños con neumopatía (mediana 311 pg/ml; límites 76-1.341), o que en los controles sanos (mediana 89 pg/ml; límites 88-292). Así pues, según los autores, el límite de N-BNP que serviría para diferenciar entre un lactante cardiópata de uno con neumopatía estaría en 2.940 pg/ml, y por encima de esta cifra el valor predictivo positivo en un paciente cardiópata es del 100%. Además, también observan un descenso significativo de los valores del N-BNP en los casos con ICC después del tratamiento. Estos hallazgos permitirían tener un nuevo parámetro para el diagnóstico rápido y preciso en un servicio de urgencias pediátricas ante el lactante con dificultad respiratoria aguda, así como también para valorar la mejoría de la función cardíaca en los lactantes con ICC.
Tratamiento médico
Respecto al tratamiento inmunodepresor en las miocarditis, varios estudios en adultos demuestran que no es efectivo, en niños hay más discusión y hay pocos casos descritos. Gagliardi et al21 hacen un estudio prospectivo en 114 niños con MD. Realizan una biopsia y los dividen en 3 grupos según la histología: grupo A (miocarditis aguda con células inflamatorias); grupo B (miocarditis borderline) y grupo C (sin miocarditis). Junto con el tratamiento convencional, en los grupos A y B asocian inmunodepresores (ciclosporina y prednisona) durante 6 meses y, según la evolución histológica posterior, suspenden el tratamiento o lo prolongan hasta 1 año. La supervivencia fue del 96% al año y del 83% a los 13 años en los grupos A y B, frente al 61% al año y el 32% a los 13 años en el grupo C. En cuanto al trasplante cardíaco o muerte: grupo A 1/35 (3%), grupo B 10/35 (29%), grupo C 30/44 (68%). En los grupos A y B la recuperación de la fracción de eyección fue parcial o completa en los primeros 6 meses, pero no en el grupo C.
Estos autores concluyen que la mejor supervivencia a largo plazo de estos niños probablemente fue debida a la inmunodepresión. Es un estudio interesante, pues es una serie larga (114 casos pediátricos), pero no es un estudio doble ciego donde se compare a los tratados con immunodepresión con los tratados con tratamiento convencional y en el que la decisión del tratamiento se basa en la biopsia, la cual no está exenta de riesgos. Entre los riesgos del tratamiento inmunodepresor está una posible persistencia de la infección viral y en el estudio no consta si se valora la persistencia del virus con proteína C reactiva y serología.
Otro tema interesante es la utilización del enalapril para la prevención de la dilatación aórtica en pacientes con síndrome Marfan, tal como se refiere en el artículo publicado por Yetman et al22, donde se incluyó de forma prospectiva a 58 pacientes con afección cardiovascular. Su edad media era de 12 años y se realizó un seguimiento de 3 años. A 32 se les administró enalapril (2,5 mg/ 2 veces al día); a 24, atenolol (niños con peso > 12,5 kg, en una dosis inicial de 1 mg/kg/día); y a 2, propanolol (peso < 12,5 kg, en una dosis de 1 mg/kg/2 veces al día). Los autores constataron que el grupo tratado con enalapril presentaba una mejoría de los parámetros valorados (distensibilidad aórtica, reducción del índice de rigidez), así como un menor incremento del diámetro de la raíz aórtica. En cualquier caso, serán necesarios nuevos estudios que confirmen estos resultados.
Respecto al tratamiento de la hipertensión arterial pulmonar (HAP) en niños, la prostaciclina ha demostrado una reducción de la mortalidad y una mejoría de los síntomas funcionales, pero su administración en forma de infusión intravenosa continua limita su indicación en niños. El bosentano (un bloqueador de los receptores A y B de la endotelina) se administra por vía oral y ha demostrado su efecto beneficioso en adultos y niños. Sobre este aspecto trata el trabajo de Rosenzweig et al23, que estudiaron a 86 niños con HAP arterial idiopática, asociada a cardiopatía congénita o a conectivopatía, con clase funcional (OMS) I-IV, a los cuales administró bosentano solo o asociado con un prostanoide. La mediana de tratamiento fue 14 meses (2-28 meses). En un 46% mejoró la clase funcional, mientras que en el 44% no se modificó. La presión arterial pulmonar y las resistencias pulmonares disminuyeron de forma significativa durante el tratamiento. La supervivencia al año fue del 98% y a los 2 años del 91%. Los autores concluyen que el bosentano administrado solo o asociado con un prostanoide es seguro y puede ser eficaz para tratar la HAP en el niño.
Por otro lado, respecto al tratamiento con bosentano en los casos de HAP severa y síndrome de Eisenmenger, es interesante un estudio reciente de Apostolopoulou et al24 en el que se valora el tratamiento con bosentano en 21 pacientes con HAP y cardiopatía (reparada o no), 15 con síndrome de Eisenmenger. Los pacientes estaban en clase funcional II-IV y recibieron bosentano durante 16 semanas. Con el tratamiento hubo una mejoría de la clase funcional, la capacidad de ejercicio (duración ejercicio en cinta rodante, test de marcha de 6 min y consumo máximo de O2) y de los parámetros hemodinámicos (la presión arterial pulmonar media pasó de 87 ± 4 a 81 ± 4 mmHg, el gasto cardíaco pulmonar pasó de 3,2 ±0,4 a 3,7 ± 0,5 l/min/m2 y la relación flujo pulmonar/flujo sistémico pasó de 1,2 ± 0,2 a 1,4 ± 0,2, así como también del índice de resistencias vasculares pulmonares). Respecto a este tema, destaca también el trabajo de Christensen et al25, que hacen un estudio retrospectivo en 9 pacientes con síndrome de Eisenmenger y clase funcional III-IV, a los que tratan con bosentano; estos autores consiguen una mejoría en 6 de ellos (67%), con un aumento de la clase funcional y un incremento en la saturación de O2 del 79 ± 5 al 88 ± 6% (p = 0,03).
Según estos resultados, parece ser que el bosentano mejora a corto y medio plazo los parámetros clínicos, de ejercicio y hemodinámicos en los pacientes con HAP relacionada con una CC, así como en los casos asociados con síndrome de Eisenmenger, mejorando la oxigenación y la clase funcional con efectos secundarios mínimos.
Respecto al tratamiento con carvedilol en niños con miocardiopatía, Rusconi et al26 hacen una revisión de 24 casos diagnosticados de MD (edad media 7,2 ± 6,4 años), con FEVI < 40%, a los que se añadió carvedilol al tratamiento convencional, de 14,3 a 23,3 meses después del diagnóstico. La dosis inicial y la máxima fueron: 0,15 ± 0,09 y 0,98 ± 0,26 mg/kg/día. Veintidós pacientes toleraron el carvedilol con un seguimiento de 26,6 ± 14,7 meses, mejorando su fracción de eyección del 24,6 ± 7,6 al 42,2 ± 14,2%; hubo una mejoría de su clase funcional en 15, 1 murió y 3 fueron trasplantados. Según los autores, la adición de carvedilol al tratamiento convencional mejora la función cardíaca y los síntomas, y es bien tolerado, aunque se precisa un control adecuado por si empeora la insuficiencia cardíaca o se desencadena asma.
Los bloqueadores beta (BB) están considerados como tratamiento de elección en los pacientes con el síndrome del QT largo (SQTL). Para valorar el efecto de los BB en niños con SQTL, Villain et al27 revisan la evolución de 122 casos (edad media 6,4 ± 3,7 años). El diagnóstico se hizo en el primer mes de vida en 26 pacientes (en 7 se detectó bradicardia intrauterina). Los dividieron en dos grupos: sintomáticos (n = 61) y asintomáticos (n = 61), estos últimos pertenecientes a formas familiares, clasificándolos además según el valor del QTc, el sexo y el genotipo, de acuerdo con la estratificación de riesgo propuesta por Priori et al28. En 64 casos se utilizó nadolol, en 30 propanolol y en 10 acebutolol.
Se hizo un cribado de las mutaciones en 118 casos y se detectaron en 48 de los pacientes sintomáticos y en 56 de los asintomáticos, sin ninguna diferencia en su distribución (KCNQ1 en 61, HERG en 36, SCN5A en 2 y 5 tenían 2 mutaciones).
Hubo 4 pacientes que murieron. Los 118 supervivientes fueron seguidos durante 7,5 ± 5,3 años con sólo BB. Se implantó un marcapasos profiláctico en 8, de los cuales 5 eran recién nacidos, debido a bloqueo auriculoventricular 2/1.
Los autores concluyen que la evolución de los niños tratados correctamente con BB fue buena y el 95,5% estuvo asintomático (no se detectaron eventos cardíacos en los pacientes con la mutación KCNQ1, ni en los diagnosticados por la historia familiar).
Cuando a pesar del tratamiento con BB haya síntomas o persista la arritmia, recomiendan hacer un estudio de los genotipos para identificar otros tipos de SQTL con genotipo diferente al KCNQ1, que pueden precisar un tratamiento adicional con marcapasos o desfibrilador implantable, como los recién nacidos con LQT2 y trastornos del comportamiento, los casos de pacientes con LQT3, así como en los casos en que se detecten 2 mutaciones en el mismo paciente.
ARRITMIAS
El síndrome de Wolf-Parkinson-White (WPW) se observa frecuentemente en niños asintomáticos y es difícil valorar el riesgo real de presentar una arritmia que pueda conducir a una muerte súbita. Varios autores han intentado valorar la eficacia del estudio electrofisiológico (EEF) en niños asintomáticos con síndrome de WPW para estratificar el riesgo de presentar una arritmia grave. Así, Sarubbi et al29 hacen un estudio retrospectivo en 62 niños (edad 9,8 ± 5,1 años), asintomáticos, con síndrome de WPW, a los que realizaron un EEF para valorar el riesgo de arritmia. Durante el estudio, 36 (58%) presentaron una taquicardia auriculoventricular (TAV) por reentrada (22 en situación basal y 14 después de administrar isoproterenol), y 9 presentaron una fibrilación auricular (FA). Concluyen que hay una proporción importante de niños sanos con preexcitación que puede tener una TAV por reentrada o una FA durante el EEF.
También es interesante, aunque controvertido, el trabajo realizado por Pappone et al30 en el que estudian la eficacia de la ablación por radiofrecuencia en niños asintomáticos con WPW. Para ello hacen un EEF a 165 afectados (edad entre 5-12 años); 105 los consideran de bajo riesgo para arritmias y 60 de alto riesgo. Estos últimos los dividen en dos grupos, según practiquen o no ablación (20 ablación y 27 no ablación). Durante el seguimiento (34 meses) 1 niño (5%) del grupo ablación presenta arritmia (TAV) y 12 (44%) del grupo control (TAV o FA, con fibrilación ventricular en 2 y muerte súbita en 1).
De los 105 pacientes de bajo riesgo, el 8% tuvo arritmias (TAV en 6 y FA en 2). Los autores proponen que los niños con WPW en los que durante el EEF no se induzca arritmia, o se induzca una FA de menos de 30 s, no requieren ablación por radiofrecuencia, y los casos en que se induzca TAV por reentrada o FA de más de 30 s deberían someterse a un estudio de mapeo detallado y ablación profiláctica de todas las vías accesorias.
Para evitar el riesgo que supone el EEF en los niños en cuanto al procedimiento invasivo, algunos autores (Brembilla-Perrot et al31) hacen el EEF por vía transesofágica en niños con WPW (13 con síntomas, 25 con TAV y 32 asintomáticos), detectando un 22% de arritmias potencialmente malignas en niños asintomáticos.
La valoración de un EEF para determinar el riesgo de arritmia en niños asintomáticos con WPW dependerá de la edad del niño, dado que los menores de 5 años pueden tener una resolución espontánea, y también de la actividad deportiva que realice. En todo caso tendrá que hacerse una valoración individual del riesgo/beneficio del procedimiento.
La FA es rara en niños y adolescentes, y generalmente se asocia con CC o miocardiopatía. Se ha descrito una forma familiar de FA y también casos de FA aislada en adolescentes; a este aspecto se refiere el artículo publicado por Nanthakumar et al32, en que se describen los hallazgos electrofisiológicos y la evolución después de la ablación por radiofrecuencia en una serie consecutiva de 9 adolescentes con FA sin cardiopatía estructural. La FA era paroxística en 6 y permanente en 3, y dos de ellos tenían una miocardiopatía inducida por la taquicardia. En todos fracasó el tratamiento antiarrítmico. En 5 casos encontraron que el foco estaba en las venas pulmonares, en 2 en la aurícula izquierda, en 3 en la crista terminalis y en 1 caso en la crista y las venas pulmonares. La ablación fue un éxito en 8 casos. En el seguimiento (35 meses), 2 tuvieron recaídas. Las limitaciones del estudio es la exclusión de las formas secundarias de FA.
CARDIOPATÍAS CONGÉNITAS EN ADULTOS
El avance de la medicina y sobre todo de la cirugía ha dado lugar a que las CC no sean sólo una problemática de la edad pediátrica. Se estima que un 85% de los pacientes que nacen con una CC alcanzara la edad adulta y que, de éstos, un 40% requerirá a lo largo de su vida un control y un tratamiento médico y/o quirúrgico especializado.
Engelfriet et al33, a partir de datos procedentes de registro europeo (Euro Heart Survey), han publicado recientemente una descripción de la población europea de adultos con una CC, de su morbilidad y mortalidad durante un período de 5 años. Se observa que es una población joven, con una mortalidad relativamente baja, pero con una morbilidad elevada en dicho período. En cualquier caso, es importante mencionar que la inclusión de pacientes en este registro tenía carácter retrospectivo y era totalmente voluntaria, por lo que no es posible descartar un sesgo en la inclusión.
Afortunadamente, si hace escasos años sólo podíamos hablar de tratamiento quirúrgico para la corrección de determinadas CC, en la actualidad disponemos de técnicas percutáneas que pueden resolver muchos problemas, algunos de ellos derivados de una cirugía previa. En la población adulta, Faella34, en su artículo publicado en Revista Española de Cardiología, exponen las aplicaciones actuales de dicha técnica en el tratamiento de las CC del adulto, en el que comunica la experiencia de su grupo en anomalías como la estenosis pulmonar valvular, la estenosis aórtica valvular, la coartación aórtica, la recoartación posquirúrgica, la estenosis de las ramas de la arteria pulmonar, la CIV, la comunicación interventricular, el ductus arteriosus persistente y las embolizaciones arteriales. Estos autores concluyen que el tratamiento intervencionista en las CC del adulto es un procedimiento factible y de bajo riesgo, que sus indicaciones son cada vez más frecuentes, algunas de primera elección, y es posible realizarlo a cualquier edad, incluso en pacientes de alto riesgo, si bien, como en todo procedimiento intervencionista, la curva de aprendizaje es obligatoria.
En la población de adultos con una CC, un grupo importante está constituido por los pacientes con hipertensión pulmonar y, concretamente, por los pacientes que se enmarcan dentro del denominado síndrome de Eisenmenger. De especial interés resulta la lectura del artículo de Bouzas y Gatzoulis35, en el que se hace una revisión completa, a la vez que de fácil lectura, de este síndrome, de su repercusión en otros órganos y sistemas, y de sus escasas posibilidades terapéuticas, a la vez que se mencionan las nuevas opciones farmacológicas de que disponemos en la actualidad, pero resaltando la escasez de estudios que permitan su aplicación de manera indiscriminada.
CARDIOLOGÍA INTERVENCIONISTA
La cardiología intervencionista continúa ampliando sus campos de actuación. Respecto al cierre de la CIA ostium secundum con dispositivo Amplatzer, se refieren series con seguimientos más prolongados que confirman los buenos resultados iniciales36. El riesgo de perforación cardíaca es mayor con dispositivos de diseño más traumático, pero aun con el Amplatzer se producen en alrededor del 0,1% de los pacientes implantados, por lo que debe vigilarse este aspecto en el seguimiento37.
Desde hace algunos años realiza el cierre percutáneo de la CIV. En defectos membranosos se han publicado los resultados con el dispositivo Amplatzer® membranous VSDO38,39. Se trata de series iniciales, con un seguimiento corto, en pacientes por lo general mayores y con defectos más bien pequeños. El procedimiento es técnicamente complejo, pero los resultados son muy esperanzadores. Debemos esperar series más amplias, evoluciones mayores y mayor precisión en las indicaciones. Otros dispositivos utilizados en CIV membranosa son el parche transcatéter de Sideris40 y el Pfm VSD Nitinol Coil, utilizado también para CIV musculares41.
El cierre percutáneo de CIV musculares con Amplatzer® Muscular VSDO presenta las mismas dificultades técnicas que el de las membranosas, pero la indicación es más clara por el menor riesgo de lesionar estructuras valvulares y sistema de conducción42. Otros dispositivos utilizados para CIV musculares son Clamshell Septal Occluder y sus modificaciones (CardioSEAL® y STARFlex®)43.
En ausencia del stent pediátrico ideal, continúan valorándose nuevos diseños, como el stent premontado Palmaz-Génesis, de bajo perfil y aplicable como tratamiento paliativo en niños pequeños44; por otro lado, se amplía la experiencia con el stent Cheatham-Platinum (CP stent), simple o recubierto, con buenos resultados iniciales45.
Persiste la controversia respecto al tratamiento más adecuado para la coartación nativa, entre cirugía e intervencionismo. Hay pocas dudas respecto a que la coartación aórtica neonatal ductus dependiente es tributaria de cirugía, pero a partir de los 3 meses de edad las opiniones difieren y, en ausencia de estudios prospectivos aleatorizados, hay informaciones que permiten apoyar cualquier opción, si bien cada vez hay más tendencia hacia el tratamiento intervencionista46-48.
Otra vertiente del mismo problema es la indicación de angioplastia o stent primario en el tratamiento de la coartación aórtica del adolescente y adulto. En general no se considera necesario el stent, salvo en casos complicados (segmentos largos de hipoplasia ístmica, coartación tortuosa, recoartación tras cirugía o angioplastia ineficaz49,50).
Los stents recubiertos Cheatham-Platinum (CP stent) se han utilizado en el tratamiento de aneurismas, lesiones complejas y en el tratamiento de lesiones combinadas (coartación y ductus); los resultados iniciales son buenos, con la limitación de que no pueden sobredilatarse51.
En cardiopatías con flujo pulmonar dependiente de ductus se está utilizando el implante de stent en el ductus como alternativa a la fístula sistémico-pulmonar para tratamientos paliativos de corta duración52. Asimismo, se aplica, con resultados prometedores, en la paliación de cardiopatías con flujo sistémico dependiente de ductus, SHCI y cardiopatías afines, bien como procedimiento híbrido (stent del ductus en quirófano y banding quirúrgico de ramas pulmonares) o totalmente intervencionista (stent del ductus y banding intravascular de ambas ramas con dispositivo Amplatzer® Pulmonary Artery Flow Restrictor)53,54.
Otros procedimientos híbridos (actuación combinada de cirujano y cardiólogo intervencionista), además de la paliación inicial del SHCI son: la finalización de la anastomosis cavopulmonar total con stents recubiertos tras preparación quirúrgica al realizar la anastomosis cavopulmonar bidireccional, el implante de stents en estenosis pulmonares poco accesibles o complejas, y el cierre de CIV percutáneo o perventricular sin circulación extracorpórea asociado con la corrección quirúrgica de otros defectos55,56.
La perforación percutánea con radiofrecuencia de la válvula pulmonar en la atresia pulmonar con septo íntegro es un tratamiento eficaz pero no carente de complicaciones. La mortalidad en relación con el procedimiento es de 5-10% y entre 10-20% de pacientes requiere flujo pulmonar adicional mediante stent del ductus o fístula sistémico-pulmonar, con una mortalidad hospitalaria total de hasta el 15%57,58.
Se ha presentado un nuevo dispositivo pensado para la oclusión de comunicaciones vasculares anómalas (colaterales sistémico-pulmonares, fístulas arteriovenosas y venovenosas, etc.). Se trata del Amplatzer vascular plug (AVP, AGA Medical, Golden Valley, MN). Es un dispositivo autoexpandible de nitinol de forma cilíndrica, similar en su estructura a los otros dispositivos Amplatzer®, disponible en diámetros de 4 a 16 mm y liberable por vainas 5 a 8 Fr59.
CIRUGÍA EN LAS CARDIOPATÍAS CONGÉNITAS
Los resultados del trasplante cardíaco pediátrico continúan mejorando. Según el último informe de la Internacional Society for Heart and Lung Tranplantation, el número de procedimientos está estabilizado alrededor de 360 al año. La supervivencia inmediata actual se sitúa en el 85% para los pacientes < 1 años y casi en el 90% para todas las edades, con una vida media prevista de 13, 13 y 11 años para los grupos de menos de 1, de 1-10 y de 11-17 años, respectivamente. Se desarrolla enfermedad vascular coronaria del injerto en alrededor del 14% de los supervivientes a los 7 años60. La modificación de Sano a la intervención de Norwood (sustitución del Blalock-Taussig modificado por un conducto entre el VD y las arterias pulmonares) ofrece resultados reproducibles y simplifica el manejo en el postoperatorio inmediato, que es más estable, lo que ha permitido reducir la mortalidad en muchos centros. Por otra parte, la mortalidad interestadios y el porcentaje de pacientes en los que se completa la derivación cavopulmonar con buen resultado son comparables a los de las series con Norwood clásico61,62.
Se continúa investigando en el campo de los conductos valvulados. Los resultados a medio plazo con el conducto Contegra (vena yugular bovina con su válvula, tratada con glutaraldehído y disponible en diámetros de 12 a 22 mm) son desiguales63-64; aún así, tiene la ventaja que supone disponer de conductos para pacientes pequeños con escasa disponibilidad de homoinjertos. Las perspectivas futuras son de conductos valvulados biocompatibles, desarrollados por ingeniería tisular a partir de células autólogas cultivadas sobre un armazón poroso biodegradable, que ya se han utilizado como conducto no valvulado en arterias pulmonares y como conducto extracardíaco en la derivación cavopulmonar65.
La realización de la corrección anatómica (switch arterial) en la transposición de grandes arterias (TGA) con septo íntegro es problemática tras los 15 días de vida, debido a la posible incapacidad del VI para hacer frente a la presión sistémica sin acondicionamiento previo con banding pulmonar. Kang et al66 comparan 275 pacientes operados antes de las 3 semanas con 105 pacientes operados después, con resultados similares en ambos grupos. Estos autores concluyen que el switch arterial puede ofrecerse hasta los 3 meses, sobre todo si se dispone de oxigenación con membrana extracorpórea, aunque en los pacientes mayores de 2 meses es útil valorar el grado de «preparación espontánea» del VI66.
Legendre et al67 publican los resultados del seguimiento de 1.198 pacientes tras corrección anatómica de TGA, en los que se valora la incidencia de complicaciones coronarias. La supervivencia libre de éstas es del 92,7; 91 y 88,2% a 1, 10 y 15 años, respectivamente, con curva de incidencia bimodal, alta en postoperatorio inmediato y con lento ascenso a partir de los 6 años. Estos pacientes deben ser seguidos a largo plazo67.
En pacientes con transposiciones complejas, la cirugía tipo Rastelli se realiza en la actualidad con una baja mortalidad inicial, pero hay una sustancial mortalidad y morbilidad tardías. Kreutzer et al68 publican la experiencia del Children's Hospital de Boston con 101 pacientes intervenidos, con una mortalidad precoz total de 7% y sin mortalidad en los últimos 7 años. Sin embargo, a los 15 años la tasa de supervivencia libre de fallecimiento o trasplante fue de 68% y sólo el 21% sobrevivía sin reintervención. Presentaron arritmias tardías graves 9 pacientes y hubo 5 muertes súbitas68.
¿Hay una alternativa al Rastelli? Las técnicas de translocación aórtica en cualquiera de sus variantes (operación de Nikaidoh, reparación a l'etage ventriculaire [REV], operación de Yamagishsi) presentan aparentes ventajas (procuran una reconstrucción más anatómica, mejoran los flujos intracardíacos y pueden preservar la función cardíaca, evitan la reducción de la cavidad ventricular derecha por la tunelización), pero son técnicamente complejas y, aunque en principio están pensadas para evitar el uso de conductos extracardíacos, esta meta no se consigue siempre o es al precio de dejar insuficiencia pulmonar significativa. Faltan estudios prospectivos y con se ries amplias, por lo que en principio estarían especialmente indicadas en casos de malos candidatos al Rastelli: CIV restrictiva o de septo de entrada, VD pequeño, cabalgamiento de válvulas auriculoventriculares y trastornos coronarios que impidan una ventriculotomía derecha distal69.
Los pacientes con discordancia auriculoventricular y ventriculoarterial (transposición congénitamente corregida) forman un grupo poco frecuente de CC de complejo tratamiento quirúrgico. El tratamiento clásico supone la reparación de los defectos asociados sin modificar la discordancia ventriculoarterial, lo que conduce a largo plazo a una alta proporción de fracasos del VD, o la alternativa de paliación con derivación cavopulmonar, en todo caso con resultados mediocres y con supervivencias del 61% a 15 años70. La corrección auténtica sería la realización doble switch (auricular y ventricular) que reconstruiría la concordancia ventriculoarterial. En este sentido, Langley et al71 publican una serie de 54 pacientes tratados con esta técnica, con una mortalidad hospitalaria del 5,6% y supervivencias del 89,7% a los 9 años, con un 77,5% de ellos libre de reintervención. Para los autores es la cirugía de elección, aunque reconocen que hay casos en que su realización no es posible o es muy complicada, en los que puede ser de aplicación la técnica clásica o la utilización de derivación cavopulmonar total o parcial con corrección 1½71.
Correspondencia: Dra. R.M. Perich Duran.
Unidad de Cardiología Pediátrica. Hospital de Sabadell-Corporació Parc Taulí.
Parc Taulí, s/n. 08208 Sabadell. Barcelona. España.
Correo electrónico: Rperich@cspt.es