La ecocardiografía, la tomografía computarizada multidetectores, la resonancia magnética y la cardiología nuclear contribuyen a prevenir la enfermedad coronaria. La ecocardiografía, con el estudio del grosor íntima-media carotídeo, la rigidez arterial y la dilatación mediada por flujo en la arteria braquial, identifica a individuos asintomáticos en riesgo de enfermedad coronaria tributarios de terapias preventivas agresivas. El score de calcio es un predictor independiente de eventos cardiacos y modifica scores de riesgo clínico como el de Framingham. La coronariografía por tomografía multidetectores y la resonancia magnética visualizan la pared y la luz arterial y detectan placas con y sin calcificaciones antes que la coronariografía invasiva. La cardiología nuclear permite la evaluación de la repercusión funcional de la lesión aterosclerótica mediante el análisis combinado de la perfusión y la función ventricular.
Palabras clave:
cardiología nuclear.
coronariografía invasiva.
coronariografía por tomografía computarizada de múltiples detectores.
enfermedad coronaria.
factores de riesgo coronarios.
resonancia magnética.
La aplicación de medidas epidemiológicas en la segunda mitad del siglo xx logró disminuir las tasas de mortalidad por afecciones cardiovasculares, especialmente de la enfermedad coronaria (EC). A pesar de este resultado, la mortalidad por EC ocupa los primeros lugares en muchos países por un enlentecimiento en la disminución, lo que se atribuye, entre otras causas, a un aumento de los factores de riesgo coronarios (FRC)1-3.
Las técnicas de imagen no invasivas —ecocardiografía, tomografía computarizada de múltiples detectores (TCMD), resonancia magnética (RM) y cardiología nuclear (CN), todas en pleno desarrollo4— contribuyen a la prevención al diagnosticar precozmente la EC y evitar o facilitar técnicas invasivas.
El incremento mundial de procedimientos de revascularización coronaria es índice de la magnitud de la EC y de su insuficiente prevención.
La aplicación de las técnicas de imagen depende de la clínica y la evaluación de sus riesgos y beneficios. Un examen diagnóstico resulta útil si: a) identifica a los pacientes con elevado y bajo riesgo de eventos cardiacos futuros; b) conlleva una estrategia de tratamiento diferente en pacientes de alto riesgo; c) mejora el pronóstico de estos pacientes gracias al tratamiento empleado, y d) se demuestra su coste-efectividad.
Existen dos líneas de pensamiento con referencia al empleo de la evaluación de riesgo por técnicas de imagen en cardiología tras aplicar un score de riesgo clínico, como el de Framingham5. La primera aboga por su uso para determinar isquemia en pacientes con alto riesgo, particularmente en diabéticos6,7. Esto también podría aplicarse a pacientes con riesgo clínico intermedio8, y se ha propuesto su aplicación a los pacientes con síndrome metabólico o historia familiar de EC prematura9,10. La segunda línea aboga por no emplear técnicas de imagen en pacientes de alto riesgo, ya que hay que tratarlos a todos hasta lograr objetivos de prevención secundaria, y esto no se alterará por los resultados de dichas pruebas. Sin embargo, no existen ensayos clínicos que comparen ambas estrategias, y la detección de isquemia puede beneficiar a los pacientes asintomáticos.
A continuación presentamos el papel de estas técnicas en la prevención de la EC.
ECOCARDIOGRAFÍADetección ecocardiográfica de aterosclerosis subclínica en la prevención primaria cardiovascularEl ultrasonido carotídeo, la determinación de la rigidez arterial y la dilatación mediada por flujo en la arteria braquial son útiles para identificar a individuos tributarios de terapias preventivas agresivas, mejorar la predicción del riesgo cardiovascular y conducir a la reclasificación de estos pacientes4. Estas técnicas no invasivas, disponibles y poco costosas, resultan de utilidad en la estratificación y prevención de la EC11.
Grosor íntima-media carotídeo y presencia de placa ateromatosaRecientes estudios han demostrado el valor predictivo del ultrasonido carotídeo en la estratificación de riesgo cardiovascular, incluso en individuos clasificados como de bajo riesgo según el score de riesgo de Framingham (SRF)12-14. La mayoría de los informes consideran como anormal un valor de grosor íntima-media carotídeo (GIMc) > 1mm, independientemente de la edad y el sexo, y que es un factor de riesgo equivalente15,16 (otros estiman un valor de 0,9mm)16. Se recomienda el uso de nomogramas que permitan identificar el percentil carotídeo individual, alto (≥ p75, riesgo cardiovascular incrementado), medio (p25-p75, riesgo no alterado) y bajo (< p25, riesgo disminuido), de acuerdo con la edad, el sexo y la raza del paciente17,18.
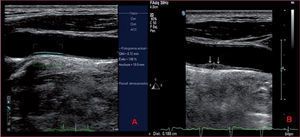
La presencia de placas de ateroma carotídeas en combinación con la medición del GIMc (figs. 1A y B) ofrece mejor representación de la enfermedad vascular subclínica y del riesgo cardiovascular19.
Existe un importante número de informes de pacientes sin EC conocida (con más de 1.000 participantes) que demuestran que el incremento del GIMc es un predictor de infarto agudo de miocardio, accidente cerebrovascular o muerte por causa cardiovascular (tabla 1)20-26. Igualmente, otros estudios prospectivos con al menos 1.000 participantes demostraron que el riesgo relativo asociado a la presencia de placas ateromatosas fue igual o ligeramente superior al GIMc21,26,27. Por estas razones, la determinación del GIMc y de la placa ateromatosa se considera razonable para la estratificación del riesgo cardiovascular en adultos asintomáticos con riesgo intermedio (clase IIA, nivel de evidencia B)4.
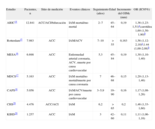
Estudios prospectivos en relación con el GIMc y el riesgo de eventos cardiovasculares adversos en pacientes sin enfermedad cardiovascular conocida
| Estudio | Pacientes, n | Sitio de medición | Eventos clínicos | Seguimiento (años) | Edad | Incremento del GIMc (mm) | OR (IC95%) |
| ARIC14 | 12.841 | ACC/ACI/bifurcación | IAM mortal/mo mortal | 2–7 | 45–64 | 0,19 | 1,36 (1,23-1,51)a;carotídea 1,69 (1,50-1,90)b |
| Rotterdam15 | 7.983 | ACC | IAM/ACV | 7–10 | > 55 | 0,163 | 1,56 (1,12-2,18)a;1.44 (1,00-2,08)b |
| MESA16 | 6.698 | ACC | Enfermedad arterial coronaria, ACV, muerte por causa cardiovascular | 5,3 | 45–84 | 0,19 | 1,30 (1,10-1,40) |
| MDCS17 | 5.163 | ACC | IAM mortal/no mortal/muerte por causa coronaria | 7 | 46–68 | 0,15 | 1,29 (1,13-1,46) |
| CAPS18 | 5.056 | ACC | IAM/ACV/muerte por causa cardiovascular | 3–5,9 | 19–90 | 0,16 | 1,17 (1,08-1,26) |
| CHS29 | 4.476 | ACC/ACI | IAM | 6,2 | > 65 | 0,2 | 1,46 (1,33-1,60) |
| KIHD20 | 1.257 | ACC | IAM | 3 | 42–60 | 0,11 | 1,11 (1,06-1,16) |
ACC: arteria carótida común; ACI: arteria carótida interna; ACV: accidente cerebrovascular; GIMc: grosor íntima-media carotídeo; IAM: infarto agudo de miocardio.
La rigidez arterial puede evaluarse por diversos métodos28. Si bien la hipertensión sistólica sola acompañada de un aumento en la presión del pulso en adultos mayores de 50 años constituye un indicador suficiente para establecer el aumento de rigidez de la aorta, se han buscado otras medidas indirectas que permitan diagnosticar la rigidez con mayor precisión.
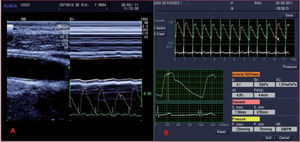
La ultrasonografía Doppler ha logrado reproducir la curva del volumen de las arterias periféricas de mediano calibre. Con un transductor de haces paralelos se visualiza, preferentemente de manera transversal, la arteria muscular-elástica (fig. 2A) y, mediante software adecuado, se puede medir el movimiento pulsátil, su distensibilidad y el tiempo que tarda el pulso arterial en ir y retornar (fig. 2B).
A pesar de que existen múltiples medidas específicas de la rigidez arterial, la velocidad de la onda del pulso aórtico es, sin duda, la más estudiada29. En la población general, se ha demostrado que es un predictor independiente de mortalidad cardiovascular y de incidencia de enfermedad arterial coronaria durante el seguimiento30,31.
La relativa falta de uniformidad en los protocolos de medición, los problemas concernientes a su reproducibilidad y la elevada dependencia del operador son dificultades que impiden la generalización de los resultados encontrados. Por lo tanto, aún no se recomienda la determinación de la rigidez arterial para la evaluación del riesgo cardiovascular en adultos asintomáticos (clase III, nivel de evidencia C)4.
Función endotelial mediada por flujoLa dilatación mediada por flujo (DMF) es una medida de la cantidad de óxido nítrico liberado por el endotelio vascular. La disminución en la DMF se considera una manifestación temprana y potencialmente reversible de EC32,33.
Hay evidencias de la asociación de diversos FRC clásicos con la disfunción endotelial. Las terapias farmacológicas y los cambios en el estilo de vidas dirigidos a mejorar el riesgo cardiovascular mejorarían también, en la mayoría de los casos, la función vasodilatadora del endotelio34,35.
Desde que Celermajer et al36 introdujeron este parámetro ultrasonográfico, algunos autores sostienen la hipótesis de que la DMF es un «barómetro» de la acumulación de lesiones en el endotelio vascular, por lo que una medición exacta de la DMF sería una importante vía para estimar el riesgo cardiovascular total37,38.
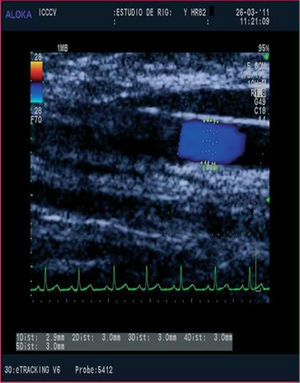
El ultrasonido de alta resolución de la arteria braquial durante la hiperemia reactiva se utiliza como método para determinar la función vascular periférica39 (fig. 3). El método tradicional de estimación por ecocardiografía es ampliamente conocido y su explicación se sale del objetivo de esta revisión40.
Un metaanálisis de 211 estudios que evaluó la relación entre la DMF y la presencia de eventos cardiovasculares, en un total de 11.984 pacientes, demostró que el incremento en la información pronóstica aportada por la DMF se atenuaba en el grupo de pacientes de mediano y alto riesgo según el SRF; sin embargo, se relacionó con múltiples factores de riesgo y eventos cardiovasculares en pacientes de bajo riesgo40-42 (tabla 1).
TOMOGRAFÍA COMPUTARIZADA DE MÚLTIPLES DETECTORESConsta de dos técnicas radiográficas: la detección y cuantificación del calcio coronario y la coronariografía por tomografía computarizada de múltiples detectores (CTCMD).
La presencia de calcio en las arterias coronarias se considera casi patognomónica de aterosclerosis, pues la enfermedad de Monckeberg no afecta a las coronarias, aunque se han descrito calcificaciones en pacientes con insuficiencia renal avanzada y diabéticos de difícil control4,43.
La puntuación o score de calcio (SCa) introducida por Agatston44 tiene las ventajas de que no necesita ayuno del paciente, esfuerzo físico ni administración de medicamentos o contraste, aunque la ausencia de calcio no niega la EC, pues existen placas no calcificadas constituidas por lípidos, tejido inflamatorio y fibroso que atenúan poco los rayos X y son invisibles por el SCa. El SCa tiene la desventaja de que no detecta las placas blandas o no calcificadas y no distingue entre placas mixtas y calcificadas. Se desconoce algunos aspectos fisiopatológicos de la calcificación de la placa ateromatosa y resultan polémicos45.
El SCa es un FRC independiente para predecir eventos cardiacos y el riesgo relativo aumenta proporcionalmente con la puntuación y puede modificar el SRF45.
Coronariografía por tomografía computarizada de múltiples detectoresLa CTCMD es una técnica joven, en plena evolución, pero todavía con deficiencias y aspectos polémicos46-49. No se han redactado guías para la aplicación de la CTCMD, aunque sí documentos de expertos4,49.
Recientemente se ha reducido la dosis de radiaciones de la CTCMD de 12 a 3mSv, y hasta 1mSv con equipos de doble fuente o de 250 y 320 filas de detectores en pacientes seleccionados, con técnica helicoidal, sincronización electrocardiográfica prospectiva (triggering), obtención de datos en un solo latido cardiaco, pitch alto y menos kilovoltios. Con equipos de 64 cortes se logran dosis de 1–3,5mSv con técnica secuencial y sincronización electrocardiográfica prospectiva50.
La coronariografía invasiva (CORINV) por cateterismo arterial sólo permite visualizar la luz coronaria, aunque por su mejor resolución espacial y temporal es el patrón de referencia para el diagnóstico de la EC y permite un procedimiento invasivo terapéutico51.
En pacientes con riesgo intermedio de EC, que por sus manifestaciones clínicas y otras técnicas tienen mayor probabilidad de no tenerla, la CTCMD es de gran valor por su alta sensibilidad y su valor predictivo negativo cercano al 100%, lo que evita la CORINV52,53.
Se han logrado buenos resultados en pacientes con sospecha de EC obstructiva, aunque la precisión diagnóstica es subóptima, pues los artefactos por movimientos del paciente, frecuencia cardiaca alta, extrasístoles, obesidad y calcificaciones pueden confundirse con estenosis coronarias. Al evaluar la precisión diagnóstica, hay que considerar la prevalencia de EC en la población estudiada4,52,53.
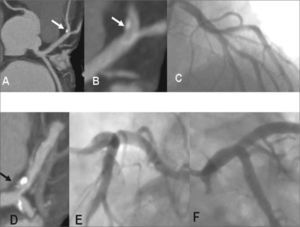
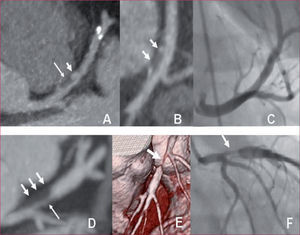
La ventaja de la CTCMD sobre la CORINV es que, además de la luz, visualiza la pared arterial y detecta antes que la CORINV las placas calcificadas, no calcificadas y mixtas cuando aún no protruyen hacia la luz o no son obstructivas4,54. Esto tiene gran importancia, pues ya en 198855 se señaló que las placas ateromatosas < 50% son más proclives a la erosión y la rotura, con mayor riesgo de ocasionar un síndrome coronario agudo, a veces como primera manifestación clínica de la EC, lo que se ha corroborado por la CTCMD54 (fig. 4). Además, en los estadios iniciales de la placa ateromatosa puede ensancharse o remodelarse el vaso sin comprometerse la luz vascular, que se estrecha progresivamente al aumentar el tamaño de la placa56 (fig. 5).
A: tomografía, reconstrucción curvada, placa mixta en descendente anterior (flecha). B: vista ampliada. C: coronariografía invasiva; no hay estenosis (otro paciente). D: tomografía, plano axial; placa mixta en tronco y descendente anterior (flecha); otra calcificación en circunfleja. E-F: coronariografía invasiva sin estenosis.
A: tomografía, plano axial; placa no calcificada; descendente anterior; remodelado positivo (flecha larga); contraste en la placa (flecha corta); placas calcificadas distales. B: vista ampliada. C: coronariografía invasiva sin estenosis. D: tomografía, plano axial, de otro paciente; placa en tronco y descendente anterior, no calcificada, con remodelado positivo (flechas cortas) y estenosis tubular (flecha larga). E: reconstrucción en 3D; estenosis (flecha). F: coronariografía invasiva; estenosis (flecha).
El remodelado positivo, las placas no calcificadas y la penetración de contraste en la placa se han asociado a su vulnerabilidad, pero se requieren estudios de imagen y anatomopatológicos más profundos56-58.
Es importante identificar las placas llamadas vulnerables, pues parte de los pacientes con estas placas son asintomáticos y su primera, y a veces última, manifestación es un síndrome coronario agudo. Estas placas suelen ocupar menos del 50% de la luz vascular y se catalogan como no significativas y no tributarias de revascularización, pero clínicamente sí son significativas y deben aplicarse enérgicas medidas preventivas. Las características de las placas vulnerables no están completamente definidas, pero se ha adelantado con técnicas de imagen invasivas y estudios histopatológicos de pacientes fallecidos súbitamente. El diagnóstico precoz de estas placas sería factible extrapolando las características observadas por técnicas invasivas a la CTCMD y a la resonancia magnética (RM)56-58.
Las placas ateromatosas que reducen el diámetro de la luz vascular menos de un 50% se consideran no obstructivas y hemodinámicamente «no significativas», pero desde el punto de vista clínico sí son significativas y, al no ser tributarias de revascularización, las medidas preventivas cobran gran importancia.
Las dosis bajas de radiación no se pueden aplicar todavía a todos los pacientes, lo que limita la CTCMD. Su uso depende de las características clínicas, los recursos disponibles y la evaluación del riesgo/ beneficio.
El estudio triple rule out mediante TCMD, tema polémico, se utiliza en el diagnóstico del dolor torácico agudo con clínica y electrocardiograma no concluyentes para precisar el diagnóstico entre síndrome coronario agudo, disección aórtica y tromboembolia pulmonar59.
Otra condición relacionada con la EC donde la CTCMD resulta de utilidad es en los puentes aortocoronarios arteriales y venosos. La oclusión de los puentes es de gran especificidad por CTCMD, aunque el estado de los vasos nativos es discutible. Se ha avanzado en el estudio de los stents coronarios, pero todavía hay dificultades. Donde sí hay consenso de que la CTCMD supera a la CORINV es en las anomalías coronarias4,52,53,60.
RESONANCIA MAGNÉTICALa RM tiene la ventaja de que no requiere radiaciones ni medios de contraste yodados y, al igual que la CTCMD, permite visualizar la luz y la pared coronaria y detectar precozmente las placas ateromatosas no calcificadas y el remodelado vascular4. Con la RM se puede estudiar además la función cardiaca, el flujo sanguíneo y la viabilidad61,62.
Recientemente, con equipos de 3T, 32 canales y otros avances, se han observado ventajas o tendencia favorable de la CTCMD sobre la RM con CORINV como patrón de referencia61,62.
La RM está contraindicada en pacientes con claustrofobia y en presencia de cuerpos extraños ferromagnéticos implantados con fines terapéuticos o por accidente. Uno de sus inconvenientes es lo prolongado del estudio4.
CARDIOLOGÍA NUCLEARLa utilización de las técnicas de medicina nuclear en cardiología (CN) permite, ante todo, la evaluación de la repercusión funcional de la lesión aterosclerótica, lo que la diferencia de otras técnicas de imagen que se ocupan fundamentalmente de la evaluación anatómica. Actualmente, gracias al desarrollo de compuestos marcados con tecnecio-99m, como sestamibi y tetrofosmina, la tomografía de emisión monofotónica (más conocida por sus siglas en inglés de single-photon emission computed tomography [SPECT]) permite la adquisición de las imágenes sincronizada con la onda R del electrocardiograma (ECG) o adquisición gatillada. La adquisición gatillada permite obtener, con un solo estudio, información acerca del estado de la perfusión miocárdica, la función ventricular general y regional e incluso de la sincronía intraventricular mediante el análisis de las imágenes de fase.
Otro aspecto particularmente interesante en cuanto a las técnicas de CN es que ofrecen el único medio no invasivo para el estudio de la inervación cardiaca adrenérgica, cuya importancia en la predicción y prevención de la muerte súbita cardiaca y de las arritmias ventriculares, de interés para la evaluación de los desfibriladores automáticos implantables, se ha demostrado recientemente63,64.
Por otra parte, la tomografía por emisión de positrones (PET), mediante radioisótopos de vida media ultracorta, permite la evaluación del flujo sanguíneo coronario y de la reserva de flujo coronario ante situaciones de estrés, así como del metabolismo miocárdico, mediante protocolos validados e introducidos en la práctica clínica.
Ahora bien, ¿cómo integrar estas posibilidades que nos ofrecen las técnicas nucleares en la prevención cardiovascular? En primer lugar, es necesario relacionarlas con los diferentes niveles de prevención. En la prevención primaria, encaminada a evitar el desarrollo de la EC, indudablemente el control de los FRC es el elemento clave, y las técnicas de imagen, como las de CN, no tienen papel alguno. Sin embargo, en la prevención secundaria, para identificar y detectar la enfermedad en sus estadios iniciales, en los que es posible limitar su progresión y evitar complicaciones, como el infarto de miocardio (IM), la necesidad de revascularización o la muerte cardiaca, así como en la prevención terciaria, en pacientes coronarios que requieren una adecuada estratificación de riesgo que permita seleccionar el tratamiento apropiado y evaluar sus resultados en el seguimiento, es donde las técnicas de CN mantienen su aplicabilidad. A continuación abordaremos ambos aspectos.
Cardiología nuclear en la prevención secundaria de la enfermedad coronariaDe acuerdo con las guías conjuntas de ACC/AHA/ASNC Appropriate Use Criteria for Cardiac Radionuclide Imaging65, el empleo de la gammagrafía de perfusión miocárdica (GPM) en pacientes sin EC demostrada debe basarse en su riesgo de sufrir eventos cardiacos adversos. De esta forma, no está indicada para pacientes con bajo riesgo, al contrario que en aquellos que presentan un riesgo elevado. Para pacientes con riesgo intermedio y ECG no interpretable, puede considerarse su realización. Si se tiene en cuenta el SCa, la GPM está indicada si SCa ≥ 400 o si el paciente tiene SCa 100–400 y riesgo elevado.
Equivalentes de riesgoHay pacientes con enfermedades que comportan un riesgo cardiovascular similar al de aquellos con EC demostrada, como la diabetes mellitus, otras enfermedades ateroscleróticas (enfermedad arterial periférica, aneurisma aórtico abdominal, enfermedad de arteria carótida) y la disfunción eréctil, donde la utilidad de la GPM aún no se ha estudiado suficientemente, pero en la que la detección temprana de isquemia resulta un tema de interés a la vez que controvertido. Por su elevada incidencia (171 millones de personas afectadas en el año 2000, y se anticipa el doble de esta cifra para 2030)66, tomaremos el ejemplo de la diabetes en este grupo. Se ha demostrado que la EC causa el 75% de las muertes de diabéticos67, pero muy frecuentemente es silente68 con isquemia entre el 21 y el 59% detectada por la presencia de defectos reversibles de perfusión en la GPM69,70. No obstante, y luego de los estudios prospectivos realizados, incluido el DIAD7,69, la GPM se recomienda en diabéticos asintomáticos si hay neuropatía autonómica o evidencia de enfermedad vascular71. Anand et al72, por su parte, desarrollaron una estrategia por etapas en la que se realizaba GPM sólo si se detectaba la presencia de aterosclerosis mediante el SCa (valores ≥ 100). Esta estrategia combinada podría contribuir a una mejor estratificación de riesgo en diabéticos asintomáticos.
Poblaciones especialesRecientemente se ha demostrado que la GPM SPECT puede ser particularmente coste-efectiva en subgrupos especiales en los que la aparición de eventos cardiacos está estrechamente relacionada con la gravedad y la extensión de los defectos de perfusión en la GPM73. De ahí que la GPM pueda utilizarse para decidir la conveniencia de un tratamiento agresivo en pacientes con riesgo elevado, evitando intervenciones innecesarias en aquellos con resultados normales o ligeramente anormales. A este respecto, trataremos dos subgrupos: pacientes con enfermedad renal crónica y mujeres.
La enfermedad renal crónica incrementa significativamente el riesgo de eventos cardiacos74, y la enfermedad cardiovascular es la primera causa de muerte en estos pacientes75. Los pacientes asintomáticos con enfermedad renal crónica tienen una probabilidad intermedia de tener una EC silente, y se ha demostrado que la presencia de isquemia inducible en la GPM tiene una precisión diagnóstica excelente y un valor pronóstico independiente para predecir los eventos cardiacos y la mortalidad por cualquier causa.
En las mujeres, quienes en muchas ocasiones presentan un cuadro clínico atípico, también es importante lograr precisar mejor el diagnóstico, sobre todo si consideramos que la enfermedad cardiovascular es la causa de la tercera parte de las muertes de mujeres en todo el mundo. La American Heart Association77 publicó un algoritmo para la evaluación de mujeres sintomáticas con probabilidad intermedia/alta de presentar EC, que tiene en cuenta, como primera línea de investigación, una prueba ergométrica (si el ECG en reposo es normal y la paciente es capaz de realizar ejercicio físico) o una GPM (si es diabética, el ECG de reposo es anormal o la capacidad de ejercicio es cuestionable). Específicamente en el caso de las mujeres, frecuentemente con menor nivel de entrenamiento físico que los varones, si no es posible alcanzar una frecuencia cardiaca submáxima (el 85% de la frecuencia cardiaca máxima calculada) suficiente para el diagnóstico antes de la inyección del radiofármaco, resulta conveniente combinar el estrés físico con el farmacológico.
Cardiología nuclear en la prevención terciaria de la enfermedad coronariaEn la tabla 2 se presentan las recomendaciones actuales para la realización de GPM en diferentes escenarios clínicos de la EC, adaptadas de Marcassa et al78.
CONCLUSIONESDe todo lo que antedece, se puede considerar que no hay dudas de que las técnicas de imagen no invasivas apoyadas en la clínica son de gran importancia en la valoración y la prevención de la EC. Al encontrarse todas en pleno desarrollo, es de esperar que haya nuevos adelantos en un futuro cercano que modifiquen sustancialmente sus actuales indicaciones, incluso la fusión de algunas de ellas. La técnica ideal es la que no requiera radiaciones ni contraste y pueda aplicarse incluso a pacientes de alto riesgo, o al menos la que requiera una dosis mínima de radiaciones y contraste con equipos de alta resolución.
CONFLICTO DE INTERESESNinguno.