Este estudio de la práctica real, el primero de su tipo en población española, tuvo como objetivo explorar el riesgo de eventos cardiovasculares graves y de muerte por todas las causas tras la agudización de la enfermedad pulmonar obstructiva crónica (EPOC) en una gran cohorte de pacientes con esta enfermedad.
MétodosSe incluyó a pacientes con un código de diagnóstico de EPOC entre 2014 y 2018 de la base de datos sanitarios BIG-PAC. El resultado principal fue la combinación de un primer evento cardiovascular grave (síndrome coronario agudo, descompensación de insuficiencia cardiaca, isquemia cerebral, arritmia) o muerte por todas las causas después de la inclusión en la cohorte. Los modelos de riesgos proporcionales de Cox dependientes del tiempo estimaron las HR para diferentes periodos de exposición (1-7, 8-14, 15-30, 31-180, 181-365 y >365 días) después de una agudización de cualquier gravedad y después de una agudización moderada o grave por separado (frente a tiempo sin exposición antes de una primera agudización después de la inclusión en la cohorte).
ResultadosDurante una mediana de seguimiento de 3,03 años, 18.901 de los 24.393 pacientes (77,5%) sufrieron al menos 1 agudización moderada/grave y 8.741 (35,8%), el resultado principal. El riesgo de eventos cardiovasculares graves aumentó después del inicio de una agudización moderada/grave de la EPOC en comparación con el periodo sin exposición, más pronunciado durante los primeros 7 días tras el inicio de la agudización (HR=10,10; IC95%, 9,29-10,97), aunque permaneció aumentado incluso más de 365 días después (HR=1,65; IC95%, 1,49-1,82).
ConclusionesEl riesgo de eventos cardiovasculares graves o muerte aumentó después del inicio de una agudización moderada/grave, lo que evidencia la necesidad de una atención multidisciplinaria proactiva de los pacientes con EPOC para prevenir las agudizaciones y abordar otros factores de riesgo cardiovascular.
Palabras clave
En España, la enfermedad pulmonar obstructiva crónica (EPOC) es una importante preocupación de salud pública debido a su prevalencia estimada de casi un 12%1 y sus repercusiones socioeconómicas2. En 2016 la EPOC fue la cuarta causa de mortalidad más frecuente en España3. Las personas que viven con EPOC tienen un riesgo de enfermedad cardiovascular superior al de quienes no sufren EPOC4,5, como consecuencia de unos factores de riesgo y una fisiopatología comunes6,7. En España, en el estudio CONSISTE se observó que la prevalencia de la enfermedad cardiovascular era sustancialmente mayor en los pacientes con EPOC que en aquellos sin ella: insuficiencia cardiaca (IC) (el 25 frente al 1%, arritmia (el 16 frente al 5%) y cardiopatía isquémica (el 13 frente al 5%)8. Estas estimaciones se observaron también en el estudio AvoidEx en España cuanto a fibrilación auricular (FA) (15%), IC (14%) y cardiopatía isquémica (10%) en los pacientes con EPOC9.
En estudios previos se ha descrito un aumento del riesgo de eventos cardiovasculares durante y después de las agudizaciones de la EPOC10–16, en especial en cuanto infarto de miocardio (IM)11–13,15,16, ictus11–16, IC12 y arritmias10. Sin embargo, algunos de los resultados se basan en análisis post hoc de ensayos controlados y aleatorizados10,13, que es posible que no reflejen la población con EPOC de la práctica clínica real; otros proceden de estudios observacionales realizados en Reino Unido11,16, Estados Unidos12, Dinamarca15 y Países Bajos14.
El EXAcerbations of COPD and their OutcomeS on CardioVascular diseases (EXACOS-CV) es un programa de varios estudios observacionales retrospectivos longitudinales, llevados a cabo por separado en Canadá, España, Italia, Alemania, Países Bajos, Reino Unido, Japón, Estados Unidos, Francia y China que emplearon las bases de datos administrativas más apropiadas de cada país. Ya se había publicado anteriormente el diseño general del estudio17. En las publicaciones del programa EXACOS-CV hasta la fecha, se han observado elevaciones uniformes del riesgo de eventos cardiovasculares tras las agudizaciones en los pacientes con EPOC de varios países, como Canadá, Alemania, Países Bajos y Reino Unido18–21. Aquí se presentan los resultados del estudio EXACOS-CV en España. Los objetivos fueron los siguientes: a) estimar la tasa de incidencia (TI) y el riesgo de un evento cardiovascular grave o de muerte por cualquier causa relacionado con el tiempo transcurrido tras una agudización moderada o grave, en conjunto, y para tipos específicos de eventos cardiovasculares; b) estimar esta asociación con las agudizaciones moderadas y graves por separado, y c) estimar esta asociación en los pacientes de nuevo diagnóstico.
MÉTODOSDiseño y población del estudioLos datos se obtuvieron a partir de la base de datos anonimizada BIG-PAC. Esta contiene datos clínicos de aproximadamente 2 millones de personas de centros de atención primaria y hospitales de 7 áreas de salud de 7 comunidades autónomas (un área por comunidad) de España. Los datos de BIG-PAC proceden de información médica recopilada de manera sistemática en centros de atención primaria, hospitales de referencia y farmacias del Sistema Nacional de Salud de España. La información procedente de diferentes fuentes se integra, anonimiza y transfiere a la base de datos BIG-PAC para fines de investigación. La base de datos se ha empleado mucho en los últimos años22,23. Se dispone de las historias clínicas integradas relacionadas con el médico de atención primaria, la atención especializada, el hospital y los servicios de urgencias, la dispensación de farmacia para pacientes ambulatorios y hospitalizados y la fecha de fallecimiento (registrada por un médico de atención primaria).
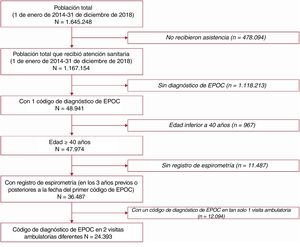
La fecha de inclusión en la cohorte es la del primer diagnóstico de EPOC identificado, que se determinó en la base de datos mediante una de las opciones siguientes: al menos 2 visitas ambulatorias con un código de diagnóstico de EPOC o al menos 1 visita ambulatoria con un código de diagnóstico de EPOC junto con una indicación de espirometría (en los 3 años anteriores a la fecha del código de EPOC o después de esta) o al menos 1 diagnóstico hospitalario con código de EPOC. Si se identificaban 2 o más fechas de diagnóstico en las visitas hospitalarias o ambulatorias, la fecha de inclusión en la cohorte se definía como la primera de ellas. En el momento de la inclusión en la cohorte, los pacientes elegibles para la inclusión tenían edad ≥ 40 años y un diagnóstico de EPOC entre el 1 de enero de 2014 y el 31 de diciembre de 2018. Este criterio de inclusión por edad se considera un método estándar para mejorar la especificidad de un algoritmo para detectar a las personas con EPOC cuando se usan datos secundarios. Se excluyó a los pacientes que tenían déficit de alfa-1-antitripsina (Clasificación Internacional de Enfermedades, Novena Revisión [CIE-9 273.8 y 273.9] o Décima Revisión [CIE-10 E88.01]). Los códigos para el diagnóstico de EPOC y para las agudizaciones relacionadas con ella, según lo definido en el manual de codificación del Ministerio de Salud de España, se indican en la tabla 1 del material adicional.
La cohorte incidente fue un subgrupo de la cohorte global con presunta EPOC de nuevo diagnóstico, lo cual se definía por no tener ningún diagnóstico de EPOC en los 24 meses previos a la inclusión en la cohorte.
El estudio se llevó a cabo cumpliendo la Declaración de Helsinki y fue aprobado por el Comité de Ética del Consorci Sanitari de Terrassa (protocolo AZ-EXA-2022-06, 13 de junio de 2022). Este es un estudio de datos secundarios en el que se emplean datos totalmente anonimizados y no requirió el consentimiento de los pacientes.
SeguimientoSe dio seguimiento a los pacientes desde la inclusión en la cohorte hasta la aparición del objetivo de interés o la censura para el análisis (31 de diciembre de 2019 o pérdida del seguimiento), lo que sucediera antes.
ExposiciónLas exposiciones de interés fueron las agudizaciones moderadas o graves aparecidas durante el seguimiento. Las agudizaciones moderadas se definieron como las que requerían visita ambulatoria con un código diagnóstico de EPOC (tabla 1 del material adicional) y la dispensación de corticoides orales y/o antibióticos en un plazo de 5 días tras la visita y durante un máximo de 15 días. Se verificaron los registros para comprobar que los corticoides orales y los antibióticos se hubieran prescrito para el tratamiento de una agudización. En el caso de los antibióticos se confirmó también que no hubiera ninguna infección aguda no pulmonar concurrente. Las agudizaciones graves se definieron como las que requerían una visita en un servicio de urgencias u hospitalización ≥ 1 noche con un código de diagnóstico de alta de agudización de la EPOC (tabla 1 del material adicional). Las definiciones de las agudizaciones moderadas o graves utilizadas en este estudio coinciden con las de la Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2022 en vigor cuando se llevó a cabo el estudio24.
El tiempo de exposición se definió como el transcurrido después del inicio de una agudización y se dividió en 6 subperiodos (1-7, 8-14, 15-30, 31-180, 181-365 días y >365 días). El tiempo sin exposición se definió como el transcurrido desde la inclusión en la cohorte hasta la primera agudización moderada o grave o el final del seguimiento (aparición de un evento del objetivo o censura para el análisis) (figura 1 del material adicional).
ObjetivosEventos de interés incluidos: a) síndrome coronario agudo (SCA): infarto agudo de miocardio y angina inestable; b) descompensación de la IC; c) isquemia cerebral: ictus isquémico y accidente isquémico transitorio; d) arritmias: FA de nuevo diagnóstico y otras arritmias, incluida la parada cardiaca reanimada, y e) muerte por cualquier causa. Los eventos cardiovasculares graves no mortales fueron los que motivaron hospitalización durante al menos 1 noche con un código de alta principal o secundario para el evento que no causaba la muerte en el hospital (tabla 2 del material adicional). Las muertes se identificaron a través de los registros de los médicos de atención primaria, y la causa de la muerte hospitalaria se determinó mediante los códigos diagnósticos de ingreso y se clasificó como «respiratoria», «cardiaca» u «otras»; las muertes ocurridas fuera del hospital se clasificaron como de causa «desconocida».
El objetivo principal fue la combinación del tiempo hasta un primer evento cardiovascular no mortal grave de cualquier tipo o hasta la muerte por cualquier causa. Los objetivos secundarios fueron el tiempo hasta un primer evento cardiovascular no mortal grave de cada uno de los tipos; la muerte se consideró un evento de censura para el análisis.
Análisis estadísticoPara los análisis se emplearon los programas SPSSWIN versión 23 y R Project for Statistical Computing versión 4.0.3. No se imputaron los datos no disponibles. La ausencia del código médico se consideró ausencia de la condición.
Los análisis se llevaron a cabo en la cohorte global (es decir, todos los pacientes elegibles para el estudio) y en la cohorte incidente. Las características demográficas basales de ambas cohortes se describen en su totalidad y también las de los pacientes que sufrieron o no al menos 1 agudización durante el seguimiento. Se utilizó un gráfico de equilibrio de covariables para comparar las características iniciales de los pacientes que tuvieron en algún momento del seguimiento una agudización moderada o grave con las de los pacientes que no (figura 2 del material adicional).
Se calcularon los valores de TI bruta/100 años-paciente con los intervalos de confianza de Poisson exactos del 95% (IC95%) para todos los eventos de valoración principales y secundarios de interés en los periodos con y sin exposición tras el inicio de una agudización moderada o grave.
Se ajustaron modelos de regresión de riesgos proporcionales de Cox25 con indicadores binarios de cada periodo de exposición como covariables dependientes del tiempo para estimar los valores de hazard ratio (HR) correspondientes a los cambios en las tasas de: a) el objetivo principal después de una agudización moderada o grave; b) el objetivo principal después de una agudización moderada o una agudización grave, por separado; c) cada uno de los objetivos secundarios u otros objetivos después de una agudización moderada o grave; d) el objetivo principal después de una primera, segunda y tercera (o más) agudización moderada o grave en la cohorte incidente.
Los modelos se adaptaron con y sin ajuste por factores de confusión preespecificados. Estos factores fueron: edad, sexo, año de inclusión en la cohorte, tabaquismo, trastorno de consumo de alcohol, comorbilidades, visitas al médico de atención primaria, número de agudizaciones previas y uso de medicación, junto con factores de riesgo cardiovascular como diabetes mellitus, enfermedad hipertensiva e IC previa, entre otros (tabla 1). En los análisis de cada uno de los tipos de eventos cardiovasculares y de la mortalidad por cualquier causa se incluyeron los eventos cardiovasculares competidores como covariables dependientes del tiempo. Para los eventos cardiovasculares no mortales, se censuró del análisis a partir del momento de la muerte de los pacientes.
Características demográficas y basales de los pacientes con EPOC, en general y clasificados según hubieran tenido o no una agudización durante el seguimiento
| Todos los pacientes | Ninguna agudización durante el seguimiento totala | ≥ 1 agudización durante el seguimiento totala | |
|---|---|---|---|
| N=24.393 | n=5.492 | n=18.901 | |
| Edad (años) | |||
| Media | 67,9±11,6 | 62,4±4,3 | 69,5±12,5 |
| Mediana | 68,2 [59,2-76,5] | 63,5 [59,8-65,9] | 71,8 [58,7-78,7] |
| Sexo (mujeres)b | 5.308 (21,8) | 1.194 (21,7) | 4.114 (21,8) |
| Factores de riesgo conductuales | |||
| Consumo de tabaco | |||
| Fumadores | 7.800 (32) | 3.725 (67,8) | 4.075 (21,6) |
| Exfumadores | 12.302 (50,4) | 801 (14,6) | 11.501 (60,8) |
| No han fumado nunca | 4.291 (17,6) | 966 (17,6) | 3.325 (17,6) |
| Trastorno de consumo de alcohol | 1.044 (4,3) | 356 (6,5) | 688 (3,6) |
| Comorbilidades asociadas | |||
| Obesidad | 4.131 (16,9) | 1.349 (24,6) | 2.782 (14,7) |
| Diabetes mellitus tipo 2 | 4.190 (17,2) | 611 (11,1) | 3.579 (18,9) |
| Trastornos del metabolismo de las lipoproteínas | 12.263 (50,3) | 3.972 (72,3) | 8.291 (43,9) |
| Cardiopatías isquémicas | 4.345 (17,8) | 686 (12,5) | 3.659 (19,4) |
| Enfermedades hipertensivas | 14.576 (59,8) | 2.834 (51,6) | 11.742 (62,1) |
| IC y edema pulmonar | 5.311 (21,8) | 829 (15,1) | 4.482 (23,7) |
| Hipertensión pulmonar | 833 (3,4) | 113 (2,1) | 720 (3,8) |
| Tromboembolia venosa | 1.833 (7,5) | 257 (4,7) | 1.576 (8,3) |
| Enfermedad cerebrovascular | 2.408 (9,9) | 325 (5,9) | 2.083 (11) |
| Arritmia | 2.765 (11,3) | 409 (7,4) | 2.356 (12,5) |
| Asma actual | 2.490 (10,2) | 373 (6,8) | 2.117 (11,2) |
| Enfermedad renal crónica, insuficiencia renal | 2.598 (10,7) | 350 (6,4) | 2.248 (11,9) |
| Enfermedad mental grave | 3.633 (14,9) | 513 (9,3) | 3.120 (16,5) |
| Trastorno de ansiedad | 9.248 (37,9) | 1.745 (31,8) | 7.503 (39,7) |
| Número de visitas al MG en los 12 meses previos a la inclusión en la cohorte | |||
| Media | 7±3,5 | 3,9±2,2 | 7,9±3,3 |
| Mediana | 7 [5-9] | 4 [2-5] | 8 [6-10] |
| Número de agudizaciones (moderadas/graves) en los 12 meses previos a la inclusión en la cohorte | |||
| 0 | 20.153 (82,6) | 5.074 (92,4) | 15.079 (79,8) |
| 1 | 2.139 (8,8) | 382 (7,0) | 1.757 (9,3) |
| 2 | 1.312 (5,4) | 36 (0,7) | 1.276 (6,8) |
| ≥ 3 | 789 (3,2) | 0 | 789 (4,2) |
| Uso de medicaciónc | |||
| Uso de medicación inhalada de acción prolongada para la EPOC | 22.433 (92) | 4.948 (90,1) | 17.485 (92,5) |
| ICS | 14.451 (59,2) | 3.063 (55,8) | 11.388 (60,3) |
| LABA | 16.127 (66,1) | 3.409 (62,1) | 12.718 (67,3) |
| LAMA | 10.617 (43,5) | 2.248 (40,9) | 8.369 (44,3) |
| Inhalador de acción corta | 23.432 (96,1) | 5.000 (91,0) | 18.432 (97,5) |
| SABA | 23.307 (95,5) | 4.945 (90,0) | 18.362 (97,1) |
| SAMA | 2.546 (10,4) | 527 (9,6) | 2.019 (10,7) |
| Roflumilast | 447 (1,8) | 83 (1,5) | 364 (1,9) |
| Cualquier fármaco cardiaco | 22 285 (91,4) | 4.912 (89,4) | 17.373 (91,9) |
| Cualquier fármaco metabólico | 15.188 (62,3) | 3.248 (59,1) | 11.940 (63,2) |
EPOC: enfermedad pulmonar obstructiva crónica; IC: insuficiencia cardiaca; ICS: corticoide inhalado; LABA; agonista β2 de acción prolongada; LAMA; antagonista muscarínico de acción prolongada; MG: médico general; SABA: agonista β2 de acción corta; SAMA: antagonista muscarínico de acción corta.
El seguimiento total se definió como el tiempo transcurrido entre la inclusión en la cohorte y la primera de las siguientes opciones que ocurriera: el 31 de diciembre de 2019, la pérdida del seguimiento o el inicio del primer evento cardiovascular agudo grave de interés de cualquier tipo, incluida la muerte por cualquier causa.
Según lo registrado en las historias clínicas electrónicas obtenidas de la base de datos anonimizada BIG-PAC.
El uso de medicación se definió como la dispensación de una medicación de cada una de las clases (que podría formar parte de una combinación a dosis fijas), como mínimo en una ocasión en los 12 meses anteriores a la fecha de inclusión en la cohorte.
Los valores expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
De los 1.645.248 individuos de la base de datos BIG-PAC, se incluyó en la cohorte total (figura 1) a 24.393; de ellos, tenían EPOC de nuevo diagnóstico 12.713 (cohorte incidente). Se presentan las características demográficas y basales de la cohorte total (tabla 1) y de la cohorte incidente (tabla 3 del material adicional). En la comparación de los pacientes que nunca o en alguna ocasión sufrieron una agudización moderada o grave durante el seguimiento, las agudizaciones previas y la edad fueron las covariables con mayor diferencia entre los grupos, con valores de diferencias medias estandarizadas >0,1 (figura 2 del material adicional). Las medianas [intervalo intercuartílico] de seguimiento hasta la aparición de un primer evento cardiovascular, la muerte o la censura para el análisis fueron de 3,03 [1,04-5,90] y 2,46 [1,20-3,99] años en la cohorte total y la cohorte incidente. En la cohorte total, 14.299/24.393 pacientes (58,6%) presentaron al menos 1 agudización moderada y 2.314 (9,5%), al menos 1 agudización grave antes de un primer evento cardiovascular o la censura para el análisis; 18.865/24.393 (77,3%) tuvieron al menos 1 agudización moderada y 5.270/24.393 (21,6%), al menos 1 agudización grave durante el periodo total de seguimiento. En conjunto, 18.901/24.393 pacientes (77,5%) sufrieron al menos 1 agudización moderada o grave, con una media de 3,9(2,9) agudizaciones por paciente durante el periodo total de seguimiento.
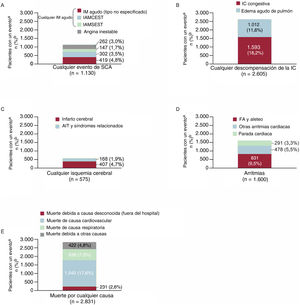
Análisis de la cohorte totalEventos cardiovasculares graves, incluida la muerte por cualquier causa, tras el inicio de una agudizaciónDurante el seguimiento, 8.741/24.393 pacientes de la población total (35,8%) presentaron al menos 1 evento cardiovascular grave no mortal (n=5.910; algún SCA, descompensación de IC, isquemia cerebral o arritmia) o muerte por cualquier causa (n=2.831) (figura 2). El evento cardiovascular grave no mortal más frecuente (29,8%) fue alguna descompensación de la IC (2.605/8.741), y de las 2.831 muertes por cualquier causa, las relacionadas con causas cardiovasculares fueron las más frecuentes (1.540; 54,4%).
Primer evento de interés (eventos cardiovasculares graves no mortales, según el tipo o muerte por cualquier causa) durante el seguimiento. AIT: accidente isquémico transitorio; FA: fibrilación auricular; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IC: insuficiencia cardiaca; IM: infarto de miocardio; SCA: síndrome coronario agudo.
aEn pacientes con múltiples eventos cardiovasculares durante el seguimiento, solamente se considera el primero de ellos, de modo que la suma de los pacientes de cada una de las categorías es igual al número total de pacientes.
bPorcentaje calculado empleando el número total de pacientes con eventos (8.741) como denominador.
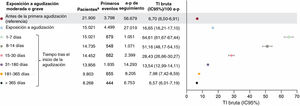
La TI bruta (IC95%) cada 100 años-paciente de un primer evento cardiovascular grave de cualquier tipo o muerte por cualquier causa fue 6,70 (6,50-6,91) durante el tiempo sin exposición antes de sufrir una agudización (o la censura para el análisis en ausencia de ella). Las TI brutas aumentaron en el periodo de 1 a 7 días tras el inicio de una agudización moderada o grave (64,61 [61,67-67,44]) y disminuyeron a 7,98 (7,42-8,59) en los días 181 a 365 y a 6,57 (6,01-7,19) más de 365 días tras el inicio de la agudización (figura 3). En la tabla 4 del material adicional se presentan las TI brutas de cada tipo de evento cardiovascular.
Valores brutos de la TI (IC95%) de un primer evento cardiovascular grave (evento no mortal o muerte por cualquier causa) en los periodos de tiempo con y sin exposición después del inicio de una agudización moderada o grave. Los periodos sombreados (incluido el tiempo anterior a la primera agudización y todo el periodo de seguimiento de los pacientes que no presentaron ninguna) son los considerados sin exposición a agudizaciones. a-p: años-paciente: IC95%: intervalo de confianza del 95%; TI: tasa de incidencia.
aNúmero de pacientes, de la población total de 24.393, que aportan al menos 1 día de datos en este periodo.
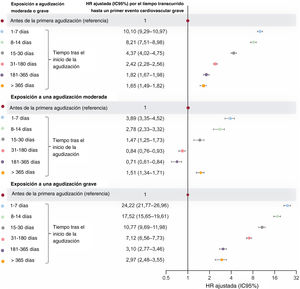
Por lo que respecta al tiempo sin exposición, la tasa de un primer evento cardiovascular grave, incluida la muerte por cualquier causa, aumentó en 10,1 veces los días 1 a 7 tras el inicio de una agudización moderada o grave; la tasa continuó estando aumentada pasados 365 días del inicio de la agudización (HR con ajuste completo, figura 4; HR sin ajustar, tabla 5 del material adicional).
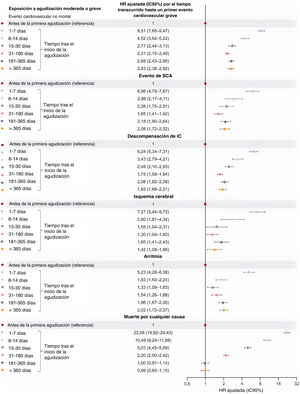
HR ajustada (IC95%) por el tiempo transcurrido hasta un primer evento cardiovascular grave (evento no mortal o muerte por cualquier causa) dentro de los periodos con exposición tras el inicio de una agudización moderada/ grave, moderada y grave, en comparación con el tiempo sin exposición (modelos multivariable con ajuste completo). Los periodos sombreados (incluidos el tiempo anterior a la primera agudización y todo el periodo de seguimiento de los pacientes que no presentaron ninguna) son los considerados sin exposición a agudizaciones. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Se observaron patrones similares de aumento del riesgo en los periodos siguientes al inicio de las agudizaciones moderadas y de las agudizaciones graves (figura 4). Hubo un aumento de 24,2 y 17,5 veces en la tasa en los días 1 a 7 y 8 a 14 tras el inicio de la agudización grave. El riesgo después de una agudización grave se redujo con el paso del tiempo, pero continuaba siendo significativamente superior pasados más de 365 días del inicio de la agudización en comparación con lo observado durante el tiempo sin exposición. Hubo un aumento de 3,9 y 2,8 veces en las tasas en los días 1 a 7 y 8 a 14 tras el inicio de una agudización moderada.
Riesgo de un evento cardiovascular grave, incluida la muerte por cualquier causa, según el tipo de evento tras el inicio de la agudizaciónEl riesgo de cada uno de los tipos de eventos cardiovasculares no mortales aumentó durante cada periodo especificado en los 365 días posteriores al inicio de una agudización moderada o grave, y se observaron aumentos sustanciales en las primeras 2 semanas (HR con ajuste completo, figura 5; HR sin ajustar, tabla 5 del material adicional). Las tasas de muerte por cualquier causa aumentaron en 22,1 y 10,5 veces los días 1 a 7 y 8 a 14 tras el inicio de la agudización, y el aumento se mantuvo los días 31 a 180.
HR ajustada (IC95%) por el tiempo transcurrido hasta un primer evento cardiovascular grave (según el tipo de evento) dentro de los periodos con exposición tras el inicio de una agudización moderada o grave, en comparación con el tiempo sin exposición (modelos multivariables con ajuste completo). Los periodos sombreados (incluidos el tiempo anterior a la primera agudización y todo el seguimiento de los pacientes que no presentaron ninguna) son los considerados sin exposición a agudizaciones. HR: hazard ratio; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; SCA: síndrome coronario agudo;.
Durante el seguimiento por el objetivo principal, 7.216/12.713 pacientes con EPOC incidente (56,8%) sufrieron al menos 1 agudización moderada o grave.
Durante el periodo total de seguimiento del estudio, 9.225/12.713 pacientes incidentes (72,6%) presentaron al menos 1 agudización moderada o grave; 8.551/12.713 (67,3%), al menos 2, y 6.652/12.713 (52,3%), al menos 3.
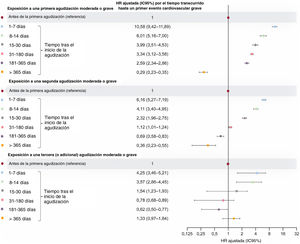
El aumento máximo del riesgo de un primer evento cardiovascular grave se produjo tras el inicio de la primera agudización moderada o grave; la exposición a una segunda, una tercera o más agudizaciones también aumentó el riesgo de eventos cardiovasculares en comparación con el tiempo sin exposición previo a la primera agudización (figura 6). La TI fue máxima en los días 1 a 7 tras el inicio de la agudización y tendió a ser inferior durante los periodos más alejados del inicio de la agudización.
HR ajustada (IC95%) por el tiempo transcurrido hasta un primer evento cardiovascular grave de cualquier tipo (evento no mortal o muerte por cualquier causa) dentro de los periodos con exposición tras el inicio de una primera, segunda y tercera (o adicional) agudización moderada o grave en comparación con el tiempo sin exposición (modelo multivariable con un ajuste completo; pacientes de nuevo diagnóstico). Los periodos sombreados (incluidos el tiempo anterior a la primera agudización y todo el seguimiento de los pacientes que no presentaron ninguna) son los considerados sin exposición a agudizaciones. Los valores de HR cuantifican los riesgos por separado de un evento cardiovascular grave después de una primera, segunda y tercera (o adicional) agudización moderada o grave en comparación con el tiempo sin exposición sin agudizaciones. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
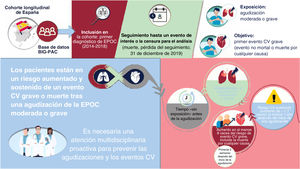
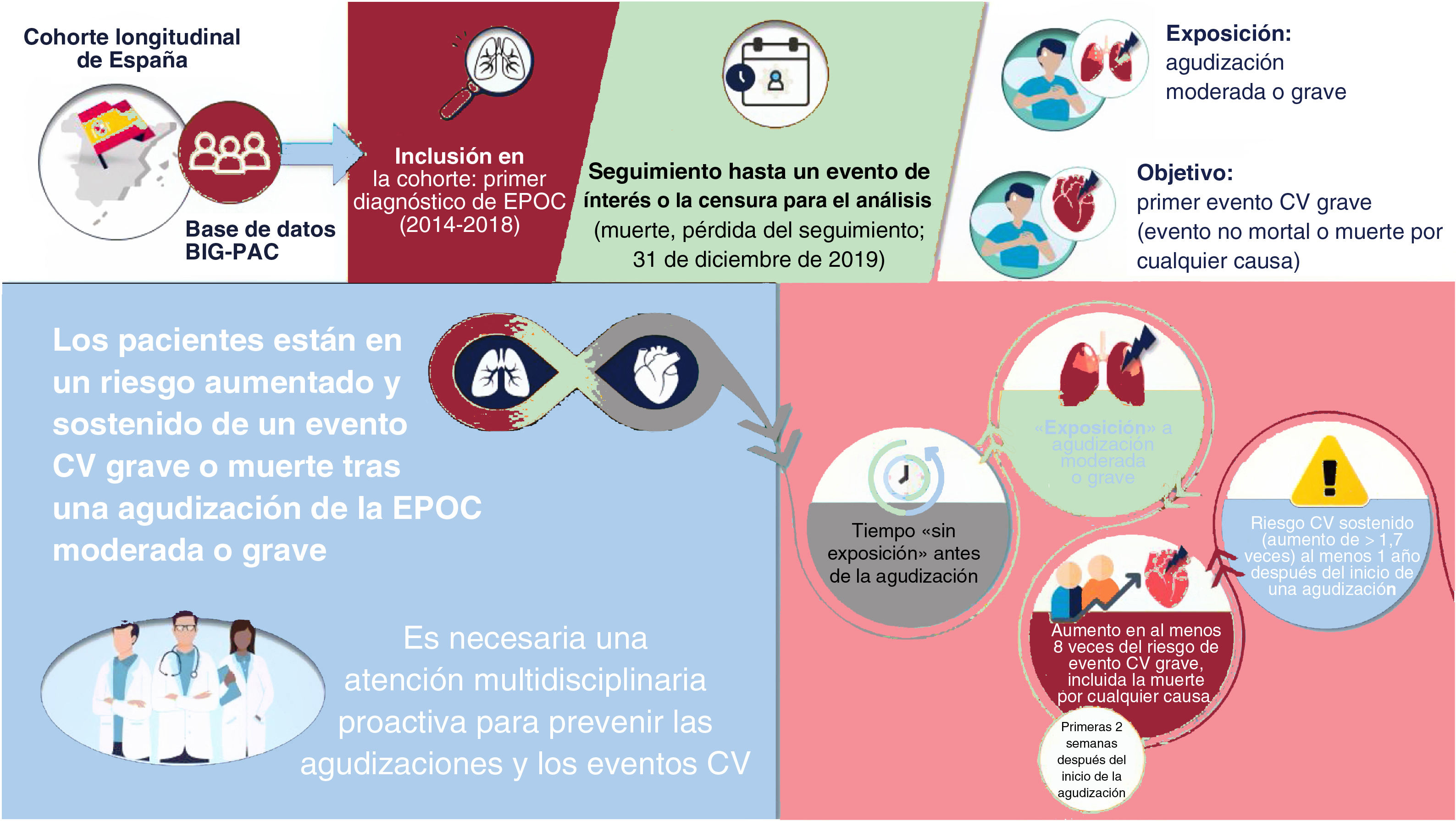
En este estudio de la práctica clínica real que evaluó el riesgo de eventos cardiovasculares tras las agudizaciones de la EPOC en España, estas se asociaron con un aumento del riesgo de eventos cardiovasculares graves o muerte por cualquier causa. El riesgo aumentó sustancialmente en el año siguiente a una agudización moderada o grave, y el aumento máximo se observó durante las primeras 2 semanas tras el inicio de la agudización. En la figura 7 se presenta una visión general del estudio, los resultados y la interpretación.
El riesgo cardiovascular aumentó después de las agudizaciones tanto moderadas como graves. Aunque las agudizaciones graves aumentaron el riesgo en mayor medida que las moderadas y durante más tiempo (es decir, más de 1 año), el riesgo de eventos cardiovasculares graves continuó estando sustancialmente aumentado hasta 30 días después del inicio de una agudización moderada. Pese a emplearse una definición estricta de las agudizaciones moderadas, un 77,3% de los pacientes sufrieron al menos 1 agudización moderada durante el periodo total de seguimiento, que fue de un promedio de aproximadamente 3 años. La elevada tasa de agudizaciones moderadas en esta población de España y su asociación con eventos cardiovasculares graves resaltan la importancia de prevenir cualquier agudización, sea cual sea su gravedad.
Se observó aumento del riesgo de diferentes tipos de eventos cardiovasculares, lo cual indica que puede intervenir en ello una gran variedad de mecanismos fisiopatológicos. El riesgo persistente de eventos cardiovasculares graves hasta 1 año después de la agudización indica la participación de mecanismos con un efecto a largo plazo, más allá de la inflamación sistémica asociada al periodo temprano de la agudización. Se han propuesto diversos mecanismos para explicar cómo la EPOC aumenta el riesgo de estrés cardiaco y eventos cardiopulmonares, entre ellos inflamación sistémica7,26, hiperinsuflación7,27, hipoxia7 y disfunción endotelial28,29. Estos mecanismos pueden verse potenciados durante las agudizaciones, con el efecto adicional de una hipercoagulabilidad7,26–28.
Incluso los pacientes que tuvieron una primera agudización moderada o grave presentaron un aumento del riesgo de eventos cardiovasculares graves. Estos resultados resaltan aún más la importancia de prevenir todas las agudizaciones y deben motivar futuras investigaciones para esclarecer de qué manera el riesgo cardiovascular tras las agudizaciones puede depender del número acumulado de estas.
Por lo que respecta a los eventos cardiovasculares no mortales, los valores de HR ajustada por SCA y descompensación de la IC fueron de los más frecuentes en la primera semana tras el inicio de la agudización y más de 365 días después. Además, el primer evento cardiovascular no mortal más frecuente fue la descompensación de la IC. Esto tiene importancia clínica en la población española, ya que el SCA es una de las principales causas de muerte y morbilidad30 y la IC supone una importante preocupación de salud pública31,32; tanto el SCA como la IC se asocian con unos costes sustanciales de asistencia sanitaria30,31. Cabe destacar que los ingresos hospitalarios por IC aumentaron de 2003 a 201532, y el estudio HF-PATHWAYS indicó la necesidad de mejorar la optimización del tratamiento de los pacientes con IC y fracción de eyección reducida, que fue el fenotipo observado en el 51,7% de los pacientes en ese análisis22.
En este análisis, se observó menor riesgo de eventos cardiovasculares que en el periodo sin exposición los días 31 a 365 tras una agudización moderada (HR <1) frente a un riesgo superior más de 365 días tras la agudización (HR >1). El motivo de esta observación no está clara, pero podría estar relacionada con factores de confusión no medidos. Una reducción de casos vulnerables podría contribuir también a producir el resultado observado tras más de 365 días de la agudización.
Los resultados generales en esta población de pacientes con EPOC de España coinciden con lo observado en otros países participantes en el programa EXACOS-CV18–21. Al igual que en el presente estudio, en los estudios EXACOS-CV de Reino Unido18, Canadá19, Países Bajos20 y Alemania21, a los 12 meses del inicio de una agudización moderada o grave, las tasas de eventos cardiovasculares habían sido máximas en las primeras 2 semanas tras la agudización. En los distintos países, el riesgo de eventos cardiovasculares fue máximo en los días 1 a 14 tras la agudización en Reino Unido (HR ajustada [HRa]=3,19) y los días 1 a 7 tras la agudización en Canadá (HRa=15,86), Países Bajos (HRa=15,3) y Alemania (HRa=8,6). En el presente análisis, el riesgo de eventos cardiovasculares en España alcanzó también un máximo los días 1 a 7 tras la agudización (HRa=10,10), lo cual indica que estos datos, a grandes rasgos, están en línea con la gama de valores observados en otros países. Además, aunque los valores de HR de aumento del riesgo cardiovascular se reducían a medida que se alejaban del inicio de la agudización, el riesgo elevado persistió hasta 1 año en todos los países (HRa de 1,08 a 1,84).
Este estudio también aporta una perspectiva respecto a la carga de la enfermedad cardiovascular en los pacientes con EPOC de España. En la cohorte total al inicio del estudio, la prevalencia de enfermedades cardiovasculares y metabólicas —obesidad, diabetes mellitus tipo 2, trastornos del metabolismo de las lipoproteínas, cardiopatía isquémica, enfermedades hipertensivas, IC y arritmias— fue >10%. Esta observación concuerda con lo indicado por estudios previos de los factores de riesgo cardiovascular en los pacientes con EPOC en España5,8. En el estudio español CONSISTE, las prevalencias de IC (el 24,7 frente al 1,4%), arritmia (el 16,1 frente al 4,7%) y cardiopatía isquémica (el 12,5 frente al 4,7%) fueron significativamente mayores en los pacientes con EPOC que en aquellos sin EPOC8. La presencia de estos trastornos en nuestro estudio hizo que la mayoría de los pacientes estuvieran tomando medicaciones cardiacas (91,4%) o metabólicas (62,3%). Además, durante el tiempo sin exposición, hubo una incidencia sustancial de eventos cardiovasculares, con una TI (IC95%)/100 años-paciente de 6,70 (6,50-6,91) de un primer evento cardiovascular grave. En comparación, en un estudio de cohorte poblacional de Cataluña de 2018, los valores de TI de enfermedad cardiovascular/1.000 años-paciente fueron de entre 6,64 y 22,8 (varones) y entre 2,58 y 16,32 (mujeres) en personas de edad entre 40 y ≥ 70 años33. Por lo tanto, incluso en ausencia de agudizaciones, los pacientes con EPOC de España presentan una prevalencia elevada de comorbilidades cardiovasculares.
Esta prevalencia elevada de morbilidades cardiovasculares y metabólicas, junto con la relación observada entre las agudizaciones de la EPOC y los eventos cardiovasculares graves, resalta la carga sustancial de riesgo cardiopulmonar en esta población. La guía de EPOC de España (GesEPOC) recomienda considerar si hay una enfermedad cardiovascular cuando la EPOC de un paciente está mal controlada pese a tratamiento inhalatorio y de que la expresión clínica principal sea la disnea34. Las estrategias para reducir el riesgo cardiopulmonar y la mortalidad prematura deben incluir la optimización de los tratamientos cardiovasculares a fin de controlar el riesgo cardiovascular y para la EPOC con objeto de prevenir las agudizaciones. Un estudio previo en España, en que también usó la base de datos BIG-PAC, respalda la importancia de optimizar el tratamiento y señala que los pacientes con EPOC que inician un tratamiento triple con un único inhalador evidencian una mejoría clínicamente relevante en persistencia en el tratamiento respecto a los que utilizan un tratamiento triple con varios inhaladores, y que ello comporta una reducción de las tasas de agudización y mortalidad23. En otros estudios se ha demostrado también que el inicio temprano del tratamiento reduce el riesgo de agudización y mejora los resultados35,36.
Aunque este estudio demostró que las agudizaciones de la EPOC son factores independientes del riesgo de un evento cardiovascular grave, no es fácil establecer una causalidad. Sin embargo, algunos aspectos del estudio y las fuentes de información externas pueden ser criterios útiles para evaluar la causalidad según lo propuesto por Hill37. En primer lugar, otros estudios en los que se ha explorado la asociación entre las agudizaciones de la EPOC y los posteriores eventos cardiovasculares aportan de manera uniforme resultados similares, sea cual sea el diseño de estudio y la base de datos empleada10,13,18–21, y la intensidad de la asociación observada en el presente estudio es sustancial. En segundo lugar, la exposición precedió al resultado, según indican los periodos de tiempo que van más allá de la fase sintomática (días 1-7). En tercer lugar, hay mecanismos fisiopatológicos bien descritos que subyacen a la asociación entre la EPOC y el aumento de riesgo de un deterioro funcional o anatómico cardiovascular6,7, y estos mecanismos apuntan a que una agudización de la EPOC puede actuar como desencadenante de eventos cardiovasculares graves.
LimitacionesEste estudio tiene limitaciones que deben tenerse en cuenta al interpretar sus datos, como la calidad variable de los datos procedentes de historias clínicas electrónicas, en especial por lo que respecta al riesgo de errores de diagnóstico. Por ejemplo, el solapamiento de síntomas entre la EPOC y la IC puede dificultar el diagnóstico diferencial38,39. Hay elementos comunes en la experiencia de disnea de los pacientes con EPOC o con IC congestiva40. Dado que existe un riesgo de error diagnóstico de un evento cardiovascular agudo grave interpretándolo como una agudización de la EPOC, el lapso de los días 1 a 7 tras el inicio de la agudización podría propiciar errores de clasificación y debe interpretarse teniéndolo presente. Sin embargo, el riesgo elevado más allá del periodo inicial de 7 días y luego hasta los 365 días y más allá indica que estas observaciones no se deben únicamente a un error de clasificación. Además, hay riesgo de que una agudización o un evento cardiovascular pasen inadvertidos cuando se emplea una base de datos secundarios, sobre todo si el paciente no ha informado a su médico o no ha acudido a un hospital que recopile los datos utilizados en el estudio. En nuestro estudio, la ausencia de un código médico se consideró indicativo de ausencia del trastorno; en las bases de datos administrativas, o hay un código (es decir, un código para un diagnóstico o para un procedimiento), lo cual significa que el paciente tiene el diagnóstico o se le ha practicado el procedimiento, o no lo hay, lo cual significa que el paciente no tiene la enfermedad, no se le ha practicado el procedimiento o falta la información. Por consiguiente, no es posible identificar o imputar la información que realmente falta en relación con los registros médicos. En los análisis de este estudio, todos los pacientes aportaron datos a los modelos.
Los posibles factores de confusión no medidos y los efectos de cohorte podrían haber influido también en los resultados. Concretamente, un efecto de supervivencia en el riesgo podría asociarse a una segunda y tercera (o adicional) agudización, ya que los pacientes tienen que permanecer en la cohorte durante el tiempo suficiente para esos eventos se produzcan. Por último, aunque no se incluyeron en el estudio biomarcadores de la congestión (p. ej., péptido natriurético cerebral) o de lesión miocárdica (p. ej., troponinas de alta sensibilidad), su consideración podría haber sido útil para aportar información a un primer diagnóstico diferencial e instaurar el tratamiento apropiado.
Una fortaleza clave de este estudio es que utilizó una cohorte poblacional de pacientes con EPOC, sin seleccionar solo a quienes tenían una enfermedad más grave. Además, la base de datos BIG-PAC es representativa de la población española22, por lo que estos resultados son generalizables a la población con EPOC de la práctica clínica real en España.
CONCLUSIONESEn este estudio se exploró, por primera vez, el riesgo de eventos cardiovasculares graves y muerte en una cohorte amplia de pacientes con EPOC de España. La prevalencia de la enfermedad cardiovascular fue alta, y las tasas de hospitalización por un evento cardiovascular grave o de muerte por cualquier causa aumentaron durante 180 o más días tras el inicio de una agudización de la EPOC. Aunque las agudizaciones graves se asociaron con un aumento del riesgo de eventos cardiovasculares, incluso una sola agudización aumentó también ese riesgo; en consecuencia, no debe minimizarse la repercusión clínica de las agudizaciones moderadas.
Estos resultados resaltan la necesidad de una atención multidisciplinaria proactiva de los pacientes con EPOC, con objeto de prevenir las agudizaciones y, posiblemente, abordar otros factores de riesgo cardiovascular y comorbilidades. Un abordaje proactivo debe incluir una mejora de los objetivos de prevención de los eventos cardiopulmonares en los pacientes con EPOC y una optimización del tratamiento farmacológico para los trastornos cardiovasculares y la EPOC.
- –
En los pacientes con EPOC de España hay una considerable carga de enfermedad cardiovascular.
- –
Las agudizaciones de la EPOC tanto moderadas como graves aumentan el riesgo de eventos cardiovasculares graves y muerte.
- –
No hay estudios previos en la práctica clínica real que hayan evaluado el riesgo de eventos cardiovasculares tras una agudización moderada o grave de la EPOC en España.
¿QUÉ APORTA DE NUEVO?
- –
En este análisis, los aumentos máximos de la TI se produjeron 2 o más semanas después del inicio de la agudización.
- –
El aumento del riesgo de eventos cardiovasculares se mantuvo durante al menos 1 año tras el inicio de la agudización.
- –
Los resultados de este estudio resaltan la necesidad de una atención multidisciplinaria proactiva de los pacientes para reducir el riesgo cardiopulmonar y la mortalidad prematura.
Este estudio fue financiado por AstraZeneca.
CONSIDERACIONES ÉTICASEl estudio se llevó a cabo cumpliendo la Declaración de Helsinki y fue aprobado por el Comité de Ética del Consorci Sanitari de Terrassa (protocolo AZ-EXA-2022-06, 13 de junio de 2022). Este es un estudio de datos secundarios totalmente anonimizados y no se necesita el consentimiento informado de los pacientes. El sexo se consideró un factor de confusión en nuestros modelos (tal como se describe en el párrafo final del apartado «Métodos») y las dimensiones relativas al sexo se presentan en los resultados. El sexo estaba registrado en las historias clínicas electrónicas obtenidas de la base de datos BIG-PAC anonimizada que incluía datos de hospitales y centros de atención primaria.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALEn la elaboración de este manuscrito no se han utilizado aplicaciones de inteligencia artificial.
CONTRIBUCIÓN DE LOS AUTORESBase conceptual, S. Santos, J. Sánchez-Covisa, K. Rhodes y C. Nordon; administración del proyecto, J. Sánchez-Covisa, I. Hernández, C. Corregidor y C. Nordon; recursos, J. Sánchez-Covisa, I. Hernández, C. Corregidor y C. Nordon; metodología, J. Sánchez-Covisa, L. Escudero, K. Rhodes y C. Nordon; gestión de los datos, I. Hernández; análisis formal, I. Hernández; validación, S. Santos, N. Manito, J. Sánchez-Covisa, I. Hernández, C. Corregidor, L. Escudero y C. Nordon; investigación, J. Sánchez-Covisa, C. Corregidor, K. Rhodes y C. Nordon; visualización, S. Santos, N. Manito, J. Sánchez-Covisa, I. Hernández, C. Corregidor, L. Escudero y C. Nordon; supervisión, S. Santos, N. Manito, J. Sánchez-Covisa, I. Hernández, C. Corregidor, L. Escudero, K. Rhodes y C. Nordon; financiación, J. Sánchez-Covisa, L. Escudero, C. Nordon; redacción — revisión y corrección, S. Santos, N. Manito, J. Sánchez-Covisa, I. Hernández, C. Corregidor, L. Escudero, K. Rhodes y C. Nordon.
CONFLICTO DE INTERESESS. Santos declara pagos por presentaciones y/o participación en consejos asesores científicos de AstraZeneca, Chiesi, GlaxoSmithKline, Grifols, Menarini, Novartis y Pfizer. N. Manito declara pagos por conferencias médicas y participación en consejos asesores científicos de AstraZeneca. J. Sánchez-Covisa, C. Corregidor, L. Escudero, K. Rhodes y C. Nordon son empleados de AstraZeneca y pueden poseer acciones y/u opciones de compra de acciones de la compañía. I. Hernández es empleado de Atrys Health, que fue contratada por AstraZeneca para la realización de este estudio.
Con la orientación de los autores, dieron apoyo a la redacción médica Sarah Piggott, MChem y Kirsty Ainscough, PhD, CMC Connect, una división de IPG Health Medical Communications, con la financiación de AstraZeneca, cumpliendo las directrices de Buenas Prácticas Clínicas (GPP 2022)41.