El presente artículo presenta las características y resultados del trasplante cardiaco realizado en pacientes de 16 o más años desde que empezó su actividad en España en mayo de 1984. Se realiza un análisis descriptivo de las características de receptores, donantes, procedimiento quirúrgico y resultados de los trasplantes cardiacos realizados en España hasta el 31 de diciembre de 2013. Durante 2013 se han realizado 219 procedimientos en pacientes de 16 o más años de edad en el momento del trasplante, con lo que la serie histórica consta de 6.632 trasplantes en pacientes de esas edades. En los últimos años, se observa un empeoramiento del perfil clínico tanto de los receptores (el 32% mayores de 60 años, el 23% con insuficiencia renal grave, el 19% con diabetes mellitus insulinodependiente, el 27% con cirugía cardiaca previa, el 15% con ventilación mecánica) como de los donantes (el 45% mayores de 45 años, el 25% con discordancia de peso > 20%) y el procedimiento (el 28% con tiempo de isquemia > 4 h y el 37% procedimientos urgentes). La supervivencia a 1, 5, 10 y 15 años es del 77, el 65, el 53 y el 37% respectivamente. Estas cifras permanecen estables desde 1995. La actividad de trasplante cardiaco en España muestra un lento declive en los últimos años. A pesar del claro empeoramiento en las características de donantes, receptores y tiempos quirúrgicos, se mantienen unos resultados en mortalidad comparables a los de nuestro entorno.
Palabras clave
Desde 1991, el Registro Español de Trasplante Cardiaco (RETC) viene publicando la descripción de las características clínicas y quirúrgicas y los resultados globales de los procedimientos de trasplante cardiaco (TxC) que se realizan en España1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24. Para afrontar la complejidad creciente del RETC y las distintas peculiaridades de las poblaciones objetivo de estudio, a partir de este año se presentarán informes diferenciados para la población pediátrica (receptores menores de 16 años) y la población adulta (receptores con 16 o más años en el momento del trasplante). El presente artículo describe los datos referentes a la población adulta trasplantada hasta el 31 de diciembre de 2013. Como ya es conocido, la mayor fortaleza del RETC reside en la inclusión y actualización exhaustiva de todos los procedimientos de TxC realizados en todos los hospitales de nuestro país desde mayo de 1984, independientemente de sus características y resultados. Además, la recogida de datos se realiza prospectivamente en una base de datos común consensuada y actualizada por todos los grupos.
MétodosPacientes y centrosDe los 17 centros que han aportado los datos al RETC de los pacientes trasplantados con 16 o más años de edad, actualmente permanecen activos 16 (Tabla 1). El número de procedimientos realizados en esta población anualmente se resume en la Figura 1. Los tipos de procedimientos realizados en 2013 y en la serie total se resumen en la Tabla 2.
Tabla 1. Centros participantes (por orden de realización del primer trasplante) en el Registro Español de Trasplante Cardiaco (1984-2013).
| 1. | Hospital de la Santa Creu i Sant Pau, Barcelona |
| 2. | Clínica Universitaria de Navarra, Pamplona, Navarra |
| 3. | Hospital Universitario Puerta de Hierro, Majadahonda, Madrid |
| 4. | Hospital Universitario Marqués de Valdecilla, Santander, Cantabria |
| 5. | Hospital Universitario Reina Sofía, Córdoba |
| 6. | Hospital Universitario y Politécnico La Fe, Valencia |
| 7. | Hospital General Universitario Gregorio Marañón, Madrid |
| 8. | Fundación Jiménez Díaz, Madrid * |
| 9. | Hospital Universitario Virgen del Rocío, Sevilla |
| 10. | Hospital Universitario 12 de Octubre, Madrid |
| 11. | Hospital Universitario de A Coruña, A Coruña |
| 12. | Hospital Universitario de Bellvitge, L’Hospitalet de Llobregat, Barcelona |
| 13. | Hospital Central de Asturias, Oviedo, Asturias |
| 14. | Hospital Clínic i Provincial, Barcelona |
| 15. | Hospital Universitario Virgen de la Arrixaca, El Palmar, Murcia |
| 16. | Hospital Universitario Miguel Servet, Zaragoza |
| 17. | Hospital Clínico Universitario, Valladolid |
* Este centro realizó trasplantes en el periodo 1989-1994.
Figura 1. Número anual de trasplantes en pacientes de 16 o más años en el momento del trasplante.
Tabla 2. Registro Español de Trasplante Cardiaco (1984-2013). Tipo de procedimiento en pacientes de 16 o más años de edad.
| Procedimiento | 2013 | 1984-2013 |
| Trasplante cardiaco de novo | 211 | 6.338 |
| Retrasplante | 3 | 156 |
| Trasplantes combinados* | 5 | 138 |
| Corazón-pulmón | 2 | 65 |
| Corazón-riñón | 3 | 65 |
| Corazón-hígado | — | 8 |
| Total | 219 | 6.632 |
* Seis de estos procedimientos fueron retrasplantes cardiacos.
La base de datos consta de 175 variables clínicas preestablecidas de manera consensuada por todos los grupos que recogen datos de receptor, donante, técnica quirúrgica, inmunosupresión y seguimiento. Desde 2013, los datos se introducen y se actualizan en formato electrónico en tiempo real mediante una aplicación disponible en internet específicamente diseñada para tal propósito. El soporte de la base es un fichero de Microsoft Excel. Este procedimiento sustituye al anterior, en el que cada centro enviaba los datos al Director del Registro en formato Microsoft Access mediante correo electrónico. Una CRO (contract research organization) externa (actualmente ODDS, S.L.) se encarga del mantenimiento de la base de datos, el control de calidad y el análisis estadístico.
La aprobación por el Comité Ético, la auditoría y el registro en el Ministerio de Sanidad se ha realizado según lo dispuesto en la Ley Orgánica de Protección de Datos 15/1999.
EstadísticaLas variables se presentan como media ± desviación estándar y porcentaje. Los resultados se categorizan según el año del trasplante dividiendo la muestra total en seis grupos de 5 años (1984-1988, 1989-1993, 1994-1998, 1999-2003, 2004-2008 y 2009-2013). Las diferencias entre grupos se analizan mediante un test no paramétrico para la tendencia temporal (tau de Kendall). Las curvas de supervivencia se han calculado mediante el test de Kaplan-Meier y la comparación entre ellas, con el método de log–rank test. A menos que se establezca de otra manera, los análisis de supervivencia incluyen los primeros trasplantes aislados, excluyendo retrasplantes y trasplantes combinados. Para el análisis específico del trasplante urgente en el periodo 2009-2013, se calculó la tasa de mortalidad a los 30 días del trasplante como número de muertes/1.000 pacientes-día de seguimiento. La comparación entre grupos de urgencia y el trasplante electivo se realizó mediante la razón de tasas (tasa de mortalidad grupo urgente/tasa de mortalidad trasplante electivo). Se ha considerado diferencia significativa las comparaciones con valor de p < 0,05.
ResultadosCaracterísticas de los receptoresEn 2013, los receptores tenían una media de edad de 52 ± 12 años; el 71% eran varones, con diagnósticos basales de miocardiopatía isquémica (28,1%), dilatada idiopática (20%), valvular (9,5%) y otras etiologías (42,4%). Como en años previos, en 2013 se aprecia también un porcentaje importante de pacientes con comorbilidades de reconocido impacto pronóstico a corto y medio-largo plazo, como creatinina > 2 mg/dl (28,1%), bilirrubina > 2 mg/dl (17%), diabetes mellitus insulinodependiente (20,6%), enfermedad pulmonar obstructiva crónica moderada-grave (12,4%), infección en los 15 días previos al trasplante (18,4%), cirugía cardiaca previa (32%) o ventilación mecánica previa al trasplante (17,9%).
Las características de los pacientes trasplantados según la era de trasplante se resumen en la Tabla 3. Se observa una tendencia muy significativa a mayor edad del receptor en el momento del trasplante. La media de edad del receptor se ha incrementado más de 10 años en el último lustro (2009-2013) en comparación con el periodo 1984-1988. En el periodo 2009-2013 prácticamente 1 de cada 3 trasplantados es mayor de 60 años. Igualmente, ha habido un incremento muy significativo en el porcentaje de mujeres trasplantadas y de cardiopatías con etiologías no convencionales (que incluyen una miscelánea de miocardiopatía hipertrófica, miocardiopatía restrictiva, displasia arritmogénica, cardiopatías congénitas en edad adulta, miocarditis, etc.). Se constata asimismo un incremento en condiciones de riesgo como disfunción renal, diabetes mellitus insulinodependiente, infección en los 15 días previos al trasplante y necesidad de ventilación mecánica previa al trasplante. En cambio, el retrasplante (un 2,4% de la serie total) ha permanecido aproximadamente estable en los sucesivos periodos del estudio, con tasas del 3,0, el 2,7, el 1,9, el 2,3, el 3,5 y el 1,7% respectivamente (p = 0,829 para la tendencia).
Tabla 3. Características del receptor de 16 o más años en el RETC (1984-2013) (excluidos retrasplantes y trasplantes combinados).
| 1984-1988 (n = 191) | 1989-1993 (n = 950) | 1994-1998 (n = 1.388) | 1999-2003 (n = 1.482) | 2004-2008 (n = 1.224) | 2009-2013 (n = 1.103) | Tendencia, p | |
| Edad (años) | 42,3 ± 10,8 | 49,3 ± 11,1 | 53,2 ± 10,4 | 52,6 ± 11,1 | 52,6 ± 11,5 | 53,5 ± 11,6 | < 0,001 |
| > 60 años, % | 1,0 | 12,3 | 26,1 | 24,9 | 26,7 | 32,2 | < 0,001 |
| Varones, % | 86,9 | 87,0 | 82,1 | 82,4 | 79,3 | 75,3 | < 0,001 |
| IMC | 23,4 ± 3,2 | 24,8 ± 3,7 | 25,4 ± 3,7 | 25,7 ± 4,2 | 25,6 ± 4 | 25,5 ± 4 | < 0,001 |
| Etiología de base, % | < 0,001 | ||||||
| Dilatada | 32,3 | 30,9 | 29,9 | 31,4 | 28,3 | 25,7 | |
| Isquémica | 30,2 | 37,5 | 39,1 | 34,9 | 29,4 | 30,6 | |
| Valvular | 10,1 | 11,6 | 9,3 | 7,4 | 9,5 | 7,6 | |
| Otras | 27,5 | 20,0 | 21,7 | 26,3 | 32,8 | 36,1 | |
| RVP (UW) | 2,7 ± 1,5 | 2,5 ± 1,7 | 2,3 ± 1,8 | 2,3 ± 1,8 | 2,4 ± 1,9 | 2,3 ± 2,1 | 0,003 |
| Creatinina > 2 mg/dl, % | – | 14,1 | 12,4 | 16,7 | 20,6 | 23,2 | < 0,001 |
| Bilirrubina > 2 mg/dl, % | 19,3 | 19,4 | 19,2 | 16,0 | 19,8 | 17,0 | 0,116 |
| Diabetes mellitus insulinodependiente, % | 8,3 | 8,0 | 10,3 | 15,8 | 17,3 | 18,6 | < 0,001 |
| EPOC moderada-grave, % | 6,5 | 10,1 | 13,1 | 10,9 | 10,7 | 9,0 | 0,020 |
| Infección previa, % | 2,7 | 4,3 | 6,8 | 10,2 | 12,6 | 14,3 | < 0,001 |
| Cirugía cardiaca previa, % | 20,0 | 23,9 | 28,1 | 23,3 | 24,3 | 27,0 | 0,015 |
| Ventilación mecánica pretrasplante, % | 4,1 | 7,8 | 8,3 | 9,2 | 14,1 | 15,3 | < 0,001 |
| Trasplante urgente, % | 7,5 | 18,5 | 21,6 | 22,1 | 28,7 | 36,9 | < 0,001 |
EPOC: enfermedad pulmonar obstructiva crónica; IMC: índice de masa corporal; RVP: resistencias vasculares pulmonares; UW: unidades Wood.
En 2013, la media de edad de los donantes era 43,9 ± 11,9 años. El 52,1% de ellos tenían una edad ≥ 45 años y el 55,5% eran varones. En el 10,4% de los casos, el peso del donante fue un 20% mayor que el del receptor, y sucedió lo contrario en el 20,9%. En el 25,1% de los casos, se implantó un injerto de donante mujer en un receptor varón.
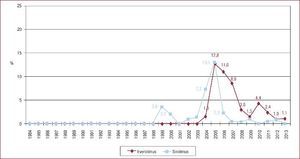
Las características de los donantes por periodo se resumen en la Tabla 4. Las causas de muerte del donante por periodo se resumen en la Figura 2. A lo largo de los periodos descritos se aprecia un incremento de los accidentes cerebrovasculares como principal causa de muerte, en contraposición a los traumatismos craneoencefálicos.
Tabla 4. Características del donante y tiempo de isquemia en trasplantes realizados en pacientes de 16 o más años en el Registro Español de Trasplante Cardiaco (1984-2013) (excluidos retrasplantes y trasplantes combinados).
| 1984-1988 (n = 191) | 1989-1993 (n = 950) | 1994-1998 (n = 1.388) | 1999-2003 (n = 1.482) | 2004-2008 (n = 1.224) | 2009-2012 (n = 1.103) | Tendencia, p | |
| Edad (años) | 25,2 ± 8,2 | 27,4 ± 10,3 | 31,1 ± 11,7 | 33,3 ± 12,6 | 36,3 ± 12,7 | 41,2 ± 12,1 | < 0,001 |
| Edad > 45 años, % | 1,2 | 9,2 | 16,9 | 23,3 | 31,7 | 45,3 | < 0,001 |
| Varones, % | 86,8 | 77,2 | 70,6 | 72,3 | 69,0 | 65,1 | < 0,001 |
| Donante mujer, receptor varón, % | 11,8 | 18,8 | 22,4 | 19,3 | 20,5 | 20,8 | 0,025 |
| Peso (kg) | 69 ± 9,6 | 70,7 ± 11,8 | 70,9 ± 11,7 | 73,5 ± 13,8 | 75,1 ± 13,2 | 76,3 ± 13,2 | < 0,001 |
| Razón peso receptor:donante | 0,97 ± 0,18 | 1,0 ± 0,18 | 1,02 ± 0,21 | 1,02 ± 0,52 | 1,04 ± 1,03 | 0,99 ± 0,82 | 0,43 |
| Razón peso receptor:donante > 1,20, % | 11,1 | 13,7 | 18,1 | 14,9 | 14,1 | 8,6 | < 0,001 |
| Razón peso receptor:donante < 0,8, % | 14,8 | 11,6 | 10,5 | 13,4 | 16,5 | 16,3 | < 0,001 |
| Tiempo de isquemia (min) | 130 ± 54 | 166 ± 61 | 180 ± 60 | 185 ± 61 | 198 ± 63 | 209 ± 62 | < 0,001 |
| < 120 min, % | 50,3 | 22,8 | 19,2 | 17,7 | 13,6 | 10,0 | < 0,001 |
| 120-180 min, % | 30,0 | 37,5 | 30,3 | 28,0 | 25,2 | 21,1 | |
| 180-240 min, % | 17,1 | 30,6 | 37,3 | 36,2 | 37,7 | 40,5 | |
| > 240 min, % | 2,7 | 9,1 | 13,3 | 18,1 | 24,3 | 28,4 | |
| Procedencia del injerto, % | < 0,0001 | ||||||
| Local | 18,2 | 21,2 | 22,1 | 26,8 | 20,5 | 15,9 | |
| Regional | 59,1 | 43,3 | 42,5 | 41,1 | 39,7 | 36,3 | |
| A distancia | 22,7 | 35,5 | 35,4 | 32,1 | 39,8 | 47,8 |
Figura 2. Evolución de las causas de muerte de los donantes cardiacos, por periodos.
En 2013, el tiempo de isquemia promedio fue 208 ± 58 min, con un 27,1% de los pacientes con isquemias > 4 h, tiempo a partir del cual se compromete de manera clínicamente significativa la viabilidad del injerto. Estos hallazgos resumen la tendencia observada en los últimos años (tabla 4). El tiempo de isquemia ha venido incrementándose a lo largo de la serie temporal, de tal manera que en el periodo 2009-2013 este excede en casi 1,30 h el tiempo en el periodo inicial 1984-1988. En el periodo más reciente (2009-2013), casi uno de cada tres procedimientos se realizó con un tiempo de isquemia > 4 h (tabla 4). La procuración del órgano a distancia se ha ido incrementando con el tiempo de manera estadísticamente significativa, de tal manera que en el periodo 2009-2013 se produjo en el 48% de los casos (tabla 4).
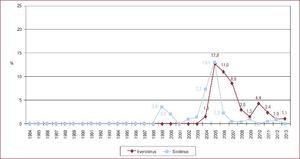
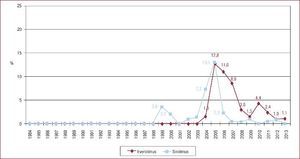
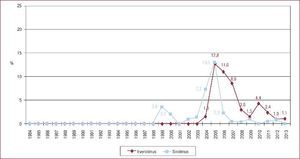
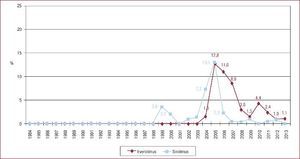
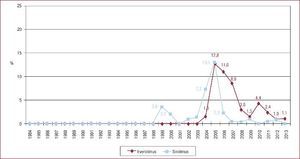
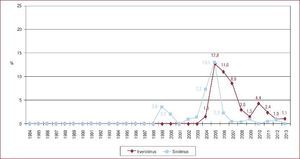
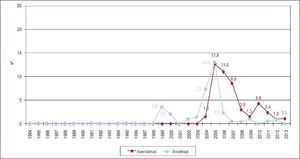
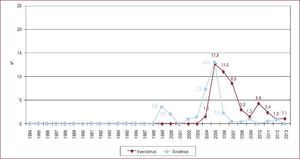
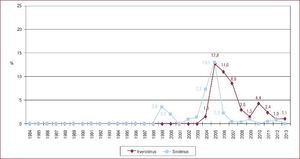
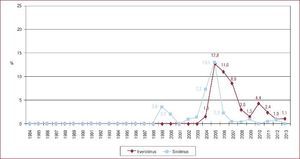
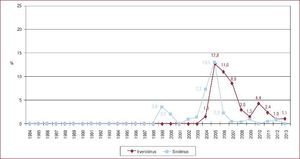
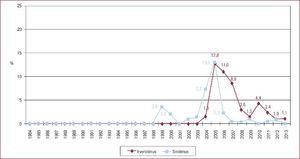
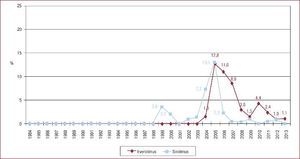
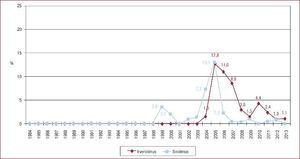
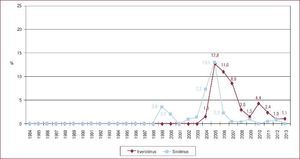
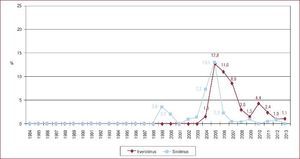
Trasplante cardiaco urgenteEl porcentaje de pacientes trasplantados con carácter de urgencia, aunque con amplias variaciones interanuales, ha ido incrementándose de manera progresiva y particularmente en el último quinquenio (Figura 3). En 2013 se ha alcanzado el porcentaje más alto de la serie (el 48,7% del total de procedimientos).
Figura 3. Evolución anual del porcentaje de trasplantes urgentes en pacientes trasplantados con 16 o más años de edad.
La característica más llamativa de los trasplantes urgentes es la utilización creciente de dispositivos de asistencia circulatoria (DAC) diferentes del tradicional balón de contrapulsación antes del trasplante (Figura 4). Esta tendencia es particularmente acusada a partir de 2009. Así, en 2009-2013, un 14,8% de todos los trasplantes se realizaron con algún tipo de estos dispositivos, frente al 15,5% con balón de contrapulsación. Un análisis más detallado de este periodo más reciente muestra, además, un cambio progresivo en el tipo de asistencia utilizada (Figura 5). El trasplante urgente realizado con balón de contrapulsación o sin ningún tipo de asistencia (por dificultad de inserción del balón, regurgitación aórtica grave o tormenta arrítmica) supuso un 70,3% del total de trasplantes urgentes en 2009. Los demás casos de ese año se distribuyeron casi equitativamente entre los trasplantes con oxigenación por membrana extracorpórea (14,3%) y DAC tipo pulsátil (13,1%). En cambio, en 2013 el uso aislado de balón se había reducido al 52%, mientras se duplicaba (29,4%) el uso de oxigenación por membrana extracorpórea y aumentaba el uso de DAC de tipo continuo (12,7%) en detrimento de los de tipo pulsátil (5,9%).
Figura 4. Distribución del tipo de asistencia ventricular previa al trasplante (porcentaje sobre población total de pacientes trasplantados con 16 o más años de edad), por periodos. DAV: dispositivo de asistencia ventricular; ECMO: membrana de oxigenación extracorpórea.
Figura 5. Distribución anual del tipo de dispositivo de asistencia circulatoria (porcentaje sobre el total de trasplantes urgentes) en pacientes trasplantados con 16 o más años de edad en el periodo 2009-2013. BCIA: balón de contrapulsación intraaórtico; ECMO: membrana de oxigenación extracorpórea.
InmunosupresiónEn 2013, el 85,3% de los receptores recibieron algún tratamiento inmunosupresor de inducción, en su inmensa mayoría con basiliximab (83,4%). En la Figura 6 se aprecia cómo la inducción ha ido incrementándose progresivamente hasta su uso casi generalizado actual. En el periodo más reciente (2009-2013), se induce a más del 80% de los pacientes con inhibidores de la interleucina 2 (basiliximab o daclizumab, fundamentalmente el primero).
Figura 6. Distribución (porcentaje de la población total) de la inmunosupresión de inducción en pacientes trasplantados con 16 o más años de edad, por periodos. ALG-ATG: globulina antilinfocitaria-globulina antitimocitaria.
La inmunosupresión de inicio en 2013 se realizó mayoritariamente con tacrolimus (79,4%) como inhibidor de la calcineurina, micofenolato mofetilo (97,5%) como antiproliferativo y corticoides (97,6%). En el análisis de la serie histórica, se constata el uso predominante de tacrolimus respecto a ciclosporina desde 2007 (Figura 7) y de micofenolato mofetilo respecto a azatioprina desde 2002 (Figura 8). En la Figura 9 se resumen los fármacos usados en la inmunosupresión inicial y al final del seguimiento para la serie total. En un seguimiento promedio de 6,8 años, el 58,1% de los pacientes continuaban en tratamiento con corticoides. Al cierre del seguimiento del presente análisis, un 26,4% de los pacientes estaban en tratamiento con un inhibidor de la m-TOR (everolimus, 22,3%; sirolimus, 4,1%) (Figura 9). La mayor parte del uso de estos fármacos se produce en la fase de mantenimiento del trasplante. Como inmunosupresión de inicio, solo se utilizaron de manera apreciable entre los años 2003 y 2007 (Figura 10).
Figura 7. Distribución anual (porcentaje de la población total) de los inhibidores de la calcineurina en inmunosupresión de inicio en pacientes trasplantados con 16 o más años de edad.
Figura 8. Distribución anual (porcentaje de la población total) de los antimitóticos en inmunosupresión de inicio en pacientes trasplantados con 16 o más años de edad. MMF: micofenolato mofetilo.
Figura 9. Porcentaje sobre la población total de uso de inmunosupresores en terapia de inicio y de mantenimiento en pacientes trasplantados con 16 o más años de edad. MMF: micofenolato mofetilo; SMF: ácido micofenólico.
Figura 10. Distribución anual (porcentaje de la población total) de los inhibidores de la m-TOR en inmunosupresión de inicio en pacientes trasplantados con 16 o más años de edad.
SupervivenciaEn la Figura 11 se resume la evolución de la mortalidad quirúrgica (primeros 30 días tras la cirugía) por años y quinquenios. En 2013 fue del 12,3%, ligeramente inferior, aunque sin significación estadística, a la de la cohorte histórica (15,2%).
Figura 11. Evolución anual del porcentaje de mortalidad quirúrgica precoz (primeros 30 días tras el trasplante) en receptores de 16 o más años de edad en el momento del trasplante. En la parte superior del gráfico, porcentajes promedio correspondientes a los periodos de estudio.
Con última actualización el 31 de diciembre de 2013, la supervivencia actuarial en el conjunto de la serie a 1 mes y a 1, 5, 10, 15 y 20 años se resume en la Figura 12. Esto supone una mortalidad promedio de un 2-3% anual aproximadamente, con una mediana de supervivencia de 10,9 años. Se aprecian diferencias significativas (p = 0,001) entre la supervivencia en el periodo 1984-1993 y las de 1994-2003 y 2004-2013. Entre estos dos últimos, parece haber tendencia a mejor supervivencia a partir del octavo año de trasplante en 2009-2013, sin significación estadística, lo cual se tendrá que confirmar con un seguimiento más largo. Las diferencias entre periodos se establecen durante el primer año de seguimiento postrasplante, y las curvas posteriores se mantienen prácticamente paralelas entre periodos (Figura 13).
Figura 12. Curva de supervivencia global de toda la serie de pacientes trasplantados con 16 o más años de edad.
Figura 13. Curvas de supervivencia para los decenios 1984-1993, 1994-2003 y 2004-2013.
Para la serie total, el trasplante urgente tiene una supervivencia significativamente peor (p < 0,00001) que la del trasplante electivo (Figura 14). Analizando el periodo 2009-2013, en el que el uso de DAC supone un porcentaje apreciable de los trasplantes realizados con carácter urgente, se observan diferencias significativas entre trasplante electivo, trasplante urgente realizado con balón de contrapulsación (urgente sin asistencia) y trasplante urgente realizado con DAC (Fig. 15). Las diferencias entre las curvas se establecen a partir de un exceso de mortalidad precoz (aproximadamente hasta los 6 meses del trasplante) en los urgentes. En ese periodo, el trasplante urgente presenta una tasa de mortalidad a los 30 días un 48% mayor que el electivo (p = 0,013). Sin embargo, respecto al trasplante electivo, las diferencias solo son significativas (p = 0,008) para los trasplantes urgentes realizados con oxigenación por membrana extracorpórea previa (Figura 16).
Figura 14. Curvas de supervivencia para la serie total del trasplante cardiaco electivo y urgente en receptores de 16 o más años en el momento del trasplante.
Fig. 15. Curvas de supervivencia para el periodo 2009-2013 del trasplante cardiaco electivo, urgente sin asistencia (balón de contrapulsación) y urgente con asistencia (oxigenación con membrana extracorpórea y dispositivos de asistencia ventricular tanto pulsátil como continua) en receptores de 16 o más años en el momento del trasplante.
Figura 16. Comparación de la razón de tasas de mortalidad precoz (primeros 30 días tras el trasplante) para el trasplante urgente (panel izquierdo), el trasplante urgente con balón de contrapulsación o dispositivos de asistencia circulatoria (panel central) y la oxigenación por membrana extracorpórea y dispositivos de asistencia ventricular en receptores de 16 o más años en el momento del trasplante. Todos los valores de p se refieren a la comparación respecto al trasplante electivo. BCIA: balón de contrapulsación intraaórtico; DAC: dispositivos de asistencia circulatoria; DAV: dispositivos de asistencia ventricular (pulsátil o continua); ECMO: membrana de oxigenación extracorpórea.
Causas de fallecimientoEn la serie total, las causas individuales más frecuentes fueron infección (13,9%), enfermedad vascular del injerto (el 12,4%, incluidos muerte súbita y «rechazo crónico»), fallo multiorgánico (12%), neoplasias (10,7%) y fallo agudo del injerto (8,1%). El rechazo agudo solo supuso un 3,9% de las causas de muerte totales. Las causas de fallecimiento cambian según el periodo postrasplante que se considere (Figura 17). En el primer mes postrasplante, el 40% de los fallecimientos se producen por fallo primario del injerto. Después del primer mes y hasta cumplir el primer año, el rechazo agudo y sobre todo las infecciones son la principal causa de muerte. Después del primer año, la causa mayoritaria son los tumores y las distintas manifestaciones de la enfermedad vascular del injerto (rechazo crónico, muerte súbita).
Figura 17. Causas de muerte según tiempo desde el trasplante en los receptores de 16 o más años en el momento del trasplante. FAI: fallo agudo del injerto.
DiscusiónEl presente análisis es el primero en la historia del RETC que se realiza específicamente para pacientes adultos, definidos como aquellos con edad ≥ 16 años en el momento del trasplante. Un informe dedicado a la población pediátrica se publica en este mismo suplemento. Esta segregación se basa principalmente en criterios científicos, ya que las poblaciones en estudio presentan marcadas diferencias en cuanto a características clínicas de los pacientes, procedimientos, tiempo en lista de espera, etc., con eventuales efectos significativos en los resultados. Permite asimismo un manejo más adecuado de una base de datos cada vez más grande y compleja y adapta la presentación a los procedimientos de registros internacionales, más específicamente el registro de la International Society for Heart and Lung Transplantation.
Este año se cumplen 30 años desde la realización del primer TxC viable en España. El carácter exhaustivo del RETC, con la inclusión de todos los pacientes trasplantados en España y con pérdidas de seguimiento prácticamente inexistentes, permite una visión en perspectiva y consistente de este procedimiento en nuestra población. No obstante, un análisis profundo explicativo de dichas tendencias no siempre es posible a partir del RETC, pues carece de algunos datos importantes, como el número de pacientes incluidos en lista de espera o el tiempo en lista de espera antes del trasplante.
En 2013 parece confirmarse la tendencia a la disminución en el número absoluto de trasplantes realizados, de forma similar a lo observado en el ámbito europeo25, junto con un incremento drástico en el porcentaje de procedimientos realizados con carácter de urgencia, que este año han alcanzado prácticamente el 50% del total, la cifra más alta de la serie histórica. Este incremento de urgencias es paralelo al aumento de trasplantes realizados con DAC, cuyo porcentaje prácticamente ha igualado este año el de los realizados con el tradicional balón de contrapulsación. En nuestra opinión, estos datos muestran un cambio histórico en el escenario del tratamiento de la insuficiencia cardiaca avanzada, tanto aguda como crónica, y suponen un reto organizativo y asistencial del sistema nacional de trasplante y de los hospitales con programas de trasplante al que necesariamente habrá que hacer frente de manera dinámica en los próximos años. Además, es predecible que esta tendencia se consolide en años venideros debido a la ampliación de la disponibilidad de los dispositivos de asistencia y el aumento de la pericia de los grupos trasplantadores en su manejo.
En el cambio de escenario descrito se incluyen también las significativas tendencias observadas en las características de receptores, donantes y el proceso quirúrgico del procedimiento. En general, es perceptible lo que se puede considerar empeoramiento de las condiciones en que se realiza el trasplante. Así, los receptores presentan edades más avanzadas, etiologías diferentes de las tradicionales miocardiopatía dilatada idiopática o isquémica, y más comorbilidades clínicamente significativas (disfunción renal, diabetes mellitus, infección previa, cirugía cardiaca o ventilación mecánica previas al trasplante). De igual manera, se usa a donantes de edad más avanzada (hasta ahora considerados subóptimos) y con causas de fallecimiento más relacionadas con comorbilidades significativas previas. Por último, es progresivamente más frecuente obtener el injerto a distancia, con la consiguiente prolongación del tiempo de isquemia, y aumentan los trasplantes con discordancia de sexo (particularmente los de receptor varón de donante mujer).
A pesar del aparente deterioro general de las condiciones del TxC, los resultados en mortalidad se mantienen e incluso muestran una ligera tendencia a mejorar, de momento no estadísticamente significativa. En nuestra opinión, esto indica fundamentalmente la rápida adaptación de nuestros experimentados equipos a las nuevas situaciones clínicas. Es probable que una parte de esta estabilidad en los resultados globales, particularmente los referidos al medio y largo plazo, se deba a los cambios en la inmunosupresión, con el paso a terapias más eficaces y con mejor perfil de seguridad. En este sentido, es llamativa la escasa repercusión de la incidencia de rechazo agudo en la mortalidad. No obstante, persisten las principales causas de muerte a medio-largo plazo, como la infección, las neoplasias y la enfermedad vascular del injerto, que al menos en parte podrían reducirse en un futuro como consecuencia de protocolos de inmunosupresión más individualizados.
Particular atención merece el análisis de los resultados en el contexto referido de trasplante urgente con uso creciente de DAC. El trasplante en situación de urgencia continúa teniendo mayor mortalidad que el electivo, particularmente debido al exceso de mortalidad precoz. Sin embargo, en el último quinquenio se observa que la realización de trasplante urgente con balón de contrapulsación presenta resultados prácticamente superponibles a los del trasplante electivo. El exceso de mortalidad se concentra, en cambio, en los trasplantes realizados con DAC, particularmente con el uso previo de membrana de oxigenación extracorpórea (ECMO). Un análisis mecanístico de este hallazgo está fuera del alcance del presente informe. No obstante, es probable que la adquisición de la curva de aprendizaje justifique en parte estos hallazgos, por lo que podría observarse una mejora en los próximos años. Por otra parte, es más probable que los peores resultados obtenidos con la ECMO reflejen las dificultades para mantener en mejor condición al paciente antes del trasplante, situación que es más fácilmente alcanzable con dispositivos de más larga duración.
ConclusionesEl TxC es actualmente la terapia de elección para los pacientes con insuficiencia cardiaca avanzada sin contraindicaciones absolutas. En España, asistimos a un cambio rápido del escenario clínico en que se realiza el trasplante, con procedimientos realizados en condiciones cada vez más complejas. La introducción progresiva de nuevas técnicas de asistencia circulatoria impone retos organizativos y asistenciales que han empezado a manejarse con creciente éxito, pero que todavía requieren un esfuerzo continuo, individual y colectivo para ofrecer resultados óptimos a nuestros pacientes.
AgradecimientosAgradecemos el soporte estadístico realizado por ODDS, S.L.
FinanciaciónEl Registro Español de Trasplante Cardiaco está parcialmente financiado por una beca no condicionada de Novartis.
Conflicto De InteresesF. González-Vílchez y M. Crespo Leiro: remuneración por participar en revisiones y desarrollo de presentaciones educativas de Roche, Astellas y Novartis.
AbreviaturasDAC dispositivos de asistencia circulatoria RETC Registro Español de Trasplante Cardiaco TxC trasplante cardiaco
AnexoColaboradores del Registro Español de Trasplante Cardiaco 1984-2013
| Hospital Universitario Puerta de Hierro, Majadahonda, Madrid | Javier Segovia-Cubero, Inés Sayado y Luis Alonso-Pulpón |
| Hospital Universitario y Politécnico La Fe, Valencia | Luis Martínez-Dolz, Ignacio Sánchez-Lázaro y Mónica Cebrián |
| Hospital Universitario de A Coruña, A Coruña | Maria J. Paniagua-Martín, Raquel Marzoa-Rivas y Eduardo Barge-Caballero |
| Hospital Universitario Reina Sofía, Córdoba | José M. Arizón del Prado, Amador Lopez-Granados y Juan Carlos Castillo-Dieguez |
| Hospital Universitario Marqués de Valdecilla, Santander, Cantabria | Manuel Cobo-Belaustegui, Miguel Llano-Cardenal, Jose A. Vázquez de Prada |
| Hospital General Universitario Gregorio Marañón (adultos), Madrid | Jesús Palomo, Adolfo Villa, Juan Fernández-Yáñez, Iago Sousa y Pablo Díez |
| Hospital Universitario 12 de Octubre, Madrid | Juan Delgado, María J. Ruiz, Pilar Escribano, Miguel A. Gómez y Marta Paradina |
| Hospital de la Santa Creu i Sant Pau, Barcelona | Eulàlia Roig, Vicenç Brosa, Sonia Mirabet, Laura López y Josep Padró |
| Hospital Universitario Virgen del Rocío, Sevilla | Ernesto Lage, José Manuel Sobrino y Diego Rangel |
| Hospital Universitario de Bellvitge, L’Hospitalet de Llobregat, Barcelona | Nicolás Manito, Josep Roca-Elías, José González-Costello y Joel Salazar-Mendiguchía |
| Clínica Universitaria de Navarra, Pamplona, Navarra | Gregorio Rábago, Beltrán Levy y Rafael Hernández |
| Hospital Clínic i Provincial, Barcelona | Félix Pérez Villa, Monserrat Cardona, Marta Farrero y M. Ángeles Castel |
| Hospital Universitario Central de Asturias, Oviedo, Asturias | José L. Lambert y Beatriz Díez de Molina |
| Hospital Universitario Virgen de la Arrixaca, El Palmar, Murcia | Iris Garrido |
| Hospital Universitario Miguel Servet, Zaragoza | Teresa Blasco, María L. Sanz-Julvé y Ana Portolés |
| Hospital Clínico Universitario, Valladolid | Luis de la Fuente, Javier López-Díaz y Amada Recio |
Autor para correspondencia: Servicio de Cardiología, Hospital Universitario Marqués de Valdecilla, Avda. Valdecilla s/n, 39008 Santander, Cantabria, España. Correo electrónico: (F. González–Vílchez). cargvf@gmail.com