En los pacientes con alto o muy alto riesgo cardiovascular, es primordial tratar los factores de riesgo y alcanzar los objetivos terapéuticos recomendados en las guías de práctica clínica para evitar el progreso y las futuras manifestaciones de la enfermedad. Una vez alcanzados los objetivos terapéuticos, puede persistir un riesgo elevado de progresión de la enfermedad, que se conoce como riesgo residual. Las guías de práctica clínica recomiendan valorar el riesgo residual de los pacientes que ya han alcanzado los objetivos. Para los pacientes con riesgo residual elevado, se recomiendan actuaciones orientadas principalmente a mejorar el perfil lipídico y se proponen medidas terapéuticas que pueden disminuir la incidencia de eventos cardiovasculares.
En este artículo se revisan la orientación de las guías y consensos recientes sobre el concepto de riesgo residual, sus fundamentos y las recomendaciones para mejorar la evolución de los pacientes con riesgo residual elevado.
Palabras clave
Las guías de práctica clínica hacen recomendaciones sobre actuaciones diagnósticas y terapéuticas sobre la base de los resultados de estudios científicos o, en ausencia de estudios sobre un aspecto específico, en la opinión de expertos en la materia. Hay diferentes grados de recomendación dependiendo del acuerdo que la respalda, sobre la base de datos científicos u opiniones de expertos, y se clasifican según la fuerza de la evidencia que las sustenta. En las tablas 1 y 2 se expone la clasificación habitualmente utilizada en las guías de práctica clínica de la Sociedad Europea de Cardiología1
Nivel de recomendación y grado de evidencia según la clasificación de la Guía de Prevención Cardiovascular de la Sociedad Europea de Cardiología1
| Definición | Significado | |
|---|---|---|
| Clase I | © | Está recomendada o indicada |
| Clase II | Resultados científicos conflictivos y/o divergencia de opinión sobre la utilidad o eficacia de un procedimiento o tratamiento | |
| Clase IIa | Mayor peso de la evidencia u opinión en favor de su utilidad o eficacia | Se debe considerar |
| Clase IIb | Utilidad o eficacia menos establecida por la evidencia u opinión | Se puede considerar |
| Clase III | Resultados científicos y/o acuerdo generalizado de que un procedimiento o tratamiento no es útil o efectivo y en algunos casos podría ser peligroso | No se recomienda |
| Nivel de Evidencia | Significado |
|---|---|
| A | Resultados derivados de múltiples ensayos clínicos aleatorizados o metanálisis |
| B | Resultados derivados de un único ensayo clínico aleatorizado o grandes estudios no aleatorizados |
| C | Consenso de opinión de expertos y o pequeños estudios, estudios retrospectivos o registros |
Las recomendaciones para prevenir problemas cardiovasculares son diferentes y dependen del riesgo de cada persona o paciente. Por eso las guías de prevención aportan criterios para clasificar a los pacientes según el nivel de riesgo de eventos futuros. La guía de prevención cardiovascular de la Sociedad Europea de Cardiología1 recoge 2 grupos de alto o muy alto riesgo:
- 1.
Grupo de muy alto riesgo:
- a.
Pacientes con enfermedad ateroesclerótica: demostrada por manifestaciones clínicas o técnicas de imagen (placas en angiografía, tomografía computarizada [TC] o ecograma carotídeo; no se incluye el incremento del grosor intimomedial).
- b.
Pacientes con diabetes mellitus (DM) tipo 2 o (tipo 1 después de los 40 años) y daño grave en órgano diana manifestado por alguno de los siguientes:
- •
Enfermedad renal crónica con filtrado glomerular < 45 ml/min/1,73 m2.
- •
Enfermedad renal crónica con filtrado glomerular entre 45 y 59 ml/min/1,73 m2 y microalbuminuria (cociente albúmina/creatinina en orina 30-300 mg/g).
- •
Proteinuria (cociente albúmina/creatinina en orina > 300 mg/g).
- •
Presencia de daño microvascular en al menos 3 territorios (por ejemplo, microalbuminuria, retinopatía y neuropatía).
- •
- c.
Enfermedad renal crónica grave con:
- •
Filtrado glomerular < 30 ml/min/1,73 m2.
- •
Filtrado glomerular entre 30 y 44 ml/min/1,73 m2 y cociente albúmina/creatinina en orina > 30 mg/g.
- •
- a.
- 2.
Grupo de alto riesgo:
- a.
Personas con un riesgo de enfermedad cardiovascular en los próximos 10 años estimada según las escalas SCORE2 y SCORE2-OP, > 7,5% en menores de 50 años, > 10% entre 51 y 69 años y > 15% en mayores de 70 años.
- b.
Pacientes con DM2 sin enfermedad cardiovascular ni lesión de órganos diana.
- c.
Pacientes no diabéticos con enfermedad renal crónica moderada (filtrado glomerular entre 30 y 44 ml/min/1,73 m2) y cociente albúmina/creatinina en orina < 30); con filtrado glomerular entre 45 y 59 ml/min/1,73 m2 y cociente albúmina/creatinina en orina entre 30 y 300 o pacientes con filtrado glomerular ≥ 60 ml/min/1,73 m2 y cociente albúmina/creatinina > 300.
- d.
Personas con hipercolesterolemia familiar y altas concentraciones de colesterol.
- a.
Los principales factores modificables del riesgo de enfermedad cardiovascular son la elevada concentración sanguínea de lipoproteínas que contienen apolipoproteína B (la mayoría de las cuales son lipoproteínas de baja densidad (LDL), la presión sanguínea elevada, el consumo de cigarrillos y la diabetes mellitus.
La Guía de Prevención de la Enfermedad Cardiovascular de la Sociedad Europea de Cardiología establece recomendaciones para el control de estos factores, con objetivos claros que se debe alcanzar para disminuir el riesgo de nuevas manifestaciones cardiovasculares1–3:
- •
Consumo de cigarrillos: abandono del hábito (clase I, nivel de evidencia A).
- •
Hipertensión arterial: conseguir cifras de presión arterial sistólica < 140 mmHg, < 130 mmHg si es bien tolerada, y presión diastólica < 80 mmHg (clase I, nivel de evidencia A).
- •
Lípidos: se recomienda una reducción de un 50 % y un valor de colesterol unido a lipoproteínas de baja densidad) (cLDL) objetivo de 55 mg/dl en pacientes con enfermedad cardiovascular previa (clase I, nivel de evidencia A). Para los pacientes con muy alto riesgo menores de 70 años sin enfermedad cardiovascular, esta recomendación es de clase IIa y nivel de evidencia C), y para pacientes con alto riesgo menores de 70 años, se recomienda un objetivo de cLDL de 70 mg/dl (clase IIa y nivel de evidencia C). Para los pacientes con un segundo acontecimiento cardiovascular en 2 años, es razonable que se trate de alcanzar un cLDL de 40 mg/dl o menos (clase IIb, nivel de evidencia B).
- •
Diabetes mellitus: el objetivo es obtener que la glucohemoglobina (HbA1c) sea < 7% (clase I, nivel de evidencia A) en la mayoría de los pacientes. Se recomienda utilizar inhibidores del cotransportador de sodio y glucosa tipo 2 (iSGLT2) o agonistas del receptor del péptido glucagón-like tipo 1 (aGLP-1) en los pacientes con enfermedad cardiovascular establecida (clase I, nivel de evidencia A).
Se aconseja disminuir el consumo de alcohol a menos de 100 g/semana y un estilo de vida saludable con respecto a la dieta, pobre en grasas saturadas y rica en fibra, con una dieta de tipo mediterráneo (clase Ia, nivel de evidencia A), realizar ejercicio aeróbico (clase Ia, nivel de evidencia A) y de fuerza (clase Ia, nivel de evidencia B) y mantener un peso adecuado (índice de masa corporal entre 20 y 25)
CONCEPTO DE RIESGO RESIDUAL. DISLIPEMIA ATEROGÉNICADespués de alcanzados los objetivos terapéuticos para los factores de riesgo cardiovascular, en pacientes adherentes al tratamiento y con buen cumplimiento de las recomendaciones sobre el estilo de vida, el riesgo de nuevos eventos cardiovasculares disminuye, pero persiste elevado y es heterogéneo.
El concepto de riesgo residual nació de la comprobación de que el tratamiento con estatinas disminuye el riesgo de nuevos problemas cardiovasculares, pero aún persiste un importante riesgo de eventos en pacientes con enfermedad cardiovascular previa o DM. El tratamiento con estatinas disminuye aproximadamente un 30% el riesgo de sufrir un nuevo evento cardiovascular, pero persiste el 70% restante4.
Las guías y consensos sobre prevención de la enfermedad cardiovascular en la práctica clínica definen el riesgo residual como el riesgo estimado, generalmente en pacientes con enfermedad cardiovascular ateroesclerótica establecida, después de los cambios realizados en el estilo de vida y del tratamiento de los factores de riesgo cardiovascular1,3.
Para los pacientes con enfermedad cardiovascular establecida, estas guías recomiendan la valoración individual del riesgo de nuevos acontecimientos cardiovasculares, una vez que se han alcanzado los objetivos terapéuticos de los factores de riesgo cardiovascular, ya que este riesgo varía considerablemente.
En los pacientes con síndrome coronario agudo (SCA), enfermedad vascular progresiva o DM y enfermedad vascular, el riesgo de recurrencia de la enfermedad cardiovascular es elevado. En otros pacientes con enfermedad cardiovascular establecida, el riesgo residual es menos evidente y puede estimarse a través de factores clínicos como la edad, los cambios en los factores de riesgo y los modificadores de riesgo o utilizando una calculadora de riesgo residual.
La guía de prevención de enfermedad cardiovascular de la Sociedad Europea de Cardiología enumera 2 instrumentos que pueden utilizarse para calcular el riesgo residual de los pacientes con enfermedad cardiovascular una vez controlados los factores de riesgo: Secondary manifestation of arterial disease risk score (SMART), que estima el riesgo residual a 10 años de un nuevo evento cardiovascular en pacientes con enfermedad coronaria, arteriopatía periférica o enfermedad cerebrovascular (está disponible como calculadora en la app ESC CV Risk) y European action in secondary and primary prevention y intervention to reduce events risk model (EUROASPIRE), que estima el riesgo de recurrencia a 2 años en pacientes con enfermedad coronaria.
El score SMART se deriva de un estudio de cohortes de 5.788 pacientes y la incidencia de infarto agudo de miocardio (IAM), ictus o muerte cardiovascular a 10 años. En el modelo predictivo se incluyen edad, sexo, tipo y años desde el evento cardiovascular previo, tabaquismo, DM, tratamiento antitrombótico, presión arterial sistólica, creatinina, proteína C reactiva, colesterol total, colesterol unido a lipoproteínas de alta densidad (cHDL) y cLDL. Se observó que un 21% de los pacientes tenían un riesgo bajo de un nuevo evento (< 10%) y el 23% tenía un riesgo muy alto (> 30%)5.
El score EUROASPIRE se deriva de los registros europeos EUROASPIRE IV y V, sobre 8.000 pacientes y se validó en 4.484 para la incidencia de muerte cardiovascular u hospitalización por IAM, ictus, insuficiencia cardiaca, cirugía coronaria o intervención coronaria percutánea. Los pacientes con hospitalización previa por insuficiencia cardiaca, ictus o intervención coronaria, con antecedentes de DM o enfermedad arterial periférica, con mayor concentración de colesterol no-HDL, menor filtrado glomerular, signos de ansiedad o depresión y que vivían en un país con alta incidencia de enfermedad cardiovascular presentaban una mayor incidencia de eventos cardiovasculares a los 2 años6.
Además del efecto de la falta de adherencia al tratamiento o a las recomendaciones sobre el estilo de vida, gran parte del riesgo residual se deriva de anormalidades lipídicas en pacientes cuyo objetivo de cLDL se ha alcanzado. Esto ocurre en una situación caracterizada por concentraciones de triglicéridos altas y de cHDL bajas, que se ha denominado dislipemia aterogénica. Esta situación no es infrecuente y hasta 2 tercios de los pacientes con enfermedad cardiovascular tratados con estatinas tienen bajas concentraciones de cHDL, mientras que se ha observado que hasta el 50% de los pacientes con enfermedad cardiovascular tienen cifras de triglicéridos > 150 mg/dl4.
Los valores de cLDL pueden ser normales o bajos en la dislipemia aterogénica, pero las partículas de LDL contienen más triglicéridos y menos colesterol y, al metabolizarse por la lipasa hepática, se transforman en LDL pequeñas y densas, que son más oxidables y aterogénicas. Las personas con LDL pequeñas y densas requieren mayor número de partículas para transportar la misma cantidad de colesterol, es decir, a igual concentración de cLDL, el número de LDL pequeñas circulantes es mayor, lo que supone mayor probabilidad de daño en el subendotelio vascular. La dislipemia aterogénica es frecuente en pacientes con obesidad, DM, insuficiencia renal crónica o síndrome metabólico7.
Las guías de práctica clínica nos recuerdan que las lipoproteínas aterogénicas son las < 70 nm que contienen apolipoproteína B (ApoB), incluidas las lipoproteínas de muy baja densidad (VLDL) y de densidad intermedia (IDL), además de las LDL. En general, las cifras de cLDL reflejan de modo fiable la concentración de lipoproteínas que contienen ApoB, pero no es así en pacientes con dislipemia aterogénica, ya que puede coexistir cifras de cLDL bajas y concentraciones elevadas de lipoproteínas ricas en ApoB. La determinación directa de ApoB es la opción más fiable para medir el riesgo cardiovascular de estos pacientes. La determinación de ApoB no está tan ampliamente disponible como las de colesterol total, cLDL y cHDL, y la determinación de colesterol no-HDL (colesterol total menos cHDL) sería una mejor medición del riesgo lipídico que el cLDL, ya que incluye todas las lipoproteínas aterogénicas ricas en ApoB (LDL, IDL y VLDL).
Los objetivos de ApoB o colesterol no-HDL recomendados son:
- •
ApoB, 65 mg/dl y colesterol no-HDL, 85 mg/dl cuando el objetivo de LDL sea 55 mg/dl.
- •
ApoB, 80 mg/dl y colesterol no-HDL, 100 mg/dl cuando el objetivo de LDL sea 70 mg/dl.
- •
ApoB, 100 mg/dl y colesterol no-HDL, 131 mg/dl cuando el objetivo de LDL sea 100 mg/dl.
Aunque las cifras de cLDL marcan el objetivo que deben alcanzar los pacientes con alto o muy alto riesgo cardiovascular, es necesario determinar las concentraciones de cHDL y triglicéridos para valorar una posible dislipemia aterogénica. Las concentraciones plasmáticas de cHDL bajas o de triglicéridos > 150 mg/dl se asocian con un aumento del riesgo (residual) en pacientes con enfermedad cardiovascular conocida.
TRATAMIENTO DE LAS ALTERACIONES LIPÍDICASLos fármacos recomendados (clase I, nivel de evidencia A) para alcanzar los objetivos de cLDL en pacientes con alto o muy alto riesgo son las estatinas, que pueden combinarse con ezetimiba o inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (PCSK9). Se puede valorar la opción de agregar un secuestrador de ácidos biliares a las estatinas si no se consiguen los objetivos de cLDL-c (IIb C). Para los pacientes que no toleran las estatinas, se recomienda el tratamiento con ezetimiba (IIa C) y añadir inhibidores de la PCSK9 si es necesario (IIb C)1,2. Se ha recomendado también la utilización de ácido bempedoico junto con estatinas y/o ezetimiba para los pacientes que no alcanzan los objetivos de cLDL o no toleran las estatinas (IIb B)8. Se ha demostrado que el ácido bempedoico disminuye las concentraciones de cLDL, colesterol no-HDL, ApoB y proteína C reactiva de alta sensibilidad y en el estudio CLEAR OUTCOMES, realizado en pacientes con alto riesgo cardiovascular e intolerancia a estatinas, el ácido bempedoico disminuyó el combinado de muerte cardiovascular, infarto de miocardio no mortal, ictus no mortal y revascularización coronaria en comparación con placebo9.
El ejercicio físico y un estilo de vida saludable son los mejores medios de aumentar el cHDL. No se ha mostrado ningún beneficio con las medidas farmacológicas específicamente dirigidas a incrementar la concentración de cHDL, como los inhibidores de la proteína de transferencia de éster de colesterol, que aumentan la concentración sanguínea de cHDL; aunque despertaron una gran expectativa, no se han demostrado beneficios clínicos significativos en los ensayos clínicos realizados2.
Para los pacientes con alto riesgo y cifras de triglicéridos > 200 mg/dl, se recomienda el tratamiento con estatinas (clase I, nivel de evidencia A) y cambios en el estilo de vida. Si los triglicéridos persisten elevados (> 200 mg/dl) después del tratamiento con estatinas y un estilo de vida cardiosaludable, se recomienda añadir fenofibrato o bezafibrato (clase IIb, nivel de evidencia B)1.
El tratamiento con fibratos disminuye el cLDL y los triglicéridos y aumenta el cHDL. Se ha demostrado que estos fármacos disminuyen la incidencia de eventos cardiovasculares, pero estos beneficios están en duda en los pacientes previamente tratados con estatinas10. En el estudio ACCORD (Action to Control Cardiovascular Risk in Diabetes) en pacientes con alto riesgo cardiovascular, la adición de fenofibrato a los tratados con simvastatina no redujo la incidencia de eventos cardiovasculares. En el análisis de subgrupos, sin embargo, los pacientes con valores de triglicéridos > 204 mg/dl y cHDL ≤ 34 mg/dl presentaron una tasa de eventos primarios (IAM, ictus o muerte cardiovascular) del 12,4% en el grupo tratado con fenofibrato y del 17,3% en el grupo tratado con placebo (ambos de pacientes también tratados con simvastatina)11. Este resultado positivo aún no se ha probado en estudios prospectivos.
El tratamiento con fibratos se recomienda para pacientes con valores de triglicéridos muy altos (≥ 900 mg/dl) para evitar la pancreatitis, junto con otras medidas como abstinencia de alcohol, tratamiento de la DM, etc. En combinación con estatinas, pueden aumentar el riesgo de rabdomiólisis; pueden utilizarse fenofibrato y bezafibrato, debe evitarse el gemfibrozilo (particularmente con simvastatina, pravastatina o lovastatina) y vigilar la aparición de síntomas musculares.1
En pacientes con alto o muy alto riesgo y triglicéridos > 135 mg/dl después del tratamiento con estatinas y estilo de vida cardiosaludable, las guías de práctica clínica también recomiendan otra opción de tratamiento con ácidos grasos poliinsaturados omega-3 o con icosapento de etilo, en grado similar a los fibratos (clase IIa o IIb, nivel de recomendación B).
Los ácidos grasos omega 3 son el ácido eicosapentaenoico (EPA) y el ácido docosahexaenoico (DHA), pero ambos tienen propiedades biológicas y electrofisiológicas diferentes. El estudio GISSI Prevenzione mostró que 1 g/día de una combinación de EPA y DHA en pacientes que habían sufrido un infarto de miocardio en los últimos 3 meses redujo un 20% a los 3,5 años el combinado de muerte cardiovascular, IAM e ictus12. Pero el estudio GISSI Prevenzione se realizó a finales de los años noventa, y la tasa de revascularización y el uso de estatinas era escaso. Estudios posteriores de combinación de ambos ácidos grasos resultaron negativos en demostrar un beneficio clínico en prevención primaria o secundaria. Un ensayo clínico más reciente, el STRENGTH, comparó el tratamiento con 4 g/día de una formulación de EPA y DHA frente a placebo en pacientes con alto riesgo, con y sin enfermedad cardiovascular previa, concentraciones de triglicéridos altas y de cHDL bajas, y no observó un beneficio clínico13.
El icosapento de etilo es un éster etílico estable del EPA aprobado por la Food and Drugs Administration (FDA) de Estados Unidos como complemento alimenticio para personas con valores elevados de triglicéridos (> 500 mg/dl)14. Su importancia en el tratamiento de los pacientes con alto riesgo cardiovascular proviene de los resultados del estudio REDUCE-IT (Reduction of Cardiovascular Events with Icosapent Ethyl Intervention Trial) en el que mostró, en pacientes con alto riesgo previamente tratados con estatinas, cLDL entre 41 y 100 mg/dl y triglicéridos entre 135 y 499 mg/dl, que se producía una reducción de eventos clínicos cardiovasculares frente a placebo15. La incidencia de muerte cardiovascular, infarto agudo de miocardio, ictus, revascularización o angina inestable se presentó, después de una mediana de 4,9 años de seguimiento, en el 17% de los pacientes tratados con icosapento de etilo y el 22% del grupo de placebo (Hazard ratio [HR] = 0,75; intervalo de confianza del 95% [IC95%], 0,68-0,83). El icosapento de etilo es el único tratamiento del que se ha demostrado que disminuye los eventos clínicos en los pacientes tratados con estatinas y triglicéridos > 150 mg/dl por un mecanismo diferente de la disminución del cLDL.
Aunque el estudio REDUCE-IT se publicó en 2019, varias guías y consensos publicados posteriormente establecen una recomendación de clase IIa o IIb, probablemente porque no se observaron grandes cambios en el perfil lipídico del grupo de tratamiento con icosapento de etilo (mediana de reducción de triglicéridos, 18% [39 mg/dl]), las dudas sobre el posible efecto negativo del aceite mineral utilizado como placebo (mediana de incremento del cLDL en el grupo de placebo, 7 mg/dl [10,2%] frente a un incremento de 3,1 mg/dl [2%] en el grupo de icosapento de etilo) y el desconocimiento del mecanismo biológico del beneficio clínico1-3,8.
En el documento de consenso para la utilización de icosapento de etilo en pacientes con hipertrigliceridemia, elaborado entre la Sociedad Española de Cardiología y la Sociedad Española de Diabetes, se propone tratar con IPE a los pacientes de alto o muy alto riesgo ya tratados con estatinas y con niveles plasmáticos de triglicéridos entre 200 y 499 mg/dl16.
Hace unos meses se publicó una guía del National Institute for Health and Care Excellence (NICE) que evalúa la utilidad del icosapento de etilo combinado con el tratamiento con estatinas para la reducción del riesgo cardiovascular de los pacientes con cifras elevadas de triglicéridos17. En esa guía se recomienda la utilización del icosapento de etilo (2 g cada 12 h) en pacientes con:
- •
Antecedentes de enfermedad cardiovascular (síndrome coronario agudo, revascularización arterial, enfermedad coronaria, ictus o arteriopatía periférica).
- •
Tratamiento con estatinas.
- •
Concentración de triglicéridos en ayunas > 150 mg/dl.
- •
Concentración de cLDL entre 40 y 100 mg/dl.
El Consenso Latinoamericano para el tratamiento del riesgo residual metabólico considera que el riesgo residual (el que persiste después de alcanzar los objetivos para los factores de riesgo clásicos) es un concepto que, aunque nacido de las alteraciones lipídicas y su tratamiento, debe extenderse a otros factores que influyen en el desarrollo de la enfermedad cardiovascular3. Este concepto de riesgo residual es el generalmente aceptado y otras recomendaciones de las guías para reducir el riesgo residual se orientan a mecanismos no relacionados con el perfil lipídico.
DIABETES MELLITUSLos nuevos fármacos antidiabéticos inhibidores del cotransportador de sodio-glucosa tipo 2 (iSGLT2) y los agonistas del receptor del péptido similar al glucagón tipo 1 (GLP-1) han mostrado beneficios cardiovasculares adicionales al control glucémico, independientemente del tratamiento con metformina. Se ha demostrado que estos fármacos reducen los eventos cardiovasculares, la mortalidad total y cardiovascular, la hospitalización por insuficiencia cardiaca y el deterioro de la función renal18,19.
Los resultados de los ensayos clínicos realizados indican que los iSGLT2 tienen un mayor beneficio en pacientes con insuficiencia cardiaca o deterioro de la función renal y los agonistas del receptor de GLP-1 en pacientes con enfermedad cardiovascular establecida. Ambos fármacos son eficaces para disminuir el peso corporal, con una mayor eficacia de los agonistas GLP-1, efecto que también disminuye el riesgo cardiovascular relacionado con la obesidad20.
La guía de prevención cardiovascular de la Sociedad Europea de Cardiología recomienda los iSGLT2 o los agonistas del receptor GLP-1 para pacientes con DM y enfermedad cardiovascular (clase I, nivel de evidencia A), mientras que para los pacientes diabéticos y con lesión de órgano diana sin enfermedad cardiovascular la recomendación no está clara (clase IIb y nivel de evidencia B). Para los pacientes con insuficiencia cardiaca o enfermedad renal crónica, los iSGLT2 son los fármacos recomendados (clase I, nivel de evidencia A). Para los pacientes diabéticos sin enfermedad cardiovascular, insuficiencia cardiaca o enfermedad renal crónica, la utilización de ambos fármacos debe considerarse como terapia preventiva (clase IIA, nivel de evidencia B).1
TRATAMIENTO ANTITROMBÓTICOEl efecto protector antiagregante plaquetario del ácido acetilsalicílico (AAS), a dosis de 75-100 mg/día, está bien establecido (clase I, nivel de evidencia A) en pacientes con antecedentes de infarto agudo de miocardio o revascularización. En los pacientes con enfermedad coronaria, alto riesgo isquémico y alto riesgo hemorrágico, debe considerarse la adición de un inhibidor de P2Y12 (clopidogrel, ticagrelor o prasugrel) o rivaroxabán a dosis de 2,5 mg/12 h (clase IIA, nivel de evidencia A).
Con la doble antiagregación plaquetaria con AAS y ticagrelor (60 mg/12 h) prolongada, se ha demostrado reducción de los eventos cardiovasculares en comparación con AAS solo (el 7,77 frente al 9,04%; HR = 0,84; IC95%, 0,74-0,95) en pacientes con IAM previo (entre 1 y 3 años), después de un seguimiento de 3 años21.
La combinación de rivaroxabán 2,5 mg/12 h añadido al AAS frente a AAS solo ha mostrado disminución de la incidencia de un combinado de infarto de miocardio, ictus o muerte cardiovascular en pacientes con enfermedad coronaria estable (el 4 frente al 6%; HR = 0,74; IC95%, 0,64-0,86) tras un seguimiento medio de 1,95 años, aunque con una mayor incidencia de hemorragias (el 4 frente al 3%; HR = 0,77; IC95%, 0,65-0,90) principalmente gastrointestinales22. Así, la combinación de rivaroxabán y AAS es una opción de tratamiento para los pacientes con un alto riesgo isquémico siempre que el riesgo hemorrágico sea bajo.
INFLAMACIÓN Y RIESGO CARDIOVASCULARLa inflamación tiene un importante papel en el desarrollo de la arterioesclerosis, y varios estudios con tratamientos antiinflamatorios han mostrado resultados positivos para prevenir la progresión de la enfermedad y los eventos clínicos.
El primer estudio publicado sobre tratamiento antiinflamatorio fue el CANTOS23. Este estudio, realizado en 10.061 pacientes con infarto agudo de miocardio y proteína C reactiva de alta sensibilidad > 2 mg/l, probó que el canakinumab, un anticuerpo dirigido contra la interleucina 1β, en inyección subcutánea cada 3 meses, disminuye la incidencia del combinado de muerte cardiovascular, ictus o infarto agudo de miocardio. Sin embargo, produjo un aumento de las infecciones que, junto con su elevado coste, frenó el desarrollo de este producto en esta indicación.
Dos estudios demostraron el efecto positivo de la colchicina, un fármaco antiinflamatorio, en pacientes con enfermedad coronaria previa. En el estudio COLCOT, el tratamiento con colchicina (0,5 mg/24 h) frente a placebo disminuyó la incidencia de eventos cardiovasculares en pacientes que había sufrido un infarto agudo de miocardio 30 días antes24. La incidencia de muerte cardiovascular, parada cardiaca resucitada, infarto agudo de miocardio, ictus u hospitalización urgente por angina inestable con revascularización fue del 5,5% en el grupo tratado con colchicina frente al 7,1% en el grupo tratado con placebo (HR = 0,77; IC95%, 0,61-0,96; mediana de seguimiento, 22,6 meses). Resultados similares con la misma dosis de colchicina se observaron en el estudio LoDoCo2 en pacientes con enfermedad coronaria crónica, pero se observó un incremento no significativo en la mortalidad total25.
La recomendación actual de tratamiento con colchicina para pacientes con enfermedad coronaria e insuficiente control de los factores de riesgo o con tratamiento óptimo y recurrencias es de clase IIb con nivel de evidencia A.
CONCLUSIONESRiesgo residual es aquel que persiste una vez alcanzados los objetivos terapéuticos recomendados de cLDL, glucemia e hipertensión arterial y adoptadas las medidas saludables de estilo de vida. Las guías de práctica clínica recomiendan determinar el riesgo residual de los pacientes con alto o muy alto riesgo. El tratamiento del perfil lipídico aterogénico (concentraciones de triglicéridos altas y de cHDL bajas) y el incremento del tratamiento antitrombótico o adición de colchicina deben ser individualizados (clase IIa o IIb).
El icosapento de etilo se ha recomendado recientemente en la guía del NICE para la prevención secundaria de pacientes en tratamiento con estatinas, buen control del cLDL y triglicéridos > 150 mg/dl. Los nuevos fármacos antidiabéticos iSGLT2 o agonistas del receptor de GLP-1 son una importante ayuda terapéutica para disminuir el riesgo cardiovascular de los pacientes diabéticos con enfermedad cardiovascular, insuficiencia cardiaca o enfermedad renal crónica.
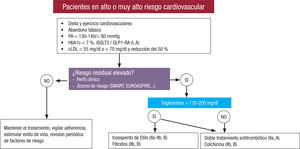
La figura 1 resume las recomendaciones de las guías de práctica clínica de publicación más reciente sobre el riesgo residual y las opciones terapéuticas para disminuirlo.
Ilustración central. Esquema de las recomendaciones de las guías de práctica clínica sobre el tratamiento del riesgo residual. cLDL: cholesterol unido a lipoproteínas de baja densidad; EUROASPIRE: European action in secondary and primary prevention y intervention to reduce events6; GLP1-RA: agonistas del receptor del péptido similar al glucagón tipo 1; HbA1c: glucohemoglobina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2; PA: presión arterial; SMART: Secondary Manifestations of Arterial Disease5.
Los autores han participado en la redacción del manuscrito y la revisión de forma proporcional y aceptan su publicación.
INFORMACIÓN SOBRE EL SUPLEMENTOEste artículo forma parte del suplemento titulado “Riesgo cardiovascular residual: nuevos enfoques”, el cual ha sido financiado por la sección de Riesgo Vascular y Rehabilitación Cardiaca de la Sociedad Española de Cardiología.