El objetivo de este estudio es analizar la prevalencia, los factores de riesgo y el pronóstico hospitalario y a largo plazo de los pacientes con síndrome coronario agudo y función renal normal que presentan nefropatía tras intervencionismo coronario percutáneo.
MétodosEstudio observacional, retrospectivo y unicéntrico con seguimiento prospectivo de 470 pacientes consecutivos ingresados por síndrome coronario agudo sin shock cardiogénico y sometidos a intervencionismo coronario percutáneo sin insuficiencia renal preexistente (creatinina al ingreso ≤1,3mg/dl). La nefropatía tras intervencionismo coronario percutáneo se ha definido como un incremento de la creatinina basal ≥0,5mg/dl o≥25% del valor basal. La media de seguimiento fue 26,7±14 meses.
ResultadosDe los 470 pacientes, 30 (6,4%) presentaron nefropatía tras intervencionismo coronario percutáneo. Los factores independientes predictores de insuficiencia renal aguda fueron la hemoglobina al ingreso (odds ratio=0,71) y la troponina I máxima previa al intervencionismo (odds ratio=1,02). En el seguimiento a largo plazo, los pacientes cuya función renal se deterioró presentaron mayor incidencia de mortalidad total (5 [16,7%] frente a 27 [6,1%]; p=0,027). En el análisis de regresión de Cox, la nefropatía tras intervencionismo coronario percutáneo no resultó predictora independiente de la mortalidad total, pero podría ser predictora de la mortalidad cardiaca (hazard ratio=5,4; intervalo de confianza del 95%, 1,35-21,3; p=0,017).
ConclusionesLa nefropatía tras intervencionismo coronario percutáneo en pacientes con síndrome coronario agudo y función renal preexistente normal no es infrecuente e influye en la supervivencia a largo plazo.
Palabras clave
El incremento de la creatinina plasmática tras un intervencionismo coronario percutáneo (ICP) no es infrecuente y se ha asociado a un pronóstico adverso1. El desarrollo de nefropatía tras ICP se asocia a un importante aumento de la morbimortalidad y a incremento de las estancias y los costes hospitalarios2–4. Las causas de insuficiencia renal aguda tras un procedimiento de revascularización coronaria percutánea son muy variadas e incluyen nefrotoxicidad del contraste, alteraciones hemodinámicas, toxicidad farmacológica y ateroembolia. El grado de insuficiencia renal preexistente es el mayor factor de riesgo de nefropatía tras ICP, por lo que las medidas nefroprotectoras se centran en este subgrupo de pacientes3,5,6. Sin embargo, los pacientes con síndrome coronario agudo (SCA) tratados mediante ICP pueden constituir también una población con mayor riesgo de nefropatía tras ICP4,7. Pocos estudios han evaluado específicamente la prevalencia y el pronóstico a largo plazo de la nefropatía tras ICP en pacientes con SCA y función renal normal. El mejor tratamiento de esta grave complicación es la prevención. En las guías actuales de la Sociedad Europea de Cardiología para el manejo de pacientes con SCA sin elevación persistente del segmento ST, solo se recomiendan medidas nefroprotectoras para pacientes con SCA e insuficiencia renal crónica8, por lo que la realización de estudios en los pacientes con función renal normal podría identificar un subgrupo que también se beneficie de estas medidas preventivas.
El objetivo de este estudio es analizar la prevalencia, los factores de riesgo y el pronóstico hospitalario y a largo plazo de los pacientes con SCA sin insuficiencia renal preexistente que presentaron deterioro de la función renal tras un procedimiento de revascularización coronaria percutánea.
MÉTODOSDurante los años 2007-2011 un total de 602 pacientes consecutivos pertenecientes al área fueron sometidos a ICP por SCA con o sin elevación del segmento ST. Se excluyó del análisis a los pacientes con insuficiencia renal detectada al ingreso (valor de creatinina al ingreso >1,3mg/dl, n=126) y a los pacientes en situación de shock cardiogénico (n=6). El grupo de estudio está formado por 470 pacientes (media de edad, 65±12 años; mujeres, 89 [18,9%]) con SCA y sin insuficiencia renal preexistente ni shock cardiogénico sometidos a revascularización percutánea.
Se trata de un estudio observacional, retrospectivo y unicéntrico en el que las variables se recogieron de manera prospectiva. Se registraron en la base de datos de la unidad distintas variables clínicas y epidemiológicas como edad, sexo, factores de riesgo cardiovascular, otras comorbilidades y tratamiento previo. Se realizó analítica con hemograma y bioquímica a la llegada a urgencias, curva de marcadores de necrosis miocárdica (6 y 12h) y analítica completa a las ocho de la mañana del día siguiente al ingreso. Tras el ICP, como parte del protocolo habitual del centro, se realizó nueva curva de marcadores de necrosis miocárdica a las 6 y a las 12h y valoración de la función renal al día siguiente. La cantidad y el momento de la extracción de análisis adicionales se realizaron según el criterio del médico responsable. Se registró el valor de creatinina al ingreso y durante la hospitalización. El aclaramiento de creatinina se estimó mediante la fórmula simplificada Modification of Diet in Renal Disease9,10.
Cateterismo y tratamientoEl ICP se realizó según la técnica estándar, utilizando el acceso radial en la mayoría de los casos (394 [83,8%]). En todos los casos, los medios de contraste utilizados fueron iohexol (Omnipaque 350® y Omnipaque 300®) e iodixanol (Visipaque 320®). Se registró el número de vasos principales afectados en la coronariografía, la vía de acceso, la dosis de contraste, el tiempo de escopia, el número de stents utilizados y su tipo. También se registró el tratamiento antitrombótico empleado, las complicaciones hemorrágicas en relación con el acceso, el éxito angiográfico y la presencia de alguna complicación durante el procedimiento. La decisión de instaurar una pauta de hidratación tras el cateterismo, el tipo y la dosis de fluidoterapia y la necesidad de terapia de sustitución renal quedaron a criterio del médico responsable del paciente.
Seguimiento y objetivosA todos los pacientes sometidos a ICP en la institución, se les da seguimiento prospectivo durante un mínimo de 12meses (media de seguimiento, 26,7±14,0meses). Los datos de seguimiento se obtuvieron mediante revisión de la historia clínica electrónica del hospital y entrevistas telefónicas realizadas de manera sistemática y estandarizada al mes, al año y al final del seguimiento. Los objetivos analizados son la mortalidad y las complicaciones intrahospitalarias, los eventos cardiovasculares y la mortalidad cardiaca y total en el seguimiento a largo plazo.
DefinicionesLa nefropatía tras ICP se definió como un incremento ≥25% o ≥0,5mg/dl del valor de creatinina sérica en las 72h siguientes al procedimiento6,11,12. Se definió infarto agudo de miocardio como la elevación de troponina I por isquemia miocárdica aguda y el infarto tras ICP, según los criterios de la última clasificación universal de infarto de miocardio (elevación de troponina I > 1 ng/ml en pacientes con valores basales normales o aumento>20% en pacientes con troponina elevada en situación de estabilidad o en disminución, asociado a datos clínicos, electrocardiográficos o de imagen de isquemia o hallazgos angiográficos compatibles con alguna complicación)13. La fracción de eyección del ventrículo izquierdo (FEVI) se estimó por ecocardiograma. El shock cardiogénico se definió como una presión arterial sistólica<90mmHg durante ≥1h acompañada de hipoperfusión tisular, que precisó soporte inotrópico y/o implante de balón intraaórtico de contrapulsación. Se consideró mortalidad cardiaca la debida a SCA, insuficiencia cardiaca y arritmia ventricular. Se definió éxito angiográfico como la presencia de un flujo Thrombolysis In Myocardial Infarction≥2 en ausencia de estenosis residual > 50%. Se clasificaron las complicaciones hemorrágicas relacionadas con el acceso vascular utilizando la escala Bleeding Academic Research Consortium14. Se consideró revascularización de la lesión diana la necesidad de un nuevo procedimiento de revascularización (percutáneo o quirúrgico) del segmento coronario con stent, realizado en presencia de reestenosis angiográfica (estenosis > 50%) y síntomas o signos de isquemia miocárdica. Se definió revascularización del vaso diana a la nueva revascularización percutánea o quirúrgica del vaso previamente tratado en presencia de estenosis grave (> 70%) y síntomas o signos de isquemia miocárdica.
Análisis estadísticoPara el análisis de los datos se empleó el paquete estadístico SPSS versión 20. Las variables cuantitativas se describen como media±desviación estándar. Las variables categóricas se describen como valor absoluto y porcentaje. Las diferencias en los resultados de una variable cuantitativa entre los dos grupos de pacientes se analizaron mediante el test de la t de Student y las diferencias entre variables categóricas, mediante el test de la χ2 de Pearson o el exacto de Fisher, según procediese. Se realizó un análisis de regresión logística por pasos hacia atrás para determinar los factores independientes predictores de nefropatía tras ICP. Las variables incluidas en este análisis fueron las relacionadas significativamente con aparición de disfunción renal en el modelo univariable y las consideradas de relevancia clínica: hemoglobina al ingreso, troponina I máxima previa al ICP, creatincinasa máxima previa al ICP, tasa de filtrado glomerular, FEVI, volumen de contraste y proteína C reactiva al ingreso. Todas estas variables se recogieron antes de que apareciera la nefropatía tras ICP. Los resultados se expresan como odds ratio (OR) y su intervalo de confianza del 95% (IC95%). La supervivencia libre de muerte total y muerte cardiaca en los grupos con y sin nefropatía tras ICP se comparó mediante el análisis de Kaplan-Meier (log rank test). Se realizó un análisis de regresión de Cox multivariable por pasos hacia atrás para determinar los predictores independientes de mortalidad total y cardiaca. Las variables incluidas en estos análisis son las descritas como principales predictoras de mortalidad en el contexto de SCA8: edad, FEVI (variable continua), hemoglobina al ingreso (variable continua), diabetes mellitus y nefropatía tras ICP. Los resultados se expresan en hazard ratio (HR) y su IC95%. Se consideró estadísticamente significativo un valor de p < 0,05.
RESULTADOSCaracterísticas basales y prevalencia de nefropatía tras intervencionismo coronario percutáneoDe los 470 pacientes analizados, 30 (6,4%; IC95%, 4,3-8,9%) presentaron nefropatía tras ICP a pesar de valores de creatinina plasmática normales al ingreso; 2 pacientes (0,4%) precisaron diálisis. Las tablas 1 y 2 muestran las características basales y los datos angiográficos y del procedimiento intervencionista de los pacientes que tuvieron nefropatía tras ICP frente a los que no.
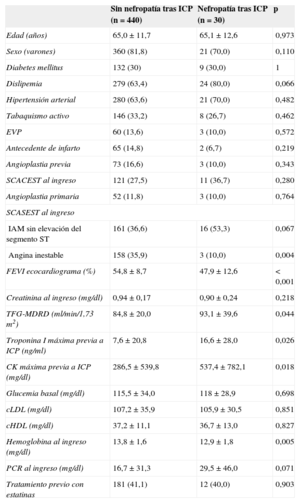
Datos clínicos y de laboratorio de los pacientes según presentaran o no nefropatía tras intervencionismo coronario percutáneo
| Sin nefropatía tras ICP (n=440) | Nefropatía tras ICP (n=30) | p | |
|---|---|---|---|
| Edad (años) | 65,0±11,7 | 65,1±12,6 | 0,973 |
| Sexo (varones) | 360 (81,8) | 21 (70,0) | 0,110 |
| Diabetes mellitus | 132 (30) | 9 (30,0) | 1 |
| Dislipemia | 279 (63,4) | 24 (80,0) | 0,066 |
| Hipertensión arterial | 280 (63,6) | 21 (70,0) | 0,482 |
| Tabaquismo activo | 146 (33,2) | 8 (26,7) | 0,462 |
| EVP | 60 (13,6) | 3 (10,0) | 0,572 |
| Antecedente de infarto | 65 (14,8) | 2 (6,7) | 0,219 |
| Angioplastia previa | 73 (16,6) | 3 (10,0) | 0,343 |
| SCACEST al ingreso | 121 (27,5) | 11 (36,7) | 0,280 |
| Angioplastia primaria | 52 (11,8) | 3 (10,0) | 0,764 |
| SCASEST al ingreso | |||
| IAM sin elevación del segmento ST | 161 (36,6) | 16 (53,3) | 0,067 |
| Angina inestable | 158 (35,9) | 3 (10,0) | 0,004 |
| FEVI ecocardiograma (%) | 54,8±8,7 | 47,9±12,6 | < 0,001 |
| Creatinina al ingreso (mg/dl) | 0,94±0,17 | 0,90±0,24 | 0,218 |
| TFG-MDRD (ml/min/1,73 m2) | 84,8±20,0 | 93,1±39,6 | 0,044 |
| Troponina I máxima previa a ICP (ng/ml) | 7,6±20,8 | 16,6±28,0 | 0,026 |
| CK máxima previa a ICP (mg/dl) | 286,5±539,8 | 537,4±782,1 | 0,018 |
| Glucemia basal (mg/dl) | 115,5±34,0 | 118±28,9 | 0,698 |
| cLDL (mg/dl) | 107,2±35,9 | 105,9±30,5 | 0,851 |
| cHDL (mg/dl) | 37,2±11,1 | 36,7±13,0 | 0,827 |
| Hemoglobina al ingreso (mg/dl) | 13,8±1,6 | 12,9±1,8 | 0,005 |
| PCR al ingreso (mg/dl) | 16,7±31,3 | 29,5±46,0 | 0,071 |
| Tratamiento previo con estatinas | 181 (41,1) | 12 (40,0) | 0,903 |
cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; CK: creatincinasa; EVP: enfermedad vascular periférica; FEVI: fracción de eyección del ventrículo izquierdo; IAM: infarto agudo de miocardio; ICP: intervencionismo coronario percutáneo; PCR: proteína C reactiva; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST; TFG-MDRD: tasa de filtrado glomerular-Modification of Diet in Renal Disease.
Los datos expresan media±desviación estándar o n (%).
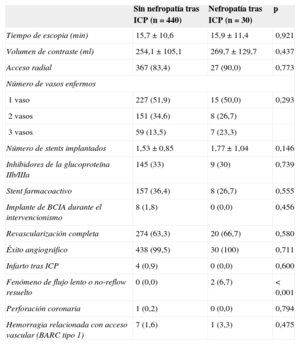
Datos angiográficos y del procedimiento intervencionista según apareciera o no nefropatía tras intervencionismo coronario percutáneo
| Sin nefropatía tras ICP (n=440) | Nefropatía tras ICP (n=30) | p | |
|---|---|---|---|
| Tiempo de escopia (min) | 15,7±10,6 | 15,9±11,4 | 0,921 |
| Volumen de contraste (ml) | 254,1±105,1 | 269,7±129,7 | 0,437 |
| Acceso radial | 367 (83,4) | 27 (90,0) | 0,773 |
| Número de vasos enfermos | |||
| 1 vaso | 227 (51,9) | 15 (50,0) | 0,293 |
| 2 vasos | 151 (34,6) | 8 (26,7) | |
| 3 vasos | 59 (13,5) | 7 (23,3) | |
| Número de stents implantados | 1,53±0,85 | 1,77±1,04 | 0,146 |
| Inhibidores de la glucoproteína IIb/IIIa | 145 (33) | 9 (30) | 0,739 |
| Stent farmacoactivo | 157 (36,4) | 8 (26,7) | 0,555 |
| Implante de BCIA durante el intervencionismo | 8 (1,8) | 0 (0,0) | 0,456 |
| Revascularización completa | 274 (63,3) | 20 (66,7) | 0,580 |
| Éxito angiográfico | 438 (99,5) | 30 (100) | 0,711 |
| Infarto tras ICP | 4 (0,9) | 0 (0,0) | 0,600 |
| Fenómeno de flujo lento o no-reflow resuelto | 0 (0,0) | 2 (6,7) | < 0,001 |
| Perforación coronaria | 1 (0,2) | 0 (0,0) | 0,794 |
| Hemorragia relacionada con acceso vascular (BARC tipo 1) | 7 (1,6) | 1 (3,3) | 0,475 |
BARC: Bleeding Academic Research Consortium; BCIA: balón de contrapulsación intraaórtico; ICP: intervencionismo coronario percutáneo.
Los datos expresan media±desviación estándar o n (%).
El grupo de pacientes que presentó nefropatía tras ICP mostraba menores FEVI y concentración de hemoglobina previas al ICP, mayor elevación de marcadores de necrosis miocárdica (troponina I y creatincinasa), menor prevalencia de angina inestable y una tendencia a cifras de proteína C reactiva más altas y mayor prevalencia de dislipemia e infarto sin elevación del segmento ST. En el análisis de regresión logística, los factores independientes predictores de nefropatía tras ICP fueron la concentración de hemoglobina al ingreso (OR=0,706; IC95%, 0,545-0,914; p=0,008) y el máximo valor de troponina I previo al ICP (OR=1,016; IC95%, 1,002-1,031; p=0,025).
Pronóstico de la nefropatía tras intervencionismo coronario percutáneoEvolución intrahospitalariaDurante el seguimiento hospitalario, los pacientes con nefropatía tras ICP presentaron en mayor proporción fenómeno de flujo lento o no-reflow resuelto (el 6,7 frente al 0%; p<0,001) y mayor mortalidad intrahospitalaria (el 6,7 frente al 0,5%; p<0,001), pero no hubo mayor número de complicaciones hemorrágicas relacionadas con el acceso vascular ni mayor presencia de infarto tras ICP. Todas la complicaciones hemorrágicas relacionadas con el acceso vascular fueron Bleeding Academic Research Consortium tipo 1 (hemorragias leves que no requirieron estudio ni tratamiento adicional ni prolongaron la estancia hospitalaria).
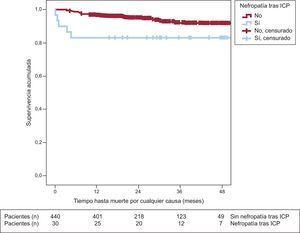
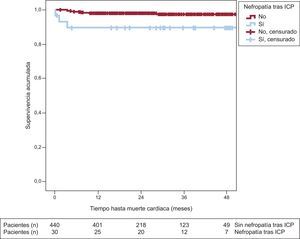
Seguimiento a largo plazoEn el seguimiento a largo plazo, los pacientes con nefropatía tras ICP presentaron mayores incidencia de mortalidad cardiaca (3 [10%] frente a 9 [2%]; p=0,008) y mortalidad total (5 [16,7%] frente a 7 [6,1%]; p=0,027) (tabla 3). Los pacientes cuya función renal se deterioró tras el ICP presentaron menor supervivencia en el seguimiento a largo plazo (43±3,4 frente a 51,4±0,6 meses; log rank test, p=0,024). En las figuras 1 y 2 se observan las curvas de supervivencia de mortalidad total y cardiaca estratificadas según la aparición de nefropatía tras ICP.
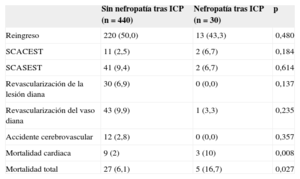
Eventos a largo plazo en los pacientes con y sin nefropatía tras intervencionismo coronario percutáneo
| Sin nefropatía tras ICP (n=440) | Nefropatía tras ICP (n=30) | p | |
|---|---|---|---|
| Reingreso | 220 (50,0) | 13 (43,3) | 0,480 |
| SCACEST | 11 (2,5) | 2 (6,7) | 0,184 |
| SCASEST | 41 (9,4) | 2 (6,7) | 0,614 |
| Revascularización de la lesión diana | 30 (6,9) | 0 (0,0) | 0,137 |
| Revascularización del vaso diana | 43 (9,9) | 1 (3,3) | 0,235 |
| Accidente cerebrovascular | 12 (2,8) | 0 (0,0) | 0,357 |
| Mortalidad cardiaca | 9 (2) | 3 (10) | 0,008 |
| Mortalidad total | 27 (6,1) | 5 (16,7) | 0,027 |
ICP: intervencionismo coronario percutáneo; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
Los datos expresan n (%).
En el análisis de regresión multivariable de Cox, los predictores independientes de la mortalidad total fueron la edad (HR=1,079; IC95%, 1,032-1,127; p=0,001), la FEVI (HR=0,962; IC95%, 0,936-0,988; p=0,005) y la concentración de hemoglobina previa al procedimiento (HR=0,659; IC95%, 0,531-0,819; p<0,001). Los predictores independientes de mortalidad cardiaca fueron la edad, la FEVI, la diabetes mellitus y la nefropatía tras ICP (HR=5,4; IC95%, 1,35-21,30; p=0,017) (tabla 4).
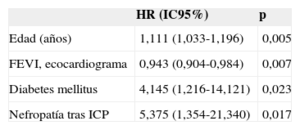
Análisis de regresión multivariable de Cox: predictores independientes de mortalidad cardiaca
| HR (IC95%) | p | |
|---|---|---|
| Edad (años) | 1,111 (1,033-1,196) | 0,005 |
| FEVI, ecocardiograma | 0,943 (0,904-0,984) | 0,007 |
| Diabetes mellitus | 4,145 (1,216-14,121) | 0,023 |
| Nefropatía tras ICP | 5,375 (1,354-21,340) | 0,017 |
FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; ICP: intervencionismo coronario percutáneo.
La nefropatía inducida por contraste es una complicación común en pacientes sometidos a procedimientos invasivos y se ha asociado con una morbimortalidad incrementada1–4. La incidencia de nefropatía inducida por contraste en los estudios realizados es variable. Esta variabilidad resulta de las diferencias en la presencia de factores de riesgo, de la cantidad y el tipo de contraste utilizado y de la definición de nefropatía inducida por contraste adoptada por cada estudio. Aunque el riesgo de nefropatía inducida por contraste en la población general es bajo12, la incidencia puede ser considerablemente superior en determinados subgrupos de riesgo. Identificar a los pacientes en riesgo de presentar nefropatía tras ICP podría ser de inmenso valor, ya que el tratamiento profiláctico se podría dirigir a la población de alto riesgo. Para una mejor estratificación de los pacientes, se han hecho esfuerzos para desarrollar herramientas o escalas de riesgo que permitan identificar a los pacientes con más posibilidades de presentar nefropatía tras ICP6,15. En este sentido, la función renal basal es el más poderoso predictor de nefropatía inducida por contraste tras el ICP3–6. De hecho, las guías actuales únicamente recomiendan el uso de tratamiento profiláctico para pacientes con función renal alterada8, aunque dicha aproximación tiene escasas sensibilidad y especificidad. Hay pocos estudios que evalúen la nefropatía tras ICP en el subgrupo de pacientes con función renal normal. Solo se ha encontrado un estudio que evaluara la incidencia y los resultados de la nefropatía tras ICP en pacientes con función renal normal, el de Roy et al16, y en ese estudio solo se analizaba a pacientes diabéticos. Rihal et al4 identificaron el infarto agudo de miocardio como un predictor independiente de insuficiencia renal aguda tras un cateterismo cardiaco. Por lo tanto, la población analizada en este estudio (pacientes con SCA y función renal normal) es una población poco evaluada en la literatura médica.
El presente trabajo demuestra que la nefropatía tras ICP en pacientes con SCA y función renal normal no es infrecuente (el 6,4%; IC95%, 4,3-8,9%). En este subgrupo de pacientes los predictores independientes de nefropatía tras ICP son las concentraciones de hemoglobina al ingreso y de troponina antes del ICP. A los pacientes con SCA que presenten una baja concentración de hemoglobina al ingreso y aumento de marcadores de necrosis miocárdica (fundamentalmente troponina), se los debería seguir más estrechamente y se tendría que considerar estrategias de nefroprotección sistemáticas. El escaso número de pacientes diabéticos (141), junto con la exclusión de aquellos con nefropatía diabética, podría justificar que no se haya detectado mayor riesgo de nefropatía tras ICP en los diabéticos de la muestra.
Actualmente se desconoce el mejor tratamiento para la prevención de la nefropatía tras ICP. Sin embargo, sí existe una serie de recomendaciones profilácticas con demostrada utilidad en los estudios realizados, como la retirada de fármacos nefrotóxicos11, utilizar bajas dosis de contraste, utilizar medios de contraste de baja osmolaridad o isoosmolares17,18, evitar la repetición de procedimientos en 48–72h, evitar situaciones de hipovolemia y utilización de diferentes protocolos de hidratación19,20, combinados o no con N-acetilcisteína21,22. Recio-Mayoral et al23 han comunicado que una pauta de hidratación rápida con bicarbonato y N-acetilcisteína fue eficaz en la prevención de la nefropatía por contraste en pacientes sometidos a cateterismo urgente.
Pronóstico de la nefropatía tras intervencionismo coronario percutáneoLos pacientes que presentaron nefropatía tras ICP tuvieron mayor mortalidad hospitalaria (el 6,7 frente al 0,5%; p<0,001). En esta línea, estudios previos han publicado tasas de mortalidad hospitalaria del 13,9% de los pacientes que presentaron deterioro de la función renal tras un cateterismo cardiaco urgente, frente al 0,6% de la población que no adquirió insuficiencia renal7.
Los pacientes que sobreviven a un episodio de insuficiencia renal aguda tras un procedimiento de revascularización percutánea pueden continuar en riesgo de eventos a largo plazo. En el presente estudio, en el que se realizó un seguimiento medio de 26,7±14 meses, la mortalidad total y cardiaca fueron llamativamente más elevadas en el grupo que contrajo nefropatía tras ICP. Además, estas curvas mostraban que la reducción de la supervivencia tuvo lugar fundamentalmente en los primeros 12 meses tras el deterioro de la función renal. Es posible que los pacientes con función renal normal que presentan nefropatía tras ICP tengan peor pronóstico en los primeros 12 meses y que después, al ser pacientes cuyas cifras de creatinina habitualmente se normalizan en el seguimiento, igualen su riesgo al del resto de la población.
Por lo tanto, estos datos ponen de manifiesto el impacto pronóstico negativo de la nefropatía tras ICP independientemente de los valores basales de creatinina sérica. Aunque la nefropatía tras ICP puede ser un marcador de deterioro hemodinámico y otras comorbilidades, que a su vez son importantes en el pronóstico de estos pacientes, se mostró como un posible predictor independiente de mortalidad cardiaca tras el ajuste por estas variables. Por este motivo, se debería monitorizar la función renal de todos los pacientes con SCA que se vayan a someter a ICP, incluidos los pacientes con función renal normal al ingreso. Probablemente, la nefropatía tras ICP en la población de pacientes estables hemodinámicamente (sin shock cardiogénico) pueda ser un marcador de mayor daño miocárdico o de aterosclerosis más agresiva, lo que afectaría fundamentalmente a la mortalidad cardiaca. El hecho de que en este estudio la mortalidad cardiaca solo sea el 37,5% de la mortalidad total podría explicar que no se haya detectado la nefropatía tras ICP como predictor independiente de mortalidad total.
Limitaciones y fortalezasAunque los datos demográficos, clínicos y angiográficos se recogieron de manera prospectiva, se trata de un análisis retrospectivo, con las limitaciones inherentes a este tipo de estudios. El tamaño muestral puede haber limitado la potencia del estudio para detectar una asociación significativa entre el deterioro de la función renal tras ICP y otros factores de riesgo de nefropatía tras ICP como la diabetes mellitus o el volumen de contraste. No se recogieron variables de gran impacto en la mortalidad como la frecuencia cardiaca, la presión arterial y la clase Killip. De haberse registrado dichas variables, los modelos predictivos y, por lo tanto, el valor pronóstico de la nefropatía tras ICP podrían haber sido diferentes. El hecho de que después de las primeras 24h las analíticas se hayan realizado según el criterio del médico responsable puede que haya motivado que no se identificara a algún paciente con nefropatía tras ICP. Dado que a los pacientes con SCA se los mantiene ingresados varios días, se realizan varias baterías analíticas durante el ingreso, que generalmente el daño renal agudo tras la inyección de contraste suele tener lugar en los primeros 3 días tras el procedimiento y en el 80% de los casos la elevación de creatinina sérica se produce en las primeras 24h11, cabe pensar que el posible número de pacientes no identificados debe ser mínimo. El diseño del estudio no permite determinar la importancia relativa de la ateroembolia o de las alteraciones hemodinámicas frente a la administración de contraste en el desarrollo de disfunción renal. El bajo número de muertes cardiacas (12 pacientes) obliga a tomar con precaución los resultados del análisis multivariable en relación con este evento, pero puede ser un importante generador de hipótesis para estudios con mayor tamaño muestral.
Uno de los puntos fuertes del estudio es que los resultados se basan en un registro exhaustivo y consecutivo de pacientes de esta área de salud hospitalizados por SCA, de los que se ha obtenido gran cantidad de información clínica, analítica y angiográfica durante su estancia hospitalaria y se han registrado diversas variables evolutivas a muy largo plazo.
CONCLUSIONESLa nefropatía tras ICP en pacientes con SCA y función renal normal no es una complicación infrecuente. En estos pacientes, la concentración de hemoglobina al ingreso y los valores de troponina previos al intervencionismo resultaron predictores independientes de nefropatía tras ICP. Esta complicación es un marcador de mal pronóstico hospitalario y a largo plazo. Por este motivo, se debería monitorizar la función renal de todos los pacientes con SCA que vayan a someterse a ICP y se tendría que considerar estrategias de nefroprotección incluso para aquellos con función renal normal al ingreso, especialmente en el subgrupo de pacientes con anemia y elevación de troponina.
CONFLICTO DE INTERESESNinguno.