Tradicionalmente el objetivo de la anticoagulación para el paciente con fibrilación auricular se centra principalmente en la prevención del ictus. Pero lo cierto es que estos pacientes tienen numerosas comorbilidades que también condicionan el pronóstico de manera muy importante y es necesario abordar. Esto también debería condicionar la elección del mejor tratamiento anticoagulante para el paciente en alto riesgo cardiovascular. En general, la eficacia y la seguridad de los 4 anticoagulantes orales de acción directa frente a warfarina son consistentes, independientemente de que el paciente tenga antecedentes de ictus/ accidente isquémico transitorio, diabetes mellitus, insuficiencia renal o infarto de miocardio. En el caso del rivaroxabán, varios estudios muestran que podría reducir el riesgo de infarto de miocardio y generar menos complicaciones renales que la warfarina. En un subestudio del ROCKET-AF, en pacientes con diabetes mellitus, el rivaroxabán redujo significativamente (20%) la mortalidad cardiovascular y estudios de práctica clínica muestran que el rivaroxabán no solo reduce significativamente el riesgo de eventos cardiovasculares mayores, sino también el riesgo de enfermedad arterial periférica. Como resultado de todo ello, el rivaroxabán podría considerarse como una opción preferente para la anticoagulación de los pacientes con fibrilación auricular no valvular y alto riesgo cardiovascular, por las ventajas adicionales que proporciona en esta población.
Palabras clave
Se estima que la prevalencia actual de fibrilación auricular (FA) en la población adulta se sitúa en torno al 3%. Esta cifra aumenta de manera considerable tanto con la edad como con la presencia de ciertas comor-bilidades, como hipertensión arterial, diabetes mellitus, insuficiencia cardiaca, enfermedad coronaria o enfermedad renal crónica1-7.
La anticoagulación es la piedra angular en el tratamiento de los pacientes con FA para disminuir el riesgo de ictus, que es su complica-ción más grave8. De hecho, la mortalidad por ictus asociada con la FA es muy elevada, y en algunas series llega incluso al 30-50% al año del evento9,10, y entre los supervivientes, el riesgo de discapacidad y recu-rrencias también es muy importante8. Por ello, salvo contraindicación o un bajo riesgo de ictus, los pacientes con FA deberían recibir indefi-nidamente tratamiento anticoagulante1.
Ahora bien, el tratamiento anticoagulante no solo debería perse-guir la reducción del riesgo de complicaciones tromboembólicas, sino también una protección vascular general, que va más allá de la reduc-ción del riesgo de ictus1. Dado que los pacientes con FA tienen fre-cuentemente numerosas comorbilidades, es obligatorio conocer qué tratamientos anticoagulantes proporcionan un mayor beneficio, no solo para la población con FA en general, sino también para los pacientes que tienen un mayor riesgo cardiovascular11-13.
Los anticoagulantes orales de acción directa (ACOD) tienen demos-trada una mayor protección que la de los antagonistas de la vitamina K (AVK), con un menor riesgo de ictus, hemorragias mayores, hemo-rragia intracraneal y mortalidad por cualquier causa14. Sin embargo, en la elección del ACOD más adecuado para cada paciente en con-creto, convendría tener en cuenta la protección integral ofrecida por cada uno de ellos.
Paciente con fa no valvular y antecedentes de ictus/ accidente isquémico transitorioAunque en general la FA aumenta el riesgo de ictus hasta en 5 veces, este riesgo es aún mayor para los pacientes con antecedentes de ictus/accidente isquémico transitorio (AIT)1,8,15. De los pacientes con FA que sobreviven a un ictus, hasta en un 60% de los casos la inca-pacidad resultante es elevada16, con un gran riesgo de recurrencias al año, que alcanza el 7-12%, según las series8,10,17. Por ello, es obligada la prevención de nuevos ictus en los pacientes con FA que ya hayan tenido un ictus/AIT1. La guía de la EHRA de 2018 sobre el tratamiento con ACOD tras un ictus recomiendan comenzar con la anticoagulación en ausencia de contraindicaciones, y cuando no se espere que haya un riesgo significativamente aumentado de transformación hemorrágica secundaria. Esto es al menos 3 días tras un ictus isquémico leve, al menos 6-8 días tras un ictus moderado y al menos 12-14 días tras un ictus grave, y después de excluir la transformación hemorrágica por una prueba de imagen18.
En cuanto al tratamiento anticoagulante, se ha demostrado que los AVK reducen significativamente el riesgo de recurrencia de ictus en pacientes con FA y antecedentes de enfermedad cerebrovascular: del 12 al 4%, con un aceptable perfil de seguridad19,20. No obstante, se ha observado que la mayoría de los casos de recurrencia ocurren en pacientes con cifras de la razón internacional normalizada (INR) infraterapéuticas21. Esto es muy relevante, ya que el control de la anti-coagulación con los AVK en la práctica clínica es bastante pobre. Así, estudios realizados en diferentes ámbitos asistenciales en España (cardiología, medicina interna, neurología, atención primaria) han mostrado que aproximadamente el 40-55% de los pacientes presen-tan un mal control de la INR de manera habitual22-25. En conjunto, los datos provenientes de los ensayos clínicos que comparan los ACOD con warfarina en los pacientes con antecedentes de ictus/AIT mues-tran una reducción significativa del riesgo de ictus o embolia sisté- mica en un 14%, junto con un menor riesgo de hemorragias mayores (tabla 1). Además, no hay que olvidar que los ACOD reducen de manera muy marcada el riesgo de hemorragia intracraneal en compa-ración con los AVK14. Aunque en todos los ensayos clínicos fundamen-tales de los ACOD frente a warfarina los resultados de eficacia y segu-ridad fueron independientes de los antecedentes de ictus/AIT, no en todos los estudios se incluyó una alta proporción de pacientes con antecedentes de enfermedad cerebrovascular. Mientras que en el estudio ROCKET-AF el 52% de los pacientes tenían antecedentes de ictus/AIT, fueron el 20% en el estudio RE-LY, el 19% en el ARISTOTLE y el 28% en el ENGAGE AF-TIMI 48, por lo que el rivaroxabán dispone de una mayor evidencia en este contexto26-29. En el estudio RE-LY, los resultados de eficacia y seguridad de ambas dosis de dabigatrán frente a warfarina fueron acordes, independientemente de los antece-dentes de ictus/AIT, excepto para el dabigatrán 110 mg con la mortali-dad vascular26. En el resto de los estudios (ROCKET-AF, ARISTOTLE y ENGAGE AF-TIMI 48), la eficacia y la seguridad relativas del rivaroxa-bán, el apixabán y el edoxabán frente a warfarina fueron indepen-dientes del antecedente de ictus/AIT, aunque en términos absolutos el beneficio podría ser mayor, al tener un mayor riesgo basal de compli-caciones tromboembólicas27-29.
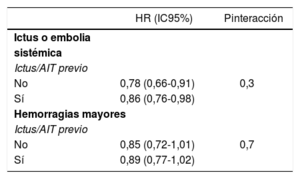
Eficacia y seguridad de los ACOD frente a los AVK según los antecedentes de ictus o AIT
| HR (IC95%) | Pinteracción | |
|---|---|---|
| Ictus o embolia | ||
| sistémica | ||
| Ictus/AIT previo | ||
| No | 0,78 (0,66-0,91) | 0,3 |
| Sí | 0,86 (0,76-0,98) | |
| Hemorragias mayores | ||
| Ictus/AIT previo | ||
| No | 0,85 (0,72-1,01) | 0,7 |
| Sí | 0,89 (0,77-1,02) | |
Tabla elaborada con datos de Ruff et al14. ACOD: anticoagulantes orales de acción directa; AIT: accidente isquémico transitorio; AVK: antagonistas de la vitamina K; HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Aunque son importantes los resultados de los ensayos clínicos, también lo es conocer si estos resultados son aplicables a los pacien-tes de la práctica clínica. Se ha observado que, en la práctica clínica, la introducción de los ACOD se ha asociado con una reducción de los ictus isquémicos, sin un aumento significativo de las hemorragias, y tanto en prevención primaria como en secundaria30. El estudio REAFFIRM analizó en pacientes con antecedentes de ictus o AIT la efectividad y la seguridad del rivaroxabán, el apixabán y el dabigatrán frente a warfarina en la práctica clínica. El ACOD que aportó un mayor beneficio clínico neto (ictus isquémico/hemorragia intracraneal) fue el rivaroxabán, con una reducción significativa del 55% (tabla 2)31.
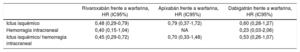
Efectividad y seguridad del rivaroxabán, el apixabán y el dabigatrán frente a la warfarina en pacientes con antecedentes de ictus o AIT
| Rivaroxabán frente a warfarina, HR (IC95%) | Apixabán frente a warfarina, HR (IC95%) | Dabigatrán frente a warfarina, HR (IC95%) | |
|---|---|---|---|
| Ictus isquémico | 0,48 (0,29-0,79) | 0,79 (0,37-1,72) | 0,60 (0,28-1,27) |
| Hemorragia intracraneal | 0,40 (0,15-1,04) | NA | 0,23 (0,03-2,06) |
| Ictus isquémico/ hemorragia intracraneal | 0,45 (0,29-0,72) | 0,70 (0,33-1,48) | 0,53 (0,26-1,07) |
Tabla elaborada con datos de Coleman et al31. AIT: accidente isquémico transitorio;
HR: hazard ratio; IC95%: intervalo de confianza del 95%; NA: no aplicable.
Finalmente, estudios recientes muestran que el inicio precoz de riva-roxabán tras un ictus reduce significativamente el riesgo de recurren-cias, con bajas tasas de hemorragias32.
Paciente con fa no valvular, diabetes y riesgo cardiovascularLos pacientes con diabetes mellitus tipo 2 tienen un riesgo de FA aumentado: hasta el 50%1,33,34. Este riesgo es mayor en los diabéticos con un mal control glucémico, así como en aquellos con una diabetes de larga evolución35,36. Existen múltiples mecanismos que explican la interrelación entre la diabetes y la FA: entre otros, la resistencia a la insulina, el estrés oxidativo, la inflamación, la activación del sistema renina angiotensina o la disfunción endotelial, que van a provocar un remodelado auricular eléctrico, estructural y autonómico que facilita el desarrollo de FA37-39.
El paciente diabético con FA tiene un riesgo de ictus incrementado, por lo que se recomienda la anticoagulación para disminuir el riesgo de complicaciones tromboembólicas1. Al analizar en general los resul-tados de los ensayos clínicos fundamentales, en la población diabé-tica, en comparación con warfarina, los ACOD redujeron significativa-mente (20%) el riesgo de ictus o embolia sistèmica (hazard ratio [HR] = 0,80; intervalo de confianza del 95% [IC95%], 0,69-0,93) y un 10% el de hemorragia mayor (HR = 0,90; IC95%, 0,68-1,04)14. Aunque los resultados de cada estudio eran acordes con los de la población glo-bal, la proporción de pacientes con diabetes incluidos en los estudios fundamentales fue mayor con rivaroxabán (ROCKET-AF, el 40%; ENGAGE AF-TIMI 48, el 36%; ARISTOTLE, el 25%; RE-LY, el 23%), y esto hace que sea el ACOD con la mayor representación de población dia-bética en los ensayos clínicos fundamentales40-43.
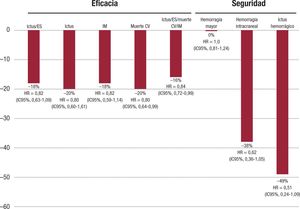
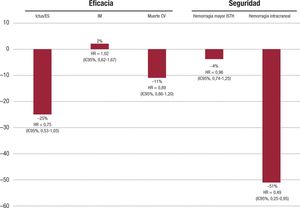
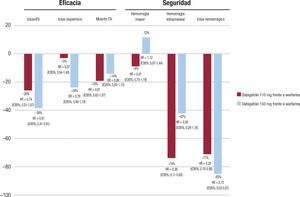
Los pacientes con diabetes mellitus tipo 2 y FA no valvular tienen un riesgo incrementado de ictus, pero también de eventos adversos cardiovasculares mayores (MACE) que incluyen muerte cardio-vascular, ictus o infarto de miocardio, así como de eventos adversos mayores de las extremidades (MALE) como la amputación y los pro-cedimientos de revascularización40,44. Por lo tanto, a la hora de plan-tear el mejor tratamiento anticoagulante, probablemente se deba valorar no solo la eficacia en términos de reducción en la incidencia de ictus, sino también en el riesgo de MACE y MALE, con el objetivo de conseguir una protección integral del paciente diabético. En un análi-sis preestablecido del ROCKET-AF realizado en la población diabética, en comparación con warfarina, con el rivaroxabán se observaron reducciones significativas, del 20% del riesgo de muerte de origen car-diovascular, del 16% en la variable combinada de ictus, embolia sisté- mica, muerte cardiovascular e infarto de miocardio, y tendencia a un menor riesgo de ictus, infarto de miocardio, hemorragia intracraneal e ictus hemorrágico, sin aumento del riesgo de hemorragia mayor (Figura 1)40. En los estudios ARISTOTLE (apixabán) y RE-LY (dabiga-trán), no se observó una reducción significativa en la mortalidad de origen cardiovascular en comparación con la warfarina (Figura 2 y Figura 3)41,42,45.
Eficacia y seguridad del rivaroxabán frente a la warfarina en pacientes con diabetes mellitus tipo 2 y fibrilación auricular no valvular en el estudio ROCKET-AF40. CV: cardiovascular; ES: embolia sistémica; HR: hazard ratio; IC95%: intervalo de confianza del 95%; IM: infarto de miocardio.
Eficacia y seguridad del apixabán frente a la warfarina en pacientes con diabetes mellitus tipo 2 y fibrilación auricular no valvular en el estudio ARISTOTLE. Figura elaborada con datos de Exekowitz et al41. CV: cardiovascular; ES: embolia sistémica; HR: hazard ratio; IC95%: intervalo de confianza del 95%; IM: infarto de miocardio; ISTH: International Society of Thrombosis and Haemostasis.
Eficacia y seguridad del dabigatrán frente a la warfarina en pacientes con diabetes mellitus tipo 2 y fibrilación auricular no valvular en el estudio RE-LY. Figura elabora-da con datos de Brambatti et al45. CV: cardiovascular; ES: embolia sistémica; HR: hazard ratio; IC95%: intervalo de confianza del 95%; IM: infarto de miocardio.
Estos resultados del rivaroxabán en el paciente diabético se han confirmado en los estudios de práctica clínica33,46. Así, en un estudio en el que se incluyó a pacientes con diabetes mellitus tipo 2 y FA no valvular que iniciaron tratamiento bien con rivaroxabán (n = 10.700), bien con warfarina (n = 13.946), el tratamiento con rivaroxabán se asoció con reducciones significativas, del 25% en el riesgo de MACE y del 63% en el riesgo de MALE, sin aumentar el riesgo de hemorragias33. Aunque en una población diferente (pacientes con enfermedad car-diovascular ateroesclerótica estable) y con una dosis diferente, mucho menor («dosis vascular», 2,5 mg 2 veces al día), el tratamiento con rivaroxabán también reduce los riesgos de MACE y de MALE47,48.
Paciente con fa no valvular y función renal alteradaLos pacientes con enfermedad renal crónica están en mayor riesgo de FA49. De hecho, se estima que la prevalencia de FA en los sujetos con insuficiencia renal llega al 7-18%, lo que supone un incremento del riesgo de FA de entre 2 y 6 veces respecto a la población gene-ral50,51. Existen múltiples mecanismos que explican el aumento en el riesgo de FA del paciente con enfermedad renal crónica. Por un lado, existen factores de riesgo que son comunes a ambas entidades y, por lo tanto, incrementan el riesgo tanto de FA como de insuficiencia renal: hipertensión arterial, diabetes mellitus, cardiopatía isquémica o insuficiencia cardiaca. Por otra parte, en la enfermedad renal cró-nica se produce sobrecarga hemodinámica e hipertrofia del ven-trículo izquierdo, activación de diferentes sistemas neurohormonales (renina-angiotensina-aldosterona, sistema nervioso simpático), aumento del estrés oxidativo y de marcadores de inflamación y alte-raciones del metabolismo mineral, todo lo cual va a producir altera-ciones eléctricas y estructurales que se traducirán en fibrosis miocár-dica y dilatación de la aurícula izquierda y, en último término, favorece la aparición de FA49,52,53.
Los pacientes con FA y enfermedad renal crónica tienen un mayor riesgo de complicaciones tromboembólicas, principalmente debido al estado de hipercoagulabilidad y protrombótico, junto con las altera-ciones del metabolismo calciofosfórico que ocurren en estos pacien-tes49,54,55. Además, frecuentemente se asocian otras comorbilidades, como hipertensión arterial o diabetes, que incrementan aún más este riesgo. Aunque el deterioro de la función renal se asocia con aumento en el riesgo de hemorragias, esto ocurre sobre todo en pacientes con insuficiencia renal grave y en menor medida en los sujetos con insufi-ciencia renal moderada. Por ello, la mayoría de los pacientes con FA y enfermedad renal crónica van a requerir anticoagulación de por vida para disminuir el riesgo de ictus1,49. Se ha señalado incluso que la insuficiencia renal debería incorporarse a las escalas de riesgo como un factor de riesgo de tromboembolia56.
Aunque el objetivo principal de la anticoagulación es la disminu-ción del riesgo de ictus y embolia sistémica1, en el paciente con FA y enfermedad renal crónica hay que buscar una protección integral que no se limite a la prevención de las complicaciones tromboembólicas, sino que también prevenga las complicaciones renales49. Aunque varios estudios han demostrado que los AVK reducen significativa-mente el riesgo de ictus con un aceptable perfil de seguridad57,58, el tratamiento con AVK se asocia con un daño estructural y deterioro progresivo de la función renal, sobre todo cuando hay un mal control de la INR (nefropatia por warfarina)49,59. Los diferentes estudios ofre-cen cifras muy variables, dependiendo de la definición y el tipo de población, llegando al 20-63%, según los casos59.
Los ensayos clínicos fundamentales han demostrado en su con-junto, que en los pacientes con insuficiencia renal moderada (aclara-miento de creatinina de 30-49 ml/min), los resultados de eficacia y seguridad de los ACOD frente a la warfarina coinciden con los datos generales14. En el estudio RE-LY, la eficacia de ambas dosis de dabiga-trán frente a warfarina fue independiente de la función renal, si bien parece que habría un menor riesgo de hemorragias mayores en los sujetos con un filtrado glomerular ≥ 80 ml/min/1,73 m260. En el estu-dio ARISTOTLE, aunque los pacientes con deterioro presentaron un mayor riesgo de eventos cardiovasculares y hemorragias, la eficacia y la seguridad relativa del apixabán frente a la warfarina fue indepen-diente de la presencia de insuficiencia renal61. En el ENGAGE AF-TIMI 48, aunque hubo un aparente descenso de la eficacia relativa en cuanto a la prevención de las complicaciones tromboembólicas con el edoxabán frente a la warfarina en las franjas altas de aclaramiento de creatinina, el beneficio clínico neto fue favorable al edoxabán inde-pendientemente de la función renal62.
En el estudio ROCKET-AF, un 21% de los pacientes tenían un aclara-miento de creatinina de 30-50 ml/min. A pesar del mayor riesgo de ictus y hemorragias de los pacientes con enfermedad renal crónica moderada, la eficacia y la seguridad del rivaroxabán frente a la warfa-rina coincidieron con los resultados del estudio general63. Asimismo, en los pacientes incluidos en el estudio ROCKET-AF que presentaron deterioro de la función renal, un grupo de pacientes con mayor mor-talidad, el rivaroxabán redujo significativamente, en un 50%, el riesgo de ictus o embolia sistèmica, en comparación con warfarina64. Estu-dios de práctica clínica diaria han confirmado este efecto beneficioso del rivaroxabán en cuanto a la reducción de ictus isquémico: hasta el 45% frente a la warfarina en sujetos con FA y enfermedad renal cró-nica, sin un incremento del riesgo de hemorragias mayores65.
Diferentes estudios han puesto de manifiesto que, en comparación con los AVK, el rivaroxabán se asocia con reducciones del riesgo de complicaciones renales (lesión renal aguda, evolución a enfermedad renal terminal o diálisis, reducción del filtrado glomerular o duplica-ción de la creatinina sérica). A raíz de estos datos, y aunque las dife-rencias no parecen clínicamente relevantes, algunos autores han señalado que, en comparación con los AVK, el rivaroxabán podría con-siderarse «nefroprotector»66-68. En el estudio de Yao et al., parece que este efecto beneficioso no ocurre con la misma intensidad con todos los anti-Xa, ya que, mientras que el rivaroxabán produjo reducciones significativas del riesgo de complicaciones renales, este efecto benefi-cioso no se observó con el apixabán68.
Paciente con fa no valvular e infarto de miocardioLos pacientes con FA tienen incrementado el riesgo no solo de ictus, sino también de muerte cardiovascular e infarto de miocardio. En un metanálisis de 15 estudios de cohortes, la presencia de FA aumentó el riesgo de infarto de miocardio en un 54% (RR = 1,54; IC95%, 1,26-1,85), el de insuficiencia cardiaca en más de 4,5 veces (RR = 4,62; IC95%, 3,13-6,83) y casi el doble el de muerte por cualquier causa (RR = 1,95; IC95%, 1,50-2,54)69. Además, el riesgo de infarto de miocardio no es constante, sino que aumenta con la evolución de la enfermedad70.
Aunque la complicación más temible en el paciente con FA no anti-coagulado es el ictus, en el sujeto correctamente anticoagulado son la muerte de origen cardiovascular y la insuficiencia cardiaca, y en menor medida el ictus71. En consecuencia, a la hora de plantear el mejor tratamiento antitrombótico, no hay que valorar solo la eficacia en reducir el riesgo de ictus, sino también buscar la protección cardio-vascular integral.
Distintos estudios han demostrado que los AVK tienen un efecto positivo en la reducción de los MACE en general y del infarto de mio-cardio en particular, pero solo en pacientes con un control excelente de la INR (tiempo en rango terapéutico > 65-75%)72. Desafortunada-mente, en la práctica clínica habitual el control adecuado de la anti-coagulación es bastante pobre en general22-25, por lo que no parece la mejor opción en este contexto clínico. De hecho, en la última guía europea de síndrome coronario crónico, para los pacientes con FA y cardiopatía isquémica se prefieren los ACOD a los AVK, y en caso de que se usaran los AVK, solo sería adecuado para los pacientes con un tiempo en rango terapéutico > 70%73.
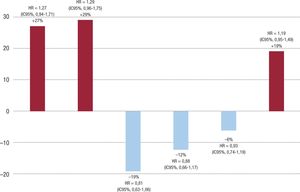
Con respecto a los ACOD, en un metanálisis de 13 ensayos clínicos con más de 100.000 pacientes incluidos, en comparación con warfa-rina, los ACOD redujeron la mortalidad cardiovascular en un 12% (RR = 0,88; IC95%, 0,82-0,94) y la mortalidad por cualquier causa en un 9% (RR = 0,91 ; IC95%, 0,87-0,96)74. En cuanto al riesgo de infarto de miocardio, aunque en general los ACOD tienen un riesgo similar al de los AVK, parece que no todos los ACOD se comportarían de la misma manera75-77. Así, mientras que en el estudio RE-LY hubo una tendencia a más riesgo de infarto de miocardio con el dabigatrán en compara-ción con la warfarina75, el riesgo fue similar con el apixabán en el estudio ARISTOTLE y con el edoxabán en el ENGAGE AF-TIMI 4843,78. En cambio, el rivaroxabán es el que ofrecería un mayor beneficio en la reducción en el riesgo de infarto de miocardio en pacientes con FA no valvular (Figura 4) y enfermedad tromboembólica venosa43,74,78,79. En un metanálisis realizado específicamente con rivaroxabán, se observó una reducción significativa del 18% en el riesgo de infarto de miocar-dio en comparación con los grupos de control, que incluyeron warfa-rina, enoxaparina o placebo (odds ratio [OR] = 0,82; IC95%, 0,72-0,94; p = 0,004)80. Un reciente metanálisis de 28 ensayos clínicos, con cerca de 200.000 pacientes con y sin FA, confirmó este beneficio del rivaro-xabán en cuanto a la reducción de los infartos de miocardio81.
Riesgo de infarto de miocardio en los ensayos clínicos de fase III de los ACOD frente a la warfarina (las diferencias no fueron significativas). Figura elaborada con datos de Giugliano et al43, Chai-Adisaksopha et al74, Loffredo et al77 y Granger et al78. ACOD: anticoagulantes orales de acción directa; HR: hazard ratio; IC95%: intervalo de confianza del 95%.
En el paciente con FA y cardiopatía isquémica, ya sea en el con-texto de un síndrome coronario agudo o crónico, en ocasiones es necesario realizar una intervención coronaria percutánea (ICP)82,83. En esta situación, el tratamiento debe perseguir un doble objetivo: la prevención del ictus y de los eventos isquémicos cardiacos. Ya en el estudio WOEST se observó que el tratamiento antitrombótico doble con AVK y un antiagregante se asociaba con un menor riesgo de hemorragias que el tratamiento antitrombótico triple con AVK y doble antiagregación, sin aumentar las complicaciones tromboem-bólicas o isquémicas84. En los últimos años se han publicado ensayos clínicos específicos con los 4 ACOD85-88. En el PIONEER AF-PCI, el riva-roxabán 15 mg ( 10 mg en caso de insuficiencia renal moderada) aña-dido a un inhibidor del P2Y12 durante 12 meses, se asoció con una reducción significativa del 41% en el riesgo de hemorragias, sin un aumento de los eventos isquémicos en comparación con el trata-miento antitrombótico triple estándar (AVK y doble antiagregación plaquetaria)85. En el estudio RE-DUAL PCI, que no incluyó a pacientes ancianos fuera de Estados Unidos con la dosis mayor), ambas dosis de dabigatrán (110 y 150 mg) se asociaron con un menor riesgo de hemorragias en comparación con el tratamiento antitrombótico tri-ple con AVK, sin un mayor riesgo de complicaciones tromboembóli-cas86. El estudio AUGUSTUS, a diferencia del resto de los ensayos clí-nicos, permitió comparar el tratamiento antitrombótico doble (apixabán o AVK más un inhibidor del P2Y12) con el tratamiento anti-trombótico triple (añadiendo ácido acetilsalicílico [AAS]) durante 6 meses. El grupo con un menor riesgo de hemorragias fue el trata-miento antitrombótico doble con apixabán y un inhibidor del P2Y12, sin un aumento en el riesgo de eventos isquémicos87. El estudio ENTRUST-AF PCI con edoxabán fue el único de los ensayos clínicos que no logró demostrar superioridad frente el tratamiento antitrom-bótico triple con AVK en cuanto a la reducción en el riesgo de hemo-rragias88. Aunque existen diferencias relevantes entre los 4 ensayos clínicos, especialmente en cuanto al diseño, en general han demos-trado que el tratamiento antitrombótico doble con un ACOD y un an-tiagregante disminuye el riesgo de hemorragias frente al tratamiento triple clásico, sin una disminución de la eficacia85-88. Por lo tanto, la combinación de un ACOD con un antiagregante probablemente se debería considerar en la actualidad como el tratamiento estándar, y reservar el tratamiento antitrombótico triple (mejor con ACOD que con AVK) para los pacientes con un mayor riesgo de trombosis del stent, durante un tiempo variable (1 semana-6 meses), dependiendo del equilibrio entre el riesgo de trombosis del stent y el riesgo hemo-rrágico73.
En el estudio PIONEER AF-PCI con rivaroxabán, se observó que estos resultados (menor riesgo de hemorragias junto con una eficacia similar en cuanto al riesgo de MACE, trombosis del stent e ictus)85 fue-ron independientes de la vía de acceso, de que la revascularización fuera electiva o urgente y el tipo y el número de stents88 o el grado de control de la INR con los AVK90. Asimismo, tras la ICP, las hospitaliza-ciones tanto por complicaciones cardiovasculares como por las hemo-rragias fueron menos frecuentes con el rivaroxabán, lo que se tradujo en un menor coste total91. En consecuencia, de forma similar que con otros ACOD, el tratamiento antitrombótico doble con rivaroxabán y un antiagregante plaquetario se podría considerar una opción de pri-mera línea para los pacientes con FA sometidos a ICP.
DiscusiónAunque tradicionalmente la valoración principal del paciente con FA se ha limitado a la prevención de las complicaciones tromboembó- licas a través de la anticoagulación, lo cierto es que estos pacientes tienen numerosas comorbilidades que también condicionan el pro-nóstico de manera muy importante y es necesario atender. La guía europea de práctica clínica señala que los únicos 2 abordajes que han logrado mejorar el pronóstico en el paciente con FA son la anticoagu-lación y el control de las comorbilidades1. En consecuencia, a la hora de escoger el mejor tratamiento anticoagulante, habrá que seleccio-nar los fármacos que proporcionen una protección más integral.
Los pacientes con FA y antecedente de ictus/AIT tienen un riesgo excepcionalmente elevado de sufrir nuevos eventos tromboembóli-cos, por lo que la prevención adecuada con la anticoagulación es obligada1. En este contexto, los ACOD superan ampliamente a los AVK, por su mejor perfil de eficacia (menos riesgo de ictus) y seguri-dad (menos riesgo de hemorragias mayores e intracraneales)14. Ahora bien, en la práctica clínica, parece que no todos los ACOD ofre-cerían la misma protección en la prevención de los ictus11. En este sentido, se ha demostrado en la práctica clínica habitual que el riva-roxabán reduce el riesgo de ictus11, incluso de los pacientes más complejos, lo que principalmente se podría atribuir a una menor probabilidad de errores en la dosificación en la práctica clínica, por su mayor simplicidad de selección de dosis, al depender únicamente de la función renal92-94.
En los últimos años ha cambiado el paradigma del tratamiento de la diabetes mellitus tipo 2 con la aparición de fármacos que mejoran el pronóstico cardiovascular, que van más allá del simple control metabólico95. En estos pacientes, la guía recomienda el empleo de los ACOD antes que los AVK95. En comparación con los otros ACOD, la reducción del 20% en la mortalidad cardiovascular con rivaroxabán frente a warfarina observada en el estudio ROCKET-AF40 y el menor riesgo de MACE y MALE encontrado en estudios de práctica clínica33 podrían suponer una ventaja adicional en esta población.
Al contrario de lo que ocurre con los ACOD, el ajuste de la dosis con los AVK se hace de manera independiente de la función renal18, pero lo cierto es que el tratamiento con AVK conduce a un mayor deterioro de la función renal que el que cabría esperar por el envejecimiento y las comorbilidades de los pacientes49. En consecuencia, la búsqueda de la máxima protección de la función renal debería ser otro de los objetivos en el paciente con FA. En este sentido, los estudios de la práctica clínica apuntan que el rivaroxabán ofrecería una adecuada nefroprotección68.
En el paciente correctamente anticoagulado, la principal causa de muerte no sería el ictus, sino la muerte de origen cardiovascular, el infarto de miocardio y la insuficiencia cardiaca1,71. En un reciente metanálisis se ha demostrado que el rivaroxabán reduce el riesgo de infarto de miocardio en el paciente con FA, y que este efecto benefi-cioso es superior al de los otros ACOD81. Estos resultados, junto con los del estudio COMPASS (en otro contexto clínico)47, podrían situar el rivaroxabán como la alternativa terapéutica preferente para el paciente con FA y cardiopatía isquémica. Finalmente, el estudio PIO-NEER AF-PCI es el primer ensayo clínico realizado con los ACOD que ha demostrado que la estrategia del tratamiento antitrombótico doble con un ACOD (rivaroxabán) y un antiagregante plaquetario era supe-rior al tratamiento antitrombótico triple tradicional con AVK y trata-miento antitrombótico doble.
ConclusionesEl objetivo de la anticoagulación en el paciente con FA no debería limitarse únicamente a la prevención de las complicaciones trom-boembólicas, sino que también debe buscar la protección integral. En este sentido, habría que usar preferentemente las alternativas tera-péuticas que proporcionen un mayor beneficio cardiovascular general en diferentes perfiles de pacientes, sobre todo aquellos con un mayor riesgo vascular.
En concreto, el rivaroxabán podría considerarse como un anticoa-gulante de primera línea para el paciente en alto riesgo cardiovascular no solo por su mayor facilidad de uso, sino por todas las ventajas adi-cionales que proporciona en estos pacientes complejos.
AgradecimientosContent Ed Net (Madrid) proporcionó asistencia editorial en la redacción de este manuscrito, con financiación de Bayer Hispania.
Conflicto de interesesV. Barrios ha recibido honorarios por ponencias y asesorías para Bayer, BMS/Pfizer, Boeringer Ingelheim y Daiichi Sankyo. D. Vivas ha recibido honorarios por consultoría de Bayer. F. Atienza Fernández ha sido consultor para Medtronic, MicroPort y Bayer. R. Diaz Simón no tiene conflictos de intereses. A. Sanchez Purificación ha colaborado en actividades financiadas por Bayer, Sanofi, Amgem, Menarini, Novo Nordisk, Astra y Shire. G. Barón-Esquivias ha recibido honorarios por consultoría de Bayer.