La hipertensión resistente es un problema clínico por la dificultad de su tratamiento y el aumento de morbimortalidad que conlleva. Se ha demostrado que la denervación renal por catéter mejora el control de estos pacientes. Se describen los resultados de la creación de una unidad multidisciplinaria para la implementación de la denervación renal en el tratamiento de la hipertensión resistente.
MétodosUn equipo compuesto por nefrólogos y cardiólogos diseñó un protocolo para la selección, la intervención y el seguimiento de los pacientes. Se incluyó a 197 pacientes con hipertensión esencial mal controlada pese a la toma de tres o más fármacos. A la técnica de ablación descrita, se añadió el soporte de un navegador basado en angiografía rotacional. Se comparó la presión arterial basal y tras el seguimiento utilizando el test de Wilcoxon para muestras apareadas.
ResultadosSe excluyó a 108 (55%) pacientes con hipertensión seudorresistente. A los otros 89, se les administraron antialdosterónicos, a los que respondieron 60 pacientes (30%). Fueron candidatos a denervación los 29 (15%) pacientes restantes. Se realizó ablación a 11 pacientes, con una presión arterial de 164/99mmHg, en tratamiento con 4,4 fármacos. Tras un seguimiento de 72 días, las presiones arteriales sistólica y diastólica se redujeron en 25mmHg (p=0,02) y 10mmHg (p=0,06) respectivamente. En 10 pacientes (91%) se suspendió al menos un fármaco.
ConclusionesLa denervación renal implementada mediante un programa multidisciplinario ofrece una mejora en la presión arterial similar a la de estudios previos, con mayor reducción de fármacos antihipertensivos.
Palabras clave
La hipertensión arterial es un problema de salud pública de primera magnitud, tanto por su elevada prevalencia como por el importante aumento de la morbimortalidad cardiovascular que conlleva1. Actualmente el tratamiento de la hipertensión tiene dos pilares: la modificación de ciertos hábitos de vida y el uso de fármacos antihipertensivos2. El control de las cifras de presión arterial (PA) sigue siendo inadecuado en casi la mitad de los hipertensos3,4 debido a la baja adherencia al tratamiento o a la ineficacia de los fármacos disponibles.
En este contexto, se define la hipertensión arterial resistente (HTAR) como la situación en que las cifras de PA son >140/90mmHg pese a la toma de tres o más fármacos, incluido un diurético, a las dosis adecuadas5. La prevalencia de HTAR no es bien conocida, pero se estima en torno al 13% de los hipertensos en tratamiento. Su presencia implica un incremento en la mortalidad y una mayor afección de órganos diana respecto al resto de la población hipertensa6.
El sistema nervioso simpático ejerce un importante papel en el mantenimiento y la progresión de la hipertensión. La inervación simpática alcanza el riñón a través de la adventicia de la arteria renal. Las fibras simpáticas eferentes producen vasoconstricción renal y aumentan la producción de renina y la retención de sodio, lo cual conlleva un aumento de la volemia y, por lo tanto, de la PA; por su parte, el simpático aferente renal, en respuesta a la hipoperfusión, modula la respuesta simpática sistémica produciendo vasoconstricción y, de este modo, también un aumento de la PA7,8.
Recientemente se ha desarrollado la denervación renal (DR) por catéter, un procedimiento basado en la aplicación de radiofrecuencia en el interior de las arterias renales con el fin de modular los mecanismos anteriormente descritos. Tras una experiencia preclínica favorable en modelos animales9, la eficacia y la seguridad de esta terapia en humanos se ha demostrado en los estudios Symplicity. En un primer estudio no aleatorizado, el Simplicity HTN-110, se demostró la factibilidad y la seguridad de la DR, sin detectarse complicaciones relacionadas con la ablación en las arterias renales. Posteriormente, el ensayo clínico Simplicity HTN-211, que incluyó a 106 pacientes aleatorizados a tratamiento estándar o DR, demostró una disminución de la presión arterial medida en consulta (PAMC) de 30/11 mmHg a los 6 meses, con una reducción del tratamiento farmacológico en un 20% de los pacientes denervados. En una extensión del seguimiento de los pacientes del Simplicity HTN-1, se evidenció que el beneficio de esta terapia se mantiene al menos en los primeros 2 años de seguimiento12.
Actualmente se dispone de poca información relativa al entorno clínico en el que se pone en práctica esta terapia, la especialidad de los facultativos que la realizan y los resultados que puede ofrecer fuera del ámbito de los ensayos clínicos.
El objetivo del presente estudio es describir la creación de una unidad multidisciplinaria de DR integrada en los servicios de nefrología y cardiología de un centro, así como la implementación y los resultados del programa de manejo de la HTAR diseñado por dicha unidad.
MÉTODOSFormación de la unidad de denervación renalSe creó un equipo multidisciplinario para la puesta en marcha de la DR, formado por nefrólogos de la unidad de hipertensión, encargados de la selección y el seguimiento de los pacientes, y cardiólogos intervencionistas de las unidades de arritmias y hemodinámica, previamente entrenados en DR, quienes realizaron los procedimientos. Se elaboró conjuntamente un protocolo clínico para la selección, la intervención y el seguimiento de los pacientes. Se diseñó un consentimiento informado específico, aprobado por la comisión de calidad del centro.
Población de estudioEntre junio de 2011 y junio de 2012, se preseleccionó a 197 pacientes con hipertensión esencial que presentaban cifras de PAMC sistólica >140 o diastólica >90mmHg pese a la toma de tres o más fármacos (incluido un diurético) y cumplían además los siguientes criterios: filtración glomerular estimada >45ml/min/1,73m2, ausencia de eventos coronarios o cerebrovasculares en los últimos 6 meses, ausencia de estenosis renal descartada mediante eco-Doppler y ausencia de contraindicaciones para cateterismo por vía femoral.
De todos los pacientes se obtuvo la PAMC al menos en tres ocasiones en cada visita, tomando la media de las últimas dos determinaciones para minimizar la reacción de alerta. Se realizó asimismo una monitorización ambulatoria de la presión arterial (MAPA) de 24 h a todos los potenciales candidatos.
A los pacientes seleccionados para DR, previamente a la ablación se realizó una angiografía por tomografía computarizada (angio-TC) de aorta abdominal dirigida a excluir a los pacientes con arterias renales pequeñas (calibre <4mm y longitud <20mm) y estudiar posibles estenosis o variantes anatómicas con vistas a la ablación.
ProcedimientoEl diseño de la intervención fue orientado parcialmente por la información de los estudios Symplicity y las recomendaciones de la compañía. Se añadió una nueva herramienta para la asistencia del procedimiento: la angiografía rotacional y la reconstrucción de la arteria renal mediante un navegador fluoroscópico (Allura 3D Rotational Angiography, Philips Medical Systems Inc.; Best, Países Bajos).
El procedimiento consistió en una aortografía rotacional con catéter pigtail introducido a través de un acceso arterial femoral y la canalización selectiva de cada arteria renal con un catéter guía para la introducción de un catéter de ablación específico (Symplicity Catheter System, Ardian/Medtronic Inc.; California, Estados Unidos) hasta la porción distal de la arteria.
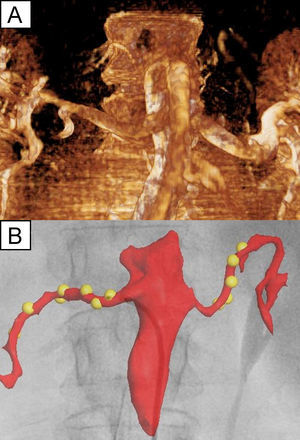
La angiografía rotacional se obtuvo mediante una inyección automática y sincronizada de 70 ml de contraste, a través de un pigtail situado en la aorta abdominal, a una velocidad de 14 ml/s durante una rotación del arco fluoroscópico de 220° en 4,4 s. Esta angiografía permite obtener un molde tridimensional de las arterias renales para su proyección en la pantalla de rayos X. De este modo es posible conocer en cada momento la posición relativa del catéter respecto a la arteria renal y marcar cada punto de aplicación de radiofrecuencia en dicho molde. La figura 1 muestra un ejemplo de la aortografía obtenida y la imagen del navegador una vez realizada la aplicación a las lesiones.
A: angiografía rotacional obtenida de la aorta abdominal y ambas arterias renales principales en uno de los pacientes. B: captura de pantalla del navegador fluoroscópico que muestra una reconstrucción anatómica basada en la imagen previa superpuesta en la escopia, así como las lesiones de radiofrecuencia (marcadas como esferas amarillas) realizadas por el catéter, que se encuentra próximo al ostium de la arteria renal derecha. Esta figura se muestra a todo color sólo en la versión electrónica del artículo.
Se realizaron aplicaciones de radiofrecuencia de 2 min y 8 W en cada arteria, previa heparinización, monitorizando un adecuado contacto radiológicamente y a través de las curvas de temperatura e impedancia que ofrece la fuente de radiofrecuencia. El objetivo de procedimiento era la generación del máximo número de aplicaciones posibles, separadas 0,5 cm entre sí, hasta un máximo de ocho por arteria. Se realizó, antes y después de la ablación, una angiografía selectiva de cada arteria renal tras nitroglicerina intraarterial, para analizar adecuadamente el vaso eliminando el componente de espasmo.
Los procedimientos se realizaron con sedación consciente administrada por los operadores. Se utilizó midazolam y fentanilo según el protocolo utilizado por nuestro laboratorio de electrofisiología para otras ablaciones dolorosas: bolo inicial de midazolam (1 o 2 mg) y fentanilo (0,05 mg) y bolos adicionales de fentanilo (0,03-0,05 mg) que se fueron administrando según respuesta.
SeguimientoEl seguimiento se realizó en la consulta de la unidad de hipertensión, con visitas programadas la semana 1 y los meses 1, 3 y 6 tras la ablación. En cada visita se realizó una valoración clínica y determinación de la PAMC. Se obtuvo además MAPA y eco-Doppler de arterias renales en los meses 1 y 6. Se obtuvieron analíticas de sangre a las 24 h de la intervención y al mes 1, con el objetivo de monitorizar la función renal.
El tratamiento con fármacos anihipertensivos fue ajustándose en cada visita a juicio del nefrólogo, en función de las cifras de PA y los síntomas del paciente.
Análisis estadísticoLas variables continuas se expresan como media±desviación estándar y las discretas, como proporciones.
Se compararon las cifras de PA antes y después de la ablación utilizando el test no paramétrico de Wilcoxon para muestras apareadas, dado el escaso tamaño de la muestra. Se utilizó un nivel de significación de dos colas p<0,05 para todas las comparaciones.
Se utilizó para el análisis de los datos el paquete estadístico SPSS 14.0 para Windows.
RESULTADOSSelección de candidatosLa MAPA realizada a los 197 pacientes con PAMC elevada mostró cifras de PA media en periodo de actividad <140/90mmHg en 108 de ellos (55%), quienes fueron etiquetados como pacientes con hipertensión seudorresistente.
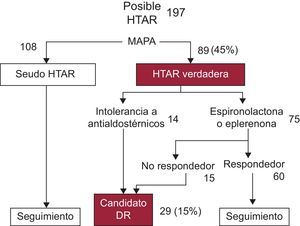
A los 89 restantes, se les administraron fármacos antialdosterónicos (espironolactona o eplerenona) para contrarrestar un posible hiperaldosteronismo secundario. Se utilizó espironolactona (dosis entre 50 y 100mg/día) o eplerenona (dosis entre 25 y 50mg/día) a criterio del nefrólogo. Durante el seguimiento 60 pacientes (30%) mejoraron las cifras de PA en al menos 20 mmHg de PA sistólica y/o 10 mmHg de PA diastólica. Se seleccionó como candidatos para DR a los 29 pacientes (15%) no respondedores o intolerantes a los antialdosterónicos. En la figura 2 se muestra un esquema del protocolo de selección utilizado.
Manejo de los pacientes con posible hipertensión arterial resistente en el estudio. Se observa que la monitorización ambulatoria de la presión arterial permitió descartar a la mayoría de los pacientes con hipertensión seudorresistente y cuál fue la respuesta a los antialdosterónicos observada, lo que permitió seleccionar sólo al 15% de los pacientes como candidatos a denervación renal. DR: denervación renal; HTAR: hipertensión arterial resistente; MAPA: monitorización ambulatoria de la presión arterial.
Se presenta en este trabajo a los primeros 11 pacientes intervenidos en nuestro centro, entre febrero y junio de 2012, que fueron seleccionados mediante el protocolo descrito. La tabla 1 muestra las características basales de dichos pacientes.
Características basales de los pacientes sometidos a ablación renal
| Edad (años) | 49±13 |
| Varones | 4 (36) |
| Peso (IMC) | 30±7 |
| Normopeso | 3 (27) |
| Sobrepeso | 3 (27) |
| Obesidad | 5 (45) |
| Comorbilidad | |
| Tabaquismo | 2 (18) |
| DM2 | 3 (27) |
| Dislipemia | 4 (36) |
| SAOS | 3 (27) |
| Insuficiencia renal | 1 (9) |
| FC (lpm) | 82±4 |
| PAMC (mmHg) | 164/99±17/14 |
| MAPA (mmHg) | |
| PA diurna | 160/98±6/9 |
| PA nocturna | 145/85±10/10 |
| PA 24h | 155/94±8/9 |
| Número de fármacos | 4,4±0,5 |
| Tipos de fármacos | |
| IECA/ARA-II | 11 (100) |
| IDR | 4 (36) |
| Antialdosterónicos | 9 (82) |
| Antagonistas del calcio | 9 (82) |
| Tiacidas | 6 (54) |
| Diuréticos de asa | 4 (36) |
| Bloqueadores beta | 4 (36) |
| Bloqueadores alfa | 2 (18) |
ARA-II: antagonistas de los receptores de la angiotensina II; DM2: diabetes mellitus tipo 2; FC: frecuencia cardiaca; IDR: inhibidores directos de la renina; IECA: inhibidores de la enzima de conversión de la angiotensina; IMC: índice de masa corporal; MAPA: monitorización ambulatoria de la presión arterial; PA: presión arterial; PAMC: presión arterial medida en consulta; SAOS: síndrome de apnea obstructiva del sueño.
Los datos expresan n (%) o media±desviación estándar.
El procedimiento se realizó sin incidencias en todos los pacientes. La angio-TC realizada previamente identificó variantes anatómicas o lesiones en las arterias renales en 2 pacientes (una arteria polar en 1 paciente y una estenosis moderada próxima al ostium de una de las arterias renales). La aortografía y la cateterización selectiva mostraron además otras cuatro variantes no descritas en la angio-TC (dos arterias polares, una bifurcación en cañón de escopeta de la arteria renal y una anastomosis de la arteria renal con la diafragmática).
Se realizaron entre cuatro y ocho aplicaciones en cada arteria renal, evitando aplicar radiofrecuencia en las variantes anatómicas y lesiones arriba mencionadas. Cada paciente recibió así una media de 12,1±1,3 aplicaciones. El procedimiento tuvo una duración total media de 92 min y un tiempo medio de escopia de 16 min. Se utilizó una media de 171±42 ml de contraste.
Durante la aplicación de radiofrecuencia, 2 pacientes (18%) presentaron bradicardización <45lpm en respuesta al dolor como única complicación propia de la ablación, que se resolvió con atropina e interrumpiendo la aplicación. No hubo espasmo arterial en ningún caso; 2 pacientes presentaron complicaciones derivadas de la punción femoral horas después de la intervención: un hematoma inguinal por fallo del dispositivo de cierre percutáneo, que se controló mediante compresión manual, y un hematoma a nivel del psoas, que cursó con dolor durante la tarde del procedimiento y fue autolimitado. En ningún caso fue necesaria una transfusión o reintervención.
Seguimiento de los pacientes denervadosTodos los pacientes fueron dados de alta en las 24 h siguientes a la intervención, salvo el que tenía un hematoma retroperitoneal, que se fue a las 72 h. Se realizó una analítica de control previa al alta a todos los pacientes, sin que ninguno sufriera deterioro de la función renal tras la ablación.
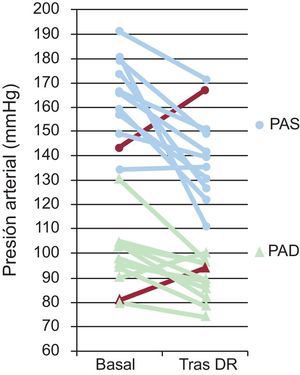
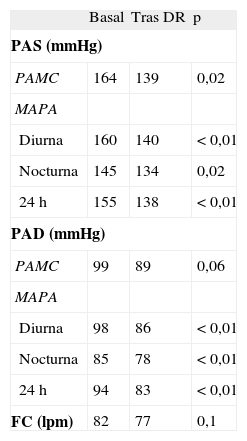
El seguimiento medio de los pacientes denervados fue de 72 días. En ese tiempo se observó un descenso medio de las cifras de PAMC de 25/10 mmHg. En la MAPA hubo un descenso en la PA diurna de 20/10mmHg; en la PA nocturna, de 11/7mmHg, y en la PA de 24 h, de 17/11mmHg. Todos los descensos de la PA fueron estadísticamente significativos (p<0,05), excepto el de la PAMC diastólica (p=0,06). La tabla 2 ofrece un resumen de las cifras de PA y frecuencia cardiaca obtenidas basalmente y tras el periodo de seguimiento. La figura 3 ofrece información pormenorizada sobre el seguimiento de la PAMC en cada uno de los pacientes denervados.
Medidas de presión obtenidas basalmente y tras el seguimiento en los pacientes denervados
| Basal | Tras DR | p | |
| PAS (mmHg) | |||
| PAMC | 164 | 139 | 0,02 |
| MAPA | |||
| Diurna | 160 | 140 | <0,01 |
| Nocturna | 145 | 134 | 0,02 |
| 24h | 155 | 138 | <0,01 |
| PAD (mmHg) | |||
| PAMC | 99 | 89 | 0,06 |
| MAPA | |||
| Diurna | 98 | 86 | <0,01 |
| Nocturna | 85 | 78 | < 0,01 |
| 24h | 94 | 83 | <0,01 |
| FC (lpm) | 82 | 77 | 0,1 |
DR: denervación renal; FC: frecuencia cardiaca; MAPA: monitorización ambulatoria de la presión arterial; PAD: presión arterial diastólica; PAMC: presión arterial medida en consulta; PAS: presión arterial sistólica.
Las comparaciones alcanzaron significación estadística con p<0,05.
Variación de las cifras de presión arterial sistólica y diastólica obtenidas en consulta basales y tras el seguimiento de los 11 pacientes sometidos a denervación renal. DR: denervación renal; PAD: presión arterial diastólica; PAS: presión arterial sistólica. Se presenta en rojo la evolución del paciente considerado no respondedor. Esta figura se muestra a todo color sólo en la versión electrónica del artículo.
Se suspendió en las distintas visitas al menos un fármaco en 10 de los 11 pacientes (91%), y en total una media de 1,4 (0-3) fármacos por paciente.
La eco-Doppler de arterias renales realizada en el seguimiento no mostró complicaciones en ningún paciente.
DISCUSIÓNEl programa de DR implementado en nuestro centro muestra resultados que confirman la evidencia científica disponible en cuanto al papel de la ablación renal en mejora del control de la PA, como se muestra por la reducción tanto de la PAMC como de la MAPA.
La selección de los candidatos se basó en la exclusión de hipertensión seudorresistente mediante valoración clínica, MAPA y la respuesta al tratamiento con antialdosterónicos. En este sentido, difiere del publicado en el ensayo Simplicity, que sólo tiene en cuenta el valor de la PA sistólica (>160mmHg) para la selección del candidato a ablación. Varios estudios observacionales han mostrado que los inhibidores de la aldosterona mejoran significativamente el control de la PA en los pacientes resistentes13–16, dada la posible aparición de hiperaldosternismo secundario. El único ensayo clínico aleatorizado disponible actualmente muestra también un efecto favorable, aunque moderado, de espironolactona frente a placebo en el control de la HTAR17. A pesar de dicha evidencia, llama la atención que sólo el 17% de los pacientes incluidos en el estudio Symplicity estuvieran tratados con antialdosterónicos, frente al 82% de los pacientes incluidos en nuestra serie, todos ellos no respondedores, en quienes se mantuvieron estos fármacos antes de la ablación. Aunque se desconoce si el tratamiento con antialdosterónicos puede mejorar la respuesta a la DR, en nuestra serie la introducción de antialdosterónicos mejoró el control de la PA en 60 de 89 pacientes (67%) con HTAR verdadera, lo que indica que, una vez excluida la población seudorresistente, un intento terapéutico con antialdosterónicos puede disminuir la necesidad de someter a ablación renal a un número importante de pacientes.
La reducción de las cifras de PAMC de 25/10 mmHg tras un seguimiento de 72 días resulta comparable a la publicada en el estudio Symplicity HTN-211, que fue de 24/8 mmHg a los 3 meses. Sin embargo, la reducción de fármacos antihipertensivos en nuestra serie fue mucho mayor que la descrita en dicho estudio (el 91 frente al 20% de los pacientes). La reducción de fármacos no estaba formalmente incluida en el ensayo clínico y sí en nuestro protocolo, lo que puede explicar, al menos en parte, la diferencia encontrada. Tan sólo la reducción de PAMC diastólica no fue estadísticamente significativa, lo que probablemente se explique por estar más influida relativamente por la reacción de alerta que la cifra de PA sistólica y las presiones obtenidas en la MAPA. Se ha mostrado sólo una tendencia a la reducción de la PAMC diastólica, que posiblemente habría sido significativa si se hubiera incluido a mayor número de pacientes.
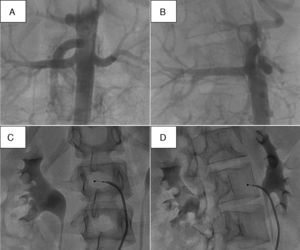
El procedimiento de DR se caracteriza por la ausencia de un objetivo agudo más allá de completar cierto número de lesiones en cada arteria. Actualmente se desconoce cuál es el número óptimo de aplicaciones que hay que realizar, que en ambos estudios Symplicity10,11 fueron entre cuatro y seis. Ante la incertidumbre sobre un potencial efecto dosis-respuesta, el procedimiento diseñado en nuestro centro se basa en la idea de producir tantas lesiones como sea posible (hasta un máximo de ocho por arteria). El número máximo de lesiones posible depende así de la longitud de la arteria tratada y de si hay o no variantes anatómicas. En este sentido, ha resultado de gran utilidad la aortografía rotacional realizada antes de la intervención, ya que permite seleccionar la proyección en que la longitud de la arteria es mayor, lo que facilita mayor número de aplicaciones (fig. 4).
Se ilustra cómo la angiografía rotacional permite seleccionar la proyección oblicua en que la longitud de la arteria es mayor. A y B: capturas de la angiografía rotacional en diferentes proyecciones oblicuas derechas de la arteria renal derecha; nótese cómo en B se aprecia mejor la longitud del vaso. C y D: proyecciones de trabajo equivalentes a las capturas de A y B respectivamente. D: proyección que permite retirar el catéter realizando un mayor número de aplicaciones que en C.
Se han identificado variantes anatómicas o lesiones en 6 de los 11 pacientes, ya sea mediante angio-TC o, más frecuentemente, durante la propia intervención. La presencia de estenosis no significativas o arterias polares no fue un criterio de exclusión de DR (y sí en los estudios Symplicity). En los 3 casos con arterias polares de la serie, se realizó la ablación sólo en la arteria renal principal. Otra opción más conservadora hubiera sido realizar la DR sólo en el riñón sin anomalías o variantes anatómicas, pero actualmente se desconoce cuál de las dos tiene un beneficio/riesgo más favorable. La presencia de bifurcaciones, ramas secundarias o estenosis en la arteria renal resalta la necesidad de una cuidadosa valoración anatómica del vaso durante el procedimiento con el fin de mantener la seguridad.
La compañía fabricante recomienda generar las lesiones en espiral a lo largo de la pared de la arteria, para tratar de modular una mayor proporción de inervación simpática y evitar posibles complicaciones como la estenosis del vaso. La fluoroscopia convencional, dado su carácter bidimensional, no permite reconocer con exactitud la posición concreta del catéter respecto a la pared de la arteria. En este sentido, el uso de un navegador fluoroscópico permite diseñar la espiral con mayor facilidad, ya que se puede marcar la posición de las aplicaciones previas (fig. 1). Otra potencial ventaja puede darse en caso de que haya que realizar una segunda ablación a un paciente no respondedor, al disponerse un mapa de las aplicaciones realizadas previamente.
En uno de los pacientes se normalizó la PA en la primera revisión, y tras presentarse síntomas de ortostatismo, se redujo el tratamiento hipotensor, con lo que sufrió una elevación de la PAMC en el último seguimiento (en la gráfica de la fig. 2, corresponde al paciente marcado en rojo). Las medidas en la MAPA fueron similares o ligeramente menores tras la ablación (la MAPA de 24 h pasó de 152/88 a 147/86mmHg), lo que indica un componente de reacción de alerta en las mediciones obtenidas en consulta. Este es el único paciente de la serie considerado no respondedor, ya que en los demás hubo un descenso de la PAMC sistólica o diastólica. Se trata de uno de los 2 pacientes con arteria polar en uno de los riñones y el de mayor edad de la serie (65 años). La proporción de no respondedores de la serie es comparable a la publicada por los investigadores del estudio Symplicity HTN-211.
Los resultados del programa han sido posibles gracias a la estrecha colaboración de médicos de distintas áreas. El importante papel de los nefrólogos de la unidad de hipertensión en la selección y el manejo del paciente resulta incuestionable. Todas las denervaciones las realizaron conjuntamente dos cardiólogos de distinto perfil: un hemodinamista y un electrofisiólogo. No obstante, no se considera necesaria la participación de ambos profesionales. Con el fin de incrementar la experiencia y garantizar mejores resultados, recomendamos que en cada centro realicen la técnica los especialistas que la hayan introducido y la hayan puesto en práctica desde el principio. Sin embargo, sí parece importante que los potenciales candidatos sean estudiados por especialistas de la hipertensión (nefrólogos, cardiólogos o internistas, en función del centro), en centros con experiencia, tal y como recomienda la Sociedad Europea de Hipertensión18.
LimitacionesSólo se muestran los primeros 11 pacientes tratados de los 29 aceptados para DR, con lo que puede haber un sesgo de selección en el grupo. No se ofrecen datos comparativos respecto a los pacientes no denervados. La selección basada en una PA sistólica >140mmHg confirmada en MAPA y tras la respuesta a los antialdosterónicos es diferente de la que ha demostrado eficacia en estudios previos10,11 (PA sistólica >160mmHg) y no puede ser validada adecuadamente por no existir un grupo control. Por el mismo motivo, puede haber un efecto placebo en la respuesta a la denervación o que esta condicione una mayor adherencia a la dieta hiposódica y al tratamiento farmacológico. La angiografía rotacional y el navegador se han utilizado sistemáticamente en todos los pacientes sin haberla comparado con el abordaje convencional, por lo que su posible repercusión en la cantidad de contraste empleada, la eficacia o la seguridad del procedimiento sigue siendo desconocida, y para ello sería necesario aleatorizar el empleo de la angiografía rotacional frente a la técnica realizada con soporte fluoroscópico convencional. Al tratarse de los primeros pacientes intervenidos en nuestro centro, la curva de aprendizaje, aunque es relativamente corta, ha podido interferir en los resultados del programa. El escaso número de pacientes denervados es la principal limitación del estudio y hace imposible obtener conclusiones sobre las variables que se asocian a mayor o menor respuesta a la terapia.
CONCLUSIONESEl protocolo diseñado en nuestro centro para la selección de los candidatos a DR excluye a la mayoría de los hipertensos con mal control y que toman tres o más fármacos debido a seudorresistencia o a la mejoría tras el uso de antialdosterónicos, lo que resalta la importancia de una adecuada valoración clínica del paciente con posible HTAR antes de indicar una DR.
La selección de los pacientes y la intervención realizada en los primeros pacientes denervados ha resultado en una mejora en la PAMC de una proporción de pacientes y en una cuantía similares a las de los estudios previos, pero con mayor reducción de fármacos hipotensores.
FINANCIACIÓNLos autores agradecen a la Fondation pour la prevention des maladies cardiovasculaires (Ginebra, Suiza) la financiación de los catéteres de ablación utilizados en el estudio.
CONFLICTO DE INTERESESNinguno.