Palabras clave
EVOLUCIÓN DEL INTERVENCIONISMO CORONARIO EN LAS ÚLTIMAS DÉCADAS: DE LA ANGIOPLASTIA CON BALÓN A LOS STENTS RECUBIERTOS DE FÁRMACOS
Desde que se realizó la primera angioplastia transluminal percutánea en el ser humano1 en 1977 hasta la actualidad, el intervencionismo coronario ha sido la modalidad terapéutica que ha evolucionado con más rapidez en comparación con cualquier otra forma de tratamiento en el campo de las enfermedades cardiovasculares. Esta técnica nació con unos resultados que hoy día no serían aceptables con los estándares actuales. En los primeros estudios, la tasa de éxito comunicada era del 86-88%, con una reestenosis del 30-40%2-8. Durante más de una década, esta técnica alcanzó una gran popularidad en la práctica clínica a pesar de que las tasas de oclusión aguda o subaguda llegaban incluso al 8%9. La angioplastia siguió adelante con unos resultados a veces decepcionantes, sobre todo en lesiones complejas, y durante años no se dispuso de estudios aleatorizados en los que se comparara con otras modalidades de tratamiento (el primer estudio aleatorizado se realizó a los 10 años de su introducción en el contexto del infarto agudo de miocardio)10. Para paliar las complicaciones de la técnica y reducir la tasa de reestenosis, a finales de los años ochenta surgieron nuevos dispositivos que presentaban, desde un punto de vista teórico, ciertas ventajas con la dilatación con balón. Se diseñaron dispositivos alternativos al balón que, en vez de aplastar y fracturar la placa, la resecaban o la pulverizaban desobstruyendo el segmento coronario estenótico. Ésta fue la base de la aterectomía, que en su momento aumentó el arsenal terapéutico del laboratorio de hemodinámica. Entre las técnicas de aterectomía, las más utilizadas fueron la aterectomía dirigida de Simpson, la de rotación (Rotablator) o la de extracción con aspiración (TEC).
Aterectomía transluminal dirigida
Fue introducida por Simpson en 1985 como alternativa a la angioplastia con balón en el tratamiento de las enfermedades arterioscleróticas de las arterias periféricas. Posteriormente, la misma técnica fue aplicada a la enfermedad coronaria con un notable éxito inicial. Por aquel entonces, numerosas publicaciones mostraron la utilidad de esta modalidad terapéutica, que permitía la resección y extracción de la placa de ateroma11-13. Este entusiasmo inicial por la aterectomía se vio mermado por la dificultad técnica de introducir un dispositivo rígido a través de un grueso catéter guía de 10-11 Fr con poca flexibilidad y escasa navegabilidad. Además, los resultados de los estudios aleatorizados que compararon los resultados de esta técnica con la angioplastia con balón no demostraron ningún tipo de beneficio. El primero de los grandes estudios aleatorizados fue el CAVEAT14, en el que se incluyó a más de 1.000 pacientes para comparar la aterectomía de Simpson con la dilatación con balón. En este estudio, con la aterectomía se obtuvo un mayor aumento de calibre intraluminal que con la angioplastia. Sin embargo, el procedimiento se asoció con una mayor tasa de complicaciones, sin diferencias significativas en términos de recurrencia clínica o reestenosis. La imposibilidad de demostrar diferencias significativas a favor de la aterectomía direccional en este estudio llevó a algunos investigadores a considerar que estos resultados podrían ser debidos a un déficit en la realización técnica de la aterectomía. Por tanto, diseñaron 2 nuevos grandes estudios aleatorizados en los que compararon de nuevo la angioplastia con balón con la aterectomía realizada de una forma óptima. Estos estudios (OARS y BOAT) demostraron un buen resultado inmediato en términos de ganancia luminal pero sin ventajas clínicas a largo plazo frente al grupo de pacientes tratados con angioplastia con balón15,16, por lo que en la actualidad la utilización de esta técnica en nuestro país ha disminuido considerablemente17.
Aterectomía rotacional (Rotablator)
A diferencia de la aterectomía direccional, cuyo mecanismo de acción es el corte y almacenamiento del material arteriosclerótico, el Rotablator produce una abrasión de la placa de ateroma pulverizándola en micropartículas (generalmente < 5 µ de diámetro) que embolizan el territorio capilar coronario y que son fagocitadas por el retículo endoplasmático, sin producir oclusión embólica significativa de los pequeños vasos. El dispositivo consta de una fresa elíptica metálica en su extremo distal con una superficie de pequeños cristales de diamante de 5-10 μ engarzadas en un eje conductor flexible que se conecta con una consola, desde donde se controla y monitoriza la velocidad de rotación. La velocidad de rotación oscila entre 140.000 y 190.000 revoluciones por minuto. Al igual que en la aterectomía direccional, esta modalidad fue acogida con entusiasmo para ser utilizada en lesiones desfavorables para la angioplastia. En los primeros años de su introducción, este dispositivo se utilizó en lesiones ostiales, calcificadas, largas, difusas y en lesiones indilatables, obteniéndose un éxito primario del 91-95% con una tasa de mortalidad del 0-3,3%18,19. El tiempo ha puesto en su lugar a esta modalidad terapéutica y, aunque no se han efectuado tantos estudios aleatorizados como en el caso de la aterectomía direccional, en la actualidad persiste con un nicho en nuestro arsenal terapéutico17. Se trata de las lesiones muy calcificadas, indilatables o en las que es imposible pasar ningún dispositivo una vez cruzada la guía coronaria. Estas lesiones son infrecuentes, pero no pueden resolverse de ninguna otra forma mediante técnicas percutáneas.
Otras modalidades técnicas de aterectomía han caído en desuso al ser superadas por otros dispositivos más eficaces.
Stents coronarios
El gran avance lo supuso la introducción en la práctica clínica del stent de Palmaz-Schatz20 en 1991. Este dispositivo permitía el sellado de la placa y de las posibles disecciones que se hubieran producido durante la dilatación con balón y, al mismo tiempo, creaba una amplia luz en el vaso tratado. Sin embargo, al ser un dispositivo metálico no estaba libre de complicaciones. La posible aparición de trombos en su interior y la trombosis de la prótesis fueron las complicaciones temidas durante los primeros 3 años de su introducción20-22. Para paliar este tipo de complicaciones, inicialmente se recomendó una terapia antitrombótica agresiva con heparina no fraccionada durante el procedimiento, seguida de una perfusión continua hasta que los anticoagulantes orales consiguieran una anticoagulación efectiva21,22. A pesar de esta anticoagulación agresiva, se producía una trombosis de la prótesis en el 5-7% de los casos y una no despreciable incidencia de complicaciones hemorrágicas20-23. No fue hasta 1994, con la llegada de los nuevos regímenes antitrombóticos consistentes en la doble antiagregación con ticlopidina y aspirina (con o sin heparina de bajo peso molecular), que estas complicaciones se redujeron prácticamente a valores < 1-2%23-27. A partir de esta fecha, el stent fue consagrado como el dispositivo más eficaz en la revascularización percutánea coronaria. Desde entonces, la industria comenzó a realizar una serie de mejoras técnicas para facilitar su implantación. El stent, que inicialmente venía suelto, se fabricó montado en el balón, consiguiéndose así un aumento en la seguridad del procedimiento. Posteriormente, la bajada del perfil del sistema balón-stent, junto con la creación de nuevas longitudes y diámetros, permitió abordar una serie de lesiones hasta entonces vetadas al tratamiento percutáneo. A mediados de la década de los noventa se había conseguido reducir la oclusión subaguda a menos de un 1-2%23-27 y la reestenosis de un 30-40% a un 20-30%28-30. A partir de este momento, toda la comunidad científica volcó sus esfuerzos en reducir esta cifra de reestenosis. Se probaron muchísimos fármacos con una teórica capacidad antimitótica y antiproliferativa, y aunque en el animal de experimentación se obtenían reducciones en el grado de proliferación neointimal, esto no se lograba traducir en resultados similares en el ser humano31. Así, hubo que esperar unos 10 años desde la introducción del stent para encontrar un nuevo remedio para reducir la tasa de reestenosis. Entre tanto, se mejoraron las técnicas coadyuvantes a la implantación del stent con la introducción y el desarrollo de los dispositivos extractores de trombo y de protección distal. En lesiones con un trombo de gran tamaño, el riesgo de su desprendimiento durante la implantación del stent podría comprometer el éxito del procedimiento32,33. Para reducir la incidencia de esta complicación se desarrollaron dispositivos de extracción de trombos que se han ido perfeccionando; en la actualidad contamos con algunos muy simplificados, que básicamente consisten en un tubo hueco conectado al vacío, frente a otros muy eficaces que requieren una tecnología más compleja34.
Sin duda, el descubrimiento más importante de la década posterior a la introducción del stent y de los regímenes antitrombóticos ha sido la introducción de los stents recubiertos de fármacos, a los que se le dedicará un capítulo en esta «Puesta al día» de revascularización miocárdica. En la tabla 1 se resumen los principales eventos históricos de la última década relacionados con la mejoría de los resultados del tratamiento percutáneo, con las fechas de introducción que podrían corresponder a un hospital medio de nuestro país.
RESULTADOS ACTUALES Y COMPLICACIONES
Desde el principio hasta la actualidad, los resultados del intervencionismo coronario dependen en gran medida del tipo de lesión que se aborde. Ya desde los comienzos, en 1988, la American Heart Association publicó unas guías de actuación para la angioplastia coronaria en la que clasificaba los tipos de lesiones en 3 categorías de riesgo35 (tabla 2). Las lesiones de tipo A tenía una probabilidad de éxito mayor del 85% y un riesgo de oclusión aguda bajo. Las lesiones de tipo B tenían una probabilidad de éxito del 60-85% y un riesgo de oclusión abrupta moderado. Por último, las lesiones de tipo C tenían una probabilidad de éxito < 60% con un riesgo alto de oclusión abrupta posprocedimiento. Más recientemente, en el año 2001, en la era del stent, se mantenía la misma clasificación de riesgo36. Sin embargo, la probabilidad de éxito en cada uno de los grupos de riesgo ha aumentado considerablemente con los dispositivos actuales.
Lesiones de bajo riesgo (tipo A)
La probabilidad de éxito aumentó con la llegada del stent28,29 y mejoró en la era de los modernos regímenes antitrombóticos23-27. La seguridad del procedimiento en este tipo de lesiones ha continuado durante estos años con la introducción de mejoras técnicas, y la probabilidad de éxito supera el 95%. Con la disponibilidad de los stents de rapamicina, el riesgo de reestenosis comunicado ha sido próximo al 0%37.
Lesiones de riesgo moderado (antiguo tipo B)
En este grupo de lesiones es preciso individualizar los resultados del intervencionismo en cada uno de los subtipos. En las lesiones moderadamente largas (10-20 mm), las excéntricas, las que presentan una calcificación moderada, un contorno irregular, una tortuosidad moderada del segmento proximal o un segmento a tratar moderadamente angulado, las tasas de éxito primario aumentaron con la llegada del stent convencional, como en el caso de las lesiones de tipo A28,29. El principal problema de la angioplastia con balón era la disección oclusiva, y en este tipo de lesiones, esta situación se podía resolver con el sellado mediante la implantación de stents adicionales. Por lo tanto, en estos grupos ya se superaba la tasa de éxito primario del balón del 60-85% a partir de mediados de la década de los noventa.
Lesiones con presencia de trombo
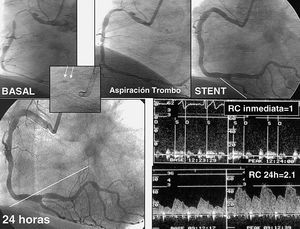
En la primera época de la angioplastia con balón este tipo de lesiones presentaron una alta incidencia de oclusiones agudas durante el procedimiento y en las primeras 24-48 h. Aunque algunos autores propusieron el uso de fármacos trombolíticos como terapia coadyuvante, éstos no consiguieron reducir en absoluto las complicaciones periprocedimiento38. A diferencia de otros tipos de lesiones de tipo B, al principio, los cardiólogos intervencionistas tuvieron reticencias para utilizar el stent en este tipo de situaciones debido a que se trataba de una estructura metálica y, por tanto, trombogénica. Se postulaba que no se resolvería el proceso trombótico que acompañaba a este tipo de lesiones. Sin embargo, la práctica demostró exactamente lo contrario: con la utilización de los stents en presencia de trombos se obtenían unos resultados excelentes32,33. La llegada de los nuevos regímenes antitrombóticos y de los inhibidores de la glucoproteína IIb/IIIa hizo mucho más seguro el procedimiento39. De nuevo, en la actualidad se alcanzan tasas de éxito más elevadas con todos estos avances y con la utilización de los dispositivos de aspiración de trombo40 (fig. 1); por tanto, hemos vuelto a pasar de una probabilidad de éxito del 60-85% a más de un 95%, con un riesgo de complicaciones < 5% en este tipo de lesiones.
Fig. 1. Ejemplo de una lesión con un gran trombo en el contexto de una angina inestable. Tras la aspiración e implantación de stents se obtiene un excelente resultado angiográfico. La reserva coronaria (RC) tarda 24 h en recuperarse. Las flechas marcan la localización del trombo en el vacío, teñido de contraste.
Lesiones ostiales y lesiones localizadas en la bifurcación
En la era de la angioplastia con balón, los resultados en este tipo de lesiones eran decepcionantes, con una alta incidencia de complicaciones. Vetrovec et al41 describieron una incidencia de oclusión del ramo colateral de hasta un 27%, donde el mecanismo de oclusión era la producción de una disección o el desplazamiento de la placa. Durante estos años, muchos cirujanos evitaron abordar este tipo de lesiones a pesar de que ya se habían descrito algunas técnicas, como el kissing balloon42 o la protección con doble guía43. La llegada del stent convencional supuso una revolución en el tratamiento de este tipo de lesiones y se describieron múltiples estrategias de implantación de stents, muchas de ellas aún vigentes. Los resultados que se obtuvieron en estos años (1994-2001), aunque aceptables, estaban lejos de los que podemos obtener actualmente. Así, la probabilidad de eventos mayores a los 6 meses (infarto, nueva revascularización o mortalidad) oscilaba entre el 50% en los pacientes en los que se trataba con stents el ramo principal y colateral y el 25-38% de los tratados con stent en el ramo principal y angioplastia en el colateral44-47. En los últimos 2 años, estos resultados han mejorado notablemente con la llegada de los stents recubiertos de fármacos. En estudios recientes48-50, los eventos mayores con stents de rapamicina a los 6 meses se han reducido a niveles tan bajos como el 7-19%, según el tipo de estrategia utilizada. Estos resultados suponen una reducción de los eventos mayores 2-3 veces en relación con las técnicas previas, e inician una nueva era en el tratamiento de las bifurcaciones mayores.
Lesiones de alto riesgo (tipo C)
De nuevo analizaremos los resultados del intervencionismo percutáneo de acuerdo con el tipo de lesión en este grupo.
Lesiones difusas (longitud > 20 mm)
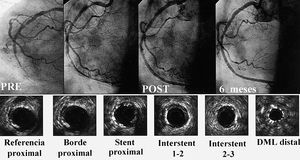
El tratamiento de este tipo de lesiones con angioplastia con balón también estaba prácticamente vetado. La experiencia inicial con stents también fue desalentadora debido a la alta incidencia de trombosis subaguda de la prótesis y al alto porcentaje de reestenosis51. La mejora en las técnicas de implantación, los nuevos regímenes antitrombóticos y los nuevos diseños de stents largos mejoraron la seguridad en el tratamiento de estas lesiones largas. Varias estrategias de implantación compitieron en la obtención de los mejores resultados: implantación de un stent único y largo, implantación de varios stents superpuestos o no y la técnica del spot stenting, sin que ninguna de ellas mostrara un claro beneficio en relación con las anteriores52-59. En las lesiones difusas (> 20 mm), con el stent convencional se obtuvo una probabilidad libre de eventos al año aproximadamente de un 80%. Sin embargo, en grupos de alto riesgo (diámetro del vaso < 3 mm) los resultados fueron peores, con una probalidad libre de eventos al año del 55%59. La probabilidad de reestenosis también fue muy variada según los diferentes autores y se comunicó60 hasta un 73% de reestenosis en pacientes con área del stent posimplante determinada por ultrasonidos < 5 mm2. La llegada de los stents recubiertos de fármacos supuso una gran mejoría en los resultados a medio plazo (fig. 2). Estudios recientes han comunicado una incidencia de eventos mayores a los 6-10 meses del 8-12%, con una tasa de reestenosis de este tipo de lesiones del 12-14%61,62. Estos resultados son de nuevo muy favorables respecto a las series históricas comentadas con anterioridad.
Fig. 2. Coronaria derecha ocluida y difusamente enferma reconstruida con múltiples stents de rapamicina. A los 6 meses la arteria se mantiene permeable y con una mínima proliferación neointimal en la ecocardiografía de seguimiento (abajo). DML: diámetro mínimo de la luz
Oclusión crónica de más de 3 meses
El abordaje de este tipo de lesiones conlleva 2 partes bien diferenciadas: la primera consiste en atravesar el segmento ocluido con una guía y la segunda en dilatar la oclusión y utilizar un dispositivo que consiga una buena luz de manera inmediata y la mantenga a largo plazo. En la primera parte del procedimiento es quizá donde menos se ha avanzado en estos 20 años. Sin embargo, una vez cruzada la lesión, los avances técnicos sí han mejorado los resultados, de forma similar a los de las lesiones descritas previamente. El perfil de los nuevos balones, las características de los stents montados y, por último, la llegada de los stents recubiertos de fármacos han sido las grandes mejoras en este subtipo de lesiones. Suero et al63 demostraron que el pronóstico de los pacientes con oclusión crónica y éxito en el procedimiento es mejor que el de los no recanalizados. Por ello, se han hecho esfuerzos para mejorar la tasa de cruce de una oclusión crónica y se han desarrollado guías especiales con una punta dura que pueda perforar el segmento obstruido. El éxito inicial en cruzar con las guías convencionales una oclusión antigua ha sido del 42-70%64, pero depende del tipo de oclusión, del tiempo de ésta y de la longitud del segmento obstruido. Aunque la industria ha diseñado guías específicas para cruzar oclusiones, no se ha conseguido un modelo ideal que sirva para resolver todos los casos. Quizá, el mayor avance en este campo sea la guía de radiofrecuencia Safe-Cross. Esta guía aplica radiofrecuencia en su extremo distal, consiguiendo así una mayor penetrabilidad, y está provista de un sistema de reflectometría que utiliza la energía lumínica para informar al operador de la ubicación de su extremo con el fin de evitar de alguna forma la perforación y el avance por caminos inadecuados a través de la pared arterial. El éxito de este nuevo dispositivo es de aproximadamente el 54% de los casos en los que se ha fallado con las guías convencionales65. Una vez cruzada la oclusión, el progreso ha sido más rápido desde la utilización de la angioplastia con balón. Las cifras de reestenosis se redujeron del 60-70% al 20-30% con la utilización del stent convencional66-69. Los stents recubiertos de fármacos han reducido aún más la cifra de recurrencia una vez cruzada la oclusión. La probabilidad de reestenosis con estos stents se ha reducido a un 9-13%70,71, con una necesidad de revascularización de la lesión tratada < 6%.
Segmento excesivamente angulado
La llegada de los stents montados, mucho más flexibles, y de las guías de alto soporte han permitido solventar este tipo de lesiones con un mayor éxito primario y menor riesgo, ya que si se producen disecciones distales se pueden sellar con nuevos stents.
Tortuosidad excesiva en el segmento proximal e imposibilidad de proteger los ramos mayores adyacentes
Estas 2 situaciones en su grado más extremo persisten hoy día sin una solución definitiva desde un punto de vista percutáneo. Si el operador no es capaz de llevar el stent al segmento lesionado o ya dilatado con balón corre el riesgo de no solucionar un compromiso severo del flujo en esta localización. Las arterias coronarias a veces presentan tortuosidades de más de 360o o ramos colaterales con curvas que prácticamente son imposibles de cruzar con los sistemas actuales. En estos casos, aunque infrecuentes, persiste la baja incidencia de éxito primario e incluso se mantiene la imposibilidad de acceder a la dilatación de la lesión por primera vez.
Injertos venosos degenerados con lesiones friables
Los injertos venosos degenerados presentan un doble inconveniente para el tratamiento percutáneo: el primero de ellos es la posibilidad de embolizar el material friable que compone la placa y producir una situación de infarto de miocardio, y la segunda es la alta tasa de recurrencia tardía, ya sea por reestenosis o por progresión en otra zona. Recientemente, Keeley et al72 comunicaron su experiencia en el tratamiento de 1.142 lesiones en injertos degenerados. Los autores tuvieron una incidencia de eventos mayores hospitalarios del 13%, incluidas 8 muertes, con unos eventos tardíos del 54% (9 muertes, 9 infartos sin onda Q y un 36% de nuevas revascularizaciones de la lesión tratada). A pesar de los numerosos avances tecnológicos y farmacológicos, la intervención percutánea sobre los injertos degenerados se asocia con una alta incidencia de complicaciones periprocedimiento y de eventos mayores durante el seguimiento. El uso de dispositivos de aspiración de trombos34,40 o filtros de protección distal73 puede proteger el lecho distal de los posibles fragmentos del trombo desprendido y disminuir el riesgo de infarto por embolia. Al mismo tiempo, los stents recubiertos de fármacos pueden reducir la probabilidad de reestenosis; sin embargo, la progresión de la enfermedad en segmentos no tratados hace difícil la solución de este tipo de lesiones por vía percutánea.
AMPLIACIÓN DE LAS INDICACIONES
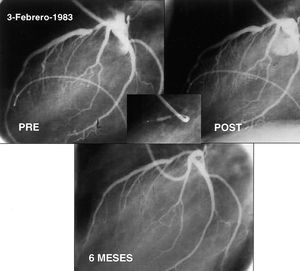
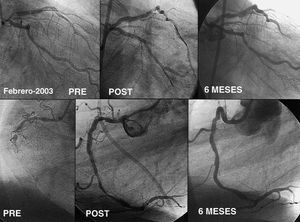
Las primeras indicaciones del intervencionismo percutáneo se limitaban a lesiones circunscritas en pacientes con enfermedad monovaso (fig. 3) y con una buena función ventricular. De esta forma se aseguraba una alta tasa de éxito en la lesión tratada y, al mismo tiempo, si se producían complicaciones, eran mejor toleradas que en pacientes con una función ventricular deprimida. Con los avances y mejoras anteriormente comentadas en todos los tipos de lesiones coronarias, esta indicación inicial se fue ampliando conforme los cardiólogos ganaban experiencia y los nuevos dispositivos resolvían los problemas mencionados con anterioridad. De esta forma, con el intervencionismo coronario se han ido abordando lesiones más complejas, pacientes de mayor riesgo y enfermedades coronarias más extensas (fig. 4). Aunque el armamento terapéutico actual es poderoso, todavía hay algunos tipos de lesiones y pacientes que no pueden ser tratados por vía percutánea. Se trata de aquellas situaciones en las que es imposible acceder a la lesión diana, ya sea por la presencia de una oclusión crónica o por una tortuosidad y calcificación severa que impida la llegada del stent al punto deseado. Salvo estas situaciones previamente comentadas, el intervencionismo coronario permite tratar con éxito a la gran mayoría de pacientes con enfermedad coronaria. La ampliación de las indicaciones pasa por los estudios comparativos con la cirugía de revascularización. Desde los comienzos se han efectuado muchos estudios alteatorizados que comparan la revascularización percutánea frente a la cirugía74. Sin embargo, el avance en el intervencionismo ha sido tan rápido que cuando los resultados a largo plazo de estos estudios estaban disponibles para ser publicados, las técnicas de intervencionismo utilizadas habían quedado obsoletas. Por tanto, en la actualidad siguen utilizándose las 2 modalidades de revascularización de forma complementaria sin que ninguna de las 2 haya demostrado un claro beneficio en términos de supervivencia frente a la otra. Sin embargo, al ser el método percutáneo más sencillo, menos invasivo y de aplicación inmediata tras el diagnóstico, muchos laboratorios han decidido abordar de manera habitual la enfermedad multivaso y las lesiones del tronco común de la coronaria izquierda.
Fig. 3. Angiografía de la primera angioplastia realizada en el Hospital Reina Sofía el 3 de febrero de 1983. Se trata de una lesión proximal fácilmente accesible en un segmento recto, concéntrica, de bordes lisos, que cumple todos los criterios para ser una lesión favorable para el intervencionismo. Se obtiene un aceptable resultado angiográfico que se mantiene en el seguimiento a los 6 meses.
Fig. 4. Ejemplo de otro paciente revasczado recientemente en nuestro hospital a los 20 años de la primera angioplastia. El paciente presenta una lesión severa del tronco común de la coronaria izquierda localizada en la bifurcación y severamente calcificada. Al mismo tiempo, la coronaria derecha presenta una oclusión de más de 3 meses de antigüedad. La bifurcación del tronco se resolvió mediante la implantación de un stent de rapamicina hacia la descendente anterior y angioplastia con balón del origen de la arteria circunfleja. La oclusión de la coronaria derecha se cruzó con una guía Safe-Cross de radiofrecuencia y el procedimiento se completó mediante la implantación de stents de rapamicina. A los 6 meses se obtiene un excelente resultado angiográfico de ambas lesiones tratadas. Veinte años atrás, este resultado obtenido durante el seguimiento resultaría impensable mediante técnicas de revascularización percutánea.
Aunque el tratamiento quirúrgico ha sido la opción preferida en la mayoría de los centros durante años para la enfermedad de tronco común75,76, la revascularización percutánea con stents se practica de forma paralela desde 1991. Originalmente, los pacientes fueron tratados en el laboratorio de hemodinámica como una necesidad por una complicación durante el procedimiento diagnóstico o en el curso de un infarto de miocardio. En pacientes críticamente enfermos, el soporte cardiopulmonar fue siempre de utilidad77. Más adelante, se empezó a tratar de forma percutánea a los pacientes rechazados para cirugía de bypass coronario78 a causa de enfermedades sistémicas concomitantes, malos lechos distales o mala función ventricular. Aunque el éxito primario inicial fue alto, las cifras de reestenosis eran una de las limitaciones del intervencionismo, ya que se había comunicado una incidencia próxima al 20%79-83. Los primeros estudios con stents de rapamicina en el tratamiento de la enfermedad de tronco han presentado resultados prometedores84, con una tasa de reestenosis del 3%. Con estos resultados quizá se pueda responder a la pregunta de si es hora de cambiar las guías de actuación, formulada recientemente en nuestra Revista85 de forma afirmativa.
PERSPECTIVAS FUTURAS
A pesar de la incorporación de todas estas mejoras técnicas surgidas en los últimos años, el progreso de la técnica no se detiene y cabe esperar que en un futuro próximo se aporten soluciones para los actuales problemas del intervencionismo. Es posible mejorar la navegabilidad y accesibilidad de los actuales stents, de manera que se aproxime a la del balón de última generación, y que se pueda acceder a las lesiones distales con múltiples tortuosidades proximales. La guía de radiofrecuencia Safe-Cross ha abierto un nuevo camino para la resolución de las oclusiones crónicas. Las nuevas generaciones de este dispositivo serán más flexibles, más navegables, capaces de tomar curvas sin perder penetración y, al mismo tiempo, conseguir una mayor seguridad.
En relación con los stents recubiertos de fármacos, ya se han iniciado estudios en los que se están investigando nuevos fármacos que puedan superar a los actualmente disponibles en términos de reestenosis y de resultados a largo plazo. Los stents reabsorbibles también están ya en fase avanzada y se podría pensar en una combinación de todas estas tecnologías. Los avances no sólo se producirán en la resolución de las lesiones coronarias, sino también en el campo de la función ventricular. Muchas veces, después de resolver las lesiones coronarias de un paciente puede persistir un grado de disfunción ventricular que limite de manera severa su capacidad funcional. La regeneración mioc& aacute;rdica con células madre inyectadas percutáneamente, ya sea por vía intracoronaria o por punción endomiocárdica, es otro gran capítulo abierto recientemente en el terreno de la cardiología intervencionista. Por tanto, es posible que en un futuro no muy lejano se consiga un aumento importante de la supervivencia de los pacientes con enfermedad coronaria y tengamos que enfrentarnos a otras formas de arteriosclerosis en otras localizaciones actualmente no resueltas con tanta eficacia.
Sección patrocinada por el Laboratorio Dr. Esteve
Correspondencia: Dr. M. Pan.
Grupo CORPAL. Hospital de la Cruz Roja.
P.o de la Victoria, s/n. 1. 14004 Córdoba. España.
Correo electrónico: grupo_corpal@arrakis.es.