En España, el 0,3% de los pacientes hipertensos son refractarios al tratamiento convencional. Las complicaciones derivadas de un control deficiente se traducen en mala calidad de vida para el paciente y un coste importante para el sistema sanitario. Barostim es un dispositivo implantable que busca reducir la presión arterial de estos pacientes. El objetivo del presente estudio es analizar el coste-efectividad de Barostim comparado con terapia farmacológica en pacientes hipertensos refractarios al tratamiento convencional (al menos tres fármacos antihipertensivos, siendo uno de ellos un diurético).
MétodosModelo de Markov adaptado a la epidemiología de la población española que simula la historia natural de una cohorte de pacientes con hipertensión arterial refractaria a lo largo de su vida. Los datos sobre efectividad de los tratamientos se obtuvieron de la literatura y los de costes, de bases de datos administrativas hospitalarias y de fuentes oficiales. Se realizaron análisis de sensibilidad determinístico y probabilístico.
ResultadosBarostim redujo los eventos clínicos asociados a la hipertensión y aumentó en 0,78 el número de años de vida ajustados por calidad. El cociente de coste-efectividad incremental para una cohorte de varones alcanzó los 68.726 euros por año de vida ajustado por calidad. Uno de los principales elementos que encarece la tecnología es el coste del recambio de la batería. Los resultados fueron robustos.
ConclusionesBarostim no es una estrategia coste-efectiva para el tratamiento de la hipertensión refractaria en España. Reducciones futuras en el precio de la batería mejorarían su cociente de coste-efectividad.
Palabras clave
Abreviaturas
La innovación en el sector salud es clave para el progreso científico, asistencial y empresarial. No obstante, las nuevas tecnologías médicas deberían suponer un alto valor añadido respecto a la práctica clínica habitual. Es por ello que la Sociedad Española de Cardiología (SEC) ha impulsado InnovaSEC como iniciativa estratégica para analizar el valor de nuevas tecnologías que quieren ser introducidas en el contexto sanitario español1. La primera nueva tecnología evaluada bajo el paraguas de InnovaSEC es el producto sanitario Barostim.
Barostim (CVRx Inc., Minneapolis, Minnesota, Estados Unidos) es un producto sanitario implantable que reduce la presión sanguínea mediante estimulación eléctrica de los barorreceptores carotídeos. Está indicado como tratamiento de segunda línea para pacientes hipertensos con resistencia al tratamiento médico convencional (definida como presión arterial sistólica [PAS] ≥ 140mmHg pese a al menos tres tratamientos farmacológicos antihipertensivos, entre ellos un diurético). La hipertensión refractaria al tratamiento afecta en España al 0,3% de los pacientes con hipertensión arterial2. Considerando que la prevalencia de hipertensión arterial entre la población mayor de 30 años en España está alrededor del 30%3, habría aproximadamente 29.000 pacientes con hipertensión arterial refractaria al tratamiento farmacológico en España.
Se considera la estimulación de los barorreceptores carotídeos como una posible opción terapéutica para la hipertensión arterial refractaria al tratamiento farmacológico en las guías de la Sociedad Europea de Hipertensión y de la Sociedad Europea de Cardiología4. A su vez, la indicación de Barostim para pacientes hipertensos refractarios al tratamiento convencional se ha mostrado coste-efectiva para la población alemana (razón de coste-efectividad, 7.797 euros/año de vida ajustado por calidad [AVAC])5. No obstante, el perfil epidemiológico de la población española y los costes del tratamiento de la hipertensión y sus complicaciones difieren de los registrados en los países del norte de Europa. Ambas variables pueden impactar considerablemente en el coste-efectividad de esta tecnología en España.
El objetivo de este estudio es analizar el coste-efectividad de Barostim como tratamiento de segunda línea para pacientes hipertensos (PAS ≥ 140mmHg) adultos, comparado con el tratamiento de estos pacientes con una pauta farmacológica adecuada (al menos tres fármacos antihipertensivos, entre ellos un diurético) en la población española, desde la perspectiva del Sistema Nacional de Salud.
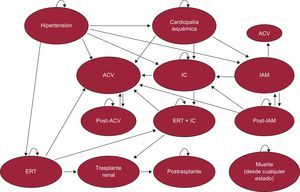
MÉTODOSDiseñoSe llevó a cabo un análisis de coste-efectividad utilizando un modelo de Markov6. En el modelo, los pacientes comienzan en un estado hipertensivo refractario a terapia farmacológica y con el tiempo pueden progresar hacia diversos estados de salud (figura 1). El tiempo se representa como ciclos fijos de 1 mes de duración hasta el final de la vida del paciente. La probabilidad de transición hacia un nuevo estado depende de las características iniciales y posteriores de los pacientes, su estado de salud y el tratamiento recibido. Cada estado de salud tiene asociados distintos niveles de calidad de vida y costes. El modelo se basó en un estudio ya realizado en población alemana5, que se adaptó al entorno español tanto en sus características epidemiológicas como sus costes sanitarios.
Los estados de salud considerados en el modelo son: hipertensión arterial, cardiopatía isquémica, insuficiencia cardiaca, infarto agudo de miocardio (IAM), accidente cerebrovascular (ACV), enfermedad renal terminal o muerte. Los IAM y ACV se representaron como estados de un ciclo de duración. En el ciclo inmediatamente posterior a un IAM o ACV, los pacientes pueden transitar hacia uno de los estados descritos anteriormente (incluida la muerte) o pueden progresar hacia un estado post-IAM o post-ACV. Los pacientes que se encuentran en un estado post-IAM pueden tener ACV, insuficiencia cardiaca o IAM recurrente o morir. Los pacientes en post-ACV solo pueden presentar un ACV recurrente o morir. Finalmente, aquellos en enfermedad renal terminal pueden recibir un trasplante de riñón y, si sobreviven, transitan hacia un estado postrasplante.
El análisis compara la terapia farmacológica frente al implante de Barostim más terapia farmacológica. Se supuso que los pacientes reciben una combinación de diuréticos, bloqueadores beta, antagonistas del calcio, inhibidores de la enzima de conversión de la angiotensina y antagonistas del receptor de la angiotensina II. Esta combinación sigue las recomendaciones de la Sociedad Europea de Hipertensión y la Sociedad Europea de Cardiología4. Se supuso que el tratamiento farmacológico se interrumpe en caso de que ocurra alguno de los eventos adversos del modelo.
Como medidas de efectividad clínica se estimó la frecuencia de eventos adversos a lo largo de la vida de los individuos, años de vida sin ajustar por calidad y AVAC7. En cuanto a los costes, se consideraron los costes directos sanitarios y los costes indirectos. Finalmente, se evaluó la razón de coste-efectividad incremental (RCEI)8.
El caso base del modelo supone un paciente varón con edad inicial de 55 años, PAS de 170mmHg, colesterol total de 190mg/dl, colesterol unido a lipoproteínas de alta densidad de 35 mg/dl y ritmo cardiaco de 79 lpm, no fumador, diabético, sin antecedentes de cardiopatía isquémica y sin hipertrofia ventricular izquierda (tabla 1 del material suplementario). La tasa de descuento utilizada fue del 3% anual9. El modelo también se estimó para una cohorte femenina con los mismos valores basales que la masculina. Las estimaciones se llevaron a cabo con el programa Stata 13.1 (StataCorp; College Station, Texas, Estados Unidos).
Probabilidades de transición entre estados de saludSe utilizaron las ecuaciones de Framingham adaptadas a la población española para estimar el riesgo de cardiopatía isquémica e IAM (REGICOR [Registre Gironí del Cor]10) y el riesgo de ACV (FRESCO11). Para la estimación del riesgo de insuficiencia cardiaca, se utilizó la ecuación original del proyecto de Framingham12, ya que se no se encontraron ecuaciones adaptadas a la población española. La probabilidad de ocurrencia de cada uno de estos eventos se reestimó en cada ciclo, lo que permitió tomar en cuenta el aumento del riesgo asociado al envejecimiento. La estimación de riesgo de enfermedad renal terminal se obtuvo del estudio de Hsu et al13.
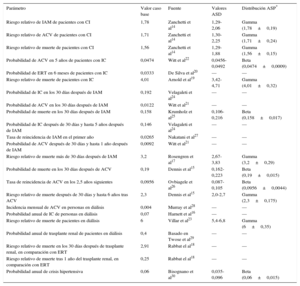
Se presumió que las probabilidades de ocurrencia de un nuevo evento en pacientes que ya han presentado alguno de los eventos del modelo son independientes del nivel de presión arterial y se calcularon a partir de riesgos relativos o probabilidades publicados14–28 (tabla 1). Por otro lado, se supuso que un 40% de los pacientes en diálisis reciben un trasplante renal anualmente29. Otro supuesto fue que los pacientes pueden experimentar una crisis hipertensiva sin que pasen a otro estado30.
Datos clínicos y probabilidades de transición
| Parámetro | Valor caso base | Fuente | Valores ASD | Distribución ASP* |
|---|---|---|---|---|
| Riesgo relativo de IAM de pacientes con CI | 1,78 | Zanchetti et al14 | 1,29-2,06 | Gamma (1,78±0,19) |
| Riesgo relativo de ACV de pacientes con CI | 1,71 | Zanchetti et al14 | 1,30-2,25 | Gamma (1,71±0,24) |
| Riesgo relativo de muerte de pacientes con CI | 1,56 | Zanchetti et al14 | 1,29-1,88 | Gamma (1,56±0,15) |
| Probabilidad de ACV en 5 años de pacientes con IC | 0,0474 | Witt et al22 | 0,0456-0,0492 | Beta (0,0474±0,0009) |
| Probabilidad de ERT en 6 meses de pacientes con IC | 0,0333 | De Silva et al20 | — | — |
| Riesgo relativo de muerte de pacientes con IC | 4,01 | Arnold et al19 | 3,42-4,71 | Gamma (4,01±0,32) |
| Probabilidad de IC en los 30 días después de IAM | 0,192 | Velagaleti et al24 | — | — |
| Probabilidad de ACV en los 30 días después de IAM | 0,0122 | Witt et al21 | — | — |
| Probabilidad de muerte en los 30 días después de IAM | 0,158 | Krumholz et al25 | 0,106-0,216 | Beta (0,158±0,017) |
| Probabilidad de IC después de 30 días y hasta 5 años después de IAM | 0,146 | Velagaleti et al24 | — | — |
| Tasa de reincidencia de IAM en el primer año | 0,0265 | Nakatani et al27 | — | — |
| Probabilidad de ACV después de 30 días y hasta 1 año después de IAM | 0,0092 | Witt et al21 | — | — |
| Riesgo relativo de muerte más de 30 días después de IAM | 3,2 | Rosengren et al17 | 2,67-3,83 | Gamma (3,2±0,29) |
| Probabilidad de muerte en los 30 días después de ACV | 0,19 | Dennis et al15 | 0,162-0,223 | Beta (0,19±0,015) |
| Tasa de reincidencia de ACV en los 2,5 años siguientes | 0,0956 | Ovbiagele et al26 | 0,087-0,105 | Beta (0,0956±0,0044) |
| Riesgo relativo de muerte después de 30 días y hasta 6 años tras ACV | 2,3 | Dennis et al15 | 2,0-2,7 | Gamma (2,3±0,175) |
| Incidencia mensual de ACV en personas en diálisis | 0,004 | Murray et al28 | — | — |
| Probabilidad anual de IC de personas en diálisis | 0,07 | Harnett et al16 | — | — |
| Riesgo relativo de muerte de pacientes en diálisis | 6 | Villar et al23 | 5,4-6,8 | Gamma (6±0,35) |
| Probabilidad anual de trasplante renal de pacientes en diálisis | 0,4 | Basado en Twose et al29 | — | — |
| Riesgo relativo de muerte en los 30 días después de trasplante renal, en comparación con ERT | 2,91 | Rabbat el al18 | — | — |
| Riesgo relativo de muerte tras 1 año del trasplante renal, en comparación con ERT | 0,25 | Rabbat el al18 | — | — |
| Probabilidad anual de crisis hipertensiva | 0,06 | Bisognano et al30 | 0,035-0,096 | Beta (0,06±0,015) |
ACV: accidente cerebrovascular; ASD: análisis de sensibilidad determinístico; ASP: análisis de sensibilidad probabilístico; CI: cardiopatía isquémica; ERT: enfermedad renal terminal; IAM: infarto agudo de miocardio; IC: insuficiencia cardiaca.
El riesgo de muerte según edad de los pacientes que no presentan ningún evento se obtuvo de las tablas de mortalidad del Instituto Nacional de Estadística31. Dicho riesgo se calculó como la diferencia entre la mortalidad por todas las causas y la mortalidad por las causas consideradas en el modelo.
UtilidadesLos niveles de utilidad asociados a cada estado de salud provienen de la literatura5,32–36 (tabla 2). La utilidad en el estado hipertensivo se obtuvo de Stein et al37.
Utilidades según estados de salud
| Estado | Valor | Fuente | Distribución ASP |
|---|---|---|---|
| Hipertensión | 0,98 | Stein et al37 | Uniforme (0,97-0,98) |
| CIa | 0,75 | Longworth et al32 | Uniforme (0,68-0,82) |
| IC | 0,60 | Calvert et al33 | Utilidad CI –0,15 |
| IAM | 0,54 | Lacey et al34 | Utilidad CI –0,21 |
| Post-IAMb | 0,69 | Lacey et al34 | Utilidad CI –0,06 |
| ACV | 0,31 | Pickard et al35 | Utilidad CI –0,44 |
| Post-ACV | 0,61 | Pickard et al35 | Utilidad CI –0,14 |
| ERT | 0,44 | Parra Moncasi et al39 | Utilidad CI –0,31 |
| ERT+IC | 0,40 | Supuesto basado en Parra Moncasi et al39 | Utilidad CI –0,35 |
| Trasplante renal | 0,13 | Supuesto basado en Borisenko et al5 | Utilidad CI –0,62 |
| Postrasplante renal | 0,71 | Parra Moncasi et al39 | Utilidad CI –0,04 |
| Muerte | 0,00 | Supuesto | — |
ACV: accidente cerebrovascular; ASP: análisis de sensibilidad probabilístico; CI: cardiopatía isquémica; ERT: enfermedad renal terminal; IAM: infarto agudo de miocardio; IC: insuficiencia cardiaca.
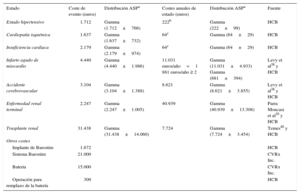
Los costes directos sanitarios provienen del Hospital Clínic de Barcelona y se calcularon como el coste promedio de los episodios ocurridos durante el año 2012 (tabla 3). Los costes para post-IAM, post-ACV y enfermedad renal terminal provienen de la literatura médica38–40, actualizados a precios de 2012.
Costes directos sanitarios
| Estado | Coste de evento (euros) | Distribución ASPa | Costes anuales de estado (euros) | Distribución ASPa | Fuente |
|---|---|---|---|---|---|
| Estado hipertensivo | 1.712 | Gamma (1.712±766) | 222b | Gamma (222±99) | HCB |
| Cardiopatía isquémica | 1.637 | Gamma (1.637±732) | 64c | Gamma (64±29) | HCB |
| Insuficiencia cardiaca | 2.179 | Gamma (2.179±974) | 64c | Gamma (64±29) | HCB |
| Infarto agudo de miocardio | 4.440 | Gamma (4.440±1.986) | 11.031 euros/año=1 881 euros/año ≥ 2 | Gamma (11.031±4.933) Gamma (881±394) | Levy et al38 y HCB |
| Accidente cerebrovascular | 3.104 | Gamma (3.104±1.388) | 8.621 | Gamma (8.621±3.855) | Levy et al38 y HCB |
| Enfermedad renal terminal | 2.247 | Gamma (2.247±1.005) | 40.939 | Gamma (40.939±13.308) | Parra Moncasi et al39 y HCB |
| Trasplante renal | 31.438 | Gamma (31.438±14.060) | 7.724 | Gamma (7.724±3.454) | Temes40 y HCB |
| Otros costes | |||||
| Implante de Barostim | 1.672 | HCB | |||
| Sistema Barostim | 21.000 | CVRx Inc. | |||
| Batería | 15.000 | CVRx Inc. | |||
| Operación para remplazo de la batería | 309 | HCB | |||
ASP: análisis de sensibilidad probabilístico; HCB: Hospital Clínic de Barcelona.
Se supuso que el implante de Barostim y el remplazo de la batería tienen el mismo coste que el asociado a la cirugía de marcapasos. El fabricante proporcionó los costes del dispositivo Barostim. Los costes del tratamiento farmacológico provienen del Vademécum41.
Costes indirectosSe computó el porcentaje de reducción en productividad causada por la discapacidad laboral o muerte como igual a 1 menos nivel de utilidad (tabla 2 del material suplementario). La productividad de una persona con plena capacidad se supuso igual al coste medio bruto de un trabajador en España en el año 2012 (30.905 euros/año)42. Por otro lado, se asumió que los mayores de 65 años no trabajan, y se les imputó una productividad de cero.
Efectividad de BarostimLa reducción de la PAS por Barostim se basó en datos publicados30,43. Se supuso que la reducción de la PAS observada en el estudio de Bakris et al43 se mantiene constante durante toda la vida del paciente (tabla 4). En las tablas 3A-D del material suplementario se describe la estrategia de búsqueda bibliográfica sobre efectividad de Barostim.
Efectividad de Barostim (reducción de la presión arterial sistólica)
| Parámetro | Caso base (mmHg) | Fuente | Valores ASD | Distribución ASP* |
|---|---|---|---|---|
| Reducción el primer mes después del implante | 0 | Supuesto basado en Bisognano et al30 | — | — |
| Reducción 2-12 meses después del implante | 26 | Bisognano et al30 | 22-30 | Gamma (26±2,2) |
| Reducción 13-24 meses después del implante | 35 | Bisognano et al30 | 31-39 | Gamma (35±2,3) |
| Reducción a partir del mes 25 después del implante | 35 | Bakris et al43 | 31-39 | Gamma (35±2,3) |
ASD: análisis de sensibilidad determinístico; ASP: análisis de sensibilidad probabilístico.
Con el fin de explorar los parámetros que tienen mayor impacto en la RCEI, se realizó un análisis de sensibilidad determinístico. Se sustituyó los valores basales de los parámetros clínicos por valores extremos, con base en los datos de la bibliografía y la experiencia clínica (tabla 1 y tabla 4).
Se llevó a cabo un análisis de sensibilidad probabilístico mediante métodos de Monte Carlo. Se efectuaron 10.000 simulaciones de AVAC y costes, cada una de las cuales se ejecutó a partir de valores aleatorios de los parámetros del modelo según lo descrito en las tabla 1, tabla 2, tabla 3 y tabla 4.
Impacto presupuestarioSe llevó a cabo un análisis de impacto presupuestario asociado a la introducción de Barostim en el Sistema Nacional de Salud. Los supuestos y principales resultados se detallan en las tablas 4–6 del material suplementario.
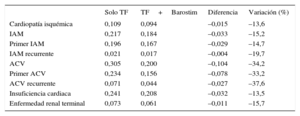
RESULTADOSBarostim redujo la probabilidad de todos los eventos adversos considerados (tabla 5). La probabilidad de tener un primer ACV disminuyó en 0,078 puntos, lo que representa una caída del 33,2% en el número de casos respecto a la terapia farmacológica óptima. Los ACV recurrentes bajaron el 37,6%. La probabilidad de un primer IAM disminuyó en 0,029 puntos, lo que implica una reducción de casos del 14,7%. Los IAM recurrentes disminuyeron el 19,7%. Los casos de cardiopatía isquémica y de insuficiencia cardiaca cayeron aproximadamente un 13,5%. Finalmente, los casos de enfermedad renal terminal bajaron un 15,7%.
Frecuencia de eventos clínicos por individuo en caso base
| Solo TF | TF+Barostim | Diferencia | Variación (%) | |
|---|---|---|---|---|
| Cardiopatía isquémica | 0,109 | 0,094 | –0,015 | –13,6 |
| IAM | 0,217 | 0,184 | –0,033 | –15,2 |
| Primer IAM | 0,196 | 0,167 | –0,029 | –14,7 |
| IAM recurrente | 0,021 | 0,017 | –0,004 | –19,7 |
| ACV | 0,305 | 0,200 | –0,104 | –34,2 |
| Primer ACV | 0,234 | 0,156 | –0,078 | –33,2 |
| ACV recurrente | 0,071 | 0,044 | –0,027 | –37,6 |
| Insuficiencia cardiaca | 0,241 | 0,208 | –0,032 | –13,5 |
| Enfermedad renal terminal | 0,073 | 0,061 | –0,011 | –15,7 |
ACV: accidente cerebrovascular; IAM: infarto agudo de miocardio; TF: terapia farmacológica.
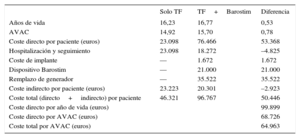
Los pacientes tratados solo con terapia farmacológica obtuvieron 14,92 AVAC. Los pacientes tratados con Barostim alcanzaron 15,7 AVAC, es decir, un incremento de 0,78 AVAC por paciente (tabla 6).
Efectividad, costes por paciente y razón de coste-efectividad (caso base)
| Solo TF | TF+Barostim | Diferencia | |
|---|---|---|---|
| Años de vida | 16,23 | 16,77 | 0,53 |
| AVAC | 14,92 | 15,70 | 0,78 |
| Coste directo por paciente (euros) | 23.098 | 76.466 | 53.368 |
| Hospitalización y seguimiento | 23.098 | 18.272 | –4.825 |
| Coste de implante | — | 1.672 | 1.672 |
| Dispositivo Barostim | — | 21.000 | 21.000 |
| Remplazo de generador | — | 35.522 | 35.522 |
| Coste indirecto por paciente (euros) | 23.223 | 20.301 | –2.923 |
| Coste total (directo+indirecto) por paciente | 46.321 | 96.767 | 50.446 |
| Coste directo por año de vida (euros) | 99.899 | ||
| Coste directo por AVAC (euros) | 68.726 | ||
| Coste total por AVAC (euros) | 64.963 |
AVAC: año de vida ajustado por calidad; TF: terapia farmacológica.
El coste directo promedio por paciente en terapia farmacológica fue 23.098 euros, mientras que para pacientes con Barostim el coste fue 76.466 euros. Los costes indirectos fueron 23.223 y 20.301 euros respectivamente. Considerando ambos costes (directos más indirectos), el coste incremental de Barostim en comparación con el tratamiento farmacológico ascendió a 50.446 euros por paciente.
La RCEI de Barostim respecto al tratamiento farmacológico sin considerar costes indirectos fue de 68.726 euros por AVAC. Considerando los costes indirectos, la RCEI de Barostim frente a terapia farmacológica fue 64.963 euros por AVAC. El componente que más peso tuvo en el coste incremental es el coste asociado al remplazo de la batería de Barostim.
Cuando el modelo se aplica a una cohorte femenina, el implante de Barostim resultó en un incremento de 0,54 AVAC. El coste directo incremental fue 60.242 euros y la RCEI se elevó a 111.337 euros por AVAC. Considerando costes indirectos, la RCEI se estimó en 107.241 euros por AVAC.
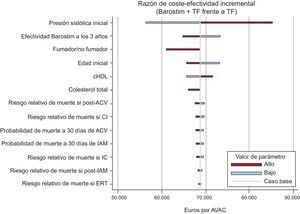
Análisis de sensibilidadEn el análisis de sensibilidad determinístico, las variables que tuvieron mayor incidencia en la RCEI fueron la PAS inicial, la efectividad de Barostim a partir de los 3 años del implante, la condición de fumador y la edad inicial del paciente. El análisis de sensibilidad determinístico muestra que ningún parámetro modifica sustancialmente la RCEI (figura 2).
Resultados del análisis de sensibilidad determinístico. ACV: accidente cerebrovascular; AVAC: año de vida ajustado por calidad; CI: cardiopatía isquémica; ERT: enfermedad renal terminal; cHDL: colesterol unido a lipoproteínas de alta densidad; IAM: infarto agudo de miocardio; IC: insuficiencia cardiaca; TF: tratamiento farmacológico.
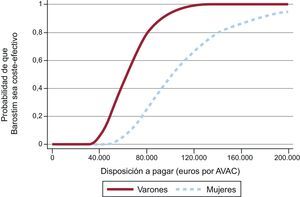
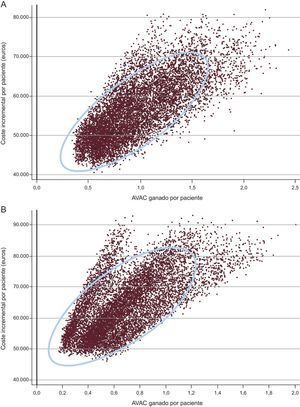
El análisis de sensibilidad probabilístico muestra que la probabilidad de que Barostim sea coste-efectivo al umbral de 30.000 euros por AVAC es cercana al 0% (figura 3). Con una disposición a pagar de 100.000 euros/AVAC, esta probabilidad asciende al 80% para varones y el 25% para mujeres. El plano de coste-efectividad (figura 4) muestra que en todos los casos Barostim produjo un aumento en el número de AVAC y tuvo un coste incremental de al menos 40.000 euros por paciente.
Este estudio es la primera evaluación económica de Barostim adaptada al contexto sanitario y social de España. Sus resultados indican que Barostim contribuye a la reducción de eventos cardiovasculares en la población de estudio. Así, el número de IAM, ACV y enfermedades renales terminales presentados por la cohorte de estudio caerían el 15,2, el 34,2 y el 15,7% respectivamente. El número de AVAC aumentaría en 0,78 respecto al tratamiento farmacológico. Sin embargo, este impacto positivo tiene asociado un importe económico considerable, con un coste directo incremental de 53.000 euros por paciente implantado. Por ello, la RCEI de Barostim respecto al tratamiento farmacológico es cercana a los 69.000 euros por AVAC sin considerar costes indirectos o aproximadamente 65.000 euros por AVAC incluyendo costes indirectos. En España, el umbral informal de coste-efectividad se estima en 30.000 euros por AVAC44. Por lo tanto, en el contexto sanitario español, el coste de Barostim es elevado respecto al beneficio en salud que produce. La RCEI también es muy superior a la del único artículo publicado, que analiza el coste-efectividad de Barostim en el sistema sanitario alemán5. La diferencia se debe en parte a que los costes sanitarios y los costes indirectos en España son menores que en Alemania, por lo que Barostim permite una reducción de estos costes menor que en el caso alemán.
La elevada RCEI hallada en el presente estudio también se debe a que Barostim se asocia a un aumento relativamente pequeño del número de AVAC. Si bien es cierto que la reducción de eventos cardiacos adversos es considerable si se mide en términos porcentuales, esta reducción es relativamente moderada si se mide en términos absolutos. En efecto, estas estimaciones indican que, por cada 100 pacientes a quienes se implanta Barostim, se evitarían 3,3 IAM, 10,4 ACV y 1,1 casos de enfermedad renal terminal. Estas cifras son sustancialmente menores que las indicadas por Borisenko et al5, quienes estiman reducciones de 5,1 IAM, 12 ACV y 2,3 enfermedades renales terminales por cada 100 pacientes implantados. La razón fundamental que explica estas diferencias es la menor incidencia de enfermedades cardiacas y cerebrovasculares en la población hipertensa en España respecto a lo observado en países del norte de Europa. Por ejemplo, según el estudio REGICOR10, un individuo con las características utilizadas en el presente estudio tiene una probabilidad a 10 años del 7,6% de presentar una enfermedad coronaria (cardiopatía isquémica o IAM). El estudio de Borisenko et al, que utiliza las ecuaciones de Framingham45, estima una probabilidad de entre un 20 y un 25%. De modo similar, según el estudio FRESCO11, el riesgo de ACV (como primer evento) en un horizonte de 10 años para la cohorte base es del 4,4%, mientras que según las ecuaciones de Framingham para ACV46 dicho riesgo es del 11%.
Un aspecto que impacta sustancialmente en el coste de Barostim es el remplazo de la batería a lo largo de la vida del paciente. Según las estimaciones del presente estudio, este coste representa casi el 50% del coste directo total. El precio actual de la batería y que se deba remplazarla cada 6 años explican este resultado. Si se ignorara este coste, la RCEI caería a 22.982 euros por AVAC. Así, reducciones futuras en el precio de la batería o mejoras en la duración de su vida útil disminuirían la RCEI.
Una de las principales limitaciones de este estudio es la falta de información robusta sobre la efectividad de Barostim en periodos superiores a los 3 años. La efectividad a largo plazo (es decir, hasta el final de la vida del paciente) que se ha incluido en el análisis se basa en datos publicados que muestran un descenso de 35 mmHg al cabo de un seguimiento medio de 2,3 años43.
En segundo lugar, no se han considerado los costes relacionados con los posibles efectos adversos asociados a Barostim. Los efectos adversos identificados se relacionan con el implante e incluyen daño permanente de nervio (4,8%), daño transitorio (4,4%) u otras complicaciones quirúrgicas (4,8%)30. Si se hubiera incorporado estos eventos al modelo, la RCEI de Barostim habría sido mayor.
Por último, en ausencia de estudios sobre riesgo de insuficiencia cardiaca en la población española, se ha cuantificado dicho riesgo siguiendo las ecuaciones de Framingham originales12, por lo que es posible que este modelo tenga una predicción exagerada del número de casos y los eventos adversos que se deriva de ellas.
CONCLUSIONESAunque a corto plazo Barostim es efectivo en la reducción de PAS y la evolución a estados de salud no deseados, a los precios actuales y considerando una disposición a pagar de 30.000 euros por AVAC, no es una opción coste-efectiva para el tratamiento de la población hipertensa refractaria al tratamiento farmacológico en el sistema sanitario español.
FINANCIACIÓNEste estudio ha recibido financiación parcial de la SEC. M. Soto recibió financiación del proyecto Plataforma de Innovación en Tecnologías Médicas y Sanitarias, PT13/0006/0009 (Fundació Clínic per a la Recerca Biomèdica, PI043029).
CONFLICTO DE INTERESESJ. Brugada es asesor del Comité Científico de CVRx.
Agradecemos a Krzysztof Lach y Gemma Seda por la ayuda prestada en la Fundació Clínic per a la Recerca Biomédica.