Palabras clave
INTRODUCCIÓN
Los tumores cardíacos primarios son una rara entidad, con una incidencia del 0,001-0,028% en series post mortem1. Los síntomas que producen son muy inespecíficos; los hallazgos en el electrocardiograma, inconstantes, y la exploración y radiografía de tórax, habitualmente anodinas. Por ello, las técnicas de imagen tienen un papel relevante en la detección y el diagnóstico diferencial de las masas cardíacas.
CASO CLÍNICO
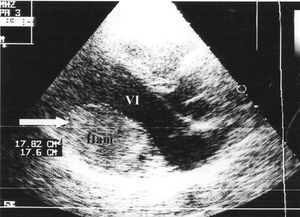
Varón de 33 años, deportista habitual, que consultó por palpitaciones y disnea de esfuerzo de 3 meses de evolución. La exploración física y la radiografía de tórax fueron normales. Se hallaron ondas T negativas profundas en II, III, aVF, V5 y V6, ya presentes en el electrocardiograma (ECG) practicado 8 años antes. Entonces fue estudiado por dolor precordial y se descartó una causa arrítmica mediante Holter-ECG, pero no se realizó ecocardiografía. En la ecocardiografía transtorácica (ETT) (fig. 1) apareció una masa intramiocárdica homogénea de 45 x 55 mm en la pared posterolateral del ventrículo izquierdo, de ecodensidad similar al miocardio. Protruía en el interior de la cavidad sin comprometer la función sistólica del ventrículo izquierdo.
Fig. 1. Ecocardiografía transtorácica, plano paraesternal en el eje largo, que muestra una masa intramiocárdica homogénea (Ham, señalada con flecha) en la pared posterior del ventrículo izquierdo (VI), que protruye en el interior de la cavidad.
La bioquímica, el hemograma y el estudio de coagulación fueron normales, y los marcadores tumorales negativos. El Holter-ECG registró una extrasistolia ventricular y auricular aislada, sin taquiarritmias.
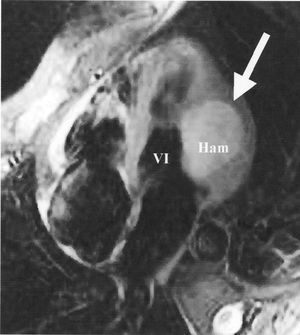
La resonancia magnética (fig. 2) confirmó la presencia de masa intramural, sin que se evidenciara infiltración miocárdica y pericárdica. La masa aparecía hiperintensa en la secuencia STIR, ligeramente hiperintensa en T1 e iso o mínimamente hipointensa en T2. Mostraba realce precoz heterogéneo tras la inyección de gadolinio.
Fig. 2. Resonancia magnética en secuencia STIR en la que se observa una imagen hiperintensa (Ham, señalada con flecha) en la pared lateral del ventrículo izquierdo (VI).
En la ventriculografía se observó un defecto de repleción en cara diafragmática, y la coronariografía mostró irrigación de la masa por obtusa marginal y la arteria coronaria derecha. No se detectaron adenopatías ni otras masas en la tomografía computarizada (TC) toracoabdominal.
Con la sospecha de tumor cardíaco benigno que provocaba obstrucción del llenado de ventrículo izquierdo indicamos cirugía. Mediante ventriculotomía izquierda, se realizó la resección parcial de la masa posterolateral del ventrículo izquierdo y la posterior implantación del músculo papilar posteromedial.
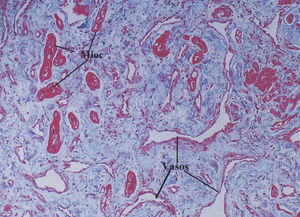
El exámen anatomopatológico (fig. 3) reveló elementos histológicos normalmente presentes en el tejido cardíaco con distribución irregular: fibras musculares hipertrofiadas, distribuidas de manera desordenada, con miocitos con núcleos grandes, rodeadas de tejidos adiposo y fibroso. El diagnóstico fue de hamartoma de células miocárdicas maduras.
Fig. 3. Corte anatomopatológico en el que se observan miocitos hipertrofiados (Mioc) y dispuestos desordenadamente, abundante tejido conectivo fibroso y vasos sanguíneos malformados (Vasos).
Tras la operación, en el Holter se detectó extrasistolia ventricular de muy escasa cantidad. La ergometría resultó negativa y alcanzó 11 METS. El paciente ha seguido un programa de rehabilitación cardíaca y se encuentra asintomático y sin eventos a los 3 años de la intervención.
DISCUSIÓN
La ecocardiografía es la técnica de elección en la aproximación inicial al estudio de masas cardíacas por su disponibilidad, bajo coste e inocuidad. Permite detectar, localizar y definir la forma, extensión, movilidad y punto de anclaje, así como distinguir la naturaleza sólida o quística.
La RM aporta información estructural y hemodinámica, pues ofrece secuencias estáticas y dinámicas y permite planos y proyecciones ilimitados. La caracterización tisular, mediante imágenes potenciadas en T1 y T2, complementa esta información. La intensidad levemente alta en T1 se observa en tejidos con contenido fibroso o muscular, nunca en presencia de grasa2, y la hipointensidad en T2 descarta que la masa contenga líquido. Estas características tisulares y la ausencia de infiltración nos hicieron considerar el fibroma como primera posibilidad. El realce tras la administración de gadolinio indica una buena vascularización, lo que va en contra del diagnóstico de fibroma, con bajos requerimientos metabólicos2, y sugiere un hemangioma o tumor maligno. Practicamos una coronariografía para definir el aporte vascular, con vistas a planificar la técnica quirúrgica. La angiografía también aporta datos sobre la presencia de arteriopatía coronaria obstructiva, malformaciones vasculares, presentes en raros casos de hematoma disecante intramiocárdico3,4 o ratifica el diagnóstico de hemangioma5.
El hamartoma es un sobrecrecimiento benigno de células diferenciadas maduras que son nativas del órgano en que se desarrolla, pero que se disponen de manera desorganizada. Resultan de una anomalía del desarrollo de células embrionarias.
La miocardiopatía hipertrófica focal y el rabdomioma están constituidos también por miocitos hipertrofiados, pero con características histológicas y patogénicas diferenciadas. Los antecedentes familiares y la preferencia por la región septal orientan hacia la miocardiopatía hipertrófica focal, mientras que la presentación en la infancia y la asociación con esclerosis tuberosa orientan hacia el rabdomioma. El diagnóstico definitivo es anatomopatológico.
Las primeras descripciones como hamartoma de células cardíacas maduras datan de 19986,7. Su localización intracardíaca se ha comunicado en series reducidas6-13. La característica esencial es la presencia de miocitos hipertrofiados, dispuestos desordenadamente, entremezclados con tejido vascular, fibroso y graso en distintas proporciones. Esta presentación histológica variada ha conducido a cierta confusión en la nomenclatura. Pueden ser únicos o, más raras veces, múltiples. Se desarrollan preferentemente en la pared ventricular, pero se ha comunicado su localización valvular9.
Una de las formas de presentación más frecuente es la taquicardia ventricular en niños y jóvenes10-13; se ha comunicado el caso de una niña de 2 años en esta Revista13. El tratamiento ha sido quirúrgico, con buenos resultados a corto plazo en todos los casos. Nuestro paciente refería palpitaciones y detectamos extrasistolia ventricular, aunque no objetivamos taquicardia ventricular.
La presentación en el adulto joven y el crecimiento lento sugieren el posible origen congénito, con posterior hipertrofia y desarrollo en los primeros años de la vida. La presencia de anomalías eléctricas hacía 8 años apoyaba esta posibilidad, ya apuntada por otros autores, que describen tumores cardíacos fibrosos primarios, no asociados a trastornos hereditarios complejos, en la infancia, adolescencia y madurez temprana2.
Correspondencia: Dra. M. Martínez Quesada.
Antonio Buero Vallejo, 1, 1.o 8. 41009 Sevilla. España.
Correo electrónico: marquesada@gmail.com