El diagnóstico y manejo terapéutico de pacientes con cardiopatías congénitas se basa en gran medida en los resultados de la ecocardiografía. Las diferentes técnicas de fusión de imagen han supuesto un reciente avance en la obtención de imágenes cardíacas. Nuestro objetivo ha sido el de evaluar la viabilidad de la fusión de la tomografía computarizada (TC) y la ecocardiografía transtorácica (ETT) 3D en niños y adultos con cardiopatías congénitas.
MétodosSe incluyeron de forma prospectiva 13 pacientes con cardiopatías congénitas y 1 paciente con corazón normal los cuales se sometieron a TC y ETT 3D como parte de su seguimiento habitual. Se describieron los pasos necesarios para completar el proceso de fusión (alineación, puntos de referencia y superposición), la navegación y la evaluación de las imágenes.
ResultadosLa edad media fue de 9,5 años [2,7-15,7], el 57% eran varones y la superficie corporal media fue de 0,9 m2 [0,6-1,7]. Se clasificaron las cardiopatías como simples (n=4, 29%), moderadas (n=4, 29%) o complejas (n=6, 42%). La fusión 3D ETT-TC fue exitosa en todos los pacientes. La mediana del tiempo total para completar el proceso de fusión fue de 735 segundos [628-1163], sin diferencias significativas según el grado de complejidad de la cardiopatía. Los puntos de referencia se modificaron significativamente en las cardiopatías congénitas complejas.
ConclusionesLa técnica de fusión 3D ETT-TC en una población de niños y adultos con diversas cardiopatías congénitas es viable y precisa según demostramos. La visualización simultánea de diferentes estructuras cardíacas podría ayudar a comprender las características anatómicas de las cardiopatías congénitas sin limitaciones en cuanto a la edad, el peso o la complejidad.
Palabras clave
La ecocardiografía es la piedra angular del diagnóstico, el tratamiento y la toma de decisiones quirúrgicas para niños y adultos con cardiopatías congénitas (CC). La ecocardiografía transtorácica (ETT) proporciona información sobre las válvulas cardiacas, en particular respecto a la estenosis o el reflujo, las derivaciones intracardiacas y la función y los volúmenes ventriculares. La ETT tridimensional (3D) ha surgido recientemente como un instrumento de mayor resolución capaz de evaluar la anatomía intracardiaca con más precisión1. Las proyecciones intracardiacas con diferentes vistas, como las frontales, proporcionan información diagnóstica que es difícil de obtener con la ETT 2D o tomografía computarizada (TC) cardiaca2. Sin embargo, la ETT 3D es difícil de utilizar en la práctica y exige una formación específica. La TC es una técnica de estudio complementario, útil especialmente para evaluar las anomalías congénitas de los vasos sanguíneos. Cuando los equipos experimentados utilizan la TC, se puede obtener una alta resolución y reducir la exposición a la radiación3.
Uno de los avances más recientes en las técnicas de diagnóstico por imagen cardiaca es la fusión de diferentes modalidades. En niños y adultos con CC, la fusión de la ecocardiografía transesofágica y la fluoroscopia durante el cateterismo facilita enormemente la comprensión de la anatomía cardiaca compleja. Este método ayuda a guiar los procedimientos intervencionistas, como el cierre percutáneo de la comunicación auricular o interventricular4,5. La fusión de TC y fluoroscopia previa al procedimiento también es útil para guiar las intervenciones percutáneas en vasos anómalos, como el implante de stents en la coartación o el de endoprótesis aórtica para excluir un aneurisma aórtico6,7.
La fusión de la TC y la ecocardiografía está actualmente en proceso de evaluación. La fusión de la TC y la ecocardiografía transesofágica se ha utilizado recientemente para guiar la anuloplastia tricuspídea transcatéter8 o para cerrar la orejuela izquierda9. La fusión de la TC y la ETT también se ha evaluado en adultos con arteriopatía coronaria10,11. Hasta la fecha, no se ha publicado información sobre la viabilidad de la fusión de la TC y la ETT en niños o adultos con CC. Sería valioso disponer de un medio que facilite la evaluación combinada de las características anatómicas intracardiacas y extracardiacas para planificar individualizadamente la cirugía cardiaca de cada paciente con CC. Sin embargo, la gran variedad de CC supone un desafío técnico para la fusión de la TC y la ETT.
El objetivo principal de este estudio preliminar es evaluar la viabilidad de la fusión de la TC y la ETT en una población de adultos y niños con una amplia variedad de CC.
MÉTODOSEn un solo hospital de tercer nivel, durante un periodo de 6 semanas entre julio y agosto de 2020, se incluyó a 14 pacientes consecutivos a quienes se realizaron tanto una TC como una ETT como parte de su atención habitual. Se utilizó la puntuación diseñada por la American Heart Association y el American College of Cardiology12 para clasificar las CC como simples, moderadas o complejas. Se observó la frecuencia cardiaca media durante la ecocardiografía. Se informó a los pacientes sobre el diseño del estudio y se obtuvo su consentimiento. Este estudio se registró en nuestra institución (FUSIONSCANECHOCC n.o 2022-565) y lo aprobó el comité de revisión institucional.
Imágenes de tomografía computarizadaLas imágenes se tomaron con TC de 512 cortes (Revolution CT, General Electric Healthcare, Estados Unidos). Se siguió el protocolo habitual de medicación previa a la prueba y no se utilizaron bloqueadores beta. La unidad de radioprotección optimizó previamente los parámetros de irradiación para lograr una buena relación entre calidad de imagen e irradiación (colimación de 0,60mm, intervalo de reconstrucción de 0,625mm y 70-80kV). Se utilizó una técnica axial prospectiva sincronizada con el electrocardiograma en un solo latido cardiaco para todos los pacientes, con una adquisición sistólica del 40 al 50% del intervalo RR. El medio de contraste (concentración de yodo, 300mg) se inyectó en una vena periférica en una dosis de 2ml/kg para pacientes con un peso corporal de hasta 40kg y de 1,5ml/kg para los que pesaban de 10 a 40kg, a un flujo de 0,6-4ml/s de acuerdo con el peso corporal. Se utilizó un algoritmo de reconstrucción iterativa (Asir-V [General Electric Healthcare] con una fuerza del 50%) y un programa informático de reconstrucción específico que reduce los artefactos del movimiento coronario (SnapShot Freeze, General Electric Healthcare). La dosis administrada a los pacientes se evaluó desde el punto de vista del índice de dosis de TC y el producto dosis-longitud (DLP). Las dosis efectivas (DE) se obtuvieron a partir de factores de conversión en tórax utilizando la fórmula DE (mSv) = DLP (mGy × cm) × k (mSv × mGy–1 × cm–1).
Ecocardiografía transtorácicaLos estudios se obtuvieron mediante un Vivid E95 GE (General Electric Healthcare, Vingmed Ultrasound, Noruega) con una sonda para adultos equipada con un transductor matricial (S4). Al final del examen, se obtuvo una imagen cardiaca en 3D de volumen completo durante 3 ciclos cardiacos utilizando la adquisición sincronizada con el ECG de gran volumen piramidal en 3D. Este paso consistió en colocar la sonda S4 para una adquisición de vista apical de 4 cámaras y seleccionar el programa 3D. Toda la cavidad del ventrículo izquierdo se incluyó en el volumen de exploración piramidal y se redujo la profundidad de imagen para maximizar la frecuencia de cuadro y las resoluciones axial y temporal. Los ajustes de ganancia se optimizaron para la visualización endocárdica. No se administró ningún medicamento para controlar la frecuencia cardiaca.
Fusión de imágenesLa fusión de la TC y la ETT se logró utilizando la primera versión del software de fusión de General Electrics disponible en el mercado. Los pasos necesarios para completar el proceso se enumeran a continuación.
Importación de imágenesSe seleccionaron y se extrajeron los cortes de TC en formato Digital and Imaging Communications in Medicine de nuestro Picture Archiving and Communication System. Se importaron manualmente, con una memoria USB o un CD, a un ecógrafo específico (Vivid E95, General Electrics) para el posprocesado y la fusión. También se podría haber importado conjuntos de datos de TC de otros fabricantes. Las imágenes de la ETT se obtuvieron en el ecógrafo específico o se importaron manualmente en formato raw. Luego, los conjuntos de datos de la TC y la ETT se fusionaron manualmente dentro de la misma ID de paciente antes del posprocesado. Cuando se combinaron los 2 conjuntos de datos, comenzó el proceso de fusión. No se registró el tiempo necesario para completar estos pasos preliminares.
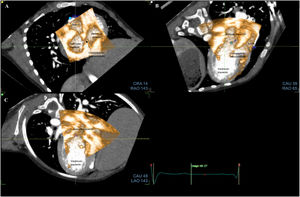
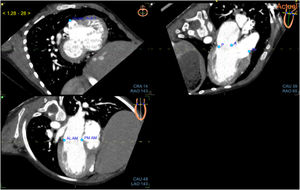
Proceso de fusiónEl proceso de fusión comenzó con alineaciones de la TC. No se requería ningún conocimiento anatómico para realizar las alineaciones y la colocación de los puntos de referencia. El objetivo era reproducir una imagen de referencia visible en la parte superior derecha de la pantalla. Se debía obtener 3 vistas estandarizadas moviendo 3 alineaciones ortogonales (líneas amarillas, verdes y blancas) de cada válvula. En la válvula mitral, las 3 vistas de referencia fueron la vista del eje corto (figura 1A), la vista apical de 3 cámaras con la aurícula izquierda, el ventrículo izquierdo y la aorta (figura 1B) y la vista apical de 2 cámaras con la aurícula y el ventrículo izquierdos (figura 1C). En la válvula aórtica, las 3 vistas de referencia fueron la horizontal (figura 2A), la sagital (figura 2B) y la coronal (figura 2C). Por último, en la válvula tricúspide, las 3 vistas de referencia fueron la del eje corto, la apical de 2 cámaras y la apical de 4 cámaras con la aurícula y el ventrículo derechos. Después de la validación de este paso, se colocaron 9 puntos de referencia anatómicos de TC de acuerdo con las imágenes de referencia propuestas por el software (3 de cada válvula; figuras 1A y B y figura 2A). Los puntos de referencia anatómicos se colocaron en las partes anterior, posterior, anterolateral y posteromedial de la válvula mitral y en la aorta en el caso de la válvula mitral, en las 3 comisuras en el caso de la válvula aórtica y en las partes anterior, posterior, lateral y septal del anillo tricuspídeo en el caso de la válvula tricúspide.
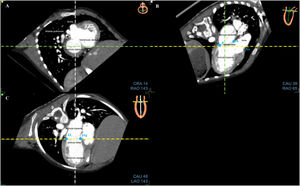
Paso 1: alineaciones y puntos de referencia de la válvula mitral en la TC. A: vista de eje corto. B: vista apical de 3 cámaras. C: vista apical de 2 cámaras; obsérvese las alineaciones ortogonales en cada panel (líneas blanca, amarilla y verde) centradas en la válvula mitral; los puntos azules son los puntos de referencia (A, anterior; P, posterior; Ao, aorta; AL, anterolateral; PM, posteromedial) que se colocarán de acuerdo con la imagen de referencia en la parte superior derecha de cada panel. TC: tomografía computarizada.
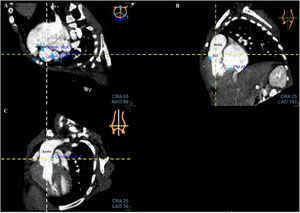
Paso 2: alineaciones y puntos de referencia de la válvula aórtica en la TC. A: vista horizontal. B: vista sagital. C: vista coronal. Obsérvese las alineaciones ortogonales en cada panel (líneas blanca, amarilla y verde) centradas en la válvula aórtica. En el panel A, los puntos azules son los puntos de referencia que se colocarán de acuerdo con la imagen de referencia en la parte superior derecha y corresponden a las comisuras. El primer punto de referencia es la comisura izquierda-derecha (1) y las otras 2 comisuras se ven hacia la izquierda. Los puntos de referencia anteriores están presentes, pero en gris. Ao: aorta; TC: tomografía computarizada.
El mismo procedimiento se llevó a cabo con las imágenes de la ETT. El software está formateado para ecocardiografía transesofágica y no para ETT. Hubo que invertir las vistas de la ecocardiografía antes de la alineación. Se tuvo que elegir una válvula para la alineación (válvula mitral, tricúspide o aórtica). La válvula mitral fue la elegida en el caso de todos los pacientes de nuestro estudio. Se colocaron 3 alineaciones ortogonales de la válvula mitral (figura 3) y luego se identificaron 3 puntos de referencia de la válvula mitral (figura 4B, C).
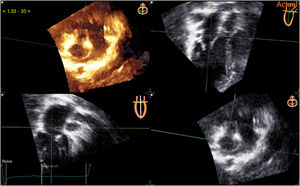
Paso 3: alineaciones de la válvula mitral en la ETT. A: ETT 3D correspondiente al panel D. B: vista apical de 3 cámaras. C: vista apical de 2 cámaras. D: vista del eje corto. Obsérvese las alineaciones ortogonales en cada panel (líneas blanca, amarilla y verde) centradas en la válvula mitral de acuerdo con la imagen de referencia en la parte superior derecha de cada panel. ETT: ecocardiografía transtorácica.
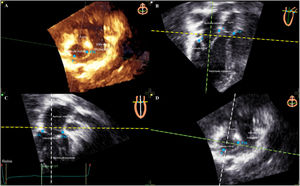
Paso 4: puntos de referencia de la válvula mitral en la ETT. A: ETT 3D correspondiente al panel D. B: vista apical de 3 cámaras. C: vista apical de 2 cámaras. D: vista de eje corto. Los puntos azules son los puntos de referencia (A, anterior; P, posterior; Ao, aorta; AL, anterolateral; PM, posteromedial) que se colocarán en los paneles B y C de acuerdo con la imagen de referencia en la parte superior derecha de cada panel. ETT: ecocardiografía transtorácica.
Las alineaciones de la TC y la ETT se describieron como fáciles o difíciles en cada paciente. Esta descripción de fácil o difícil fue subjetiva, pero se basó en el juicio de un solo cirujano que llevó a cabo todos los exámenes sin formación específica previa. Una alineación fácil se percibió como corta, sin dificultad de orientación espacial, incluso cuando hubo que invertir las vistas de la ecocardiografía. También se indicó cuando hubo que colocar los puntos de referencia en posición diferente de los puntos de referencia que servían de modelo debido a la anatomía específica de algunas CC complejas (puntos azules en la imagen reducida de la parte superior derecha de la pantalla) —por ejemplo, discordancia auriculoventricular o ventriculoarterial— o diferente orientación de las válvulas. Para verificar que se había logrado la fusión, el cirujano hacía una evaluación visual subjetiva de la calidad de la coincidencia de las capas de ETT y TC (figura 5). La calidad de la superposición se puntuó de 1 a 10. En este paso se utilizó la transparencia dinámica de la vista ecocardiográfica sobre la vista de digitalización de la TC (vídeo 1 del material adicional). Si era necesario, el eje de imágenes de la ETT podía moverse manualmente sobre la imagen de la TC para ajustar la precisión de la superposición. En cada paso, se registró el tiempo necesario y la dificultad puntuada sobre 10. La precisión del proceso se definió por la calidad de la superposición.
Paso 6: validación de las imágenes de fusión. A: vista de eje corto. B: vista apical de 3 cámaras. C: vista apical de 2 cámaras. Visualización simultánea de las imágenes de TC con la superposición de las imágenes de la ETT. La capa de la ETT se puede mover si es necesario, de modo que coincida perfectamente con las imágenes de la TC. ETT: ecocardiografía transtorácica; TC: tomografía computarizada.
Después de la superposición, podía comenzar la exploración en la imagen fusionada. La exploración permitió la evaluación de una estructura utilizando muchas modalidades al mismo tiempo: a) en 2D por 2TC: 2 clips de vídeo con ETT 2D y 2 imágenes con TC en la misma orientación (vídeo 2 del material adicional); b) en 3D por 3TC: 1 vista de ETT 3D y 3 vistas de TC diferentes; la vista de ETT 3D (esquina superior izquierda) se presenta en la misma orientación que una de las vistas de TC (inferior derecha), y la vista de TC de referencia se puede cambiar si se desea (vídeos 3 y 4 del material adicional), y c) vistas de TC, ETT 3D y ETT 2D simultáneamente.
Análisis estadísticoLas variables continuas se describen como mediana [intervalo intercuartílico]. Las comparaciones entre las mediciones de los pacientes en las 3 categorías de complejidad de la CC se hicieron con la prueba no paramétrica de Mann-Whitney. En todos los análisis se consideraron significativos los valores de p > 0,05. Los análisis estadísticos se hicieron con el software Stata, versión 11.2 (StataCorp, Estados Unidos).
RESULTADOSSe incluyó a 13 pacientes con CC consecutivos y a 1 paciente con un corazón de estructura normal, síndrome de Wolff-Parkinson-White y sospecha de anomalía de la arteria coronaria descartada por la TC. Sus principales características se describen en la tabla 1. No se excluyó a ningún paciente antes de la fusión de las imágenes.
Características demográficas de los pacientes
| Variable | ValoresN=14 |
|---|---|
| Edad (años) | 9,5 [2,7-15,7] |
| Varones | 8 (57) |
| Peso (kg) | 22,8 [12,6-59,0] |
| Estatura (cm) | 127 [89-165] |
| ASC (m2) | 0,9 [0,6-1,7] |
| Frecuencia cardiaca (lpm) | 87 [78-120] |
| Tipo de CC | |
| Simple | 4 (29) |
| Moderada | 4 (29) |
| Compleja | 6 (42) |
| Indicación de fusión | |
| Cateterismo | 4 (29) |
| Cirugía | 8 (57) |
| Diagnóstico | 2 (14) |
| Viabilidad de la fusión | 14 (100) |
ASC: área de superficie corporal; CC: cardiopatía congénita.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
La fusión de la TC y la ETT 3D fue factible en todos los pacientes. Se comenzó con la alineación de la válvula mitral de las imágenes de TC. Este paso fue fácil en la vista de eje corto de 12 pacientes (85,7%), en la vista apical de 3 cámaras de 9 (64,3%) y en la vista apical de 2 cámaras de todos los pacientes. La alineación en la vista del eje corto fue difícil en el paciente n.o 2 con retorno venoso pulmonar anómalo debido a la ausencia del tabique interauricular y en el paciente n.o 9 debido a una dilatación considerable de la aurícula izquierda, que cambió los puntos de referencia entre la aurícula y el ventrículo izquierdos. La alineación en la vista apical de 3 cámaras fue difícil en 5 pacientes debido al desplazamiento anterior de la aorta. Una vez que se logró la alineación de la válvula mitral, las alineaciones de la válvula tricúspide y de la válvula aórtica fueron fáciles.
En 8 pacientes (57,1%), los puntos de referencia de la TC se colocaron de manera diferente que los puntos de referencia que servían de modelo en el caso de la válvula mitral y la válvula tricúspide debido a la discordancia auriculoventricular, y en el caso de la válvula aórtica debido al desplazamiento de la aorta (doble salida del ventrículo derecho, dextrotransposición o levotransposición de las grandes arterias). Sin embargo, el procedimiento fue factible cuando la válvula tricúspide se consideró como la válvula mitral en el caso de discordancia auriculoventricular y la válvula pulmonar como la válvula aórtica en el caso de transposición de las grandes arterias. El punto de referencia de la válvula tricúspide fue difícil de localizar en 2 pacientes, 1 con dilatación del ventrículo derecho y el otro con transposición de las grandes arterias corregida y anomalía de Ebstein.
En relación con las alineaciones de la ETT, la alineación de la válvula mitral en la vista de eje corto fue difícil en 3 pacientes (21,4%) debido a una comunicación interventricular o al aumento de tamaño de la aurícula izquierda. La alineación de la válvula mitral en la vista apical de 3 cámaras fue difícil en 7 (50%) debido al desplazamiento de los grandes vasos y la ecogenicidad reducida de las estructuras anteriores. En 7 pacientes (50%), los puntos de referencia de la ETT se colocaron de modo diferente que los puntos de referencia que servían de modelo debido a la discordancia de la válvula.
Precisión del procesoLa tabla 2 describe el proceso de fusión según la complejidad de la CC. La calidad de superposición fue buena, con una puntuación media de 8,5/10 (figura 5). Se necesitó una ligera modificación de la capa de la ETT en la imagen de TC en 6 pacientes (43%): 2 tenían CC moderada y 4, CC compleja.
Tomografía computarizada y proceso de fusión de la ETT 3D en cardiopatías congénitas simples, moderadas y complejas
| Variable | Simple/moderada | Compleja | p |
|---|---|---|---|
| Modificación de la superposición | 2 | 4 | 0,277 |
| Alineación de la TC | NE | ||
| Punto de referencia de la TC modificado | 2 | 6 | 0,010 |
| VM | 1 | 1 | 0,692 |
| VT | 0 | 2 | 0,165 |
| VA | 1 | 5 | 0,026 |
| Dificultad de la TC (puntuación de 1 a 10) | 2,0 [1,0-3,5] | 5,5 [3,0-7,0] | 0,051 |
| Tiempo de la TC (s) | 376 [330-467] | 540 [319-820] | 0,302 |
| Alineación de la ETT | ne | ||
| Punto de referencia de la ETT modificado | 1 | 6 | 0,005 |
| VM | 1 | 1 | 1 |
| VT | 0 | 2 | 0,165 |
| VA | 1 | 5 | 0,026 |
| Dificultad de la ETT (puntuación de 1 a 10) | 2,0 [1,0-3,0] | 6,5 [5,0-7,0] | 0,005 |
| Tiempo de la ETT (s) | 293 [218-341] | 657 [275-735] | 0,093 |
| Tiempo total de fusión (s) | 696 [632-746] | 1320 [594-1.555] | 0,272 |
ETT: ecocardiografía transtorácica; NE: no especificado; TC: tomografía computarizada; VA: válvula aórtica; VM: válvula mitral; VT: válvula tricúspide.
Los valores expresan n o mediana [intervalo intercuartílico].
Las medianas de tiempo fueron 423 [329-558] s para el procesado de la TC y 302 [271-597] s para el de la ETT. La mediana del tiempo total requerido para completar el proceso de fusión fue de 735 [628-1.163] s. El tiempo total para obtener imágenes de fusión fue más largo en pacientes con CC compleja, aunque esta diferencia no fue significativa (p=0,272). Los puntos de referencia se modificaron considerablemente en pacientes con CC compleja.
Descripción de casos y utilidad de la fusiónLa tabla 3 describe las principales características de los 14 pacientes. En el paciente con corazón normal, la fusión fue simple y la navegación en todos los planos y modalidades fue informativa (vídeo 3 del material adicional). En pacientes seleccionados con CC complejas, la navegación en el corazón mediante múltiples modalidades simultáneamente se mostró útil para el diagnóstico o la planificación quirúrgica al combinar diferentes puntos de vista al mismo tiempo. A modo de ejemplo, en un paciente con doble salida del ventrículo derecho, un único panel de una imagen de fusión visualizó la comunicación interventricular, el tabique del cono del corazón, las relaciones ventriculoarteriales, el tamaño del ventrículo derecho y la ausencia de desplazamiento o cabalgamiento de una válvula auriculoventricular (figura 6; vídeos 2 y 4 del material adicional). En el vídeo 2, se observa la posición de la arteria pulmonar, que indica que una conexión directa desde el ventrículo derecho no es factible. La ETT 2D no muestra obstrucción de la comunicación interventricular en una conexión del ventrículo izquierdo con la aorta. El vídeo 4 del material adicional muestra que no había cabalgamiento entre las válvulas auriculoventriculares a través de la gran comunicación interventricular con doble afección. La TC fue útil en la vista del eje corto para visualizar la arteria pulmonar, que no se observaba en la ETT 3D.
Descripción de los 14 pacientes del estudio
| Edad (años) | Peso (kg) | Frecuencia cardiaca (lpm) | Tipo de CC | |
|---|---|---|---|---|
| Paciente 1 | 11 | 46 | 83 | Síndrome de Wolff-Parkinson-White |
| Paciente 2 | 0,9 | 6,8 | 151 | DSVD, D-TGA, retorno sistémico anómalo, EP |
| Paciente 3 | 3 | 14 | 90 | DSVD, EP |
| Paciente 4 | 21 | 67 | 72 | TF |
| Paciente 5 | 1 | 7,5 | 129 | CIV múltiple |
| Paciente 6 | 7 | 22,8 | 80 | CAV, EP |
| Paciente 7 | 11 | 40 | 82 | CIA |
| Paciente 8 | 20 | 65,1 | 78 | Estenosis de la vena pulmonar derecha |
| Paciente 9 | 11 | 22,8 | 120 | MCR |
| Paciente 10 | 15 | 79,9 | 64 | Anomalía congénita de la válvula aórtica |
| Paciente 11 | 6 | 19,5 | 118 | TGA corregida, CIV, EP |
| Paciente 12 | 18 | 59 | 70 | D-TGA, CIV, EP, derivación cavo-pulmonar total |
| Paciente 13 | 1 | 6,8 | 124 | L-TGA, CIV múltiple, EP, superposición ventricular |
| Paciente 14 | 2 | 12,6 | 101 | DSVD, L-TGA |
CAV: comunicación auriculoventricular; CIA: comunicación interauricular; CIV: comunicación interventricular; DSVD: doble salida del ventrículo derecho; EP: estenosis pulmonar; MCR: miocardiopatía restrictiva; TF: tetralogía de Fallot; TGA: transposición de grandes arterias.
Figura central. Navegación en las imágenes de fusión en un paciente con doble salida del ventrículo derecho. A: alineación de la válvula mitral de la TC en las vistas de eje corto, apical de 3 cámaras y apical de 2 cámaras. B: alineación de la válvula aórtica de la TC y puntos de referencia en las vistas horizontal, coronal y sagital. C: alineación de la válvula tricúspide de la TC y puntos de referencia en las vistas de eje corto y apicales de 2 y 4 cámaras. D: ETT 3D que muestra la doble salida del ventrículo derecho, la alineación y los puntos de referencia de la válvula mitral. El paciente tenía una doble salida del ventrículo derecho. Obsérvese la disposición ventriculoarterial con una aorta anterior y la comunicación interventricular con doble compromiso, la ausencia de un tabique conal entre los grandes vasos, la hipoplasia del anillo pulmonar y la ausencia de un desplazamiento o cabalgamiento de las válvulas auriculoventriculares. ETT: ecocardiografía transtorácica; TC; tomografía computarizada.
Este estudio muestra la viabilidad de la fusión de la TC y la ETT en 13 pacientes con CC de diversa complejidad. La fusión de la TC y la ETT combina el análisis simultáneo de imágenes de ETT 2D y 3D con las de la TC en vistas sincronizadas. La aplicación de la tecnología de imágenes de fusión a la CC todavía es escasa. Hasta donde sabemos, este es el primer estudio que muestra la viabilidad de la imagen de fusión de TC y ETT en niños y adultos con CC. Nos centramos en la viabilidad de la fusión de la TC con imágenes de ETT, ya que la ecocardiografía transesofágica previa al procedimiento rara vez se lleva a cabo en niños. Se mostró que la fusión de la TC y la ETT era factible en pacientes que abarcaban amplios intervalos de edad y peso y con diferentes complejidades de CC. Se analizaron muchas variaciones anatómicas en la CC, como discordancia auriculoventricular, discordancia ventriculoarterial, desplazamiento de las grandes arterias, superposición ventricular, anomalías de las válvulas mitral y tricúspide y anomalías de las válvulas aórtica y pulmonar. El proceso de fusión fue más largo en los pacientes con CC compleja que en aquellos con CC simple o moderada. Esto se explica en parte por la necesidad de modificar los puntos de referencia de acuerdo con la anatomía del paciente. La dificultad fue mayor en el caso de la ETT, ya que la alineación fue más difícil de obtener debido a la falta de ecogenicidad de las estructuras cardiacas muy anteriores.
En las CC simples y moderadas, la imagen de fusión fue informativa; por ejemplo, en un paciente con numerosas comunicaciones interventriculares, se localizó por imágenes de fusión una comunicación interventricular residual persistente después de la cirugía y luego se cerró por vía percutánea. La imagen de fusión parece muy informativa en el caso de las CC complejas, sobre todo cuando las conexiones ventriculoarteriales son anómalas. Una descripción precisa de las relaciones entre las estructuras intracardiacas tiene un impacto directo en el abordaje quirúrgico. Por ejemplo, se pudo observar simultáneamente las vistas de la TC y la ETT 3D de una salida doble del ventrículo derecho, lo que mostraba a los cirujanos las relaciones espaciales entre las válvulas auriculoventriculares, la comunicación interventricular y los grandes vasos.
Actualmente, las imágenes de fusión se utilizan sobre todo para guiar los procedimientos intervencionistas en las CC y las cardiopatías adquiridas. En primer lugar, la fusión de imágenes fluoroscópicas y de ecocardiografía transesofágica se ha utilizado para guiar el cierre de la orejuela izquierda, la valvuloplastia mitral percutánea, el cierre percutáneo del seno venoso o de la comunicación interauricular tipo ostium secundum, el cierre percutáneo de la comunicación interventricular o el cierre de fugas perivalvulares5,8,13–16. En segundo lugar, la fusión de la TC y la fluoroscopia fue útil para guiar la coartación o la colocación de stents en la arteria pulmonar y los implantes valvulares percutáneos15. En tercer lugar, la fusión de la TC y la ecocardiografía transesofágica mejoró la evaluación de la anatomía de la orejuela izquierda, lo que ayudó a orientar el catéter y, por tanto, reducir el tiempo de intervención9 y facilitó la anuloplastia percutánea de la válvula tricúspide, gracias a la evaluación de la gravedad y el mecanismo de la insuficiencia tricuspídea, así como el tamaño del anillo tricuspídeo y su relación espacial con la arteria coronaria derecha10.
Aunque parece que las aplicaciones de las imágenes de fusión en los procedimientos intervencionistas están experimentando un rápido desarrollo, pocos estudios se han centrado en mejorar el diagnóstico y la orientación de la cirugía cardiaca en pacientes con CC, lo que continúa siendo un desafío. Una mejor comprensión de las complejas relaciones espaciales y la anatomía de los pacientes con CC puede evitar hallazgos inesperados y reducir el tiempo de intervención. Existe evidencia clara de que la impresión de modelos en 3D puede afectar a la toma de decisiones quirúrgicas, sobre todo respecto a la reparación biventricular en CC complejas16. Sin embargo, las estructuras dinámicas, como las válvulas cardiacas y los flujos, no se pueden analizar en estos modelos.
Cuando se analizan casos de pacientes antes de una intervención, las imágenes de TC y ETT (2D y 3D) se presentan por separado. El análisis anatómico depende del ecografista que hizo la ecografía. Algunos casos son un reto y, por tanto, hay un creciente interés en la fusión de imágenes para combinar las fortalezas de estas modalidades durante las reuniones del personal con los cirujanos cardiacos, pues muestran las regiones de interés y la navegación en el corazón con una evaluación hemodinámica y anatómica simultánea. A pesar de las variaciones anatómicas en las CC, la fusión de la TC y la ETT no requiere ninguna habilidad especial en ETT 3D, pero permite la visualización de imágenes en 3D de calidad óptima. Solo es necesaria una adquisición en 3D a volumen completo del corazón, por lo que la curva de aprendizaje es corta. Además, el software permite visualizar las imágenes de TC y ecografía en 2D en el mismo eje. Estas imágenes se producen por navegación multiplanar en el conjunto de datos de volumen, no dependen de la frecuencia de adquisición del ecografista y permiten la visualización de un plano de ecografía 2D dinámico según lo soliciten los cirujanos o intervencionistas durante una reunión.
LimitacionesDespués de la importación de la TC y la adquisición de imágenes de la ETT, la mediana del tiempo total necesario para culminar el proceso de fusión fue > 12min. Este retraso no incluía el tiempo necesario para importar los datos de exploración de la TC. Importar los datos de la TC de la red local reduciría el tiempo de procesamiento general. Además, hubo una clara tendencia hacia un tiempo más largo para realizar la fusión en pacientes con CC compleja debido a la modificación de los puntos de referencia. Esto significa que el proceso se corrige manualmente y se requiere experiencia en CC para ajustar los puntos de referencia. El proceso de fusión, las alineaciones y los puntos de referencia no se guardaron en el ecógrafo. Cuando finaliza el proceso, no se puede recuperar imágenes de fusión previas, lo que aumenta claramente el tiempo de trabajo. Además, este programa está formateado para ecocardiografía transesofágica. Las mejoras en el proceso de fusión de la TC y la ETT simplificarían su uso en la práctica clínica diaria. Añadir flujo Doppler color en 3D sería útil. Si se puede lograr la fusión con cualquier imagen de TC, las imágenes de ETT deben tomarse con un ecógrafo GE.
La viabilidad de la fusión de TC y ETT en niños más pequeños no se evaluó debido a que no se disponía de una sonda pediátrica específica cuando se llevó a cabo este estudio. Se presenta poca variedad de CC porque solo se incluyó a pacientes a quienes se había hecho tanto una TC como una ETT como parte de su atención habitual. A pesar de ello, se presentan muchas variaciones anatómicas de la CC. Solo se incluyó a 3 adultos y la viabilidad de las imágenes de fusión de la TC y la ETT 3D debe evaluarse con mayor precisión en adultos con CC que pueden tener una ventana acústica pequeña. En la actualidad, el transductor matricial específicamente pediátrico hace viable la fusión de TC y ETT 3D incluso en niños más pequeños.
El software permite principalmente la visualización simultánea de imágenes de TC y 2D o 3D con la misma frecuencia. La fusión de imágenes de TC y ecografía solo se produce al final del paso de alineaciones para comprobar la precisión de la fusión. Por último, el objetivo del estudio es describir la viabilidad de las imágenes de fusión de TC y ETT en pacientes con CC, incluidos aquellos con CC compleja. Su utilidad y su valor añadido en la práctica clínica aún no se han demostrado, especialmente en la CC compleja, y debe compararse con otras modalidades innovadoras de diagnóstico por imagen, como la resonancia magnética de flujo 4D y la impresión 3D.
CONCLUSIONESSe presenta la viabilidad de las imágenes de fusión de la TC y la ETT 3D en una población de pacientes con un amplio intervalo de edad y con una amplia variedad de CC. La fusión de la TC y la ETT permite la visualización simultánea de muchas estructuras intracardiacas y puede ayudar a comprender la compleja anatomía de la CC.
Este estudio preliminar se centra en mostrar la viabilidad de la fusión de TC y ETT en una pequeña muestra de pacientes con CC con diversas anatomías. Debe estudiarse en cohortes más grandes si este instrumento ofrece información adicional útil, mejora el diagnóstico y reduce las complicaciones quirúrgicas en comparación con los protocolos estandarizados. Además, debe evaluarse la utilidad de la fusión de TC y ETT con fines de formación y comunicación.
FINANCIACIÓNNo hubo financiación.
CONTRIBUCIÓN DE LOS AUTORESContribuciones importantes a la concepción y el diseño: E. Fournier, C. Batteux, M. Mostefa-Kara y S. Hascoët. Contribuciones importantes a la obtención de datos, el análisis y la interpretación de datos: E. Fournier, C. Batteux, M. Mostefa-Kara, A. Azarine y A. Sigal-Cinqualbre. Redacción del original: E. Fournier, E. Valdeolmillos y S. Hascoët. Revisión crítica de contenido intelectual importante: E. Fournier, C. Batteux, M. Mostefa-Kara, E. Valdeolmillos, A. Maltret, S. Cohen, I. Van Aerschot, L. Guirgis, A. Azarine, A. Sigal-Cinqualbre, B. Provost, J. Radojevic-Liegeois, R. Rourssin, J. Zoghbi, E. Belli y S. Hascoët.
CONFLICTO DE INTERESESLos autores no tienen ningún conflicto de intereses en relación con este estudio.
- –
La fusión de diferentes modalidades es una de las innovaciones más recientes de la imagen cardiaca.
- –
Un instrumento que facilitara la evaluación combinada de las características anatómicas intracardiacas y extracardiacas sería valiosa para planificar la cirugía cardiaca en cada paciente con CC.
- –
Se sabe poco sobre la viabilidad de la fusión de ETT y TC en niños o adultos con cardiopatías congénitas.
- –
La fusión de TC y ETT 3D es factible en niños y adultos con CC, independientemente del grado de complejidad de la cardiopatía.
- –
Se requiere un protocolo modificado para fusionar el conjunto de datos de pacientes con CC complejas, como las anomalías de la conexión ventriculoarterial.
- –
Debe estudiarse en cohortes más grandes si este instrumento ofrece información adicional útil y mejora la evaluación preterapéutica en comparación con los protocolos estandarizados.