El objetivo de la evaluación económica es determinar el uso más eficiente de los recursos sanitarios disponibles. Las evaluaciones económicas de los desfibriladores automáticos implantables (DAI) comprenden estudios prospectivos como parte de un ensayo clínico, análisis de bases de datos clinicoadministrativas y modelos económicos. Los estudios demuestran que la relación coste-efectividad del DAI depende de distintos factores, especialmente el riesgo de muerte súbita cardiaca. En el análisis de subgrupos de pacientes la eficiencia varía según los factores de riesgo, sobre todo, disfunción ventricular izquierda, tanto en prevención primaria como secundaria. La utilización de dispositivos más baratos y de mayor longevidad implica una relación coste-efectividad más atractiva. La eficiencia del DAI es sensible al horizonte temporal considerado en el análisis. Los estudios económicos incluyen estimaciones de coste-efectividad conforme aumenta el horizonte temporal considerando diferentes asunciones.
Aunque la evaluación económica es una herramienta útil, la decisión en la distribución de recursos es más compleja debido a las preferencias y los valores sociales, como la equidad.
Palabras clave
La evaluación económica1 es el análisis comparativo de alternativas en el que se consideran sus resultados y costes. Es una herramienta para estimar la prioridad2 de unas acciones según los recursos disponibles y el beneficio que producen en los pacientes, asignando así de modo eficiente y efectivo unos recursos limitados. Por tanto, evaluar es comparar para poder decidir.
A pesar del notable incremento en el número de estudios de evaluación publicados en España3, su incorporación a las guías de práctica clínica es todavía insuficiente. En este trabajo se repasan los conceptos básicos de evaluación económica y se revisan posteriormente los estudios publicados sobre evaluación de desfibriladores automáticos implantables (DAI).
RESULTADOS: EFICACIA, EFECTIVIDAD, UTILIDAD Y BENEFICIOEficacia y efectividadLa eficacia consiste en la medida de resultados en condiciones ideales, en un ensayo clínico controlado, mientras que la efectividad mide el resultado en condiciones habituales, en la práctica clínica. Aunque pueden emplearse otras, la supervivencia es una medida de resultado frecuente. El número de años de vida o el número de vidas ganadas se emplean para valorar los resultados de las intervenciones sanitarias que reducen el riesgo de mortalidad. Ello permite comparar entre sí distintos grupos de intervenciones.
Se producen diferencias entre eficacia y efectividad por prescripciones inadecuadas o por tratarse de diferentes escenarios. La prescripción inadecuada4 puede deberse a una indicación incorrecta del tratamiento, una elección del fármaco o una forma de administración erróneas, o una revisión inadecuada de la terapia durante el seguimiento. Además, los ensayos controlados y la práctica clínica habitual se producen en diferentes escenarios, dado que los primeros incluyen criterios de inclusión y exclusión, así como un seguimiento más estricto del cumplimiento del tratamiento y los eventos del paciente.
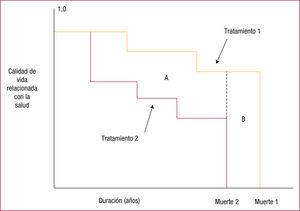
UtilidadMuchas intervenciones no sólo afectan a la mortalidad, sino también a la morbilidad; incluso en ocasiones no aumentan la cantidad de vida, pero sí su calidad. La utilidad es la preferencia o la valoración que el ciudadano tiene sobre un estado de salud. Se trataría, por tanto, de medir resultados considerando la calidad de vida y la duración de ésta (fig. 1). La unidad empleada son los años de vida ajustados por calidad5 (AVAC) que integran la mortalidad y la morbilidad. Para su cálculo se asigna a la salud en cada período un peso, una utilidad, entre 0 (estado similar a la muerte) y 1 (situación de salud plena) según la calidad de vida de ese período, de modo que los AVAC durante ese período serían el producto entre la utilidad y el número de años en esa situación.
BeneficioEn este caso se trata de dar un valor monetario a los años de vida ganados o a las complicaciones médicas evitadas. La valoración monetaria del efecto sobre la salud puede ser conflictiva, aunque, sin embargo, está implícita en cualquier decisión para asignar recursos sanitarios.
VALORACIÓN DE COSTESCostes directos e indirectosLos costes directos se refieren a los bienes y servicios empleados en una intervención y en sus efectos secundarios, incluidos los dispositivos, los fármacos, las pruebas diagnósticas, los ingresos hospitalarios, las visitas al servicio de urgencias, etc. El coste de un recurso depende de la cantidad total del recurso consumido y el valor monetario de cada unidad de dicho recurso. En los estudios de coste-efectividad, el análisis de costes debe ser exhaustivo, si bien los costes comunes a las tecnologías comparadas se pueden excluir.
Los costes indirectos son producidos por la morbilidad o la mortalidad prematura debidas a una enfermedad y se asocian al impacto que produce la enfermedad sobre el tiempo de vida sana de las personas. Estos costes con frecuencia no se incluyen en las evaluaciones económicas. Así, en una revisión6 de 228 estudios de coste-utilidad publicados entre 1975 y 1997, sólo entre el 5 y el 10% incluyeron los costes del tiempo del paciente, el tiempo de la familia y los cuidados informales o costes de producción perdida. Sin embargo, se ha estimado7 que en torno al 60% de los costes de la cardiopatía isquémica se debe a pérdidas de producción. Respecto a los gastos por pensiones, no se recomienda su inclusión en las evaluaciones económicas por tratarse de flujos monetarios redistributivos.
Otra clasificación de costes los divide en tangibles, expresados en unidades monetarias, e intangibles, que incluirían el dolor y el sufrimiento del paciente y la familia.
Costes de oportunidad y marginalEl coste de oportunidad8,9 es el valor de la mejor opción a la que se renuncia cuando se hace una elección. Por tanto, los recursos consumidos en la opción A no estarán disponibles para B, dado que los recursos son limitados y tienen usos alternativos. Realmente, el verdadero coste de la atención sanitaria no es el dinero, sino los beneficios que podrían haberse conseguido si ese dinero se hubiera empleado en la mejor alternativa1.
El coste marginal es el coste adicional de producir una unidad más de producto, el coste de la última unidad producida. En la toma de decisiones, los costes importantes son los marginales. De hecho, no realizar un análisis marginal de costes y resultados implica que estaríamos dispuestos a conseguir cualquier beneficio, aunque sea mínimo, sin considerar los costes, aunque tiendan a infinito.
EFICIENCIA. ANÁLISIS DE COSTEEFECTIVIDADEficienciaLa eficiencia es la relación entre los resultados obtenidos y su coste. Se es eficiente cuando se consigue el máximo nivel de salud a partir de unos determinados recursos, y también cuando entre varias opciones con el mismo resultado se selecciona la menos costosa. En la valoración de la eficiencia deben considerarse resultados y costes y, por tanto, menor coste no implica necesariamente mayor eficiencia, ya que dependerá de los resultados conseguidos.
La eficiencia es la base de las evaluaciones económicas y debe ser estimulada, no asumida, fomentando una conducta compatible con los intereses de la colectividad. El camino hacia la eficiencia pasa por la eficacia y la efectividad10. Tecnologías no eficaces no pueden ser efectivas, y éstas no serán eficientes por baratas que sean.
Análisis de coste-efectividadEn estos estudios se comparan programas alternativos, los resultados conseguidos con cada uno y sus costes. Es fundamental realizar una descripción clara de las alternativas comparadas. Los resultados se expresan en unidades habitualmente empleadas en clínica, con frecuencia, años de vida ganados. Los costes se miden en unidades monetarias. Para la valoración de los recursos empleados pueden usarse métodos basados en datos primarios o métodos sintéticos. Los basados en datos primarios consideran fuentes de información específica del estudio, con frecuencia prospectivas dentro de un ensayo clínico, mientras que las sintéticas emplean fuentes de información secundaria como bases de datos administrativos, menos detalladas que las anteriores.
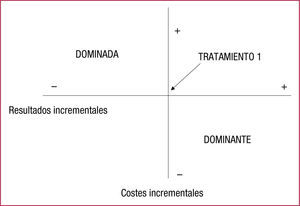
Una vez calculados los costes y los resultados, se mide el coste de la diferencia en supervivencia, es decir, el coste de cada año de vida ganado con la alternativa A frente a la alternativa B. El cociente coste-efectividad incremental (ICER) es el cociente entre la diferencia de costes y la diferencia de resultados. Se dice que una alternativa es dominada si consigue peor resultado y el coste es mayor y, por tanto, sería rechazada. Por el contrario, si el resultado es mejor y el coste menor, la alternativa sería dominante y se aceptaría (fig. 2). No obstante, en los análisis de coste-efectividad (ACE) se observa con frecuencia una mejoría en la supervivencia pero con un mayor coste. Un tipo de ACE son los análisis de coste-utilidad, en los que el resultado se mide en AVAC.
En los ACE se incluyen la perspectiva, la moneda, el descuento y el análisis de sensibilidad. La perspectiva es el punto de vista adoptado en la evaluación, es decir, quién soporta los costes. En programas con financiación pública se recomienda una perspectiva social. Además, los ACE deben incluir la moneda y el año, dadas las variaciones de su valor con el tiempo. La tasa de descuento11 actualiza los costes y ganancias de salud futuros dándoles menos valor por la preferencia de los individuos a retrasar los costes en lugar de soportarlos hoy. La preferencia temporal habitual opta por retrasar costes y adelantar beneficios. Se ha recomendado12 una tasa de descuento del 3% en los estudios de evaluación económica.
El análisis de sensibilidad es la técnica por la que se repiten las comparaciones entre costes y resultados, pero con sucesivas modificaciones de las suposiciones en las que se basan los cálculos. Se lleva a cabo un examen sistemático de la influencia de las variables y las asunciones usadas en la evaluación. Se pretende responder a preguntas como, por ejemplo, ¿qué sucede en el análisis si el coste del dispositivo se reduce a la mitad? o ¿qué sucede si el beneficio del dispositivo desaparece a los 8 años? El análisis de sensibilidad pone a prueba la robustez de las conclusiones mediante modificaciones de variables sobre las que hay incertidumbre.
¿Qué es una tecnología sanitaria eficiente?En una revisión13 de estudios internacionales publicados hasta 1997 se consideró que sería aceptable un coste por AVAC inferior a 100.000 dólares, con un valor mediano de 50.000 dólares. No obstante, algunos autores14 estiman que los valores deberían ser mayores y sometidos a revisiones periódicas. Por otro lado, los límites deberían ser distintos en cada país dependiendo de sus recursos y de la disposición de su población a invertir en salud15. En España se realizó una revisión16 de las evaluaciones económicas publicadas entre 1999 y 2001 y los criterios para considerar eficiente una tecnología. Los autores proponen como umbral de eficiencia 30.000 € por año de vida ganado.
ANÁLISIS DE COSTE-EFECTIVIDAD EN DESFIBRILADORES AUTOMÁTICOSEn diferentes estudios se ha demostrado que el DAI mejora la supervivencia en distintas enfermedades cardiacas por reducir significativamente la muerte súbita.
No obstante, dado su elevado coste entre otros factores, se ha tratado de seleccionar a subgrupos con un beneficio significativo17,18. Los estudios iniciales de costeefectividad de DAI presentaban bastantes limitaciones por basarse en opiniones de expertos19 o series de casos20, al considerar los resultados según el período de hasta el primer choque21 con las limitaciones que ello implica, o por su pequeño tamaño de muestra22 sin indicar en el estudio los intervalos de confianza. Posteriormente, a partir de ensayos clínicos controlados se han desarrollado ACE de mayor calidad. También se han empleado bases de datos clinicoadministrativas y modelos económicos sanitarios, como se indica a continuación.
ANÁLISIS DE COSTE-EFECTIVIDAD A PARTIR DE ENSAYOS CLÍNICOSSe han publicado ACE de los estudios Antiarrhythmics Versus Implantable Defibrillators (AVID)23, Canadian Implantable Defibrillator Study (CIDS)24, Multicenter Automatic Defibrillator Implantation Trial (MADIT)25, MADIT II26 y Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT)27.
Características generalesLos ACE desarrollados como subestudios en ensayos clínicos controlados tienen una alta validez interna y rigor científico. No obstante, presentan desventajas por su tamaño muestral y la duración del seguimiento. El tamaño muestral se ha calculado para valorar la eficacia y detectar diferencias en la mortalidad, pero no para obtener estimaciones del ICER y, en general, los intervalos de confianza de dicho valor son amplios, por lo que en ocasiones no pueden establecerse diferencias significativas en el análisis de subgrupos. Por otro lado, en las evaluaciones económicas, los períodos deberían ser suficientemente prolongados para medir todos los costes y beneficios relevantes. Por ello, dada la corta duración de los estudios para este fin, es frecuente que se completen con modelos y extrapolaciones. La validez externa de los resultados en estos estudios es menor que en los basados en bases de datos administrativas, por tratarse de grupos de pacientes seleccionados con un seguimiento estricto, diferente de la práctica clínica.
Valoración de costesSe procede a una recogida prospectiva de información económica dentro del ensayo clínico. Deben considerarse los recursos sanitarios más importantes utilizados en los distintos grupos y, por ello, la valoración de costes debe ser exhaustiva e incluir, en general, los costes del dispositivo y los recambios, la hospitalización inicial y los reingresos, las visitas al servicio de urgencias, la atención en las consultas externas, los procedimientos diagnósticos y terapéuticos, y los fármacos. Se aconseja presentar los resultados sobre costes como media aritmética, que proporciona más información que la mediana. Los costes propios del ensayo clínico que no se producen en la práctica clínica deben eliminarse o considerarse en el análisis de sensibilidad, como el estudio electrofisiológico en el MADIT-II. En los estudios no se incluyeron costes por pérdida de productividad. La razón esgrimida en el ACE del SCDHeFT son las bajas tasas de trabajadores activos observadas y el efecto similar en incapacidad transitoria en ambos grupos.
En los ACE de MADIT, MADIT-II y SCD-HeFT se incluyeron en la valoración los recursos empleados en la mayoría de los pacientes. En el estudio económico del CIDS se analizaron los costes de los primeros 430 pacientes (el 65% del total), mientras que en el análisis del AVID se consideraron los costes de hospitalización y fármacos antiarrítmicos en casi todos los pacientes, realizándose un análisis más detallado en 237 de ellos. Además del coste de la hospitalización inicial, se recopilaron los producidos durante el seguimiento cada mes25, cada 3 meses23,26,27 o cada 6 meses24. La información se completó mediante consulta telefónica en algunos estudios23,26,27. Los mayores costes previos al fallecimiento del paciente se consideraron en los estudios económicos de MADIT-II y SCD-HeFT. En el primero se valoraron costes 6 meses previos a la muerte, mientras que en el segundo se incluyeron los costes durante el año de fallecimiento en uno de los modelos para estimar los costes a largo plazo.
Se observó un mayor gasto hospitalario inicial en el grupo con DAI, especialmente por los costes del dispositivo y su implantación. Respecto a los reingresos, los resultados son variables, con mayores costes en el grupo con DAI en el análisis del CIDS y algo menores en AVID, MADIT y MADIT-II. En el ACE del SCD-HeFT no se encontró más necesidad de hospitalización o atención en consultas externas en los pacientes con desfibrilador.
En los ACE es frecuente que sean unos pocos recursos los que determinen el coste. Así, en la evaluación económica del AVID, la mayoría de costes se debe a la hospitalización inicial y los reingresos (el 84% en el grupo con DAI y el 73% en los pacientes con fármacos antiarrítmicos).
Coste-efectividad y comparación entre estudiosLas diferencias en la supervivencia entre los pacientes con DAI y los restantes se obtienen de cada ensayo clínico considerando todos los pacientes incluidos. Como se indicó previamente, el ICER se calcula dividiendo la diferencia de costes entre el grupo con DAI y el grupo con fármacos, y los años de vida ganados con el dispositivo. Además de la media, debe indicarse el intervalo de confianza para una información más completa de las diferencias reales.
La relación coste-efectividad del dispositivo es muy variable, con intervalos de confianza bastante amplios (tabla 1). La comparación entre los distintos estudios es difícil por las diferencias en el riesgo de los pacientes, su esperanza de vida, el beneficio proporcionado por el DAI, el tratamiento comparado (que incluye la amiodarona en algunos estudios y no en otros), el coste del desfibrilador, la frecuencia de recambios, el horizonte temporal del estudio, etc. Los costes son muy sensibles al contexto y pueden variar notablemente entre distintos países por los distintos costes del ingreso hospitalario o los sueldos de los profesionales, por ejemplo. No puede concluirse que el DAI sea o no costeefectivo, ya que depende del subgrupo de pacientes analizados y de otros factores determinantes, como se indica más adelante.
Análisis de la relación coste-efectividad a partir de ensayos clínicos
| ACE y referencia bibliográfica | Moneda | Horizonte temporal | Diferencia de supervivencia (años) | Diferencia de costes (dólares) | ICER (dólares/AVG) (IC del 95%) |
| AVID23 | Dólares de 1997 | 3 años | 0,21 | 14.101 | 66.677(30.761-154.768) |
| CIDS24 | Dólares canadienses de 1999 | 6,3 años | 0,23(-0,09 a 0,55) | 49.115 dólares canadienses(25.502-69.508) | 213.543 dólares canadienses/AVG(88.187-dominado) |
| MADIT25 | Dólares de 1995 | 4 años | 0,80(0,41-1,22) | 21.580(1000-43100) | 27.000(200-68.200) |
| MADIT II26 | Dólares de 2001 | 3,5 años | 0,167(0,033-0,301) | 39.200(29.900-48.500) | 235.000(121.000-1.212.000) |
| SCD-HeFT27* | Dólares de 2003 | Tiempo de vida | 1,63(0,66-3,1) | 62.420(46.532-88.443) | 38.389(25.217-80.160) |
ACE: análisis de coste-efectividad; AVG: año de vida ganado; IC: intervalo de confianza; ICER: cociente coste-efectividad incremental.
Estudios de prevención secundaria: AVID y CIDS. Estudios de prevención primaria: MADIT, MADIT II y SCD-HeFT. Se comparó el desfibrilador con la amiodarona (o sotalol) o el tratamiento convencional, dependiendo del estudio.
La evaluación económica se realiza en este tipo de ACE a partir de bases de datos administrativas que contienen información sobre las características de los pacientes, los tratamientos indicados, la utilización de recursos, etc. Estos análisis tienen una gran validez externa, con resultados más representativos de la población general, y se incluyen grupos de pacientes en general excluidos de los ensayos clínicos. Las bases de datos administrativas aportan un gran volumen de información con un bajo coste, lo que permite realizar evaluaciones con mayores tamaños muestrales que los ensayos clínicos y un seguimiento más prolongado. No obstante, el diseño de estos sistemas de registro tiene en cuenta el proceso de control y gestión, no su uso en ACE. Por ello, sus mayores limitaciones son la ausencia total o parcial de ciertos datos y la falta de asignación aleatoria, con la posible aparición de sesgos y factores de confusión no controlados y la consiguiente menor validez interna.
Se ha publicado un ACE28 del DAI en prevención secundaria en el que se estudia a una población no seleccionada de pacientes de Medicare ingresados con el diagnóstico principal de taquicardia o fibrilación ventricular entre 1989 y 1995. Se encontraron 7.612 pacientes con DAI, que se compararon con pacientes equivalentes sin el dispositivo (7.612 pares). Respecto a los resultados, se consideró la mortalidad global y sólo se analizaron los costes hospitalarios aunque, como se indicó previamente, explican el mayor porcentaje de costes. La moneda utilizada fue el dólar americano de 1999 y se aplicó una tasa de descuento del 3%. El seguimiento fue mucho mayor que en los ensayos clínicos controlados: 8 años. La diferencia en la supervivencia media con el DAI fue 0,5 años y se estimó un coste por año de vida ganado de 78.400 dólares (no se indican los intervalos de confianza). En el estudio se destaca que la mejora en la supervivencia con el DAI se redujo sustancialmente entre los 3 y los 8 años, mientras que la diferencia en los costes se incrementó con el tiempo.
ANÁLISIS DE COSTE-EFECTIVIDAD Y MODELOS ECONÓMICOSAspectos generalesAdemás de los métodos anteriores, los ACE pueden realizarse con un enfoque no empírico mediante modelos económicos sanitarios. También es habitual completar los ACE de ensayos clínicos con modelos para estimar la supervivencia y los costes a largo plazo.
Los modelos son esquemas teóricos que permiten hacer simulaciones económicas de procesos sanitarios relacionados con intervenciones29. Se trata de construir un modelo del curso clínico de la enfermedad y los resultados probables de las intervenciones sanitarias comparadas. Se busca representar la realidad de forma simplificada mediante la combinación de los datos de distintas fuentes (ensayos clínicos controlados, datos epidemiológicos, estudios observacionales, metaanálisis, etc.) para conocer los beneficios terapéuticos de cada intervención y sus costes asociados. Además de evitar los costes de la obtención de datos experimentales, los modelos permiten evaluar más opciones terapéuticas que los ensayos clínicos y modificar parámetros bajo distintos supuestos. Otra ventaja es que se pueden actualizar periódicamente cuando se disponga de nueva información.
La calidad de los modelos depende de la validez de la información empleada en su elaboración y de su reproducibilidad30. Se han propuesto criterios de calidad31 en los que se tienen en cuenta los datos incluidos y la estructura y la validación del modelo.
Como en cualquier tipo de análisis económico, es fundamental llevar a cabo un análisis de sensibilidad por la incertidumbre de las variables que influyen en los resultados del modelo.
Modelos de MarkovAunque hay otros modelos matemáticos, el más empleado en las evaluaciones económicas de DAI es el modelo de Markov32,33. En dicho modelo, la enfermedad se divide en un conjunto de estados de salud llamados estados de Markov (p. ej., salud perfecta, salud deteriorada, muerte). El horizonte temporal del análisis se divide en intervalos de tiempo (ciclos de Markov). El modelo asume que el paciente está siempre en alguno de los estados. Durante cada ciclo los pacientes pasan de un es. tado a otro según una probabilidad de cambio (probabilidad de transición). Siempre hay un estado final (absorbente) del que el paciente no puede salir, que habitualmente es la muerte. La simulación de un paciente se da por terminada cuando alcanza dicho estado.
Se asigna un grado de utilización de recursos y resultados sanitarios a cada uno de los estados. Repitiendo el modelo durante muchos ciclos pueden calcularse los costes y los resultados a largo plazo en grupos de pacientes con una enfermedad a los que se aplica un tratamiento.
En este modelo, las probabilidades de transición de un estado a otro dependen del estado en el que se encuentra el individuo en un momento determinado, sin depender de paso por estados anteriores (supuesto markoviano). Por tanto, el proceso no tiene memoria de los estados previos.
Los cálculos en estos modelos están facilitados por programas informáticos, en los que habitualmente se utiliza un tipo de representación llamada árbol de ciclo de Markov. Es necesario conocer la probabilidad de transición de un estado a otro, la duración de cada estado y la frecuencia con la que se evalúa el grupo de pacientes.
Coste-efectividad de desfibriladores automáticos mediante modelos de MarkovSe han publicado varias evaluaciones económicas de DAI con el empleo de modelos de Markov34–37. Owens et al34 analizaron en 1997 la relación coste-efectividad del DAI en pacientes con antecedentes de parada cardiaca, comparada con amiodarona, o amiodarona inicial con la implantación posterior de un desfibrilador en caso de recurrencia de la arritmia ventricular. Se empleó un modelo complejo con estados como taquicardia ventricular, fibrilación ventricular, afectación neurológica, toxicidad por amiodarona, etc. Se incorporaron utilidades en el análisis y se simularon reducciones del riesgo relativo de mortalidad global del 20 y el 40%. El estudio, aunque interesante en su análisis, ha perdido vigencia desde la publicación del estudio AVID.
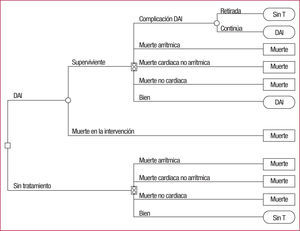
En otros estudios del mismo grupo se ha utilizado un modelo más simplificado (fig. 3). Sanders et al35 publicaron un ACE del DAI en prevención primaria tras infarto de miocardio en el que consideraron la eficacia del dispositivo y los distintos grados de disfunción ventricular izquierda. Por otra parte, Owens et al36 valoraron el efecto del DAI frente a la amiodarona según el riesgo de muerte súbita cardiaca y el cociente mortalidad súbita cardiaca/mortalidad no súbita. Ambos estudios se comentan en apartados posteriores.
Considerando 8 ensayos clínicos aleatorizados con diferentes criterios de inclusión, Sanders et al37 estudiaron la relación coste-efectividad del DAI en prevención primaria para pacientes con riesgo de muerte súbita y disfunción ventricular. Se valoró a una cohorte de pacientes con DAI o tratamiento control mediante el empleo del modelo de Markov citado, con ciclos de un mes. Se tuvieron en cuenta los riesgos de muerte cardiaca súbita o no súbita, la mortalidad por causas no cardiacas y las posibles complicaciones del desfibrilador. Las probabilidades se obtuvieron de los ensayos clínicos tras añadir datos de la población general estadounidense para estimar la mortalidad no cardiaca tras la implantación del desfibrilador. Se asumió una perspectiva social, la tasa de descuento fue un 3% anual y el horizonte temporal, el tiempo de vida del paciente. Respecto a los costes, se consideraron para la implantación del dispositivo y los recambios los costes médicos directos a partir de los sistemas de pago de Medicare y las tarifas profesionales. Para los costes de hospitalización no relacionados con el DAI se obtuvieron datos del registro de pacientes del Myocardial Infarction Triage and Intervention38,39, si bien algunos autores40 critican esto último por la probable mayor gravedad de los pacientes con DAI. Se asumió que los costes y los beneficios relacionados con el dispositivo por reducir la muerte súbita cardiaca se mantenían durante el seguimiento.
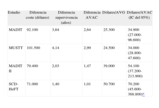
Los resultados del estudio se resumen en la tabla 2. Se han excluido los ICER del COMPANION, por ser un estudio de resincronización cardiaca, y los de CABG-Patch, DINAMIT y DEFINITE, por no mostrar un beneficio estadísticamente significativo del DAI en la mortalidad global. En los restantes, el dispositivo mejora la supervivencia comparado con el grupo control con un ICER entre 34.000 (MUSTT) y 70.200 dólares americanos de 2005/AVAC (SCD-HeFT). Al igual que en los ACE a partir de ensayos clínicos controlados, hay una gran heterogeneidad por los distintos criterios de inclusión y las diferencias en la reducción de mortalidad debida al desfibrilador. Por tanto, la relación coste-efectividad del DAI depende de la selección de pacientes y la estratificación del riesgo40. La principal limitación del estudio es la asunción de un beneficio mantenido del DAI durante la vida del paciente. Por ello, el trabajo se completó con un extenso análisis de sensibilidad en el que se incluyó la duración de la efectividad del DAI. Se concluye que, si se mantuviera al menos 7 años, el coste por AVAC continuaría siendo inferior a 100.000 dólares.
Coste-efectividad basado en un modelo de Markov
| Estudio | Diferencia coste (dólares) | Diferencia supervivencia (años) | Diferencia AVAC | Dólares/AVG | Dólares/AVAC (IC del 95%) |
| MADIT | 92.100 | 3,64 | 2,64 | 25.300 | 34.900 (27.000-96.600) |
| MUSTT | 101.500 | 4,14 | 2,99 | 24.500 | 34.000 (28.800-47.600) |
| MADIT II | 79.400 | 2,03 | 1,47 | 39.000 | 54.100 (37.200-213.900) |
| SCD-HeFT | 71.000 | 1,40 | 1,01 | 50.700 | 70.200 (45.600-368.800)* |
AVG: años de vida ganados; AVAC: años de vida ajustados por calidad; IC: intervalo de confianza.
En todos los estudios se comparó desfibrilador con tratamiento de control en prevención primaria. Moneda utilizada: dólares de 2005. Tasa de descuento: 3% anual. Horizonte temporal: tiempo de vida.
Modificado de Sanders et al37.
La evaluación económica del DAI se encuentra influida por factores que incrementan la efectividad, como el riesgo de muerte súbita cardiaca y la fracción de eyección ventricular izquierda. Además, el ICER varía según el coste del dispositivo y sus recambios, y otros aspectos tecnológicos. Otros factores determinantes son la calidad de vida del paciente y el horizonte temporal del análisis.
Riesgo de muerte súbita cardiacaComo se indicó previamente, la relación coste-efectividad del DAI mejora con la estratificación de riesgo, ya que permite seleccionar a los pacientes con mayor probabilidad de muerte súbita cardiaca. Así, en la revisión de los ACE basados en ensayos clínicos controlados se observa que las diferencias en la relación coste-efectividad de AVID, MADIT y MADIT-II se explican en parte por el distinto beneficio en la supervivencia en los grupos con DAI23,25,26 (tabla 1). Dichas diferencias entre MADIT y MADIT-II también se observan en el estudio con modelo económico de Sanders et al37 (tabla 2). Los escasos años de vida ganados en MADIT-II (0,167 años a los 3,5 años de seguimiento)26 reflejan parcialmente la heterogeneidad de los pacientes incluidos y el riesgo significativo de muerte no arrítmica (el 40% en el grupo con tratamiento convencional)41.
En un estudio de coste-utilidad, Owens et al36 valoraron con un modelo de Markov la aportación del DAI comparado con amiodarona, considerando el riesgo de muerte súbita cardiaca y la mortalidad por otra causa. Los costes medidos incluían costes médicos directos expresados en dólares americanos de 1999, con una tasa de descuento del 3% anual. El horizonte temporal fue el tiempo de vida del paciente (hasta un máximo de 40 años). Respecto a los resultados, cuando el riesgo de muerte súbita cardiaca era del 20% anual y el de mortalidad de otro tipo era del 2%, el ICER estimado fue de 29.900 dólares/AVAC. Este valor se multiplicaba con menores riesgos de muerte súbita cardiaca o mayores riesgos de mortalidad de otro origen. Los autores concluyen que la relación coste-efectividad del DAI depende de la mortalidad cardiaca global y de la relación entre la mortalidad súbita cardiaca y la debida a otra causa.
En resumen, en la evaluación económica son importantes el riesgo relativo de muerte súbita cardiaca y su relación con otras causas de muerte, tanto en prevención primaria como secundaria. En los pacientes con menor probabilidad de arritmias fatales, la relación coste-efectividad será menos favorable, al reducirse el beneficio.
Fracción de eyección ventricular izquierda y otros factores de riesgoLa fracción de eyección ventricular izquierda (FEVI) es un importante factor de riesgo de muerte súbita. De hecho, los ensayos clínicos de DAI en prevención primaria incluyen a pacientes con disfunción ventricular izquierda. Por otro lado, al analizar los ACE de estudios de prevención secundaria23,24 se observa un mejor ICER en pacientes con FEVI deprimida, dado que presentan un mayor beneficio en cuanto a la supervivencia que los pacientes con una FEVI más elevada.
La importancia de la FEVI en la evaluación económica del DAI ha sido estudiada por Sanders et al35 en la prevención primaria de pacientes con infarto de miocardio previo. Tomando como fuente principal un registro de pacientes de hospitales de Seattle, compararon con un modelo de Markov el DAI, la amiodarona y el tratamiento sin fármacos antiarrítmicos. Además de los costes médicos directos, se incluyeron los costes del viaje y de los inconvenientes para el paciente, medidos en dólares americanos de 1999, con una tasa de descuento del 3% anual. El horizonte temporal fue el tiempo de vida del paciente. En el análisis se consideraron 3 niveles de eficacia del DAI y distintos grados de disfunción ventricular. El DAI era más coste-efectivo en pacientes con una FEVI severamente deprimida. Así, con la máxima eficacia del DAI, el ICER en pacientes con FEVI<0,30 era de 46.100 dólares/AVAC frente a 178.600 dólares en los pacientes con FEVI>0,40.
Respecto a otros factores de riesgo, el estudio de subgrupos del ACE del MADIT-II26 indica que el ICER es más favorable en los pacientes con mayor riesgo (edad≥65 años, clase funcional de la New York Heart Association (NYHA)≥II, complejo QRS≥120ms, BUN≥25mg/dl), aunque las diferencias no son estadísticamente significativas. Hay discrepancias con otros ACE respecto a algunos de estos factores. En la evaluación económica de AVID23 no se detectaron diferencias en la relación coste-efectividad según la edad de los pacientes. Por otra parte, en el ACE de SCD-HeFT27, el ICER del grupo con DAI en pacientes en clase II de la NYHA fue de 29.872 dólares de 2003 por año de vida ganado, mientras que fue significativamente más caro en los que se encontraban en clase III. En el SCD-HeFT42, el 70% de los pacientes en clase II de la NYHA tuvo un 46% de reducción de riesgo con DAI y, sin embargo, el 30% de pacientes en clase III no obtuvo beneficio, aunque esta tendencia no se observó en MADIT-II.
Para mejorar la selección de pacientes con mayor eficiencia del dispositivo se ha analizado la combinación de factores de riesgo. Sheldon et al43 clasificaron a los pacientes del CIDS según la presencia de los siguientes factores: edad≥70 años, FEVI ≤0,35 y clase funcional II de la NYHA. Cuando coincidían los 3 factores, el ICER era de 23.344 dólares canadienses de 1999 por año de vida ganado (un dólar canadiense equivale aproximadamente a 0,65 dólares americanos). Por el contrario, en el grupo con un único factor de riesgo, el ICER superaba los 200.000 dólares canadienses. La relación coste-efectividad del CIDS refleja un alto porcentaje de pacientes con uno o ningún factor de riesgo. De hecho, el 87% de las muertes se concentraba en el 25% de la población con 2 o más factores de riesgo44.
En resumen, aunque hay variaciones entre los estudios, los pacientes más graves se benefician más del DAI45, con una relación coste-efectividad más atractiva.
Aspectos tecnológicos. Coste del dispositivo y de los recambiosEl coste de la terapia en todos los ACE es siempre un factor clave. En las evaluaciones económicas de DAI, la hospitalización inicial es una de las principales causas de diferencias en el coste, sobre todo por el coste del dispositivo y la estancia hospitalaria. Por ello, un menor coste del DAI y una simplificación de la implantación implicarían un mejor ICER.
En los análisis de sensibilidad de los diferentes estudios se demuestra que una reducción del coste del dispositivo mejoraría la eficiencia. Así, en la evaluación de Sanders et al37 sobre el DAI en prevención primaria se indica que si el coste del DAI se redujera 2/3, el ICER estaría cerca de 50.000 dólares/AVAC, incluso con un beneficio tan bajo como una reducción del riesgo relativo de muerte de 20-25%.
También contribuyen a mejorar la eficiencia del DAI la sustitución de los sistemas transtorácicos por transvenosos y la simplificación del procedimiento, con la consiguiente menor estancia hospitalaria inicial. En el ACE de MADIT25, el coste medio del dispositivo transvenoso es algo mayor que el sistema transtorácico, pero los costes iniciales son menores (8.800 dólares de media), lo que motiva una reducción del ICER de 27.000 a 22.800 dólares de 1995 por año de vida ganado. Por otra parte, en más de la mitad de los pacientes con DAI del estudio AVID se realizó un estudio electrofisiológico y en casi todos, un test previo al alta. Dado que normalmente todos los dispositivos son transvenosos y, en general, no se realiza un test prealta46, se reducen el tiempo de estancia hospitalaria y los costes iniciales. Por ejemplo, en el estudio AVID, la estancia media inicial disminuyó de 15 a 10 días durante la reducción del estudio. Se han descrito incluso estancias medias inferiores a los 5 días en supervivientes de una arritmia ventricular47.
Otro factor importante en la evaluación económica del DAI es su longevidad. La diferencia de costes entre los grupos estudiados en el CIDS es mayor que en AVID. Esto refleja en parte que un 34% de pacientes con DAI del CIDS necesitó un recambio de generador durante los 6,3 años de seguimiento, frente a sólo un 7% de pacientes del AVID a los 3 años. La importancia de los recambios en el ICER también se observa en el análisis de sensibilidad en Sanders et al37. El ICER variaba entre 30.800 y 62.300 dólares de 2005/AVAC con recambios a los 7 años, frente a 41.200-88.600 dólares cuando se producía cada 3 años.
Por tanto, unos costes menores y una mayor longevidad del dispositivo implicarán una relación coste-efectividad más atractiva.
Calidad de vidaAlgunas evaluaciones económicas27,34–37 han analizado los AVAC al comparar el desfibrilador y el tratamiento farmacológico. Como en otros estudios de coste-utilidad, el coste por AVAC es mayor que por año de vida ganado. Sanders et al37 asumen, basándose en estudios previos, utilidades basales de 0,88 en pacientes con disfunción ventricular seguidas de reducciones con la edad. Los años de vida ganados durante el tiempo de vida del paciente se reducen por un factor 0,73 cuando se transforman en AVAC. Consideran también que la calidad de vida no cambia con la implantación del dispositivo. Por otra parte, en el ACE de SCD-HeFT27, tras realizar entrevistas periódicas a los pacientes, las utilidades se estiman en 0,85 en ambos grupos de tratamiento después de un año de seguimiento, sin observarse cambios a los 30 meses.
La estimación de la calidad de vida es metodológicamente compleja y debe incluirse en los análisis de sensibilidad. El ICER se encuentra influido por la valoración de utilidades tanto debidas a la disfunción ventricular como a la implantación del dispositivo. Algunos autores48 han considerado una utilidad de 0,88 en pacientes con disfunción ventricular postinfarto. No obstante, la insuficiencia cardiaca congestiva con una presión venosa yugular elevada y un consumo pico de oxígeno reducido se relaciona con utilidades menores49, con las consiguientes implicaciones en la eficiencia.
Por otro lado, si la calidad de vida empeorara con la implantación del desfibrilador, el ICER sería menos favorable. No obstante, aunque no todos los estudios coinciden, se ha descrito una calidad de vida mejor o igual con DAI que con tratamiento farmacológico, excepto en casos de choques múltiples50. La calidad de vida también es peor en pacientes jóvenes portadores de DAI, con una mayor incidencia de ansiedad y depresión51.
Horizonte temporalLa eficiencia del DAI es claramente sensible al horizonte temporal considerado. Si el ACE sólo analizara los primeros meses de seguimiento se produciría un sesgo contra el DAI por el alto coste inicial y la mejoría más tardía en la supervivencia. Por tanto, la selección de un horizonte temporal excesivamente corto reduce el beneficio e implica un ICER más desfavorable. Se ha descrito52, tanto en prevención primaria como secundaria, que durante los 3 años posteriores a la implantación del dispositivo los años de vida ganados aumentan con la duración del seguimiento de forma no lineal, dependiendo del cuadrado del tiempo transcurrido desde la implantación.
La verdadera limitación se encuentra en las estimaciones a largo plazo, por ejemplo, 8, 12 y 20 años o el tiempo de vida del paciente. El ICER tras el seguimiento de los ensayos clínicos no es un buen estimador de su valor a más largo plazo, dado que influye la duración del beneficio del DAI. Por ello, los ACE basados en ensayos clínicos se completan con modelos en los que se consideran distintos escenarios a largo plazo (tabla 3).
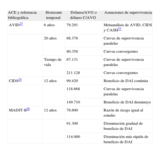
Estimaciones de la relación coste-efectividad a largo plazo
| ACE y referencia bibliográfica | Horizonte temporal | Dólares/AVG o dólares C/AVG | Asunciones de supervivencia |
| AVID23 | 6 años | 79.291 | Metaanálisis de AVID, CIDS y CASH53 |
| 20 años | 68.378 | Curvas de supervivencia paralelas | |
| 80.358 | Curvas convergentes | ||
| Tiempo de vida | 67.131 | Curvas de supervivencia paralelas | |
| 211.128 | Curvas convergentes | ||
| CIDS24 | 12 años | 99.420 | Beneficio de DAI continúa |
| 118.668 | Curvas de supervivencia paralelas | ||
| 149.710 | Beneficio de DAI disminuye | ||
| MADIT-II26 | 12 años | 78.600 | Razón de riesgo igual al estudio |
| 91.300 | Disminución gradual de beneficio de DAI | ||
| 114.000 | Disminución más rápida de beneficio de DAI |
ACE: análisis de coste-efectividad. AVG: año de vida ganado; DAI: desfibrilador automático implantable. Estudios de prevención secundaria: AVID y CIDS. Estudio de prevención primaria: MADIT-II.
Moneda: dólares de 1997 en AVID, dólares canadienses de 1999 en CIDS y dólares de 2001 en MADIT-II. Un dólar canadiense equivale a 0,65 dólares americanos, aproximadamente.
Entre los estudios de prevención secundaria, el ACE de CIDS24 considera 3 escenarios hasta los 12 años de seguimiento dependiendo de que continúe el beneficio del DAI (curvas de supervivencia divergentes), el riesgo fuera igual después del período del ensayo clínico (curvas paralelas) o el beneficio del dispositivo se redujera hasta que la supervivencia acumulada se igualara a los 12 años (curvas convergentes). Por otra parte, en la evaluación económica de AVID23 se calculó la relación coste-efectividad del DAI a los 6 años con datos del metaanálisis53 de AVID, CIDS y CASH (Cardiac Arrhythmia Study Hamburg). En la estimación posterior durante el tiempo de vida del paciente se consideraron dos posibilidades: curvas de supervivencia paralelas o convergentes. En estos estudios de prevención secundaria no hay concordancia en la evolución temporal de la relación coste-efectividad. El ICER en el ACE de CIDS mejora notablemente entre los 6 y 12 años, mientras que en la evaluación económica de AVID se produce un empeoramiento entre los 3 y 6 años y pocos cambios entre los 6 y 20 años. Al revisar otros trabajos sobre el efecto a largo plazo del desfibrilador también se encuentran discrepancias. En un subgrupo de pacientes de CIDS54 se observó que la superioridad del DAI comparado con amiodarona en la reducción de la mortalidad total aumenta con el tiempo. Por el contrario, Weiss et al28, con las limitaciones de los estudios con bases de datos administrativas, encontraron que la mayor supervivencia de los portadores de DAI se reducía entre los 3 y los 8 años.
Respecto al DAI en prevención primaria, en el ACE de MADIT25 se estima un ICER de 16.900 dólares de 1995 por año de vida ganado a los 8 años, aunque se asume que se mantienen los costes medios mensuales en los supervivientes y no se consideran variaciones del beneficio debido al dispositivo. En cambio, en la evaluación económica de MADIT-II26 se analizaron 3 alternativas: beneficio mantenido del DAI, incremento lineal del riesgo del grupo con desfibrilador igualándose los riesgos a los 12 años e incremento más rápido del riesgo seguido de una mayor mortalidad en pacientes con desfibrilador después de 7,1 años (tabla 3). Respecto al análisis de SCD-HeFT27, el ICER estimado a los 8 y 14 años es menor de 100.000 y 50.000 dólares de 2003 por año de vida ganado, respectivamente. En este estudio, el ICER se valora en 98.771 dólares por año de vida ganado durante el tiempo de vida del paciente si los riesgos entre los grupos se igualan a los 5 años de seguimiento. Finalmente, en el análisis de sensibilidad de Sanders et al37, considerando el tiempo de vida del paciente, si el beneficio del DAI cesa después de 3 años el ICER es claramente menos favorable. Sin embargo, si el efecto del dispositivo se mantiene al menos 7 años, la relación coste-efectividad del DAI frente al grupo control se mantiene por debajo de 100.000 dólares por AVAC.
Por tanto, en las evaluaciones económicas del DAI deben evitarse horizontes temporales cortos, dado el alto coste inicial y el beneficio más tardío en la supervivencia. La relación coste-efectividad a lo largo de la vida del paciente está muy influida por las estimaciones del beneficio del dispositivo a largo plazo, principal limitación de los estudios, y es pertinente considerar distintos escenarios en el análisis de sensibilidad.
ANÁLISIS COSTE-BENEFICIO DEL DESFIBRILADOR AUTOMÁTICOAunque en la evaluación económica de diferentes procedimientos sanitarios se ha empleado sobre todo el coste-efectividad, hay un interés creciente en los análisis de coste-beneficio55. En ellos, los costes y los resultados se miden en unidades monetarias y las decisiones dependen del cociente entre ambos o de la diferencia. La dificultad radica en asignar valores monetarios a elementos, como la mejora en la salud, que no se compran ni se venden en el mercado. Una de las técnicas empleadas es la valoración contingente, en la que se simula un mercado hipotético para obtener mediante un cuestionario una valoración por los individuos de los beneficios producidos por un tratamiento. Se determina la máxima disposición a pagar por ganancias en la salud. La disposición a pagar implica que los beneficios aportados se consideran superiores a la renuncia al dinero empleado. Entonces, la disposición a pagar máxima nos indicaría la magnitud del beneficio.
Se ha publicado56 un análisis de coste-beneficio de DAI frente a amiodarona en prevención primaria en Reino Unido y Francia. Se emplearon como fuentes de información el SCD-HeFT42 (que incluía a pacientes con una FEVI ≤0,35 en clase funcional II y III de la NYHA) y un metaanálisis57 de estudios con amiodarona. El horizonte temporal fue de 5 años, la moneda fueron euros de 2004 y las tasas de descuento del 3,5% en el Reino Unido y del 3% en Francia. Se diseñó un modelo de simulación de eventos para cohortes de pacientes con DAI o amiodarona. Para el cálculo del beneficio se utilizó el valor monetario de una vida humana, sin considerar la edad ni las enfermedades asociadas, basándose en estimaciones de los ministerios de transporte de ambos países mediante una valoración contingente: 2,1 millones de euros en el Reino Unido y 2 millones de euros en Francia. El beneficio se calculó multiplicando el número de vidas salvadas por el valor monetario asignado a cada vida. El cociente coste-beneficio fue 0,17 en el Reino Unido y 0,14 en Francia, es decir, claramente favorable para el uso del desfibrilador.
En este estudio se argumenta que no deben emplearse el tiempo de vida ni los AVAC como medición de resultado para no subestimar el beneficio en pacientes mayores o con enfermedades crónicas. Dicho planteamiento es discutible y controvertido por valorar cada vida independientemente de su duración. Una alternativa sería estimar el valor monetario del AVAC en ciertos contextos considerando valores sociales.
EFICIENCIA Y EQUIDADLas evaluaciones económicas son herramientas para ayudar a la toma de decisiones, pero no evitan juicios de valor. En la práctica, la decisión de emplear un determinado procedimiento o dispositivo no depende sólo de su eficiencia, sino también de otros factores, como el número de pacientes afectados, el pronóstico de la enfermedad, la disponibilidad de alternativas terapéuticas y, especialmente, los criterios de equidad58. En general, entre la población hay aversión a la desigualdad en salud. Suele preferirse una intervención algo menos eficiente para toda la población frente a otra intervención más eficiente pero de la que sólo se beneficia una parte59. La equidad se fundamenta en dos conceptos básicos60: la igualdad de acceso y la administración de igual (o similar) tratamiento para igual necesidad. Es más conflictivo determinar si la preferencia debe depender de la gravedad de la enfermedad o del beneficio potencial que podría causar el tratamiento.
Cada vez se publican más estudios sobre variabilidad de la práctica médica, que se define como variaciones sistemáticas, no aleatorias, en las tasas estandarizadas de un procedimiento. En España ha aumentado significativamente el número de desfibriladores implantados, pero con notables diferencias en las tasas de implantación entre comunidades autónomas. Así, Briones et al61 encontraron entre 4 y 21 dispositivos implantados por millón de habitantes por provincia de residencia según el conjunto mínimo básico de datos de 1998 y entre 11 y 48 por centro implantador según una encuesta en 2000. También se han detectado variaciones en años posteriores. Fitch-Warner et al62 estimaron 46 implantes por millón de habitantes en España en 2003, con oscilaciones entre 26 y 79 según la comunidad autónoma. Estos autores observaron, además, una correlación entre el número de implantes y la riqueza regional.
La interpretación de la variabilidad descrita es compleja. Pueden influir no sólo la disponibilidad de la tecnología en el centro o una desigualdad de acceso, sino también las preferencias profesionales, problemas de planificación o situaciones donde las pruebas científicas no son concluyente. Además, no necesariamente un mayor número de implantes es mejor.
La variabilidad puede considerarse un marcador sensible, pero poco específico, de una necesidad de mejora; sin embargo, el problema dista de estar resuelto.
CONCLUSIONESLa evaluación económica es la comparación entre alternativas considerando los resultados y los costes. Evaluar es comparar para poder decidir. La relación costeefectividad del DAI depende del subgrupo de pacientes analizados y de factores determinantes como el riesgo de muerte súbita cardiaca, la FEVI, el coste del dispositivo y otros aspectos tecnológicos, la calidad de vida y el horizonte temporal. Aunque hay variaciones en los estudios, los pacientes más graves se benefician más del DAI, con una relación coste-efectividad más atractiva. La principal limitación de los estudios es la estimación del beneficio del dispositivo a largo plazo. Por último, la toma de decisiones sobre el empleo del dispositivo no depende sólo de la eficiencia, sino también de otros factores como la equidad.
AGRADECIMIENTOSA Beatriz González López-Valcárcel, Catedrática de Economía Aplicada de la Universidad de Las Palmas de Gran Canaria, por la revisión del manuscrito y sus interesantes aportaciones a la versión definitiva.
A José Manuel Rodríguez Barrio, Medtronic, por sus comentarios sobre el trabajo y por la aportación de bibliografía sobre economía de la salud.
A Francisco Rodríguez, RS Medical, por aportar bibliografía sobre la relación coste-efectividad de los desfibriladores automáticos.
A Iván Moreno Torres, Profesor Asociado del Departamento de Economía y Empresa de la Universidad Pompeu Fabra de Barcelona, por sus comentarios sobre el artículo.
Dedicado a mis sobrinos, esos ángeles traviesos: Miguel, Alvaro, Cristina, Javier, Paula y Jaime.