El implante transcatéter de una prótesis aórtica es un procedimiento relativamente novedoso que ha transformado el tratamiento de los pacientes con estenosis aórtica grave. Según las guías de práctica clínica, el implante transcatéter está indicado para el tratamiento de los pacientes con estenosis aórtica grave sintomática inoperables o con alto riesgo quirúrgico tras ser seleccionados por un heart team. La valoración de la gravedad de la enfermedad y los síntomas del paciente son los primeros pasos en la selección del enfermo candidato a implante transcatéter.
Palabras clave
La estenosis aórtica degenerativa es la valvulopatía más frecuente en el mundo occidental y su prevalencia va en aumento como consecuencia del incremento de la esperanza de vida de la población1. Sabemos que en algunos países hasta un 8% de los individuos mayores de 84 años tienen estenosis aórtica grave2. En España, aproximadamente un 7% de las personas mayores de 85 años tienen algún grado de estenosis aórtica3. Si se tiene en cuenta que, según datos del Instituto Nacional de Estadística, hay aproximadamente 1,5 millones de habitantes de más de 85 años de edad4, se estima que, en nuestro medio, 100.000 van a sufrir la enfermedad. La estenosis aórtica grave degenerativa es el estadio final de una enfermedad lentamente progresiva relacionada con arteriosclerosis, inflamación, factores hemodinámicos y calcificación activa5. Una vez aparecen los síntomas, la enfermedad progresa rápidamente y son muchos los pacientes que van a requerir un recambio valvular. Es evidente, pues, que se trata de una enfermedad con gran impacto social.
En los últimos años, el implante valvular aórtico transcatéter (transcatheter aortic-valve implantation [TAVI]) se ha establecido como una alternativa válida al tratamiento quirúrgico de la estenosis valvular aórtica grave y sintomática para pacientes con contraindicación o elevado riesgo quirúrgico6–11. Este número de Revista Española de Cardiología Suplementos sobre TAVI aborda, entre otros aspectos, a qué pacientes se debe considerar candidatos a TAVI. En este artículo se revisan dos puntos fundamentales en la selección del paciente: confirmar la gravedad de la estenosis y evaluar los síntomas del paciente. Otros aspectos importantes en la selección del candidato a TAVI, como el cálculo del riesgo quirúrgico, la estimación de la fragilidad, la esperanza de vida y otros datos técnicos y anatómicos del procedimiento, no se tratan en este artículo.
Gravedad de la estenosis aórticaLa exploración física debe ser el primer paso en la aproximación al diagnóstico del paciente con estenosis aórtica. Tres son los elementos clave en la exploración de estos pacientes: la palpación del pulso carotídeo (disminución de la amplitud, pulso anácroto), la auscultación cardiaca (intensidad del soplo sistólico y disminución o abolición del segundo tono) y la existencia de signos de insuficiencia cardiaca. La presencia de un frémito sistólico en el mesocardio o en el foco aórtico es muy específica de estenosis aórtica grave. Es conveniente recordar que el pulso carotídeo puede ser normal en ancianos con estenosis aórtica y que algunos pacientes con estenosis aórtica grave pueden presentar un soplo sistólico de baja intensidad, sobre todo si tienen bajo gasto cardiaco, son obesos o tienen bronconeumopatía obstructiva crónica.
Tras la exploración física, el ecocardiograma es la técnica diagnóstica de elección para confirmar la estenosis aórtica, el grado de lesión valvular y su repercusión en el ventrículo izquierdo (VI). Es muy importante seguir un sistema que empieza analizando la morfología y el grado de calcificación valvulares y termina valorando el grosor, los diámetros y la función del VI. Es fundamental la estimación de la presión pulmonar y la identificación de cualquier otra lesión valvular acompañante (valvulopatía mitral).
La ecocardiografía Doppler es la técnica preferida para valorar la gravedad de la estenosis aórtica. En la práctica clínica diaria, los parámetros de ecografía Doppler más útiles para la cuantificación de la estenosis son la velocidad transvalvular aórtica máxima, el gradiente de presión transvalvular medio y el cálculo del área valvular mediante la ecuación de continuidad12. Los dos primeros son dependientes del flujo transvalvular aórtico, el cálculo del área lo es menos. La obstrucción valvular aórtica causa un incremento de la velocidad de la sangre a través del orificio valvular estenótico y genera un gradiente de presión entre el VI y la aorta. Tanto la velocidad como el gradiente de presión transvalvular aórtico aumentan según aumenta el grado de estenosis valvular. Sin embargo, la magnitud del aumento de la velocidad y del gradiente de presión en un área valvular determinada varía en función del volumen de sangre transvalvular. Así, pacientes con estenosis aórtica grave y bajo volumen de eyección (disfunción sistólica del VI) solo presentan moderados incrementos de la velocidad y el gradiente transvalvular, mientras que aquellos con estenosis valvular moderada y alto volumen de sangre transvalvular (cuando coexiste insuficiencia aórtica importante) tienen una velocidad y un gradiente transvalvular elevados12. La velocidad del flujo transvalvular aórtico se describe como la velocidad máxima instantánea y se corresponde con el gradiente de presión transvalvular aórtico máximo instantáneo según la fórmula de Bernoulli13. El gradiente transvalvular aórtico medio se puede calcular mediante Doppler o en el cateterismo promediando los gradientes de presión instantáneos a lo largo del periodo de eyección sistólico del VI.
Desde un punto de vista teórico, el cálculo del área valvular aórtica representa el parámetro ideal para cuantificar el grado de estenosis valvular. Sin embargo, su estimación mediante la ecuación de continuidad tiene una serie de limitaciones que hacen que sea muy dependiente del operador, y en la práctica es un dato menos fiable que el gradiente transvalvular en pacientes con un volumen de eyección normal. Por lo tanto, en presencia de gradientes elevados, si la válvula está muy calcificada e inmóvil, el cálculo del área valvular no es necesario. El área valvular aórtica es útil sobre todo en los pacientes con gradientes bajos y sospecha de estenosis aórtica grave con bajo flujo transvalvular. Sin embargo, como dato aislado no es suficiente para determinar el grado de estenosis y se debe considerar otros parámetros (morfología valvular, velocidad transvalvular, gradientes y diámetros, grosor y función del VI) para calcular la gravedad de la lesión valvular1.
La definición de la gravedad de la estenosis valvular aórtica se ha hecho basándose en los resultados de los estudios sobre la historia natural de los pacientes con estenosis aórtica. A modo de consenso, se ha determinado que la estenosis valvular aórtica es grave cuando la velocidad transvalvular aórtica máxima supera los 4 m/s, el gradiente transvalvular aórtico medio es > 40mmHg y el área valvular aórtica es < 1cm2 (tabla)1,12,14. Cuando el área valvular es < 0,8cm2, la estenosis aórtica se considera crítica1. En pacientes con una superficie corporal pequeña, es recomendable calcular el área valvular indexada por la superficie corporal. Un área valvular < 0,6cm2/m2 se considera grave1,14. Una medida alternativa de la gravedad de la estenosis es el cociente de velocidades entre el tracto de salida del VI y a través de la válvula aórtica (destinado a reducir el error frecuente que se produce en el cálculo del diámetro del tracto de salida del VI). La estenosis es grave cuando este cociente es < 0,25 (tabla)12. No hay que olvidar que la técnica Doppler puede subestimar o sobrestimar la velocidad aórtica y la gravedad de la estenosis en algunos pacientes. Por lo tanto, el enfoque de la enfermedad debe ser integral e incluir los síntomas del paciente, los hallazgos de la exploración física y el resultado de otras pruebas complementarias, si las hubiere. Si se dispone de ecocardiogramas previos, es fundamental comparar el resultado del ecocardiograma actual con dichos estudios para que sea posible analizar la progresión de la enfermedad: los cambios en la morfología valvular, los gradientes, el área valvular, la función ventricular y la presión pulmonar.
Aunque debe haber límites objetivos para distinguir la estenosis aórtica grave de la no grave, consideramos que esos límites deben integrarse en el cuadro clínico del paciente. Es decir, hay que considerar con estenosis aórtica grave no solo a los pacientes que hemodinámicamente superen los límites consensuados, sino también a todo aquel con estenosis aórtica y síntomas secundarios a esta enfermedad.
Estenosis aórtica de bajo flujo y bajo gradienteEn la práctica, cuando el gradiente medio es < 40mmHg y siempre que el gasto cardiaco (más exactamente el flujo transvalvular aórtico) sea normal, es improbable que el paciente tenga una estenosis aórtica grave. Sin embargo, algunos pacientes con disfunción sistólica del VI pueden tener una estenosis valvular aórtica grave (área < 1cm2) y presentar un gradiente transvalvular aórtico medio < 40mmHg (estenosis aórtica de bajo flujo y bajo gradiente). No todos los pacientes con gradientes bajos, disfunción ventricular y un área valvular pequeña tienen estenosis aórtica grave, pues algunas válvulas con una lesión moderada tienen una apertura reducida, y en realidad se trata de pacientes con cierto grado de miocardiopatía y estenosis aórtica moderada (estenosis aórtica seudograve)1. En estos casos, puede ser útil el cálculo de la velocidad transvalvular aórtica y el gradiente transvalvular durante la infusión de dobutamina a dosis bajas para distinguir la verdadera estenosis aórtica grave de la seudograve. La estenosis grave mostrará un incremento en los gradientes sin variaciones significativas en el área valvular, mientras que en la seudograve se incrementa el área valvular con discreto aumento de los gradientes1,14. Además, la ecocardiografía de estrés con dobutamina a dosis bajas también puede ayudar a identificar la presencia de reserva contráctil en pacientes con disfunción ventricular. Un incremento > 20% del volumen de eyección durante la infusión de dobutamina implica mejor pronóstico para estos pacientes. Por el contrario, la ausencia de reserva contráctil se ha asociado a muy mal pronóstico independientemente de que el paciente reciba tratamiento médico o quirúrgico15.
En los últimos años se ha descrito otro grupo de pacientes con estenosis aórtica de bajo flujo y bajo gradiente, pero en este caso con función sistólica del VI conservada16. Son pacientes con un área valvular < 1cm2, un gradiente medio < 40mmHg, un volumen de eyección indexado < 35 ml/m2 y fracción de eyección > 60%. Habitualmente son pacientes mayores, hipertensos, con ventrículos hipertróficos y un volumen ventricular pequeño. En realidad, muchos de estos pacientes pueden estar más cerca de una estenosis aórtica moderada que de una grave16. En caso de ser grave y sintomática, el pronóstico es mejor para los intervenidos que para los no intervenidos17. El diagnóstico de estenosis aórtica grave en este contexto es más exigente (área < 0,8cm2); conviene considerar otros aspectos como la exploración física, los síntomas, la comparación con estudios previos si los hubiere o la cuantificación del grado de calcificación valvular con tomografía computarizada multidetectores (se considera importante cuando la puntuación de Agatston supera las 1.000 unidades); en caso de superficie corporal pequeña, hay que indexar el área valvular1,18. Cuando haya dudas o discrepancias entre los datos clínicos y los hallazgos ecocardiográficos, se recomienda realizar un cateterismo cardiaco para determinar la gravedad de la estenosis14. Se debe tener en cuenta, sin embargo, que el cateterismo tiene sus propias limitaciones. En el cateterismo, la diferencia de presión máxima entre el VI y la aorta (gradiente pico-pico) no es una medida fisiológica real y su valor es habitualmente menor que el del gradiente de presión instantáneo máximo calculado por Doppler.
La tomografía computarizada multidetectores es muy útil para medir el área del anillo aórtico, la longitud de los velos y la distancia desde el anillo a los ostium coronarios, datos importantes si se considera la posibilidad de un TAVI. Sin embargo, si bien es una técnica útil para cuantificar el grado de calcificación valvular, no lo es para calcular la gravedad de la estenosis valvular14.
El papel del ecocardiograma transesofágico en la cuantificación del área valvular aórtica es reducido, puesto que la planimetría valvular es muy difícil y poco reproducible en válvulas calcificadas. Sí es útil en la valoración de la regurgitación mitral acompañante y también para la valoración anatómica de la raíz aórtica antes del TAVI.
Estenosis aórtica muy graveUn estudio reciente indica que, en los pacientes con estenosis aórtica asintomática pero muy grave, el recambio valvular aórtico disminuye la mortalidad comparado con el tratamiento médico19. La estenosis aórtica muy grave se ha definido de maneras distintas según los autores y las propias guías de práctica clínica. Para Kang et al19, una estenosis aórtica es muy grave cuando el área valvular es < 0,75cm2, acompañada de una velocidad transvalvular aórtica máxima > 4,5 m/s o un gradiente medio > 50mmHg. Las guías de la American Heart Association/American College of Cardiology1 entienden por muy graves los casos en que la velocidad es ≥ 5 m/s y el gradiente medio, ≥ 60mmHg14. Sin embargo, la guía de la Sociedad Europea de Cardiología considera que una estenosis es muy grave cuando la velocidad transvalvular máxima es > 5,5 m/s.
En nuestra opinión, la estenosis aórtica muy grave no es un concepto novedoso ni una situación clínica diferente de la estenosis aórtica grave. En la década de los ochenta, algunas series de pacientes con estenosis aórtica grave tenían gradientes medios > 50mmHg20,21. De hecho, en una de ellas20 el gradiente medio transvalvular aórtico fue 79 (45–140)mmHg. En cualquier caso, el valor discriminatorio de la velocidad transvalvular aórtica elegido por los autores para definir estenosis aórtica muy grave es arbitrario. Puesto que este parámetro es una variable continua, quizá habría sido más apropiado otro tratamiento estadístico. Un estudio prospectivo22 con 116 pacientes con estenosis aórtica muy grave (velocidad transvalvular máxima > 5,5 m/s) indica que los gradientes pueden tener implicaciones más importantes que el área valvular en este contexto y que estos pacientes tienen peor pronóstico si no se someten a recambio valvular. Por otro lado, el recambio valvular en ellos tiene peores resultados que en los pacientes con estenosis aórtica grave22. Otro estudio muy reciente23 ha comparado la evolución clínica de los pacientes con estenosis aórtica grave frente a la de aquellos con estenosis muy grave (velocidad máxima > 5 m/s, gradiente medio > 50mmHg o área valvular < 0,6cm2), sin cirugía. Durante el seguimiento se observó que la evolución de los pacientes con estenosis aórtica muy grave asintomática era similar a la de los enfermos con estenosis aórtica grave sintomática y peor que la de aquellos con estenosis aórtica grave asintomática. Debido a su naturaleza retrospectiva y a toda una serie de sesgos (es sorprendente que, entre los 90 pacientes sintomáticos, el 52% rechazara la cirugía), no se puede sacar conclusiones definitivas de este trabajo, y actualmente se considera que estos pacientes deben ser tratados del mismo modo que aquellos con estenosis aórtica grave.
SíntomasUna anamnesis cuidadosa es fundamental para detectar síntomas (disnea de esfuerzo, angina, mareos o síncope). En ocasiones es difícil separar las limitaciones al ejercicio normales por la edad, sobre todo en ancianos sedentarios, o las impuestas por otras comorbilidades, principalmente enfermedades respiratorias, de las secundarias a la estenosis aórtica, sobre todo cuando el paciente refiere disnea. Además, hay que tener en cuenta que algunos pacientes que reducen de manera subconsciente sus actividades y se amoldan a la enfermedad niegan tener síntomas1,14. Habitualmente, el síntoma inicial es la disnea de esfuerzo o la disminución de la capacidad de ejercicio. Otros síntomas, como el síncope o los mareos, suelen aparecen posteriormente en pacientes que no reconocieron o subestimaron los síntomas iniciales de la enfermedad.
Como ya se ha mencionado, esta es una enfermedad crónica y progresiva con un periodo de latencia muy largo, habitualmente años, en que el paciente está asintomático. Las recientes guías de práctica clínica de la American Heart Association/American College of Cardiology describen los cuatro estadios de la estenosis aórtica, que van desde que el paciente está en riesgo de sufrirla (estadio A) o se documenta una obstrucción hemodinámica progresiva (estadio B) hasta la estenosis grave asintomática (estadio C) o sintomática (estadio D). Cada uno de los estadios está definido por la morfología y la hemodinámica valvulares, las consecuencias de la obstrucción valvular para el VI y la existencia o inexistencia de síntomas. El estadio C se divide en C1 y C2, dependiendo de que el paciente no tenga o tenga disfunción del VI, respectivamente. Los pacientes con estenosis aórtica grave sintomática y gradientes elevados pertenecen al estadio D1, y al subgrupo especial de enfermos con estenosis aórtica grave sintomática con bajo flujo y bajo gradiente se le ha asignado el estadio D2 cuando presentan una fracción de eyección baja y D3 cuando esta es normal14. Desde nuestro punto de vista, esta clasificación es engorrosa, poco práctica y no añade nada al conocimiento actual de la enfermedad. Es obvio que, ante todo paciente con estenosis aórtica, se debe investigar la existencia de síntomas, definir la gravedad de la estenosis y evaluar el estado del VI.
En contra del pensamiento mayoritariamente aceptado, la historia natural de la estenosis aórtica grave no se conoce muy bien. La famosa figura 1 del muy referido artículo24 que Ross y Braunwald publicaron en 1968, en la que se muestra el curso clínico del paciente una vez comienzan los síntomas, se ha tomado como el paradigma de la historia natural de la estenosis aórtica en adultos. Sin embargo, ni el artículo ni dicha figura tienen nada que ver con los pacientes con estenosis aórtica degenerativa que tratamos actualmente. El artículo revisaba la evidencia disponible en ese momento. La media de edad al inicio de los síntomas era 48 años, y la mayoría de los pacientes tenían valvulopatía reumática o válvulas bicúspides. La media de edad al morir era 63 años y la endocarditis, la causa de muerte en un 15–20% de los pacientes. Por lo tanto, la evolución clínica descrita en ese artículo no puede aplicarse a nuestros pacientes con estenosis aórtica degenerativa.
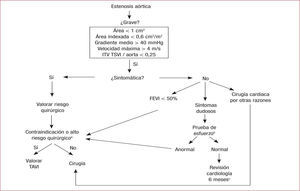
Protocolo de tratamiento de los pacientes con estenosis aórtica grave. EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; ITV: integral velocidad tiempo; TAVI: implante valvular aórtico transcatéter; TSVI: tracto de salida del ventrículo izquierdo.
aPacientes inoperables, STS ≥ 8%, EuroSCORE > 20%, edad muy avanzada, fragilidad, comorbilidades (hipertensión pulmonar grave, FEVI < 30%, aorta de porcelana, EPOC grave,
hepatopatía, enfermedad renal grave, etc.), deformidad torácica, radiación previa o cirugía coronaria previa con injertos permeables.
bPara pacientes con clínica dudosa; se considera prueba anormal la aparición de síntomas o una respuesta inapropiada de la presión arterial.
cRevisión: análisis, ECG, ecocardiograma (valórese radiografía de tórax).
Diferentes grupos han intentado investigar la historia natural de la estenosis aórtica grave asintomática; sin embargo, el hecho de que la mayoría analice conjuntamente el recambio valvular y la muerte como eventos impide sacar conclusiones definitivas, pues la mayoría de los eventos (entre el 66,6 y el 95,1%) obedecen a la cirugía valvular25–30. La mortalidad de los pacientes asintomáticos alcanzó el 3,7% (el 2,3% por año) y la muerte súbita fue menos frecuente aún. Además, pocos estudios aclaran cuántos pacientes sufrían algún síntoma antes de morir. Tampoco se conoce con certeza la evolución de los pacientes una vez aparecen los primeros síntomas, pero hay acuerdo general en que se debe considerar la cirugía o el TAVI cuando la estenosis es grave y el paciente está sintomático1,14.
Es conveniente insistir en que los síntomas del paciente no necesariamente se deben siempre a la estenosis aórtica, ni siquiera en pacientes con estenosis aórtica muy grave. Por otro lado, no todos los síntomas tienen el mismo valor pronóstico. La disnea, un síntoma frecuente en todas las series, no tiene el mismo peso pronóstico que la insuficiencia cardiaca congestiva. Desde un punto de vista práctico, es difícil diferenciar la disnea de la astenia en un paciente anciano con estenosis aórtica. A esa edad, la fatiga tras cierto grado de ejercicio se puede considerar incluso normal. De ahí que no esté muy claro el papel de la ergometría en este contexto. Hay pacientes que inconscientemente se autolimitan y niegan los síntomas. En este caso, una ergometría sí puede poner de manifiesto síntomas con un nivel de actividad física bajo. Aunque en el anciano pueda ser difícil separar las limitaciones normales al ejercicio de los síntomas debidos a la estenosis aórtica, es recomendable realizar una prueba de esfuerzo a pacientes con estenosis aórtica grave asintomática cuya capacidad funcional sea dudosa. La disnea excesiva al comienzo del ejercicio, la angina de esfuerzo, una respuesta hipotensora o la falta de un incremento progresivo de la presión arterial sistólica y el síncope de esfuerzo son síntomas probablemente secundarios a estenosis aórtica, y se debe tratar a estos pacientes como si estuvieran sintomáticos14. También se considera dato de mal pronóstico las arritmias ventriculares originadas por el ejercicio. En esta situación, el descenso del segmento ST es frecuente, pero no es específico de enfermedad coronaria. Aunque se ha señalado que una prueba de esfuerzo positiva identifica a los pacientes que, pese a estar asintomáticos, tienen una probabilidad alta de muerte súbita28, esta asociación no se ha podido demostrar en otras series31.
La angina es un síntoma frecuente. Más del 50% de los pacientes con estenosis aórtica grave que requieren recambio valvular o que van a someterse a TAVI tienen enfermedad coronaria, en parte como consecuencia de la similar patogenia de ambas entidades32,33. La gravedad de la enfermedad coronaria es mayor cuanto mayor sea el perfil de riesgo cardiovascular del paciente. El riesgo de muerte cardiovascular al año de seguimiento de pacientes con enfermedad coronaria grave y compleja a los que se realiza un TAVI es el doble que para aquellos sin enfermedad coronaria34. En estos casos, lo idóneo es resolver tanto la estenosis aórtica como la enfermedad coronaria. Sin embargo, no hay que olvidar que, en algún caso, una revascularización coronaria percutánea puede volver asintomático a un paciente previamente sintomático.
El síncope, particularmente en el anciano, puede ser secundario a muchas otras causas además de la estenosis aórtica, y su impacto pronóstico en un paciente determinado es muy variable. En la serie de Ross et al24 hubo algún paciente con síncopes durante 18 años. En general, el síncope durante el esfuerzo se debe considerar muy probablemente relacionado con la estenosis aórtica; sin embargo, el síncope de reposo y el que tiene lugar tras el esfuerzo exigen descartar otras causas antes de asumir que su causa es la estenosis valvular.
La muerte súbita tiene una incidencia muy baja entre los pacientes con estenosis aórtica asintomática, alrededor del 1% por año35. Si se tiene en cuenta la mayoría de los estudios que tratan sobre la historia natural de los pacientes con estenosis aórtica asintomática25–30, la incidencia de muerte súbita es similar (1,8%). En algún caso el paciente había tenido síntomas previamente. Por lo tanto, si tenemos en cuenta las mortalidades del recambio valvular y el TAVI, la baja probabilidad de muerte súbita no debería tener impacto en la estrategia terapéutica. Además, no hay que olvidar que la muerte súbita también puede ocurrir tras el recambio valvular, alrededor del 1% en un estudio en que se completó un seguimiento de 3 años36.
El incremento de la gravedad de la estenosis es variable, pero inevitable. Cuando la estenosis aórtica es grave y está muy calcificada, la supervivencia libre de eventos a los 2 años de seguimiento no es superior al 50%. Por lo tanto, se debería revisar a estos pacientes con un ecocardiograma de control en consulta cada 6–12 meses14. Cuando los síntomas aparecen, el pronóstico del paciente empeora si no se lleva a cabo el recambio valvular o el TAVI.
Tratamiento médicoLa hipertensión es frecuente en los pacientes con estenosis aórtica; de hecho, probablemente sea un factor de riesgo de contraer la enfermedad, al igual que los otros factores de riesgo cardiovascular clásicos. En combinación con la obstrucción valvular, es causa de la sobrecarga total de presión en el VI, por lo que se debe tratar correctamente. No está claro cuál es el tratamiento antihipertensivo de elección para los pacientes con estenosis aórtica grave, pero se debería evitar los diuréticos, sobre todo para pacientes con volúmenes ventriculares pequeños en los que podrían precipitar episodios de bajo gasto. Teóricamente, tanto los inhibidores de la enzima de conversión de la angiotensina como los bloqueadores beta pueden ser una buena elección. Los primeros, además de controlar la presión arterial, pueden tener efectos beneficiosos para la fibrosis del VI; los segundos son de elección para pacientes con enfermedad coronaria concomitante37–39. Tanto en un caso como en otro, se debe empezar con dosis bajas e incrementarlas progresivamente hasta alcanzar el control de la PA.
El resultado de algunos modelos experimentales y estudios clínicos retrospectivos favoreció el uso de estatinas para prevenir la progresión de la estenosis aórtica calcificada40–43. La evidencia científica actual es insuficiente y su uso para este fin no está justificado14. Sin embargo, la hipercolesterolemia, cuando está presente, debe tratarse de acuerdo a las guías de práctica clínica como en cualquier otro contexto clínico para la prevención primaria y secundaria de la enfermedad coronaria.
Recomendaciones para la intervención según las guías de práctica clínicaEn lo que respecta al momento de la intervención, las recomendaciones son válidas tanto para el recambio valvular como para el TAVI.
Las guías recomiendan intervenir a todo paciente con estenosis aórtica grave si tiene cualquier síntoma secundario a la estenosis1,14. En ausencia de comorbilidades importantes que limiten la esperanza o la calidad de vida, el recambio valvular aórtico está indicado para pacientes con estenosis aórtica grave sintomática. La edad per se no es una contraindicación a la cirugía, pero la realidad es que el TAVI se perfila como procedimiento de elección para los más ancianos. Cuando los síntomas aparecen en la prueba de esfuerzo, la recomendación de intervenir sigue siendo de clase I, y si durante la prueba de esfuerzo se produce una disminución de la presión arterial sistólica por debajo de la basal o cuando el incremento no es > 20mmHg respecto al valor basal, la recomendación es de clase IIa1,14.
La intervención también se recomienda (clase I) para pacientes asintomáticos con estenosis aórtica grave pero con disfunción del VI (fracción de eyección < 50%)14. En ocasiones, si la disfunción del VI no se origina por el exceso de poscarga, la función ventricular no mejorará completamente, pero el pronóstico sí44,45.
El recambio valvular aórtico está indicado para pacientes con estenosis aórtica moderada o grave que requieren cirugía cardiaca por cualquier otra razón (aneurisma de aorta ascendente, cirugía de revascularización coronaria, otra valvulopatía). Se trata de recomendaciones de clase IIa y I respectivamente1,14.
Las guías también recomiendan la intervención (clase IIa) para pacientes asintomáticos con estenosis aórtica muy grave y bajo riesgo quirúrgico (puntuación < 4 en la escala de riesgo de la Society of Thoracic Surgeons)1,14.
Para los pacientes con estenosis aórtica grave sintomática de bajo flujo y bajo gradiente y fracción de eyección del VI reducida, el tipo de recomendación está en función del resultado de la ecocardiografía de estrés con dobutamina. Si hay reserva contráctil, se recomienda la intervención (clase IIa); en caso contrario, la recomendación es de clase IIb, pues se considera que, si no hay reserva contráctil, la intervención se puede realizar pero su eficacia está menos establecida1,14. El tratamiento de los pacientes sintomáticos con estenosis aórtica grave de bajo flujo y bajo gradiente y fracción de eyección conservada es todavía más controvertido. La decisión se debe tomar integrando los síntomas, los datos de la exploración física y el resultado de las pruebas complementarias (válvula aórtica calcificada, apertura valvular muy restringida, ventrículos hipertróficos con volúmenes pequeños, etc.).
Tipo de intervenciónLa elección del procedimiento —cirugía de recambio valvular frente a TAVI— se debe realizar con base en múltiples parámetros clínicos y anatómicos, entre los que se incluyen el riesgo de la intervención, la fragilidad del paciente y las comorbilidades, el diámetro y el estado de las arterias iliacas, el diámetro del tracto de salida del VI, la presencia de aorta de porcelana, etc. La existencia de una enfermedad coronaria grave multivaso o de una lesión valvular mitral grave concomitante favorece una intervención quirúrgica. En cualquier caso, la decisión debería ser consensuada entre el médico clínico responsable del paciente, un cirujano, un hemodinamista y especialistas en imagen cardiovascular (heart team). La participación de especialistas en geriatría o anestesia también es conveniente. La figura muestra el protocolo de tratamiento del paciente con estenosis aórtica grave utilizado en nuestros hospitales.
Las guías de práctica clínica, incluso las más recientes (American Heart Association/American College of Cardiology), recomiendan recambio valvular aórtico mediante cirugía convencional para pacientes con riesgo quirúrgico bajo o intermedio (Society of Thoracic Surgeons Predicted Risk of Mortality score [STS PROM] < 8% y EuroSCORE logístico < 20%)1,14. Para los pacientes que tienen indicada cirugía de recambio valvular aórtico, pero con riesgo quirúrgico prohibitivo (riesgo predicho de muerte o morbilidad importante > 50% al año), se recomienda TAVI siempre y cuando su esperanza de vida sea > 1 año y sea probable que la intervención mejore su calidad de vida (recomendación de clase I)1,6–8,14,46. Según las guías, el TAVI es una alternativa razonable a la cirugía valvular para los pacientes que, aun teniendo indicada la cirugía, presentan un riesgo quirúrgico elevado (STS PROM ≥ 8%) (recomendación de clase IIa)9,14,46.
El éxito del TAVI radica en la adecuada selección de los pacientes. No se recomienda para pacientes con esperanza de vida < 1 año o cuyas comorbilidades sean tan importantes que impidan conseguir una mejora de la calidad de vida tras el procedimiento aunque haya tenido éxito14. La selección de los pacientes debe ser lo más objetiva posible, por lo que es conveniente incluir escalas o índices validados en la valoración de pacientes con estenosis aórtica grave, especialmente cuando se considera un TAVI47. Dado que generalmente se trata de ancianos con comorbilidades, deben incluirse los siguientes puntos:
- •
Valoración clínica que confirme que el paciente está sintomático y gradación de los síntomas según la New York Heart Association cuando se trate de disnea y de la Canadian Cardiovascular Society para la angina. La presencia de síntomas solo con grandes esfuerzos y que, por lo tanto, no limitan la actividad diaria debe hacernos ser muy prudentes antes de indicar un TAVI.
- •
Valoración del pronóstico del paciente debido a otras comorbilidades que puedan afectar a la calidad y la esperanza de vida una vez realizado el TAVI.
- •
Valoración de la capacidad del paciente para hacer las actividades cotidianas de manera independiente. Para el enfermo muy dependiente, el beneficio del TAVI es limitado.
- •
Valoración de la fragilidad. El TAVI no es una cirugía, pero no deja de ser un procedimiento agresivo que puede originar complicaciones graves, sobre todo en pacientes frágiles.
- •
Valoración anatómica: la válvula aórtica, la aorta sinusal, la aorta ascendente y las arterias iliacas deben cumplir determinados requisitos anatómicos para considerar un TAVI.
Por último, las guías de práctica clínica también hacen referencia a la valvuloplastia aórtica con balón. Esta técnica apenas se utiliza actualmente. Según las guías, se puede considerar como procedimiento «puente» a la cirugía de recambio valvular o a TAVI o también en algún paciente como medida paliativa (recomendación de clase IIb)1,14.
Conflicto de interesesNinguno.