Las arritmias cardiacas en la edad pediátrica son relativamente frecuentes, con una incidencia anual estimada de 13 casos de taquicardia supraventricular en menores de 19 años por cada 100.000 habitantes1. Se considera que actualmente el tratamiento con ablación cardiaca percutánea en esta población tiene eficacia y seguridad comparables a las series de ablación cardiaca en adultos, a pesar de que el número de casos comunicado es significativamente menor. La mayoría de la literatura relacionada con la ablación cardiaca pediátrica proviene de registros multicéntricos americanos2-4, donde se atiende a estos pacientes en unidades de referencia con gran volumen de pacientes, que supera los 100 casos anuales, y este factor se ha asociado con mejores resultados clínicos5. De todas formas, algunas series recientes de países Europeos han demostrado similares eficacia y seguridad pese a tener un número de casos significativamente menor6,7.
Independientemente de los diferentes modelos sanitarios, la ablación en pacientes pediátricos, sobre todo los menores de 12 años, presenta unas características clínicas, unos requisitos técnicos y unas necesidades asistenciales específicas que conllevan que el personal que atiende a estos pacientes esté preparado no solo para desarrollar la ablación con garantías, sino para resolver complicaciones inesperadas durante los procedimientos.
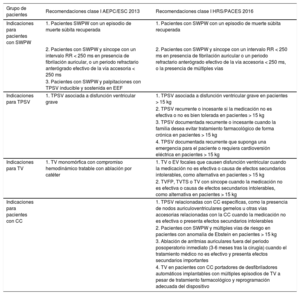
INDICACIONES DE TRATAMIENTOLas guías de recomendación para el diagnóstico y el tratamiento de las arritmias en pacientes pediátricos y con cardiopatías congénitas (CC) de la AEPC/EHRA de 20131 y la PACES/HRS de 20168 aportan información específica sobre etiología, epidemiología, diagnóstico y estrategias de tratamiento con ablación cardiaca para pacientes de 0 a 18 años (tabla 1).
Comparación de las indicaciones de ablación clase I entre las guías europeas y las americanas
| Grupo de pacientes | Recomendaciones clase I AEPC/ESC 2013 | Recomendaciones clase I HRS/PACES 2016 |
|---|---|---|
| Indicaciones para pacientes con SWPW | 1. Pacientes SWPW con un episodio de muerte súbita recuperada | 1. Pacientes con SWPW con un episodio de muerte súbita recuperada |
| 2. Pacientes con SWPW y síncope con un intervalo RR < 250 ms en presencia de fibrilación auricular, o un periodo refractario anterógrado efectivo de la vía accesoria < 250 ms | 2. Pacientes con SWPW y síncope con un intervalo RR < 250 ms en presencia de fibrilación auricular o un periodo refractario anterógrado efectivo de la vía accesoria < 250 ms, o la presencia de múltiples vías | |
| 3. Pacientes con SWPW y palpitaciones con TPSV inducible y sostenida en EEF | ||
| Indicaciones para TPSV | 1. TPSV asociada a disfunción ventricular grave | 1. TPSV asociada a disfunción ventricular grave en pacientes > 15 kg |
| 2. TPSV recurrente o incesante si la medicación no es efectiva o no es bien tolerada en pacientes > 15 kg | ||
| 3. TPSV documentada recurrente o incesante cuando la familia desea evitar tratamiento farmacológico de forma crónica en pacientes > 15 kg | ||
| 4. TPSV documentada recurrente que suponga una emergencia para el paciente o requiera cardioversión eléctrica en pacientes > 15 kg | ||
| Indicaciones para TV | 1. TV monomórfica con compromiso hemodinámico tratable con ablación por catéter | 1. TV o EV focales que causen disfunción ventricular cuando la medicación no es efectiva o causa de efectos secundarios intolerables, como alternativa en pacientes > 15 kg |
| 2. TVFP, TVTS o TV con síncope cuando la medicación no es efectiva o causa de efectos secundarios intolerables, como alternativa en pacientes > 15 kg | ||
| Indicaciones para pacientes con CC | 1. TPSV relacionadas con CC específicas, como la presencia de nodos auriculoventriculares gemelos u otras vías accesorias relacionadas con la CC cuando la medicación no es efectiva o presenta efectos secundarios intolerables | |
| 2. Pacientes con SWPW y múltiples vías de riesgo en pacientes con anomalía de Ebstein en pacientes > 15 kg | ||
| 3. Ablación de arritmias auriculares fuera del periodo posoperatorio inmediato (3-6 meses tras la cirugía) cuando el tratamiento médico no es efectivo y presenta efectos secundarios importantes | ||
| 4. TV en pacientes con CC portadores de desfibriladores automáticos implantables con múltiples episodios de TV a pesar de tratamiento farmacológico y reprogramación adecuada del dispositivo |
AEPC/ESC: Association for European Paediatric and Congenital Cardiology/European Society of Cardiology; CC: cardiopatía congénita; EEF: estudio electrofisiológico; EV: extrasístoles ventriculares; HRS/PACES: Heart Rhythm Society/Pediatric and Congenital Electrophysiology Society; SWPW: síndrome de Wolff-Parkinson-White; TPSV: taquicardia paroxística supraventricular; TV: taquicardia ventricular; TVFP: taquicardia ventricular fascicular posterior; TVTS: taquicardia ventricular del tracto de salida.
Aunque en general ambas guías son similares, hay ligeras diferencias en las indicaciones. Por ejemplo, en las indicaciones de ablación clase I para pacientes con síndrome de Wolff-Parkinson-White, si bien ambas guías incluyen como recomendación de clase I la presencia de este síndrome en pacientes con un episodio de muerte súbita recuperada, pacientes con síncope y un intervalo RR < 250 ms, correspondiente a una frecuencia cardiaca de 240 lpm en presencia de fibrilación auricular o un periodo refractario anterógrado efectivo de la vía accesoria < 250 ms, la americana también incluye como factor de riesgo en pacientes con síncopes que tengan más de una vía accesoria. De modo similar, hay diferencias entre ambas sobre el tratamiento de la taquicardia supraventricular paroxística (TSVP) sin preexcitación en pacientes sin cardiopatía, para el cual la guía de AEPC/EHRA solo incluye como indicación de clase I la presencia de TSVP asociada con disfunción ventricular grave. En la guía de HRS/PACES, aparte de la disfunción ventricular, también se incluyen entre las indicaciones de clase I la TSVP recurrente o incesante si la medicación no es efectiva o no se tolera bien en pacientes de peso por encima de unos 15 kg, en caso de deterioro hemodinámico con el síncope como síntoma asociado con la TSVP, o si se requiere cardioversión eléctrica para el tratamiento inicial de pacientes con peso superior a unos 15 kg. Finalmente, también se incluye la preferencia familiar para los pacientes con peso superior a unos 15 kg como una indicación de clase I.
Para el tratamiento de las arritmias ventriculares, las guías no muestran diferencias relevantes y tienen indicación de clase I los pacientes con taquicardia ventricular (TV) sintomática cuando el tratamiento farmacológico no sea efectivo para controlar la arritmia. De todos modos, en la guía de la HRS/PACES también se incluye como indicación de clase I la intolerancia a la medicación y la preferencia familiar como alternativa al tratamiento farmacológico para pacientes con peso por encima de unos 15 kg.
Las indicaciones de tratamiento de ablación de arritmias para pacientes con CC solo son específicas en la guía americana, que incluye como indicación de clase I a los pacientes con TSVP relacionadas con CC específicas, como la presencia de nódulos auriculoventriclares gemelos u otras vías accesorias relacionadas con la CC cuando la medicación no sea efectiva o produzca efectos secundarios intolerables. También tiene indicación de clase I la ablación de múltiples vías de riesgo en pacientes con anomalía de Ebstein, así como el tratamiento de las arritmias auriculares fuera del posoperatorio inmediato (3—6 meses tras la cirugía) cuando el tratamiento médico no sea efectivo y produzca efectos secundarios importantes. Por último, se incluye también como de clase I la ablación de TV en pacientes con CC portadores de desfibrilador automático implantable con múltiples episodios de TV a pesar del tratamiento farmacológico y la reprogramación adecuada del dispositivo, con la intención de evitar que active múltiples terapias.
Ambas guías incluyen menciones específicas para abordar la ablación cardiaca en lactantes y niños menores de 5 años, dado que hay suficiente evidencia para considerar el peso como un factor de riesgo independiente de complicaciones graves, incluso casos de muerte comunicados en la literatura9. Hasta ahora, la guía del AEPC/EHRA definía este grupo de pacientes como aquellos con peso < 15kg, pero en la última guía americana se ha optado por suavizar ligeramente este límite, refiriéndose a pacientes pequeños como aquellos de peso menor de «unos 15 kg». A pesar de esta ligera diferencia en la definición, existe consenso en ser más restrictivo con las indicaciones en este grupo de edad, optimizando el tratamiento farmacológico mediante la inclusión de múltiples combinaciones de fármacos para demorar la ablación cardiaca. Además se recomienda: a) que estos procedimientos sean realizados por electrofisiólogos con experiencia en pacientes pediátricos; b) que la ablación se realice con una estrategia específica que minimice el número de aplicaciones, y c) que se utilice la crioablación antes que radiofrecuencia en sustratos con elevado riesgo de bloqueo auriculoventricular. Por último, se menciona de manera especial el subgrupo de pacientes más pequeños, con pesos entre 3 y 7 kg o menores de 6 meses, en los que solo se debería realizar un procedimiento de ablación cardiaca de arritmias que ponen en riesgo la vida del paciente y una vez que hayan fracasado múltiples combinaciones de fármacos antiarrítmicos.
EFICACIA Y COMPLICACIONES DE LA ABLACIÓN CARDIACA PEDIÁTRICAEl conocimiento sobre la eficacia de la ablación pediátrica proviene fundamentalmente de registros retrospectivos y prospectivos americanos, en los que se observó una mejora en la tasa de ablaciones eficaces del 90,4% en el periodo 1991-1996 y del 95,2% en 1996-19992,3. Estos resultados son muy similares a los de un registro prospectivo con un total de 2.761 pacientes de 41 centros, en el que se observó una eficacia general del 93%4. En Europa existen hasta ahora 2 registros poblacionales de ablación pediátrica, el de Finlandia6 y el de la República Checa7, que muestran una tasa eficacia general final similar al de los registros americanos, en concreto del 91 y el 96% respectivamente. Estudios no poblacionales más recientes muestran una eficacia muy alta (> 98,5%) tanto en pacientes pediátricos (< 12 años) como en adolescentes, pero con una tasa de complicaciones mayor en el grupo de edad < 12 años (5,4%) y una tasa de recurrencias ligeramente mayor (el 25,5 frente al 17,6%)10. Además, se observó que la eficacia de las ablaciones variaba en función de los sustratos, y era superior en la ablación de las taquicardias por reentrada nodular (eficacia del 95-99%), seguida de las vías laterales izquierdas (eficacia > 95% en todas las series) y las taquicardias auriculares focales (eficacia del 93%). Por el contrario, las vías laterales derechas, septales derechas y septales izquierdas presentan eficacias menores, que oscilan entre el 80 y el 90%, resultados similares a los obtenidos en la ablación de las TV (eficacia de alrededor de un 75—80%).
El uso de la crioablación para el tratamiento de diferentes sustratos se ha descrito en múltiples estudios en pacientes pediátricos, con resultados de eficacia aguda entre el 83 y el 98% para las taquicardias por reentrada nodular, inferiores a los obtenidos con radiofrecuencia (95-100%). Además, también presenta una mayor tasa de recidivas que la radiofrecuencia, entre 0 y el 28% según la serie consultada. Estos datos son equiparables a los de un metanálisis reciente que comparó el uso de radiofrecuencia frente a la crioablación para la ablación de la taquicardia por reentrada nodular. En concreto, se observó una eficacia general inicial ligeramente inferior con la crioterapia (riesgo relativo [RR] = 1,44; intervalo de confianza del 95% [IC95%], 0,91-2,28) de manera estadísticamente no significativa, pero con una mayor tasa de recurrencias con la crioterapia (RR = 3,66; IC95%, 1,84-7,28)11.
En los pacientes con CC, la ablación de vías accesorias ofrece resultados ligeramente peores que la comunicada sobre los pacientes sin CC (eficacia de un 80-85%12). La ablación de taquicardias auriculares macroreentrantes en pacientes pediátricos con CC presenta unos resultados de eficacia aguda menores que en pacientes sin cardiopatía, con tasas de eficacia que oscilan entre el 66 y el 97% según la serie consultada, y con tasas de recidiva también mayores, de un 10—60%. Los resultados parecen ser peores en pacientes con transposición de grandes arterias reparadas con técnicas de Senning/Mustard y aquellos con corazones univentriculares y pacientes con reparaciones quirúrgicas en edades avanzadas, así como en los procedimientos realizados con catéteres de punta no irrigada. Estos datos son similares a los de las series de ablación de arritmias auriculares en pacientes adultos con CC13.
Los efectos secundarios inmediatos más relevantes por su gravedad son el bloqueo auriculoventricular permanente, la lesión coronaria aguda, la perforación cardiaca, las lesiones vasculares e incluso casos de muerte relacionada con el procedimiento. Además, entre los efectos secundarios a largo plazo se incluyen los efectos estocásticos de la radiación. Teniendo en cuenta que actualmente más de un 60% de los pacientes pediátricos a los que se realiza una ablación tienen como indicación evitar o suspender el tratamiento farmacológico, y que la gran mayoría de los pacientes no tienen otras comorbilidades7, una complicación grave puede tener consecuencias especialmente dramáticas para la calidad de vida de estos niños. Así pues, es especialmente relevante priorizar el tratamiento farmacológico para los pacientes más pequeños, así como extremar las medidas de seguridad durante los procedimientos de ablación modificando la técnica para ser lo menos agresivos mediante la utilización de catéteres no irrigados, crioablación en los sustratos más cercanos al sistema de conducción, limitación del número, la duración y la energía de las aplicaciones14, y uso de sistemas de navegación electroanatómica.
ESTADO ACTUAL DE LA ABLACIÓN PEDIÁTRICA EN ESPAÑAEn nuestro país, a pesar de que el uso de técnicas de ablación en la edad pediátrica tiene una larga trayectoria, hasta el momento había datos solo de algunos centros15,16. En 1997 se publicó la experiencia inicial de 5 casos de ablación en lactantes menores de 1 año15 y en 1998 se publicó la experiencia inicial de una serie de casos más amplia, con 117 pacientes menores de 18 años, con una tasa de eficacia aguda del 93% y una tasa de recurrencias del 8%16. El artículo de Alonso-García et al.17 publicado recientemente en Revista Española de Cardiología es bienvenido por varios motivos. En primer lugar, porque se trata de una serie amplia que incluye una experiencia dilatada a lo largo de 12 años de un centro de referencia. Esto enfatiza la importancia de que estos procedimientos se realicen en centros donde haya una unidad de arritmias con amplia experiencia en todos los sustratos en pacientes con CC, que además cuente con un servicio de cardiología pediátrica con dedicación especial a las arritmias, con un servicio de cirugía cardiaca pediátrica, y que además disponga de un programa estable de colaboración entre todas estas unidades y un servicio de anestesia pediátrica especialmente dedicado a cardiología pediátrica. Se debe de felicitar a los autores por los excelentes resultados, acordes con los datos publicados en la literatura, tanto en tasa de éxitos como en complicaciones. Sin duda, confirma que la ablación pediátrica puede implementarse con éxito, pero siempre en centros que cumplan estas características.
Dado que uno de los aspectos diferenciales de las ablaciones entre la población adulta y la pediátrica son las indicaciones, es interesante destacar el bajo porcentaje de pacientes de peso < 15 kg, con solo un 7,6% de los casos en la serie publicada. Estos datos están en línea con las recomendaciones actuales de actuación con estos pacientes. Aun así, habría sido interesante disponer de la información sobre las indicaciones de estas ablaciones y el tratamiento farmacológico utilizado antes de indicar la ablación.
Otro factor relevante en el artículo de Alonso-García et al.17 es el uso de la crioablación hasta en el 35,5% de los pacientes. Dado el hecho de que, como en la literatura y en esta serie, las tasas de efectividad y recidivas son más altas que cuando se utiliza radiofrecuencia, habría sido interesante una descripción de las indicaciones de uso de una u otra fuente de energía, así como algunos apuntes sobre la selección de la fuente de energía en la discusión, teniendo en cuenta que los autores comunican una tasa muy baja de bloqueo en ablaciones por reentrada nodular. También habría sido interesante una descripción más detallada de las indicaciones de uso de los sistemas de navegación.
Es importante destacar que, junto con esta serie, desde hace 2 años las ablaciones pediátricas se comunican de forma diferenciada dentro del registro nacional de ablación. En los resultados del registro nacional de ablación de 201618 se documentó que el total de ablaciones realizadas a edad pediátrica solo representaba el 2,3% del total de procedimientos y además se realizaban en múltiples centros. Se debe felicitar por esta iniciativa tanto a los responsables del registro como a los centros que las realizan y registran los resultados, porque ello permite tomar conciencia de que se trata de indicaciones que deben diferenciarse de las de adultos. Por otro lado, enfatiza la necesidad de diferenciar la tasa de éxitos y complicaciones en esta población. Otro dato que queda reflejado en el registro es la dispersión en la atención de los pacientes pediátricos en nuestro país, con un total de 369 procedimientos realizados en 35 centros. Dada la importancia de tener un volumen suficiente en cada unidad para minimizar el potencial efecto negativo de la curva de aprendizaje en estos pacientes19, este dato debe hacernos reflexionar sobre la idoneidad de centralizar los casos en centros con unidades de electrofisiología de alta complejidad y con un alto volumen de casos, que cuenten con equipos de cardiología pediátrica y cardiología de adultos con experiencia en CC y que dispongan de radiofrecuencia, crioablación, navegadores electroanatómicos, un equipo de cirugía cardiaca pediátrica con atención las 24 h del día y unidades de cuidados intensivos pediátricos con experiencia en la atención de pacientes con cardiopatías.
CONFLICTO DE INTERESESNo se declara ninguno.