La enfermedad arterial periférica (EAP) es una manifestación de la enfermedad aterosclerótica y como tal se asocia a mayor morbimortalidad. Estudios epidemiológicos han demostrado que la mayoría de los sujetos permanecen asintomáticos o presentan síntomas atípicos de la enfermedad. Es muy frecuente la relación entre los principales factores de riesgo cardiovascular y la EAP, como el tabaquismo, la diabetes mellitus y la hipertensión. El índice tobillo-brazo (ITB) es un método diagnóstico sencillo y eficaz para el diagnóstico de enfermedad arterial periférica. Numerosos estudios observacionales y ensayos clínicos han demostrado que un ITB bajo (< 0,9), incluso en pacientes asintomáticos, se asocia con mayor riesgo de eventos cardiovasculares y que este riesgo es particularmente alto en individuos con hipertensión y diabetes. En las actuales guías de actuación se ha incluido la determinación del ITB como diagnóstico de EAP y a su vez como factor pronóstico de riesgo de enfermedad, independiente de los factores de riesgo y de la enfermedad cardiovascular, y se señala que el ITB debe tener una función independiente en la predicción de eventos cardiovasculares.
Palabras clave
La enfermedad vascular aterosclerótica es un proceso inflamatorio sistémico y progresivo que puede afectar de forma simultánea a varios territorios vasculares, y la enfermedad arterial periférica (EAP) es una de sus posibles manifestaciones. La EAP afecta a un 15-20% de los sujetos mayores de 70 años, aunque esta prevalencia está subestimada, ya que el síntoma clásico de la arteriopatía periférica (la claudicación intermitente) sólo aparece en un 10% de los sujetos, y la mayoría de ellos (hasta el 50%) tienen síntomas menos específicos (como pérdida del pelo, frialdad de las extremidades y pulsos periféricos débiles) y cerca del 40% permanece asintomático1,2. De esta forma, únicamente el 25% de los individuos con EAP son diagnosticados y tratados3. La principal utilidad de identificar a los sujetos con EAP, aunque ésta sea asintomática, es que se trata de un predictor independiente de enfermedad cardiovascular e incluso se la ha considerado un equivalente de enfermedad coronaria4.
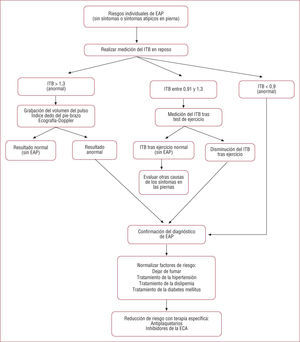
Existen diferentes pruebas para el diagnóstico de la EAP. El índice tobillo-brazo (ITB) es una técnica barata, sencilla, no invasiva y reproducible para el diagnóstico de la arteriopatía periférica. En comparación con la arteriografía de sustracción digital (considerada el estándar para el diagnóstico de EAP), el punto de corte de 0,9 del ITB tiene una sensibilidad del 76% y una especificidad del 90% para el diagnóstico de estenosis > 50%5. Se considera normal un resultado del ITB entre 0,91 y 1,3. El ITB se correlaciona indirectamente con el riesgo cardiovascular y la severidad de la enfermedad vascular, de forma que a menor ITB, mayor riesgo y mayor severidad de las lesiones. Así, un resultado de 0,7-0,9 refleja una obstrucción ligera; 0,4-0,69, una obstrucción moderada, y < 0,4 representa una enfermedad crítica. Un ITB > 1,3 indica una escasa distensibilidad arterial por calcificación vascular, por lo que algunos autores proponen que un ITB alto también se asocia a mayor mortalidad cardiovascular6. Las recomendaciones de la American Heart Association asumen determinar el ITB en pacientes según su riesgo individual y basan la toma de decisiones en el algoritmo actual de diagnóstico y tratamiento de EAP (fig. 1). Se considera que se debe determinar el ITB en sujetos con síntomas de arteriopatía periférica, en aquellos entre 50 y 69 años con algún factor de riesgo cardiovascular y en los individuos con un riesgo estimado a 10 años entre el 10 y el 20%6.
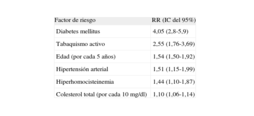
FACTORES DE RIESGO Y ENFERMEDAD ARTERIAL PERIFÉRICAComo la EAP es una manifestación más de la enfermedad aterosclerótica, sus factores de riesgo son los mismos que los de la aterosclerosis en otro territorio vascular, aunque la diabetes mellitus (DM) y el tabaquismo están relacionados más específicamente con la EAP que con la cardiopatía isquémica o el ictus7. En el Cardiovascular Health Study8 se observó que la DM tenía un riesgo relativo (RR) de presentar un ITB < 0,9 de 4,05 y el tabaquismo activo, RR = 2,55. También se observó que la hipertensión arterial (HTA), la hiperhomocisteinemia, la edad y el colesterol total se asociaban de forma significativa con la presencia de EAP (tabla 1). En los resultados del Framingham Heart Study9 se identificaron la edad, el sexo masculino, la concentración de colesterol, la HTA, el tabaquismo, la DM y la enfermedad arterial coronaria como factores de riesgo de claudicación intermitente. Así, en un metaanálisis de la Ankle Brachial Index Collaboration10 se evaluó la combinación del índice de riesgo de Framingham con el ITB para predecir eventos cardiovasculares y mortalidad. Destaca que un ITB < 0,9 se relacionó con el doble de mortalidad total, mortalidad cardiovascular y tasas de eventos coronarios mayores a los 10 años, al compararlos con las diferentes categorías de riesgo del índice de Framingham; se concluyó que la medición del ITB puede mejorar la exactitud de la predicción cardiovascular del riesgo más allá del índice de riesgo de Framingham y determinar la prevalencia de la EAP.
Factores de riesgo independientes de enfermedad arterial periférica
| Factor de riesgo | RR (IC del 95%) |
| Diabetes mellitus | 4,05 (2,8-5,9) |
| Tabaquismo activo | 2,55 (1,76-3,69) |
| Edad (por cada 5 años) | 1,54 (1,50-1,92) |
| Hipertensión arterial | 1,51 (1,15-1,99) |
| Hiperhomocisteinemia | 1,44 (1,10-1,87) |
| Colesterol total (por cada 10 mg/dl) | 1,10 (1,06-1,14) |
IC: intervalo de confianza; RR: riesgo relativo.
Basado en los resultados del Cardiovascular Health Study8.
La HTA es el factor de riesgo cardiovascular más frecuente y se relaciona con la presencia de enfermedad cardiovascular, incluida la arteriopatía periférica, aunque el RR de EAP es menor que con otros factores de riesgo como el tabaquismo o la DM. En el seguimiento de los pacientes de la cohorte de Framingham, los hipertensos tenían 2,5 veces más riesgo de tener EAP que los normotensos11.
Los mecanismos por los que la HTA favorece el desarrollo de arteriopatía periférica no están bien definidos. Alteraciones en la activación plaquetaria y la fibrinolisis, la disfunción endotelial y concentraciones anormales de factores homeostáticos pueden favorecer un estado de estrés oxidativo y el desarrollo de la respuesta inflamatoria que lleva a la formación de la placa aterosclerosa12. Con la HTA se produce un aumento de la presión arterial media y de las resistencias periféricas totales, lo que refleja una reducción en el calibre arteriolar. También la mayor rigidez arterial y la alteración en el tiempo y en la amplitud de la onda de reflexión central hacen que aumente la presión arterial sistólica en sujetos con EAP13. La mayoría de las placas ateroscleróticas en la circulación periférica tienden a aparecer en regiones en las que hay mayores fuerzas hemodinámicas (especialmente las fuerzas de cizallamiento). Estas zonas proaterogénicas suelen ser las bifurcaciones de las grandes arterias (carótidas, aorta y femorales) y el riesgo de que aparezcan estas lesiones está muy aumentado en sujetos hipertensos14. Un aspecto que tener en cuenta en la relación entre HTA y EAP es la frecuente coexistencia de estenosis de las arterias renales, que llega hasta el 34%15. Aunque no parece que la causa principal de la HTA en estos pacientes sea la vasculorrenal, la disminución de la perfusión renal conlleva una mayor activación del sistema renina-angiotensina que exacerba la HTA en estos pacientes.
Numerosos estudios han demostrado la asociación entre la HTA y la EAP. La HTA en sujetos con EAP es frecuente. En un estudio italiano, el 35% de los sujetos con EAP tenían HTA y se demostró que la presencia de ambas entidades tenía una odds ratio (OR) de 1,48 de tener un evento cardiovascular. En ese estudio también se observó que la mortalidad total se asociaba con la presencia de un ITB bajo16. En otro estudio en China, la HTA en sujetos con arteriopatía periférica fue más frecuente (55%)17. Por otro lado, la EAP en población de sujetos hipertensos es menos frecuente. La prevalencia de claudicación intermitente en pacientes con HTA varía entre el 2 y el 5%, y su prevalencia aumenta con la edad. Sin embargo, un ITB < 0,9 en sujetos hipertensos llega hasta el 27,5%18. En este estudio se evaluó el valor pronóstico del ITB en pacientes con HTA, y se observó que un ITB bajo se asociaba a más mortalidad por cualquier causa y mortalidad cardiovascular que entre los sujetos con ITB normal (OR = 1,62; intervalo de confianza [IC] del 95%, 1,11-2,2, y OR = 2,45; IC del 95%, 1,53-3,93, respectivamente). Los autores concluyen que se debería determinar el ITB a todos los individuos hipertensos como estratificación de riesgo. Sin embargo, no todos los estudios han demostrado relación entre la HTA y la arteriopatía periférica. En el Reykjavik Study se encontró que los únicos factores de riesgo relacionados con claudicación intermitente fueron la edad, el tabaquismo y la hipercolesterolemia19.
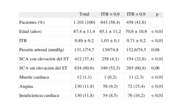
Los estudios previos se realizaron en población general; sin embargo, cuando se analizan los resultados de los estudios de prevención secundaria, la relación entre EAP e HTA es aún mayor. En este sentido, ha sido publicado recientemente el estudio PAMISCA (Prevalencia de Afectación de Miembros Inferiores en el Paciente con Síndrome Coronario Agudo)20, que evalúa la prevalencia y el pronóstico de la EAP (medida por ITB < 0,9) en pacientes que han sufrido un evento coronario agudo (tabla 2); se halló una prevalencia de EAP del 39,8%; es interesante que se observara que únicamente el 33% de los pacientes con un ITB bajo había presentado clínica de claudicación intermitente, lo que refleja la alta prevalencia de EAP subclínica en pacientes con cardiopatía isquémica aguda. En un subestudio en pacientes hipertensos21, se demostró que la prevalencia de arteriopatía periférica es alta en este tipo de pacientes (42,6%) y que la EAP se relaciona con mayor mortalidad hospitalaria (OR = 13; 1,3-82,4), mayor insuficiencia cardiaca tras el síndrome coronario agudo (OR = 1,4; 1,01-2,1) y mayor tasa combinada de mortalidad, insuficiencia cardiaca y angina (OR = 1,4; 1,04-1,9).
Diferencias clínicas y desarrollo de eventos según ITB en el estudio PAMISCA20
| Total | ITB > 0,9 | ITB < 0,9 | p | |
| Pacientes (%) | 1.101 (100) | 643 (58,4) | 458 (41,6) | |
| Edad (años) | 67,4 ± 11,4 | 65,1 ± 11,2 | 70,6 ± 10,9 | < 0,01 |
| ITB | 0,89 ± 0,2 | 1,03 ± 0,1 | 0,71 ± 0,2 | < 0,01 |
| Presión arterial (mmHg) | 131,1/74,7 | 130/74,8 | 132,6/74,5 | 0,08 |
| SCA con elevación del ST | 412 (37,4) | 258 (4,1) | 154 (32,8) | < 0,01 |
| SCA sin elevación del ST | 634 (60,6) | 349 (52,5) | 285 (60,8) | 0,06 |
| Muerte cardiaca | 12 (1,1) | 1 (0,2) | 11 (2,3) | < 0,01 |
| Angina | 130 (11,8) | 58 (9,2) | 72 (15,4) | < 0,01 |
| Insuficiencia cardiaca | 130 (11,8) | 54 (8,5) | 76 (16,2) | < 0,01 |
ITB: índice tobillo-brazo; SCA: síndrome coronario agudo.
Datos presentados como media ± desviación estándar o n (%).
Por lo tanto, teniendo en cuenta la alta prevalencia de EAP (sobre todo subclínica) en sujetos con HTA y su alto valor pronóstico, la medición del ITB debería ser sistemática, especialmente en los pacientes de prevención secundaria. Así lo reflejan las últimas guías de práctica clínica europeas de manejo de la hipertensión, en las que se recomienda la práctica de técnicas de cribado no invasivas para identificar anomalías en la estructura y la función de órganos diana relacionados con la HTA.
DIABETES MELLITUS Y ENFERMEDAD ARTERIAL PERIFÉRICALa DM es uno de los principales factores de riesgo cardiovascular y se la considera un equivalente de enfermedad coronaria. Las complicaciones vasculares de la DM se dividen en microvasculares (neuropatía, nefropatía y retinopatía diabética) y macrovasculares (cardiopatía isquémica, enfermedad cerebrovascular y arteriopatía periférica).
La fisiopatología de la EAP en pacientes diabéticos es la misma que en los no diabéticos; sin embargo, la DM tiende a producir afección vascular más distal. Además, la duración y la severidad de la DM se asocian con la presencia y la extensión de la EAP, del mismo modo que los sujetos diabéticos son más propensos a tener úlceras isquémicas, gangrena y amputación de extremidades inferiores que los sujetos no diabéticos22. También los pacientes con DM que presentan EAP tienen mayor riesgo de sufrir un evento coronario agudo o un ictus23. La resistencia a la insulina es importante en el desarrollo de la EAP, incluso en sujetos sin DM, pues incrementa el riesgo de EAP en un 40-50%24. Del mismo modo, el control de la DM influye en la aparición de EAP, de forma que por cada 1% de incremento en la hemoglobina glicosilada, se produce un incremento del riesgo de EAP del 26%25.
Numerosos estudios han demostrado la relación entre la EAP y la DM. La prevalencia de diabetes en sujetos con EAP es alta. Datos de la cohorte de Framingham reflejan que el 20% de los sujetos con síntomas de EAP eran diabéticos9. En el estudio de Rein et al26 se vio que el 38,7% de los sujetos con arteriopatía periférica eran diabéticos, el 26,1% de los no diabéticos tenían alteración en el test de sobrecarga oral de glucosa y el 23,5% de los sujetos con tolerancia normal a la glucosa presentaba alteración de la glucosa basal, por lo que se demuestra que los sujetos con EAP tienen una gran prevalencia de alteraciones del metabolismo de la glucosa. Sin embargo, la presencia de EAP en sujetos con DM es menos conocida por la mayor proporción de individuos asintomáticos que entre los no diabéticos, debido a que la presencia de neuropatía periférica puede alterar la sensibilidad al dolor y hace que la claudicación intermitente y la ausencia de pulsos distales tengan menor valor diagnóstico en este grupo de sujetos23. Los estudios que han empleado el ITB demuestran una prevalencia de EAP en sujetos diabéticos en torno a un 20-30%27. En España, Vicente et al28 demostraron que la prevalencia de un ITB bajo en sujetos con DM era del 11,3%, mientras que el 18,8% tenía un ITB patológico (< 0,9 o > 1,4), en comparación con el 4,3 y el 7%, respectivamente, de los individuos sin DM. Tras el análisis multivariable, los únicos factores independientes fueron la edad y los años de evolución de la DM28.
Diferentes estudios también han demostrado la utilidad de determinar el ITB como factor pronóstico. En este sentido, el Fremantle Diabetes Study29 evaluó la incidencia de EAP y su valor pronóstico en sujetos con DM. Se observó que la prevalencia de EAP era del 13,6% y la incidencia, del 3,7% por año durante el seguimiento. Se demostró que un ITB bajo se asociaba con mayor mortalidad cardiaca, con un incremento del riesgo del 67%. De igual modo, el PROactive Study30 demostró que el 32,1% de los sujetos diabéticos tenían EAP (valorada mediante una escala de síntomas y el ITB < 0,9), y que la EAP se relacionaba significativamente con mayor tasa del objetivo primario (combinado de mortalidad por todas las causas, infarto de miocardio no fatal, ictus, síndrome coronario agudo, tratamiento intervencionista o quirúrgico de arterias coronarias o de las piernas y amputación por debajo del tobillo), con OR = 1,64 (1,44-1,86), del objetivo secundario (tiempo hasta la muerte, infarto de miocardio no fatal o ictus), con OR = 1,46 (1,24-1,73) y de cada uno de los eventos por separado.
Por lo tanto, es evidente que la correlación entre la EAP y la DM es frecuente, los sujetos con DM suelen tener peor evolución de su arteriopatía que los no diabéticos y que la EAP supone un incremento del riesgo cardiovascular en estos sujetos. En este sentido, la American Diabetes Association recomienda determinar el ITB a todos los sujetos diabéticos mayores de 50 años y a los menores de 50 que tengan otro factor de riesgo adicional o una DM de más de 10 años de evolución. En caso de que la prueba sea normal, se debe repetir cada 5 años o cuando aparezcan síntomas o signos de EAP. En caso de que el resultado sea positivo, se aconseja un manejo terapéutico agresivo para disminuir el riesgo cardiovascular23.
CONCLUSIONESLos pacientes hipertensos y diabéticos presentan un mayor riesgo cardiovascular, que se incrementa de forma importante en presencia de EAP demostrada, aunque ésta sea asintomática. El ITB es útil tanto para valorar el diagnóstico de EAP como para estimar su pronóstico, de forma que un valor < 0,9 se asocia con mayor incidencia de eventos, tanto en sujetos hipertensos como en diabéticos. Por lo tanto, para mejorar la estratificación del riesgo cardiovascular en pacientes con HTA o DM, la determinación del ITB debe formar parte de la práctica clínica diaria, tal y como recomiendan las guías de práctica clínica actuales, para valorar la presencia de enfermedad cardiovascular y poder tomar una actitud terapéutica más agresiva para evitar la aparición de complicaciones cardiovasculares.