La nueva edición de la guía de práctica clínica de la Sociedad Europea de Cardiología sobre valvulopatías1 actualiza la versión previa del año 2017. Esta revisión está justificada por importantes cambios epidemiológicos (incidencia creciente de las etiologías degenerativas frente a la reumática), evidencia clínica cada vez más sólida acerca del valor de biomarcadores moleculares y de imagen (ecocardiografía 3D y resonancia magnética cardiaca) para la toma de decisiones y, sobre todo, resultados de ensayos clínicos aleatorizados relativos al tratamiento de la insuficiencia mitral (IM) secundaria a los tratamientos antitrombóticos en pacientes portadores de prótesis valvular tras intervención quirúrgica o percutánea, así como en la estratificación del riesgo y la selección del momento óptimo de intervención2. El documento resultante es extenso (54 páginas de texto seguidas de más de 550 referencias) y en su tabla 3 recoge en detalle las nuevas recomendaciones actualizadas en esta edición del documento. A continuación, agrupamos los aspectos que consideramos más novedosos.
REFUERZO DE LOS CENTROS ESPECIALIZADOS Y LAS DECISIONES TERAPÉUTICAS COLEGIADASEl documento enfatiza la figura de los centros de referencia en valvulopatías para así garantizar la atención de calidad centrada en el paciente. En este sentido, se enumeran en detalle los requisitos que deben de cumplir estos centros. No solo deben concentrar un gran volumen de actividad en los distintos procedimientos diagnósticos y terapéuticos, sino que deben contar con una auditoría periódica de sus resultados. Además, se refuerza la necesidad de colegiar las decisiones terapéuticas entre los distintos especialistas y subespecialistas que intervienen en el proceso (heart team). Por primera vez, entre ellos se introduce la figura de la enfermería especializada en la atención a los pacientes con enfermedad valvular.
CAMBIOS EN LOS CRITERIOS DE CUANTIFICACIÓN Y SUS INDICACIONES DE INTERVENCIÓNEl documento destaca el papel de la ecocardiografía en el diagnóstico y el tratamiento de las valvulopatías y el importante valor adicional de la ecocardiografía transesofágica 3D y la tomografía computarizada (TC) en la selección de los pacientes para tratamiento quirúrgico o percutáneo. La ecocardiografía transesofágica 3D es muy útil para detallar la anatomía valvular y valorar su reparabilidad y es fundamental para guiar los procedimientos percutáneos sobre la válvula mitral o tricúspidea. La angio-TC es esencial en la planificación de los procedimientos percutáneo para valorar los accesos vasculares y las estructuras anatómicas implicadas en cada procedimiento.
La guía no modifica sustancialmente los índices de cuantificación de las valvulopatías. Subraya las posibles limitaciones del cálculo del área valvular en la estenosis aórtica3 y la importancia de controlar la presión arterial durante el estudio. La guía destaca la utilidad de la TC para cuantificar la calcificación de la válvula aórtica, sobre todo en pacientes con estenosis aórtica con bajo flujo/bajo gradiente paradójico. En los pacientes con valvulopatía aórtica, es muy importante valorar el tamaño de la aorta ascendente, y se aconseja realizar una TC cuando el diámetro por ultrasonidos supere los 40 mm. Se establece la metodología de medición de la aorta, que se recomienda en la raíz la medida del diámetro máximo entre senos. Además, se enfatiza la importancia de integrar varios parámetros ecocardiográficos aun considerando el valor pronóstico del orificio regurgitante efectivo en la IM.
Aunque los diámetros ventriculares y la fracción de eyección (FE) son buenos parámetros para valorar la función del ventrículo izquierdo (VI), la guía recoge el potencial valor del strain longitudinal global, especialmente con valores de FE en el límite de la indicación de cirugía. En este sentido, la resonancia magnética cardiaca puede ser de gran ayuda cuando la información por ultrasonidos no sea definitiva, particularmente para la valoración del ventrículo derecho y la determinación de la fibrosis miocárdica.
INDICACIONES DE INTERVENCIÓN PARA PACIENTES ASINTOMÁTICOSLa decisión de intervenir a un paciente asintomático con valvulopatía grave es uno de los mayores desafíos. En general, nos basamos en parámetros que indican daño miocárdico y han mostrado un empeoramiento del pronóstico. En otras palabras, llegamos tarde, pues se interviene a un paciente cuando ya tiene signos que predicen una evolución desfavorable. Los estudios aparecidos en los últimos años aportan evidencia suficiente para ser más estrictos con esos puntos de corte y esto se refleja en la guía. Un aspecto importante es la mayor mortalidad de las mujeres con estenosis aórtica frente a los varones, que probablemente esté relacionada con un retraso en el diagnóstico y la indicación de intervención. También se constata una mayor incidencia de insuficiencia cardiaca después de la reparación de válvula mitral en las mujeres, probablemente debida a grados más avanzados de la enfermedad en el momento de la cirugía. Estos factores se han tenido especialmente en cuenta en las insuficiencias valvulares.
Así, para los pacientes con insuficiencia aórtica grave asintomática desaparece la recomendación basada en el diámetro telediastólico del VI, se refuerza la recomendación basada en el diámetro telesistólico (> 50 mm o >25mm/m2), que pasa de IIa a I, y se incluye como recomendación IIb la cirugía si es> 20mm/m2. Además, se mantiene la recomendación basada en la FE del VI (FEVI) (< 50%; recomendación I, nivel de evidencia B) pero se incluye una FEVI <55% como indicación IIb. De la misma manera, en la IM primaria asintomática, se mantiene como punto de corte la FEVI del 60% con recomendación I y nivel de evidencia B, pero se disminuye el punto de corte del diámetro telesistólico del VI de 45 a 40 mm.
En la estenosis aórtica grave asintomática hay cambios llamativos. En primer lugar, se ha sustituido «reemplazo quirúrgico de válvula» por «intervención», aceptando la posibilidad de que estudios ya en marcha establezcan alguna indicación del tratamiento percutáneo para pacientes asintomáticos. Se hace énfasis en la indicación según la FEVI: se aumenta el nivel de evidencia para FEVI ≤ 50% (de C a B) y se incluye una recomendación IIa para la FEVI ≤ 55%. El resto de los indicadores de peor pronóstico (estenosis muy grave, calcificación grave, progresión o aumento de BNP) aumentan su nivel de evidencia de C a B. La definición de «muy grave» es menos estricta (se pasa de velocidad máxima> 5,5 a> 5 m/s). Si bien hay trabajos que muestran una mayor mortalidad al operar a pacientes con este grado de estenosis, la evidencia de la relación del resto de parámetros con el pronóstico es débil, pues los trabajos referidos consideran evento no solo la mortalidad, muy baja, sino también la intervención quirúrgica, que es el evento predominante4. Una recomendación IIa con nivel de evidencia B parecería, pues, de demasiado peso.
La guía mantiene la recomendación de operar a pacientes asintomáticos con valvulopatía grave si está indicada la cirugía de revascularización, de la aorta ascendente o de otra válvula. Para los pacientes con indicación de cirugía no cardiaca, se remite a la guía específica. En general, en pacientes asintomáticos, la estenosis aórtica grave es la valvulopatía que puede causar más complicaciones en el perioperatorio de la cirugía no cardiaca, por lo que, si el procedimiento no es urgente y el riesgo es alto, se aconseja intervenir la válvula aórtica antes de la cirugía no cardiaca.
OPCIONES DE INTERVENCIÓN EN LA ESTENOSIS AÓRTICAPara los pacientes con estenosis aórtica grave sintomática, la guía mantiene las mismas recomendaciones de tratamiento para los diferentes subgrupos basados en el gradiente de presión transvalvular medio y el gasto cardiaco (flujo transvalvular aórtico)1. Sin embargo, esta nueva edición presenta cambios en cuanto al modo de tratamiento. Los estudios clínicos aleatorizados en pacientes con estenosis aórtica grave sintomática y riesgo quirúrgico intermedio y bajo han demostrado la no inferioridad en cuanto a la seguridad y eficacia del implante percutáneo de válvula aórtica, comparada con el reemplazo quirúrgico5. Además, el implante percutáneo tiende a ser superior al quirúrgico cuando el primero se realiza por vía transfemoral. Es importante resaltar que los pacientes con riesgo quirúrgico intermedio y bajo incluidos en esos estudios fueron predominantemente varones y con edad> 75 años en el 40% de los casos. Se excluyó a pacientes con bajo gasto cardiaco y características anatómicas desfavorables (válvula aórtica bicúspide o enfermedad coronaria de 3 vasos). Por consiguiente, el nuevo documento resalta la importancia de la discusión multidisciplinaria (heart team) considerando las características clínicas, anatómicas y del procedimiento, y por primera vez se recomienda explícitamente que la decisión sea consensuada con el paciente. En pacientes jóvenes (< 75 años) con bajo riesgo quirúrgico (STS-PROM o EuroSCORE II <4%) que no tengan contraindicada la cirugía, el remplazo quirúrgico de la válvula aórtica recibe una indicación de clase I. También la cirugía es una indicación de clase I para pacientes que no la tengan contraindicada pero que sí tengan contraindicación para implante transfemoral. En pacientes mayores de 75 años con alto riesgo quirúrgico (STS-PROM o EuroSCORE II <8%) o contraindicaciones para la cirugía, el implante percutáneo obtiene una recomendación de clase I6. Para el resto de los pacientes, tanto el implante percutáneo como el quirúrgico reciben una recomendación de clase I. El implante percutáneo por un acceso diferente del transfemoral puede considerarse para pacientes inoperables cuando la vía transfemoral no esté practicable (recomendación de clase IIb)7. La guía también destaca que debe considerarse siempre la relación entre la durabilidad de las bioprótesis aórticas y la esperanza de vida del paciente (relacionada no solo con la edad, sino también con el sexo, la fragilidad, las comorbilidades y el riesgo de futilidad).
OPCIONES DE INTERVENCIÓN DE LA VÁLVULA MITRALLa nueva guía incluye importantes aportaciones en lo que se refiere a las indicaciones de intervención sobre la válvula mitral, concretamente en la IM. La expansión y consolidación de las técnicas de reparación quirúrgica en la enfermedad degenerativa y los excelentes resultados en centros experimentados han permitido adelantar la indicación de intervención para pacientes asintomáticos con IM degenerativa (véase el apartado sobre la reducción del criterio de diámetro telesistólico). Destacable es la apreciación de la intervención precoz en pacientes asintomáticos solo se justifica cuando la reparación quirúrgica tenga alta probabilidad de ser duradera y se lleve a cabo en un centro experimentado. Se subraya la importancia de la concentración de la experiencia en valvulopatías con distintas técnicas para tratar a estos pacientes.
Por otro lado, el avance de las técnicas de reparación percutánea de la IM, principalmente con la técnica borde a borde (transcatheter edge to edge repair [TEER]), ha significado un auténtico revulsivo en la nueva edición de la guía. En la IM primaria, la cirugía de válvula mitral es la estrategia de tratamiento recomendada, y se introduce la consideración de TEER (recomendación IIb) para los casos considerados inoperables tras la valoración multidisciplinaria. Para la IM secundaria sintomática a pesar del tratamiento médico óptimo, se introduce la recomendación de clase I de actuar sobre la válvula, bien con cirugía o intervencionismo, con una recomendación de nivel IIa de la aplicación de la técnica de TEER en pacientes con IM secundaria crónica no candidatos a cirugía. La indicación se circunscribe a pacientes sintomáticos con IM secundaria grave (definida ahora en esta guía por un orificio regurgitante efectivo de 30mm2, y no de 20 como en la previa) ya en un tratamiento médico optimizado que incluya la resincronización cardiaca si tiene indicación. En pacientes de estas características y con enfermedad coronaria concomitante que requiere tratamiento, si el riesgo quirúrgico es alto, aparece una nueva recomendación de clase IIa para el tratamiento coronario percutáneo seguido de TEER. Esta indicación también se recomienda en caso de un paciente que requiera implante de percutáneo de válvula aórtica (TAVI). Para los pacientes que van a someterse a cirugía de revascularización coronaria se mantiene la indicación de clase I de cirugía valvular concomitante sobre la válvula mitral en caso de IM secundaria grave. La técnica quirúrgica debe individualizarse atendiendo a la anatomía de la válvula mitral y los ventrículos (reparación, sustitución). Para pacientes con IM secundaria grave sin otra enfermedad cardiaca o coronaria concomitante que siguen sintomáticos con el tratamiento médico optimizado, la TEER se recoge como una indicación más sólida, con clase IIa (antes IIb), para aquellos con contraindicación para cirugía y criterios predictores de buena respuesta a este tratamiento, como es IM muy grave, ventrículos menos dilatados y FEVI> 30%8. Esta indicación se mantiene en clase IIb para los demás pacientes, salvo con FEVI <15%. Así, en esta edición de la guía se recoge como opción recomendable el tratamiento quirúrgico de la IM secundaria en pacientes con FEVI entre el 15 y el 30%, mientras que en la versión anterior el corte inferior estaba establecido en 30%. Puesto que no se sustenta en nueva evidencia original, este cambio de recomendación de la cirugía para la IM secundaria parece resultado de extrapolar a la opción quirúrgica los resultados de los ensayos clínicos con TEER.
EL TRATAMIENTO DE LA VÁLVULA TRICÚSPIDEEl interés en la válvula tricúspide surge en respuesta a estudios que muestran que la insuficiencia tricuspídea (IT) funcional o secundaria sigue siendo una entidad infratratada, pero que tiene mal pronóstico. La guía abunda en la evaluación ecocardiográfica para cuantificar adecuadamente la gravedad e insisten en el abordaje multiparamétrico en recurrir a la imagen multimodalidad en caso necesario. Se destaca la superioridad de la valoración biplanar o el área guiada por ecocardiografía 3D de la vena contracta sobre la medida convencional bidimensional y se incorporan los términos de gradación massive (cuantiosa) y torrential (torrencial) por su implicación pronóstica. Se mantienen las indicaciones quirúrgicas para pacientes sintomáticos con estenosis o IT primaria grave y pacientes sometidos a cirugía valvular izquierda. Esta indicación se fundamenta en que la IT grave no tratada puede no mejorar después del tratamiento de la válvula del lado izquierdo con la reducción de la poscarga del ventrículo derecho. Además, la reintervención por IT recurrente conlleva una mayor mortalidad, y abordar la válvula tricúspide conjuntamente con la cirugía del lado izquierdo no supone mayor riesgo quirúrgico9. Por otro lado, se han introducido cambios en otros 2 aspectos: a) tendencia a operar antes a los pacientes asintomáticos con IT primaria grave a los que se considera aptos para cirugía, y b) indicaciones de dispositivos percutáneos para pacientes con IT secundaria grave inoperables.
Algunos aspectos importantes de la IT quedan sin resolver en esta versión del documento. No se proponen enfoques multiparamétricos de cuantificación de la IT que integren otros parámetros clínicos y ecocardiográficos asociados con el pronóstico (coaptación, anillo, acoplamiento ventriculoarterial pulmonar)9. La resonancia magnética cardiaca puede tener mayor utilidad de lo que refleja la guía, particularmente la valoración de los volúmenes y la FE del ventrículo derecho. Encontrar puntos de corte que predigan mejor el pronóstico probablemente mejoraría la selección del momento quirúrgico. No se discute el papel del diagnóstico invasivo en la IT secundaria a fibrilación auricular (FA) para desenmascarar disfunción diastólica o IM significativa que pasen inadvertidas por la reducción de la precarga del VI secundaria a IT. Los diuréticos pueden disminuir drásticamente la gravedad de la IT secundaria a insuficiencia cardiaca con FE reducida o conservada. Al contrario que en el documento de la ESC/EACTS, la guía norteamericana recomienda el tratamiento médico gradual dirigido (IIa) y señala la necesidad de revaluar la gravedad de la insuficiencia después de optimizar el tratamiento médico10. Respecto a la reparación percutánea de la IT secundaria, las características de los potenciales candidatos a estas técnicas no quedan aclaradas.
PAPEL DE LOS ANTICOAGULANTES ORALES DE ACCIÓN DIRECTAUna parte importante de la innovación de la presente revisión de la guía se concentra en el tratamiento antitrombótico de los pacientes portadores de prótesis valvulares. En relación con la prescripción de fármacos antitrombóticos para pacientes valvulares, la guía recomienda los anticoagulantes orales de acción directa (ACOD) para los pacientes portadores de prótesis biológicas y en FA a partir de los 3 meses del implante valvular. La seguridad y la eficacia de los ACOD en las bioprótesis durante los primeros 3 meses tras el implante quirúrgico o percutáneo de la válvula no está establecida claramente. Según la guía, se puede considerar los ACOD durante los primeros 3 meses tras el implante quirúrgico de una bioprótesis mitral en pacientes con y sin FA, pero la recomendación es de clase IIb y el nivel de evidencia C, pues el número de pacientes aleatorizados en los ensayos RIVER11 y ENAVLE12 en los primeros 3 meses tras el implante valvular era pequeño. En el ensayo RIVER (rivaroxabán frente a warfarina) se evaluó exclusivamente a pacientes con prótesis mitral y tan solo el ensayo ENAVLE (edoxabán frente a warfarina), con solo 220 enfermos, incluyó a pacientes con prótesis aórticas biológicas. Por esta razón, para los pacientes sin indicación basal de anticoagulación y los portadores de una prótesis aórtica biológica, la guía recomienda dosis bajas de ácido acetilsalicílico (75-100mg/día) o anticoagulación con antagonistas de la vitamina K (AVK) durante los primeros 3 meses tras la cirugía (recomendación IIa). En lo que respecta a pacientes con FA y enfermedad de válvula nativa, se recomiendan los ACOD en caso de estenosis aórtica, insuficiencia aórtica o IM. Los pacientes con estenosis mitral y FA deben ser anticoagulados con AVK.
ANTICOAGULACIÓN EN PORTADORES DE PRÓTESIS PERCUTÁNEAS Y MECÁNICASOtro de los cambios sustanciales reside en el tratamiento antitrombótico de los pacientes portadores de prótesis percutáneas. Así, según los resultados del estudio POPular TAVI, se recomienda antiagregación simple a largo plazo (Ia) frente a la indicación de antiagregación doble planteada en la guía previa13. Si el paciente tiene indicación de anticoagulación crónica, dada la ausencia de evidencia, no se aclara qué tipo de anticoagulante utilizar. Tras la publicación de esta guía, se han conocido los resultados del estudio ENVISAGE, en el que se demuestra la no inferioridad del tratamiento con edoxabán frente a los AVK en este grupo de pacientes, pero se ha comunicado un mayor riesgo hemorrágico en el grupo de ACOD14.
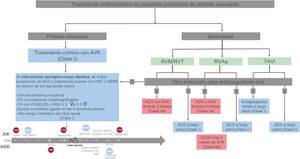
Para los pacientes portadores de prótesis mecánica se mantiene la indicación de tratamiento con AVK. Las nuevas recomendaciones se concentran en el tratamiento durante el periodo perioperatorio. Aunque basadas en el consenso de expertos (nivel C), aclaran puntos importantes, como cuándo suspender el tratamiento con AVK, a qué pacientes prescribir un tratamiento puente con heparina, cuándo reiniciar la anticoagulación en el posoperatorio y la elección del tratamiento antiagregante plaquetario concomitante (figura 1). A este efecto, es llamativo que se recomiende tratamiento puente en caso de puntuaciones CHA2DS2-VASc más bajas que las recogidas en otros documentos de consenso de la Sociedad Europea de Cardiología.
Anticoagulación para pacientes portadores de prótesis valvulares quirúrgicas y percutáneas. AAS: ácido acetilsalicílico; ACO: anticoagulación oral; ACOD: anticoagulantes orales de acción directa; AVK: antagonistas de la vitamina K; HBPM: heparina de bajo peso molecular; HNF: heparina no fraccionada; RQVA: recambio quirúrgico de válvula aórtica; RVM: recambio o reparación de válvula mitral; RVT: recambio o reparación de válvula tricúspide; TAVI: implante percutáneo de válvula aórtica.
Por último, en línea con las recomendaciones de la reciente guía para el tratamiento del sídrome coronario agudo15, para los pacientes sometidos a ICP con indicación de anticoagulación se reduce el tiempo de tratamiento antitrombótico triple a 1 semana (Ib), manteniendo el tratamiento posterior con clopidogrel hasta 6-12 meses en función del riesgo trombótico. En cualquier caso, estas pautas han de ser siempre individualizadas.
SELECCIÓN DE PRÓTESIS VALVULARES Y PROCEDIMIENTOS DE CIERRE DE LA OREJUELALa guía recomienda la reparación valvular frente al recambio por prótesis, siempre y cuando se pueda prever que los resultados serán duraderos y funcionalmente eficaces (especialmente en la IM). Respecto a la elección del tipo de prótesis que se debe implantar cuando sea imprescindible, la guía sigue manteniendo como principal recomendación (clase I) la decisión consensuada con el paciente de acuerdo con sus preferencias y su estilo de vida y considerando aspectos que van más allá de la edad o la expectativa de vida y la durabilidad de la prótesis. La existencia de alguna contraindicación formal para la anticoagulación oral con AVK excluye las prótesis mecánicas, dado que los ACOD están formalmente contraindicados con este tipo de prótesis. La edad cronológica o la expectativa de vida del paciente tienen un nivel de consideración menor (clase IIa), y tienen que equilibrarse con la durabilidad estimada de la prótesis biológica (al menos 10 años las quirúrgicas y no establecida para las percutáneas). Se mantiene la recomendación de prótesis mecánicas para los menores de 60 años en posición aórtica y menores de 65 en posición mitral, así como prótesis biológicas para los mayores de 65 años en posición aórtica y mayores de 70 en mitral.
Sin embargo, ante la falta de evidencia aleatorizada y contrastada, la guía no recoge otros aspectos potencialmente relevantes e indudablemente controvertidos. La posibilidad de llevar a cabo implantes percutáneos en prótesis biológicas degeneradas (siempre y cuando sean de tamaño suficiente) disminuiría el riesgo de intervención y tal vez permitiría bajar la edad de recomendación del primoimplante de la prótesis biológica. No obstante, el explante quirúrgico de una prótesis percutánea es un procedimiento extremadamente complejo, por lo que en pacientes muy jóvenes la prótesis biológica no sería recomendable como sustituto protésico inicial. La utilidad de dosis bajas de ACOD tras el implante de prótesis aórticas mecánicas está por determinar, con ensayos clínicos en marcha (NCT04142658) que, en caso de obtenerse resultados positivos, también permitirían modificar la edad de indicación de este tipo de prótesis.
En cuanto al cierre de la orejuela izquierda durante el procedimiento quirúrgico, se ha aumentado la recomendación (de clase IIb a IIa) para pacientes con CHA2DS2-VASc> 2 y FA, fundamentalmente a raíz de la publicación del ensayo clínico LAAOS III16. Tras cirugía cardiaca de cualquier tipo, el cierre de la orejuela izquierda disminuye la aparición de accidentes cerebrovasculares o embolias sistémicas. Los métodos de cierre de la orejuela en el citado estudio estaban claramente especificados, y se aceptan la escisión y cierre, la sutura interna directa o el uso de dispositivos de clip específicos. No se aceptaba explícitamente el cierre de la orejuela por ligadura simple, por lo que este método debe descartarse.
ABORDAJE Y TRATAMIENTO DE LA DISFUNCIÓN PROTÉSICALa guía mantiene la recomendación de seguimiento clínico y ecocardiográfico anual de los pacientes estables portadores de bioprótesis valvular (quirúrgica o percutánea). Se incide en el empleo de diferentes técnicas de imagen ante sospecha de disfunción protésica, comenzando con el ecocardiograma transtorácico. Se recomienda la ecocardiografía transesofágica sistemática ante sospecha de trombosis, endocarditis o fuga paravalvular (especialmente en posición mitral). La fluoroscopia, o en su defecto la TC si está disponible, permite evaluar la movilidad de los discos oclusores. La TC tiene un papel importante en el diagnóstico diferencial entre trombo y pannus.
La primera opción para el tratamiento de la disfunción bioprotésica es la cirugía. Sin embargo, el tratamiento percutáneo valve-in-valve puede ser una alternativa en pacientes con alto riesgo, ya sea en posición aórtica mediante abordaje transfemoral con características anatómicas favorables (IIa B) o en posición mitral y tricuspídea (IIb B). Se requiere una planificación detallada para evitar complicaciones como la obstrucción coronaria o del tracto de salida del VI. El tratamiento valve-in-ring puede ser aceptable en pacientes seleccionados, especialmente en posición mitral, y debe ser el equipo multidisciplinario el que individualice cada caso.
El tratamiento de elección de las dehiscencias periprotésicas continúa siendo quirúrgico en presencia de endocarditis o hemolisis con síntomas graves, pero el cierre percutáneo aumenta su nivel de recomendación a IIa B para los pacientes sintomáticos con alto riesgo quirúrgico.
El tratamiento agudo de la trombosis protésica no ha cambiado respecto a la versión previa. En términos generales, la cirugía es la opción preferida para la trombosis obstructiva en pacientes críticos o no obstructiva con trombo> 10 mm o fenómenos embólicos. La fibrinolisis se reserva para los casos en que la cirugía no es posible, los pacientes con muy alto riesgo quirúrgico o con trombosis en prótesis derechas. Se recomienda la anticoagulación por tiempo indefinido tras un evento de trombosis de una válvula biológica. La evaluación por TC tras el TAVI evidencia una elevada prevalencia de engrosamiento e hipoatenuación de velos, con un significado incierto. Si este hallazgo se acompaña de una reducción de movilidad de velos y aumento de gradientes, se puede considerar la anticoagulación completa.
TRATAMIENTO DE LAS VALVULOPATÍAS EN EL EMBARAZONo hay grandes cambios con respecto a la edición previa sobre el abordaje y tratamiento de las valvulopatías durante el embarazo. La guía destaca nuevamente la conveniencia de discutir el abordaje de las valvulopatías antes y durante la gestación en un equipo que incluya anestesistas, obstetras y neonatólogos. Se recuerda que, para las mujeres con una válvula mecánica, especialmente en la posición mitral, la gestación se asocia con alto riesgo de complicaciones maternas y fetales que hay que tratar cuidadosamente con la paciente antes del embarazo. Se dan recomendaciones específicas sobre el tratamiento de la estenosis mitral con área <1,5cm2 durante el embarazo. En la estenosis aórtica grave sintomática, se recomienda valvuloplastia aórtica siempre que persistan los síntomas a pesar del tratamiento médico. Se recuerda el prometedor papel del TAVI en este contexto. Debido a la alta mortalidad fetal, la cirugía con derivación cardiopulmonar debe restringirse a los casos en que la intervención percutánea no sea posible o haya fallado y la vida de la madre se vea amenazada. Se establecen recomendaciones específicas de parto por cesárea para las pacientes con estenosis aórtica o mitral grave, diámetro de la aorta ascendente> 45 mm o hipertensión pulmonar grave o que comienzan con dinámica de parto durante el tratamiento con AVK o en un plazo de 2 semanas tras suspenderlos. Se mantienen las recomendaciones en cuanto a la anticoagulación de las gestantes con prótesis mecánicas y se recuerda que el seguimiento de estas pacientes debe realizarse en centros especializados.
ÁREAS CON FALTA DE EVIDENCIA Y ASPECTOS NO RECOGIDOSAl igual que en las ediciones previas, la guía recoge en un apartado específico las áreas en que la evidencia científica es insuficiente para realizar recomendaciones sólidas. Sobre los pacientes con estenosis aórtica, se destaca la falta de información sobre la eficacia y la seguridad de los ACOD en pacientes con recambio valvular durante los 3 meses posteriores al procedimiento, la ausencia de estudios que comparen las durabilidades de las prótesis quirúrgicas y las percutáneas, el papel de la intervención en pacientes asintomáticos o el de la revascularización en pacientes con estenosis grave y enfermedad coronaria asintomática subyacente. En el campo de la IM, la falta de información se centra en los resultados a largo plazo de las intervenciones percutáneas, las indicaciones de dichas técnicas para pacientes con insuficiencia grave de etiología primaria y riesgo quirúrgico bajo, así como el potencial beneficio en supervivencia con la intervención valvular (percutánea o quirúrgica) en pacientes con insuficiencia grave secundaria. En cuanto a la IT, es controvertido el momento de la cirugía para pacientes con etiología primaria y el abordaje de la etiología secundaria. Por otra parte, los ensayos clínicos que evalúan la seguridad y la eficacia de las emergentes técnicas de tratamiento percutáneo son muy escasos.
La guía enfatiza el empleo sistemático de la ergometría convencional en el seguimiento de los pacientes asintomáticos con enfermedad valvular. Sin embargo, no hace referencia a las potenciales ventajas de la ergoespirometría para este grupo de enfermedades. Tampoco recoge la indicación de rehabilitación cardiaca tras la corrección de la valvulopatía, a pesar de que existe evidencia favorable17.
CONCLUSIONESEsta revisión de la guía llega en un momento de transición en el que se incorporan los resultados de múltiples ensayos clínicos aleatorizados en materias como el tratamiento antitrombótico tras la intervención o la reparación mitral percutáneas. Sin embargo, la falta de evidencia a muy largo plazo (> 5 años) todavía impide establecer inequívocamente el papel de las técnicas de TAVI en pacientes jóvenes con bajo riesgo. A pesar del avance de las técnicas de imagen en los últimos años, la guía enfatiza el papel central que siguen desempeñando la anamnesis, la exploración física, la ecocardiografía convencional y la ergometría (en pacientes asintomáticos) para el diagnóstico y el seguimiento de los pacientes con valvulopatías. En el momento de considerar las indicaciones de corrección, se debe empoderar al paciente. Así, en esta nueva edición del documento se destaca el papel que deben tener los profesionales para hacer al paciente partícipe de las decisiones terapéuticas que le afectan. La combinación de sus preferencias con aspectos objetivos como edad y sexo, comorbilidades, fragilidad y la potencial futilidad del tratamiento deben integrarse en un ámbito común de decisión colegiada.
FINANCIACIÓNNinguna.
CONFLICTO DE INTERESESLos documentos de declaración de conflicto de intereses de todos los autores se pueden consultar en el material adicional.
Grupo de Trabajo para la guía ESC/EACTS 2021 sobre el diagnóstico y tratamiento de las valvulopatías: Pablo Avanzas (coordinador), Javier Bermejo (coordinador), Manuel Barreiro-Pérez, Belén Cid, Victoria Delgado, J. Alberto San Román, Arturo Evangelista, Pastora Gallego, Francisco Javier García Aranda, José López-Menéndez, Marta Sitges e Isidre Vilacosta.
Comité de Guías de la SEC: Pablo Avanzas, Gemma Berga Congost, Araceli Boraita, Héctor Bueno, David Calvo, Raquel Campuzano, Victoria Delgado, Laura Dos, Ignacio Ferreira-Gonzalez, Juan José Gomez Doblas, Domingo Pascual Figal, Antonia Sambola, Ana Viana Tejedor, José Luis Ferreiro (copresidente) y Fernando Alfonso (copresidente).