La actual guía 2022 sobre evaluación cardiovascular y tratamiento de los pacientes que se someten a cirugía no cardiaca (CNC) de la Sociedad Europea de Cardiología (ESC) es una actualización de la anterior guía publicada en 20141,2. Esta guía tiene por objetivo estandarizar, con un enfoque basado en pruebas, el manejo cardiovascular perioperatorio de los pacientes que se someten a CNC. Este documento va dirigido a todos los médicos (no solo cardiólogos) que intervienen en este contexto. De hecho, la guía cuenta con la aprobación de la European Society of Anaesthesiology and Intensive Care (ESAIC). A pesar de la falta de ensayos clínicos aleatorizados en el entorno perioperatorio, la guía actual aumenta la evidencia de las recomendaciones comparado con el documento anterior y centra la atención en simplificar el manejo de los pacientes que se someten a CNC con nuevos algoritmos y figuras prácticas. Este artículo, redactado por un grupo de expertos a propuesta del Comité de orientación de la Sociedad Española de Cardiología (SEC), pretende resaltar las novedades más relevantes, los aspectos positivos o controvertidos y las implicaciones sociales de la nueva guía en la mejora de la práctica clínica local.
COMENTARIOS SOBRE LA METODOLOGÍALa estructura de esta guía es la misma que la de otras guías ESC publicadas en los últimos años. Al principio se destacan recomendaciones nuevas y revisadas, y al final se exponen los mensajes de «Qué hacer» y «Qué no hacer». Lamentablemente, hay pocos ensayos clínicos que evalúen el riesgo perioperatorio y en general los niveles de las recomendaciones son B y C. Un punto clave es la estratificación del riesgo, tanto en relación con la cirugía como con el paciente, para la cual la guía es bastante concisa y simple, basada en el consenso con la ESAIC. El documento especifica cuándo hay que hacer un electrocardiograma (ECG), determinar los biomarcadores, o hacer un ecocardiograma, una prueba de esfuerzo o un estudio de anatomía coronaria. Los autores han expuesto el tratamiento general de la CNC en una figura simple, aunque hay múltiples apartados que tratan de cómo evaluar el riesgo perioperatorio en distintas enfermedades cardiovasculares (EC) específicas. En relación con el tratamiento farmacológico perioperatorio, hay pruebas científicas más sólidas basadas en ensayos clínicos, en especial en lo que respecta a los tratamientos con bloqueadores beta y antitrombóticos. Las recomendaciones para el manejo perioperatorio de algunos tratamientos farmacológicos, tales como los inhibidores del cotransportador de sodio y glucosa de tipo 2 (SGLT-2), los diuréticos y los inhibidores de la neprilisina y del receptor de angiotensina son nuevas y útiles. Se presentan las complicaciones perioperatorias de las que hay que tener conocimiento y cómo gestionarlas. En general, es una guía muy completa, con aspectos de gran utilidad clínica y con algunos aspectos controvertidos, que deben consultarse para adaptarlos a los entornos de la práctica individual.
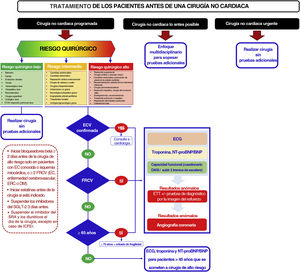
NOVEDADESEvaluación del riesgo clínicoComo novedad, comparado con la guía del 2014, se propone un nuevo diagrama de flujo en el que se tiene en cuenta el momento de la cirugía (inmediata, en cuestión de 1 o 2 días, lo antes posible, o programada) (figura 1). En el caso de la CNC que hay que realizar lo antes posible, se recomienda un enfoque individualizado y multidisciplinario. En los pacientes que requieran una CNC programada, se recomienda evaluar el riesgo antes de la intervención, idealmente al mismo tiempo que se propone la intervención. Se identifican tres grupos de riesgo en función de la edad (65 años), de los factores de riesgo cardiovascular (CV) —como hipertensión, tabaquismo, dislipidemia, diabetes y antecedentes familiares de ECV— o de la existencia de ECV. Se recomienda un chequeo cardiaco que incluya ECG, biomarcadores (troponina cardiaca de alta sensibilidad [hs-cTn; clase I], péptido natriurético B [BNP]/ prohormona N-terminal del péptido natriurético B [NT-proBNP; clase IIa]) y una evaluación de la capacidad funcional basada en las actividades de la vida diaria o en escalas (clase IIa), incluso en personas sanas de más de 65 años que vayan a someterse a una CNC de riesgo intermedio o alto. En los pacientes de 45 a 65 años sin signos, síntomas o antecedentes de ECV, hay que sopesar la posibilidad de realizar un ECG y biomarcadores antes de someterles a una CNC de alto riesgo (IIaC). Esta nueva estrategia comparada con la guía anterior tiene por objetivo identificar la lesión miocárdica perioperatoria (LMP), que constituye la complicación CV más habitual asociada a mayor mortalidad durante el primer mes tras la cirugía. Para cuantificar la capacidad funcional, se hace referencia a un modo más objetivo de estimar el riesgo cardiaco con el cuestionario Duke Activity Status Index para determinar la tolerancia al ejercicio antes de la intervención quirúrgica3.
Tratamiento de los pacientes que se someten a una cirugía no cardiaca según la guía ESC 2022. CTAV: cirugía toracoscópica asistida por vídeo; DM: diabetes mellitus; EC: enfermedad coronaria; ECG: electrocardiograma; ECV: enfermedad cardiovascular; ERC: enfermedad renal crónica; ETT: ecocardiograma transtorácico; FRCV: factores de riesgo cardiovascular; ICFEr: insuficiencia cardiaca con fracción de eyección reducida; SGLT-2: cotransportador de sodio y glucosa de tipo 2; SRA: sistema renina-angiotensina-aldosterona.
En lo que se refiere a las pruebas complementarias, se simplifican las indicaciones para el ECG perioperatorio, sin recomendar su realización sistemática en pacientes de poco riesgo a los que se practicará una CNC de bajo riesgo. En el caso de los biomarcadores, el nivel de recomendación se ha ampliado a IB para determinar la hs-cTn en los pacientes con ECV, factores de riesgo CV (edad ≥ 65 años) y síntomas indicativos de ECV previa a la CNC de riesgo intermedio-alto, y 24y 48horas después. La recomendación también se ha actualizado a IIaB para determinar el BNP o NT-proBNP en la misma situación.
En cuanto al ecocardiograma transtorácico (ETT), sigue sin recomendarse la evaluación sistemática de la fracción de eyección del ventrículo izquierdo (FEVI) antes de la cirugía porque el ETT preoperatorio previo a la CNC de alto riesgo no redujo el riesgo de aparición de complicaciones posoperatorias. Además, se hace referencia a la ecocardiografía preoperatoria dirigida con un dispositivo ecocardiográfico portátil para evaluar la presencia de ruidos, la inestabilidad hemodinámica, la función ventricular y la disnea. Esta guía deja claro que las pruebas de esfuerzo solo deberían considerarse una alternativa válida para diagnosticar enfermedad coronaria (EC) obstructiva cuando no se dispone de pruebas de diagnóstico por imagen, o para evaluar la capacidad funcional cuando la anamnesis es ambigua.
En el caso de la angiografía invasiva, las indicaciones se simplifican, de un modo parecido al del contexto no quirúrgico, y puede sopesarse en los pacientes con síndrome coronario crónico estable en quienes se ha programado la realización de una endarterectomía carotídea. Se añaden pruebas que corroboran la realización de una angiografía coronaria por tomografía computarizada para una mejor estimación del riesgo, pero el documento apunta a que es posible que los resultados deban complementarse con pruebas funcionales no invasivas para decidir la necesidad de revascularización.
Hay un apartado nuevo específico sobre la perspectiva del paciente, que destaca que debe darse tiempo para abordar las preocupaciones y proporcionar información basada en pruebas sobre las compensaciones riesgo-beneficio y las opciones de tratamiento quirúrgico, y para permitir a los pacientes participar en la toma de decisiones compartida. A diferencia de la guía 2014 anterior, hay un apartado específico en el que se hace especial referencia a la fragilidad. El documento indica que la evaluación perioperatoria de los pacientes 70 años) que requieren una CNC de riesgo intermedio o alto debería incluir un cribado de la fragilidad.
Tratamiento farmacológico en el contexto perioperatorioSe recomienda cambiar el estilo de vida y controlar los factores de riesgo CV (como dejar de fumar> 4 semanas antes de la CNC). Con respecto a las nuevas recomendaciones sobre las estrategias de reducción del riesgo farmacológico, la guía sopesa la suspensión temporal de los diuréticos el día de la CNC, así como la interrupción de los inhibidores SGLT-2 durante por lo menos 3 días antes de una CNC de riesgo intermedio o alto para minimizar el riesgo de cetoacidosis normoglucémica.
Sigue recomendándose suspender la monoterapia con antiagregantes plaquetarios y ácido acetilsalicílico para la prevención primaria en el caso de someterse a CNC. Con respecto a la prevención secundaria, en la nueva guía se afirma que el único subgrupo de pacientes que se beneficia de interrumpir el ácido acetilsalicílico, sin un riesgo muy alto de hemorragia, es el de los que se han sometido a intervención coronaria percutánea (ICP). Si el riesgo de hemorragia supera el riesgo de isquemia, debería interrumpirse la toma de ácido acetilsalicílico durante por lo menos 3 días antes de la CNC (incluso 7 días antes en intervenciones de alto riesgo como en la neurocirugía).
La duración recomendada del tratamiento antiagregante plaquetario doble (TAPD) ha cambiado en el protocolo asistencial publicado en los últimos años4–6. Por consiguiente, las nuevas recomendaciones perioperatorias relativas al DAPT ya no diferencian entre stents metálicos sin recubrimiento (SMSR) y stents farmacoactivos (SFA). Las pruebas observacionales producen resultados contradictorios sobre el impacto de interrumpir el P2Y12 en los episodios de isquemia en pacientes que se someten a CNC, y en consecuencia no pueden establecerse recomendaciones específicas. Si es posible, se recomienda retrasar la CNC programada hasta 6 meses tras la ICP programada y 12 meses después de un síndrome coronario agudo (SCA) (y mínimo un mes de TAPD tras la ICP programada y tres meses después del SCA de alto riesgo). En relación con la duración mínima del TAPD tras sufrir un SCA, los autores de esta revisión consideran que en situaciones especiales podría sopesarse interrumpir el inhibidor del P2Y12 desde el primer mes, sobre todo con las pruebas proporcionadas por los nuevos SFA. Una vez interrumpido el inhibidor del P2Y12, debería realizarse la cirugía con ácido acetilsalicílico. La decisión de ajustar el tratamiento antes de la cirugía debería tomarse teniendo en cuenta cada paciente y por consenso entre el cirujano y el cardiólogo. En la tabla 1 se presenta el intervalo de tiempo recomendado para los antiagregantes plaquetarios previos a la CNC.
Interrupción del tratamiento con antiagregantes plaquetarios previa a la cirugía no cardiaca
| Antiagregante plaquetario | Interrupción (días previos a la cirugía) |
|---|---|
| Ácido acetilsalicílico | Pacientes con ICP previa: sin interrupción* |
| Cirugía con riesgo hemorrágico alto: 7 | |
| Clopidogrel | 5 |
| Prasugrel | 7 |
| Ticagrelor | 3-5 |
ICP: intervención coronaria percutánea.
El tratamiento de la anticoagulación oral perioperatoria es una de las principales novedades del documento actual comparado con el del 2014. Así pues, la guía proporciona algoritmos prácticos y las recomendaciones siguen la misma línea que las declaraciones anteriores7–9. Con respecto a los antagonistas de la vitamina K (AVK), se recomienda un uso restrictivo del tratamiento anticoagulante perioperatorio (solo en los pacientes con alto riesgo de trombosis, como quienes llevan una válvula cardiaca mecánica). Las intervenciones invasivas con poco riesgo de hemorragia pueden realizarse sin interrumpir los AVK, y debe controlarse el cociente internacional normalizado para mantener el nivel más bajo en el intervalo terapéutico. En esta guía se detalla un enfoque práctico del tratamiento con anticoagulantes orales de acción directa (ACOD) en la CNC programada que incluye figuras prácticas basadas en el consumo de fármacos, el riesgo de hemorragia periprocedimiento y la función renal. Con respecto a procedimientos específicos, en intervenciones que conllevan un alto riesgo de hemorragia, como la anestesia espinal o epidural, o la punción lumbar que requiere una hemostasia intacta, se recomienda suspender los ACOD durante un máximo de 5 semividas. No se recomienda recorrer a un tratamiento anticoagulante perioperatorio con heparina (excepto en circunstancias excepcionales de alto riesgo trombótico). En general, puede reiniciarse la toma de ACOD al cabo de 6-8horas de la intervención con una hemostasia rápida y completa. Cuando el riesgo de hemorragia es mayor, puede posponerse hasta 48-72horas, con evaluación del uso de heparina. No hay pruebas que corroboren la recomendación de utilizar dosis menores de ACOD en este contexto. Esta nueva guía incluye el uso de sustancias específicas para revertir los ACOD en la CNC urgente. Cuando no se disponga de estos fármacos, hay que sopesar la posibilidad de recurrir al concentrado de complejo de protrombina, aunque no haya pruebas de su inocuidad y eficacia en este contexto.
Se ha añadido un subapartado sobre el tratamiento combinado con antiagregantes plaquetarios y anticoagulantes orales. En esta situación, debe posponerse la cirugía programada hasta que pueda suspenderse de manera segura el tratamiento con antiagregantes plaquetarios (6 meses tras la ICP programada o 12 meses después del SCA), aunque sería razonable individualizarlo con un enfoque multidisciplinario. En la intervención quirúrgica urgente con alto riesgo de hemorragia, pueden aplicarse medidas quirúrgicas para reducir la hemorragia y estrategias para neutralizar la anticoagulación.
En la guía del 2022 se ha incluido un nuevo apartado de tromboprofilaxis perioperatoria. Cuando esté indicado, debe iniciarse la tromboprofilaxis durante la estancia hospitalaria y hasta 12horas antes de la intervención quirúrgica, y debe proseguirse tras la intervención según la evaluación individual de riesgo de hemorragia hasta la movilización completa del paciente o hasta el alta hospitalaria. La presencia de ACOD en la dosis de tromboprofilaxis podría ser una alternativa a la heparina de bajo peso molecular tras la artroplastia total de rodilla y cadera.
El concepto de «manejo hemorrágico del paciente» (MHP) es una novedad de la guía actual. El documento proporciona recomendaciones sobre los «3 pilares» del MHP: hemoglobina preoperatoria y optimización de la concentración de hierro, reducción de la hemorragia intraoperatoria y optimización de la transfusión de sangre. Además, el tratamiento hemodinámico perioperatorio dirigido a objetivos está hoy en día totalmente validado, principalmente para orientar la fluidoterapia en pacientes que se someten a CNC de alto riesgo. Por cuestiones de seguridad, no se recomienda la toma de antiinflamatorios no esteroideos (AINE) a los pacientes con ECV, a pesar de que en estos pacientes el dolor posoperatorio se relaciona con lesiones miocárdicas.
Enfermedades específicasEnfermedad coronariaLa guía cuantifica el nivel de riesgo en pacientes con EC según su perfil de riesgo inicial (EC previa, edad avanzada, y episodio coronario agudo reciente), el riesgo de la intervención y la urgencia de la intervención quirúrgica. No hay pruebas científicas que respalden la búsqueda proactiva y, en su caso, la revascularización profiláctica de la EC en los pacientes asintomáticos con SCA. La función de la revascularización en los pacientes sintomáticos es controvertida y dependerá de tres factores: control de los síntomas con tratamiento clínico, detección del área de isquemia y participación de la arteria coronaria del tronco coronario izquierdo. En el caso de una CNC urgente que coexiste con un SCA, la decisión sobre la intervención debe hacerla, de manera individual, un equipo cardiovascular. Se recomienda revascularizar por lo menos la arteria responsable, utilizar SFA y posponer la intervención quirúrgica programada durante por lo menos 3 meses.
Insuficiencia cardiacaLa nueva guía mantiene la necesidad de evaluar de forma previa la función ventricular con ETT y péptidos natriuréticos (si no se han evaluado recientemente), aunque con una recomendación IB comparado con la recomendación IA de la versión del 2014, y mantener la necesidad de optimizar y mantener el tratamiento según las pautas de tratamiento de la insuficiencia cardiaca (IC) con un nivel de evidencia IA. La novedad que se introduce en el texto es la necesidad de controlar el volumen de sangre durante la intervención, incluso con métodos invasivos si es necesario. Se mencionan nuevos entornos clínicos, como el de los pacientes con un dispositivo de ayuda ventricular por la IC avanzada; en estos casos, la guía insiste en la necesidad de contar con un equipo multidisciplinario y realizar la cirugía en un centro con acceso a equipos expertos en ayuda ventricular (IC).
Valvulopatía cardiacaEn pacientes con estenosis aórtica sintomática grave, la guía recomienda el remplazo de la válvula aórtica o el implante percutáneo de válvula aórtica (TAVI), y reservar la valvuloplastia percutánea como última opción terapéutica para los pacientes que no son idóneos para un TAVI (clase IIb). En pacientes con estenosis aórtica asintomática grave, la intervención valvular previa a la CNC solo está indicada si la FEVI <50% en el contexto de las intervenciones de alto riesgo. En los pacientes sintomáticos y asintomáticos con FEVI baja e insuficiencia mitral primaria, se recomienda la reparación quirúrgica antes de la CNC. No obstante, en pacientes con insuficiencia mitral secundaria, el primer paso es el tratamiento clínico óptimo de la causa subyacente; si los síntomas persisten, está indicada la reparación quirúrgica o percutánea de la válvula. A diferencia de la versión del 2014, la guía actual recomienda el tratamiento quirúrgico en pacientes con insuficiencia valvular aórtica grave que requieran la intervención valvular antes de la CNC de riesgo intermedio o alto. No obstante, no se han establecido diferencias significativas en el tratamiento de la estenosis mitral significativa o de los pacientes con prótesis o profilaxis de la endocarditis infecciosa.
Arritmias conocidas o de diagnóstico reciente, cardiopatías congénitas del adulto, enfermedad pericárdica.
Se recomienda la ablación con catéter como primera opción para tratar la taquicardia supraventricular antes de una CNC programada de alto riesgo (IIaB) y la taquicardia ventricular recurrente bajo tratamiento clínico optimizado antes de una CNC programada (IB). La nueva guía incluye datos adicionales sobre el manejo perioperatorio de los dispositivos electrónicos cardiacos implantables en la CNC, incluida la primera referencia a los marcapasos sin plomo y a los desfibriladores automáticos implantables (DAI). En los pacientes con una cardiopatía congénita, se recomienda realizar la CNC programada de riesgo intermedio o alto en un centro con experiencia (IC). Por último, la guía 2022 incluye recomendaciones sobre los pacientes con enfermedad pericárdica (no mencionados en la edición del 2014).
No hay novedades importantes con respecto al abordaje de los pacientes con hipertensión previa a la CNC, excepto la recomendación de evitar las fluctuaciones de presión arterial durante la intervención, que se actualiza a IA (IIa en la versión del 2014). Con respecto a la arteriopatía periférica, la nueva guía amplía el apartado y detalla un aspecto que comparte con la versión del 2014: no se recomienda la remisión sistemática a un estudio cardiaco, a una prueba de esfuerzo o a una angiografía coronaria antes de la cirugía programada (IIIC). En los pacientes con enfermedad cerebrovascular, la guía sigue indicando estudiar y tratar la estenosis carotídea solo en pacientes con síntomas neurológicos 6 meses antes de la CNC. Evaluar la obesidad antes de la CNC es una recomendación nueva, igual que evaluar la glucohemoglobina (HbA1c) para descartar la diabetes mellitus. Por último, en un nuevo apartado dedicado a la covid-19, la guía resalta que no hay pruebas a favor de realizar el cribado CV antes de la cirugía en pacientes que se han infectado con SARS-CoV-2, pero se recomienda retrasar la cirugía programada hasta que los síntomas y la comorbilidad se hayan estabilizado.
Complicaciones cardiovasculares perioperatoriasLesión miocárdica / infarto de miocardio perioperatoriosLa guía diferencia 2 entidades:
Lesión miocárdica perioperatoria. Cualquier elevación de la hs-cTn durante las primeras 48 horas tras la CNC, sin necesidad de síntomas, cambios ECG o alteraciones contráctiles en las pruebas de diagnóstico por la imagen. Dada la analgesia posterior a este tipo de cirugía, el 90% de los pacientes con lesión miocárdica perioperatoria no tienen síntomas. Esta entidad se ha asociado a una mortalidad de hasta el 10% al mes y no hay pruebas de que alguna intervención reduzca su incidencia. El documento añade una subentidad llamada lesión miocárdica tras la CNC (MINS), en la que la causa subyacente más probable es la EC. Queda por determinar si hay umbrales más apropiados de hs-cTn que la simple elevación por encima del umbral para discriminar el pronóstico de estos pacientes.
Infarto de miocardio perioperatorio. El diagnóstico de infarto de miocardio perioperatorio requiere la elevación de la hs-cTn durante las primeras 48horas con criterios adicionales (síntomas, cambios en el ECG, pruebas de diagnóstico por la imagen o angiografía coronaria)
Fibrilación auricular y arritmias. En esta guía se ha incluido un nuevo apartado que trata específicamente de la FA posoperatoria, con un protocolo de tratamiento. Con respecto al ictus posoperatorio, se introduce una nueva recomendación con un nivel de evidencia IA en el tratamiento con ACOD en pacientes que sufren FA posoperatoria, ya que es la causa más frecuente de ictus posoperatorio. Faltan pruebas que respalden el tratamiento antitrombótico apropiado en pacientes con tromboembolismo venoso posoperatorio, ya que la cirugía mayor o el traumatismo han sido típicamente contraindicados en los ensayos de tratamiento trombolítico o anticoagulante previos. Debe iniciarse anticoagulación, preferiblemente con ACOD, dependiendo de la función renal y el riesgo de hemorragia posoperatorios, lo antes posible y durante por lo menos 3 meses. Si el paciente está inestable, debe sopesarse una trombólisis o la trombectomía mecánica quirúrgica o percutánea si hay riesgo de hemorragia. Por último, no se indican diferencias en pacientes con infarto agudo de miocardio espontáneo, IC o síndrome de tako-tsubo tras CNC, comparado con los cuidados habituales.
ASPECTOS POSITIVOSEvaluación del riesgo clínicoSe han clarificado o simplificado las indicaciones para la realización de pruebas complementarias previas a la CNC. El documento menciona de qué modo la interpretación de las concentraciones de BNP/NT-proBNP como marcadores cuantitativos de la IC con valores discriminatorios evolutivos puede facilitar la detección de la IC, el control intraoperatorio óptimo y el inicio u optimización del tratamiento de la IC tras la cirugía. El documento también resalta que un exceso de pruebas puede causar un retraso innecesario e impredecible de la intervención quirúrgica ya planificada, y añadir un riesgo procedimental independiente al riesgo total. Una cuestión muy positiva de esta guía es la mención especial a la fragilidad.
Enfermedades específicasLa guía trata por primera vez y de manera directa sobre cómo realizar intervenciones en pacientes con EC. Si antes de la CNC está indicada una ICP, se recomienda utilizar SFA de nueva generación en lugar de SMSR, o angioplastia con balón. Solo puede sopesarse un enfoque minimalista con angioplastia con balón y retraso en la colocación del stent en la combinación poco probable de una CNC que no pueda posponerse e infarto de miocardio con elevación del segmento ST concomitante con indicación de ICP. Los aspectos positivos de esta guía con respecto a los pacientes con IC son la priorización de la monitorización y el manejo de estos pacientes antes de la CNC, en los momentos previos a la cirugía, durante la cirugía y en el periodo posoperatorio. Se incluyen nuevos contextos clínicos, como la miocardiopatía hipertrófica obstructiva, y se insiste aún más en la necesidad de mantener la volemia y evitar la vasodilatación. Como aspectos positivos, la guía incluye técnicas percutáneas para tratar la considerable estenosis aórtica y la insuficiencia mitral y reducir el riesgo quirúrgico. Con respecto a la arteriopatía periférica, la guía distingue entre dos tipos de CNC cuyos riesgos difieren notablemente, y por tanto también difieren las recomendaciones para abordar la cirugía vascular y la cirugía no vascular. En la guía se afirma claramente que no debe retrasarse la CNC urgente por ninguna arritmia, salvo en los episodios de arritmia potencialmente mortal. Se proporciona una ilustración para guiar la configuración del electrocauterio unipolar (colocación del parche) en la cirugía supraumbilical y minimizar las interferencias electromagnéticas.
Estrategias generales de reducción del riesgoLa guía aclara cómo utilizar los bloqueadores beta, los inhibidores del sistema renina-angiotensina (SRA) y las estatinas antes de la CNC. Se recomienda a los pacientes que toman bloqueadores beta o estatinas proseguir con la toma durante la intervención. Se plantea la posibilidad de que los pacientes con IC estable sigan tomando inhibidores del SRA durante la intervención, y se recomienda su retirada en las situaciones restantes. Al igual que las recientes directrices sobre la EC, la nueva guía refleja la posibilidad de acortar la toma de TAPD, si se considera seguro en lo que respecta al riesgo isquémico del paciente, para evitar retrasos quirúrgicos innecesarios y reducir el riesgo de hemorragia4–6. El principal aspecto positivo de estas pautas con respecto a la anticoagulación oral es la disminución del tratamiento anticoagulante perioperatorio. Las únicas excepciones son los pacientes portadores de válvulas cardiacas mecánicas y aquellos con un riesgo de trombosis muy alto. Otra cuestión importante de esta guía es el uso de sustancias que revierten el efecto de los ACOD en este contexto. Esto puede reforzar la sensación de seguridad a la hora de administrar estos fármacos. La recomendación de una herramienta validada, como la escala de Caprini, para evaluar el riesgo de tromboembolia mejora la selección precisa de los pacientes para este tratamiento. Con relación al MHP, muchas recomendaciones perioperatorias son sólidas y fáciles de aplicar, como la determinación de la hemoglobina o el tratamiento de la anemia previo a la cirugía, principalmente con hierro.
Complicaciones cardiovasculares perioperatoriasSe proporciona un nuevo tratamiento específico de la FA posoperatoria: se introduce el concepto de riesgo aumentado de FA clínica e ictus tras un episodio de FA posoperatoria, y se recomienda la anticoagulación oral tras la FA posoperatoria según las escalas de riesgo con reevaluación a los 3 meses de seguimiento (IIaB).
ASPECTOS CONTROVERTIDOSEvaluación del riesgo clínicoNo hay ninguna referencia a la telemedicina, que podría desempeñar alguna función en el enfoque preoperatorio de los pacientes con factores de riesgo o ECV confirmada. No se hace ninguna recomendación específica sobre la función de las enfermeras en las distintas fases de la enfermedad, en especial en pacientes a los que hay que practicar una CNC lo antes posible, como los pacientes con cáncer. En términos de puntuación de riesgo, el documento indica que hay una variabilidad significativa del riesgo predicho de complicaciones cardiacas con las distintas herramientas de predicción del riesgo, y en consecuencia no está claro qué herramienta debe usarse en la evaluación preoperatoria de los pacientes o si sería mejor usar una combinación de varias. A pesar de la mención especial acerca de la fragilidad de esta guía, hay factores que no se mencionan y son importantes para determinar el riesgo preoperatorio de los pacientes, como un índice de masa corporal muy bajo o muy alto, anemia y el estado inmunitario, entre otros, que pueden influir en la EVC subyacente de los pacientes y los factores de riesgo CV, y favorecer la aparición de complicaciones cardiovasculares tras la CNC.
Enfermedades específicasEn la guía actual, no se define la función de las pruebas de esfuerzo en ningún grupo de valvulopatías antes de la CNC. Además, no se hace ninguna mención del tratamiento de los pacientes con insuficiencia tricuspídea significativa, que se ha relacionado con mayor morbilidad y mortalidad posoperatorias. Sería útil recordar la definición de arteriopatía periférica (pacientes con un índice tobillo-brazo <0,9, o aquellos a los que se ha revascularizado con anterioridad) utilizada en la guía del 2014 pero ausente en el documento actual. El documento menciona la posible utilidad de dosis bajas de rivaroxabán (2,5mg/12h) + ácido acetilsalicílico en pacientes con arteriopatía periférica a los que se practica cirugía vascular para reducir los episodios de trombosis según el estudio VOYAGER PAD10. No obstante, dado el aumento en la tasa de hemorragia mayor en el grupo tratado con rivaroxabán + ácido acetilsalicílico, el beneficio clínico neto pone en duda dicha recomendación. En pacientes con MINS y bajo riesgo de hemorragia, la guía recomienda el tratamiento con dabigatrán (110mg/12h) desde la primera semana tras la CNC, basándose en los resultados del estudio MANAGE11. Su uso para esta indicación en nuestro entorno parece poco probable. Por último, no se menciona la ablación de la FA y el aleteo dependiente de istmo como una posible estrategia de control del ritmo previa a la CNC programada, a pesar de que se trata de una indicación IA/IIA de la guía del 2020 relativa a la FA.
Estrategias generales de reducción del riesgoEl inicio preoperatorio de bloqueadores beta sigue siendo un tema de preocupación. La guía actual recomienda iniciar la toma del fármaco por lo menos una semana antes de la cirugía (empezar con una dosis baja y ajustar la dosis para conseguir una frecuencia cardiaca de 60-70 lpm) en pacientes con 2 o más factores de riesgo (EC, enfermedad cerebrovascular, insuficiencia renal o diabetes mellitus). En el documento se reconoce que no hay datos sobre el tratamiento perioperatorio de la monoterapia con ácido acetilsalicílico en pacientes con TAVI y, en consecuencia, su retirada debe evaluarse en función del riesgo de hemorragia de la intervención. Además, no está muy clara la función del tratamiento anticoagulante perioperatorio: aunque generalmente no se recomienda su uso, la guía no especifica qué pacientes se benefician de este tratamiento. Faltan estudios con buena potencia estadística que evalúen qué papel desempañan las pruebas de función plaquetaria a la hora de orientar la estrategia terapéutica en los pacientes sometidos a CNC y en tratamiento con antiagregantes plaquetarios. Con respecto a la administración de epoetina junto con hierro antes de la intervención, se requieren más estudios que permitan una recomendación. Otro aspecto controvertido del tratamiento posoperatorio es cómo llevar a cabo una analgesia eficaz, ya que no se ha confirmado la inocuidad de los fármacos antiinflamatorios no esteroideos sin ácido acetilsalicílico.
Complicaciones cardiovasculares perioperatoriasLa guía recomienda la medición sistemática de la hs-cTn antes y después de una CNC de riesgo intermedio y alto en pacientes≥65 años, con factores de riesgo CV o EC. Cualquier elevación es un signo de alarma que debería desencadenar una investigación. No obstante, en la práctica clínica esto puede ser un problema. Los términos lesión miocárdica perioperatoria e infarto de miocardio perioperatorio (IMP) son artificiales o controvertidos, especialmente porque esta guía está orientada también a médicos no cardiólogos. Sería más útil una clasificación del infarto perioperatorio de origen cardiaco o extracardiaco. Sigue siendo un reto prevenir la FA posoperatoria y la falta de evidencia impide hacer recomendaciones contundentes.
IMPLICACIONES PARA LA PRÁCTICA CLÍNICA EN ESPAÑA Y CONDICIONES SOCIOECONÓMICAS LOCALESEvaluación del riesgo clínicoLas nuevas recomendaciones deben facilitar la evaluación y el flujo de pacientes entre la anestesia, la cirugía y los servicios de cardiología, y llevar a un mejor funcionamiento y reducción de las consultas de cardiología limitando o esclareciendo el uso de pruebas complementarias tradicionalmente utilizadas en exceso, tales como el ECG y la ETT. En la guía se insiste en la necesidad de un enfoque centrado en el paciente que asegure la optimización terapéutica y minimice el riesgo perioperatorio. No obstante, no se proporcionan recomendaciones sobre cómo implementar esta necesidad organizativa en la práctica clínica y no se incluye ninguna propuesta de interacción-coordinación entre los especialistas. Tampoco se detallan los criterios para remitir a los pacientes a otros profesionales, ni se especifica en qué momento hay que realizar las pruebas complementarias. Aunque la determinación del NT-proBNP y la hs-cTn parece un enfoque prometedor, puede llevar al sobreuso de medidas periprocedimentales sin pruebas actuales sólidas, y podría retrasar de manera innecesaria la cirugía programada y sobrecargar los servicios de cardiología del sistema sanitario y, en consecuencia, suponer un gasto excesivo.
Enfermedades específicasEl enfoque específico de esta guía sobre el tratamiento de los pacientes con EC previa a los que se practica una CNC programada podría permitir la unificación de criterios de acción en todos los servicios de cardiología de España. Además, también podría permitir la redacción de protocolos clínicos asistenciales en los procesos de CNC en los que participen otras especialidades para hacerlos más eficaces. Asimismo, se espera ahorrar en pruebas e intervenciones que no muestren beneficios en este contexto. Los pacientes con IC en quienes se ha programado una CNC requerirán a menudo atención cardiológica para la evaluación prequirúrgica, con acompañamiento durante la intervención y después. Esto influye en la necesidad de recursos para poder proporcionar esta atención. La discriminación del riesgo entre la CNC vascular frente a la no vascular y el tratamiento propuesto facilitará la implementación de protocolos más eficaces basados en el proceso quirúrgico que permitan a los especialistas no cardiólogos establecer las vías de evaluación preferidas y evitar consultas y procedimientos innecesarios. El tratamiento perioperatorio de las personas que llevan un DAI se simplifica en esta nueva guía. Se prioriza el uso de un imán como el método recomendado para inhibir los tratamientos con DAI durante la CNC (la guía anterior recomendaba la desactivación por programación del dispositivo). Este cambio facilita un tratamiento posoperatorio más seguro y eficaz.
Estrategias generales de reducción del riesgoEl tratamiento anticoagulante perioperatorio es una práctica muy difusa en este contexto. Es posible que muchos médicos desconozcan las pruebas que corroboran el riesgo de hemorragia asociado a este enfoque. Esta falta de conocimientos, junto con la inercia terapéutica y el miedo a que estos pacientes sufran episodios trombóticos, dificulta que se abandone esta estrategia. Esta guía puede ayudar a difundir el mensaje de que hay pruebas suficientes para interrumpir de forma segura los anticoagulantes orales cuando esté indicado, sin tratamiento anticoagulante perioperatorio. Esto reducirá indudablemente los episodios de hemorragia y llevará a un mejor tratamiento perioperatorio. La implementación de programas de MHP implica reorganizar la evaluación preoperatoria para diagnosticar anemia o carencia de hierro y un posible tratamiento.
Complicaciones cardiovasculares perioperatoriasTal como la guía indica, la determinación de la hs-cTn antes y después de la CNC producirá un índice elevado de diagnósticos de IMP. Esta recomendación conllevará modificar el tratamiento de referencia en los servicios de cirugía y anestesia, lo que probablemente implicará una consulta al cardiólogo que no siempre puede garantizarse.
CONCLUSIONESLa nueva guía sobre evaluación cardiovascular y tratamiento de los pacientes que se someten a una CNC proporciona mensajes clave simples y prácticos para facilitar las decisiones clínicas diarias. Una nuevo diagrama de flujo, con evaluación general de los pacientes antes de la CNC, centrado en el ECG y los biomarcadores intenta facilitar el manejo preoperatorio. En esta guía el enfoque práctico sobre el tratamiento antitrombótico en la CNC programada es más detallado, e incluye figuras prácticas basadas en los fármacos administrados y el riesgo periprocedimiento. En la guía también se destaca el manejo perioperatorio en las ECV más frecuentes y se centra la atención en los cuidados específicos según el riesgo de enfermedad clínica previa del paciente. Por último, el documento incluye recomendaciones prácticas sobre cómo tratar las complicaciones posoperatorias, y se destaca un nuevo apartado sobre el infarto de miocardio y la lesión miocárdica.
FINANCIACIÓNNinguna.
CONFLICTO DE INTERESESLos documentos de declaración de conflicto de intereses de los autores se pueden consultar en el material adicional.
Grupo de trabajo para la guía ESC 2022 sobre la evaluación cardiovascular y la estrategia de tratamiento de los pacientes que se someten a cirugía no cardiaca: David Vivas (coordinador), Sergio Raposeiras-Roubin (coordinador), Guillermo Aldama, Felipe Bisbal, Clara Bonanad, Raquel Ferrandis, Román Freixa-Pamias, Rosa Fernández-Olmo, Ainhoa Robles-Mezcua, José Francisco Rodríguez Palomares, Amalia Sillero-Sillero.
Comité de guías de la SEC: Rut Andrea, Pablo Avanzas, Gemma Berga, Araceli Boraita, David Calvo, Raquel Campuzano, Victoria Delgado, Laura Dos Subirá, Juan José Gómez Doblas, Pilar Mazón, Domingo Pascual, Juan Sanchis, José M. de la Torre, David Vivas, José L. Ferreiro (presidente).
Véase contenido relacionado: https://secardiologia.es/cientifico/guias-clinicas/miscelanea/13801-2022-esc-guidelines-on-cardiovascular-assessment-and-management-of-patients-undergoing-non-cardiac-surgery