En nuestro medio hay pocos datos sobre los resultados del tratamiento quirúrgico de la insuficiencia tricuspídea grave. Nuestro objetivo es analizar los resultados clínicos y ecocardiográficos de nuestra población con insuficiencia tricuspídea grave sometida a cirugía comparándolos según el tipo de reparación o de sustitución valvular.
MétodosRealizamos un estudio retrospectivo incluyendo a 119 pacientes consecutivos con insuficiencia tricuspídea grave sometidos a cirugía de dicha válvula entre abril de 1996 y febrero de 2010.
ResultadosSe realizaron 61 anuloplastias sin anillo y 23 con anillo, y se implantaron 11 prótesis biológicas y 24 mecánicas. La mortalidad perioperatoria fue del 18,5%, y se asociaron a ella la edad y el tiempo de circulación extracorpórea. Durante el seguimiento clínico (mediana, 41 [intervalo intercuartílico, 24-89] meses), el grupo anuloplastia con anillo precisó dos reoperaciones, al igual que el grupo de prótesis mecánica, en el que se diagnosticó trombosis protésica a 4 pacientes. La mortalidad total tras seguimiento fue del 29,9%, y se asociaron a ella la edad > 70 años y el tiempo de circulación extracorpórea. La aparición de nueva insuficiencia tricuspídea grave se asoció a la edad y la anuloplastia sin anillo (p=0,04).
ConclusionesLa reparación sin anillo se asoció significativamente con recurrencia de insuficiencia tricuspídea grave. El implante de prótesis mecánica se asoció a una elevada tasa de trombosis en el seguimiento. No se encontraron diferencias significativas en la mortalidad perioperatoria o total según el tipo de reparación o sustitución valvular.
Palabras clave
Los datos disponibles sobre la historia natural de la insuficiencia tricuspídea (IT) grave señalan su mal pronóstico a largo plazo. En la mayoría de los casos la etiología es funcional, secundaria a una valvulopatía izquierda que domina el cuadro clínico1, aunque la IT puede persistir e incluso progresar tras un exitoso tratamiento de la enfermedad valvular izquierda2. Según las actuales guías de práctica clínica3, siguen siendo controvertidos tanto el momento en que se debe indicar la cirugía como la técnica más apropiada para cada caso, aunque se recomienda la cirugía reparadora antes que la sustitución valvular siempre que sea factible técnicamente, debido a sus mejores resultados4. En nuestro medio hay escasas publicaciones que aborden los resultados del tratamiento quirúrgico de la IT grave, así como del resto de la patología de dicha válvula, y además todas ellas proceden del mismo grupo de trabajo5–10. El objetivo del presente estudio es analizar los resultados clínicos y ecocardiográficos de nuestra población con IT grave sometida a tratamiento quirúrgico comparándolos según los distintos tipos de reparación o de sustitución.
MÉTODOSPoblación de estudioDiseñamos un estudio retrospectivo en el que incluimos 119 pacientes con IT grave sometidos en nuestro centro a cirugía de sustitución o reparación de la válvula tricúspide desde abril de 1996 hasta febrero de 2010; en total, las cirugías valvulares realizadas en dicho periodo fueron 1.869. La indicación de cirugía de la válvula tricúspide se estableció en todos los pacientes por la presencia de lesión tricuspídea grave y sintomática. El tratamiento realizado se decidió mediante consenso entre cardiólogos, cirujanos cardiacos y el propio paciente. Se optó por la reparación siempre que la técnica fuera factible, fundamentalmente por la ausencia de afección orgánica significativa. El tipo de reparación se estableció según la preferencia del cirujano. Desde el inicio del estudio hasta 2004, únicamente se realizaron anuloplastias sin anillo. Desde 2005 en adelante se realizaron ambos tipos de reparación en proporción 1:1. Entre 1996 y 2004 sólo se implantaron prótesis mecánicas. Desde 2005 en adelante, la razón biológicas:mecánicas fue 2:1; fueron de elección las primeras en pacientes sin indicación previa de anticoagulación permanente cuya expectativa de vida limitada no hiciera suponer la necesidad de reoperación por degeneración protésica, y en casos de reoperación por trombosis de prótesis mecánica.
Evaluación ecocardiográficaLa evaluación ecocardiográfica se llevó a cabo mediante alguno de los siguientes equipos: Acuson Sequoia, Acuson Aspen o Vingmed 750. En el examen estándar se utilizaron el modo M, el modo bidimensional y el Doppler color, pulsado y continuo, a través de los planos habituales, siguiendo las recomendaciones de la American Society of Echocardiography11. La IT se definió como grave por un chorro de regurgitación de área > 30% del área de la aurícula derecha, inadecuada coaptación de las valvas y flujo sistólico inverso en las venas hepáticas12. La presión arterial pulmonar sistólica se estimó a partir del pico de velocidad del chorro de IT.
SeguimientoSe analizaron los resultados posquirúrgicos en cuanto a morbimortalidad e IT residual y se realizó un seguimiento clínico y ecocardiográfico con los datos obtenidos en las revisiones realizadas en consulta externa de cardiología. Se definió mortalidad perioperatoria como la que acaeciera en los 30 días siguientes a la cirugía o durante el ingreso del acto quirúrgico. Respecto a las complicaciones posquirúrgicas, se analizaron las complicaciones infecciosas (endocarditis o mediastinitis), neurológicas (déficit focal neurológico persistente durante más de 24h confirmado mediante tomografía computarizada), pulmonares (intubación durante más de 1 semana, neumonía y neumotórax) y renales (insuficiencia renal definida como aumento de creatinina sérica por encima de 2mg/dl o aumento del 50% respecto a la determinación basal), la reoperación por hemorragia y el síndrome de bajo gasto posquirúrgico. Se denominó «complicación quirúrgica» a que se produjera al menos una de las complicaciones previamente descritas. En el seguimiento se analizó la mortalidad por cualquier causa, la necesidad de nueva cirugía tricuspídea, la trombosis protésica y la aparición de nueva IT grave.
Análisis estadísticoLas variables cualitativas se expresan como porcentajes; las temporales, como mediana [intervalo intercuartílico], y las restantes cuantitativas, como media±desviación estándar. Se usó la prueba de la χ2 para comparar las variables cualitativas y la de la t de Student parar comparar las continuas. Se consideraron estadísticamente significativos valores de p<0,05. Aplicamos un análisis multivariable mediante un modelo de regresión logística múltiple para identificar las variables independientes predictoras de la mortalidad perioperatoria, y así se calcularon las odds ratio (OR) y los intervalos de confianza del 95% (IC95%). Las variables relacionadas con aparición de IT grave durante el seguimiento se analizaron mediante el método de regresión de Cox, y se calcularon las hazard ratio (HR) y sus IC95%. Realizamos un análisis multivariable aplicando un modelo de regresión de Cox para identificar las variables independientes predictoras de la mortalidad total tras completar el seguimiento, y de este modo calculamos las HR y sus IC95%. El análisis de la supervivencia se realizó mediante el método de Kaplan-Meier.
RESULTADOSCaracterísticas basalesSe realizó a 61 pacientes anuloplastia sin anillo según la técnica de De Vega; a 23, anuloplastia con anillo; 11 pacientes recibieron prótesis biológica y 24, prótesis mecánica.
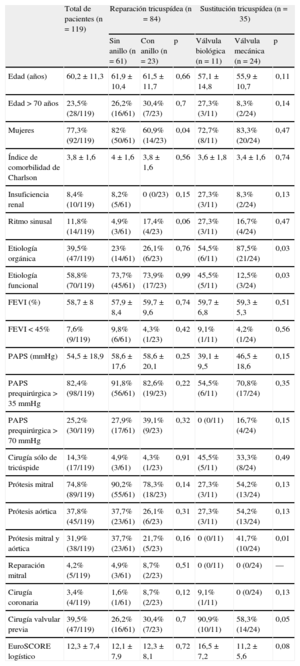
La tabla 1 muestra las características basales de los pacientes según el tipo de reparación o el tipo de sustitución valvular realizada. La etiología de la afección tricuspídea era orgánica en el 39,5% de los casos, funcional en el 58,8% y desconocida en el 1,7%. De los casos con afección orgánica, hubo 41 de origen reumático, 2 secundarios a endocarditis infecciosa derecha, 2 secundarios a prolapso, 1 de origen congénito (malformación de Ebstein) y 1 secundario a anorexígenos. Únicamente el 14,3% de las intervenciones fueron sólo de la válvula tricúspide y hasta el 31,9% implicaron implante de prótesis mitral y aórtica. El 39,5% de los pacientes ya habían sufrido reparación o sustitución valvular previamente. El 64,7% de los pacientes sometidos a intervención sólo de la tricúspide pertenecen al grupo con cirugía valvular previa, frente al 35,3% de los de cirugía multivalvular (p=0,02).
Características basales
| Total de pacientes (n=119) | Reparación tricuspídea (n=84) | Sustitución tricuspídea (n=35) | |||||
| Sin anillo (n=61) | Con anillo (n=23) | p | Válvula biológica (n=11) | Válvula mecánica (n=24) | p | ||
| Edad (años) | 60,2±11,3 | 61,9±10,4 | 61,5±11,7 | 0,66 | 57,1±14,8 | 55,9±10,7 | 0,11 |
| Edad > 70 años | 23,5% (28/119) | 26,2% (16/61) | 30,4% (7/23) | 0,7 | 27,3% (3/11) | 8,3% (2/24) | 0,14 |
| Mujeres | 77,3% (92/119) | 82% (50/61) | 60,9% (14/23) | 0,04 | 72,7% (8/11) | 83,3% (20/24) | 0,47 |
| Índice de comorbilidad de Charlson | 3,8±1,6 | 4±1,6 | 3,8±1,6 | 0,56 | 3,6±1,8 | 3,4±1,6 | 0,74 |
| Insuficiencia renal | 8,4% (10/119) | 8,2% (5/61) | 0 (0/23) | 0,15 | 27,3% (3/11) | 8,3% (2/24) | 0,13 |
| Ritmo sinusal | 11,8% (14/119) | 4,9% (3/61) | 17,4% (4/23) | 0,06 | 27,3% (3/11) | 16,7% (4/24) | 0,47 |
| Etiología orgánica | 39,5% (47/119) | 23% (14/61) | 26,1% (6/23) | 0,76 | 54,5% (6/11) | 87,5% (21/24) | 0,03 |
| Etiología funcional | 58,8% (70/119) | 73,7% (45/61) | 73,9% (17/23) | 0,99 | 45,5% (5/11) | 12,5% (3/24) | 0,03 |
| FEVI (%) | 58,7±8 | 57,9±8,4 | 59,7±9,6 | 0,74 | 59,7±6,8 | 59,3±5,3 | 0,51 |
| FEVI < 45% | 7,6% (9/119) | 9,8% (6/61) | 4,3% (1/23) | 0,42 | 9,1% (1/11) | 4,2% (1/24) | 0,56 |
| PAPS (mmHg) | 54,5±18,9 | 58,6±17,6 | 58,6±20,1 | 0,25 | 39,1±9,5 | 46,5±18,6 | 0,15 |
| PAPS prequirúrgica > 35 mmHg | 82,4% (98/119) | 91,8% (56/61) | 82,6% (19/23) | 0,22 | 54,5% (6/11) | 70,8% (17/24) | 0,35 |
| PAPS prequirúrgica > 70 mmHg | 25,2% (30/119) | 27,9% (17/61) | 39,1% (9/23) | 0,32 | 0 (0/11) | 16,7% (4/24) | 0,15 |
| Cirugía sólo de tricúspide | 14,3% (17/119) | 4,9% (3/61) | 4,3% (1/23) | 0,91 | 45,5% (5/11) | 33,3% (8/24) | 0,49 |
| Prótesis mitral | 74,8% (89/119) | 90,2% (55/61) | 78,3% (18/23) | 0,14 | 27,3% (3/11) | 54,2% (13/24) | 0,13 |
| Prótesis aórtica | 37,8% (45/119) | 37,7% (23/61) | 26,1% (6/23) | 0,31 | 27,3% (3/11) | 54,2% (13/24) | 0,13 |
| Prótesis mitral y aórtica | 31,9% (38/119) | 37,7% (23/61) | 21,7% (5/23) | 0,16 | 0 (0/11) | 41,7% (10/24) | 0,01 |
| Reparación mitral | 4,2% (5/119) | 4,9% (3/61) | 8,7% (2/23) | 0,51 | 0 (0/11) | 0 (0/24) | — |
| Cirugía coronaria | 3,4% (4/119) | 1,6% (1/61) | 8,7% (2/23) | 0,12 | 9,1% (1/11) | 0 (0/24) | 0,13 |
| Cirugía valvular previa | 39,5% (47/119) | 26,2% (16/61) | 30,4% (7/23) | 0,7 | 90,9% (10/11) | 58,3% (14/24) | 0,05 |
| EuroSCORE logístico | 12,3±7,4 | 12,1±7,9 | 12,3±8,1 | 0,72 | 16,5±7,2 | 11,2±5,6 | 0,08 |
FEVI: fracción de eyección del ventrículo izquierdo; PAPS: presión arterial pulmonar sistólica.
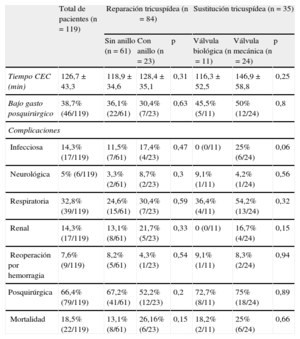
La tabla 2 resume el tiempo de circulación extracorpórea, las complicaciones posquirúrgicas y la mortalidad perioperatoria según el tipo de reparación o de sustitución valvular. No encontramos diferencias significativas en ninguno de los citados parámetros entre los dos tipos de reparación ni entre los dos tipos de sustitución. La mortalidad perioperatoria total fue del 18,5% (22 pacientes).
Resultados quirúrgicos según el tipo de reparación o sustitución valvular
| Total de pacientes (n=119) | Reparación tricuspídea (n=84) | Sustitución tricuspídea (n=35) | |||||
| Sin anillo (n=61) | Con anillo (n=23) | p | Válvula biológica (n=11) | Válvula mecánica (n=24) | p | ||
| Tiempo CEC (min) | 126,7±43,3 | 118,9±34,6 | 128,4±35,1 | 0,31 | 116,3±52,5 | 146,9±58,8 | 0,25 |
| Bajo gasto posquirúrgico | 38,7% (46/119) | 36,1% (22/61) | 30,4% (7/23) | 0,63 | 45,5% (5/11) | 50% (12/24) | 0,8 |
| Complicaciones | |||||||
| Infecciosa | 14,3% (17/119) | 11,5% (7/61) | 17,4% (4/23) | 0,47 | 0 (0/11) | 25% (6/24) | 0,06 |
| Neurológica | 5% (6/119) | 3,3% (2/61) | 8,7% (2/23) | 0,3 | 9,1% (1/11) | 4,2% (1/24) | 0,56 |
| Respiratoria | 32,8% (39/119) | 24,6% (15/61) | 30,4% (7/23) | 0,59 | 36,4% (4/11) | 54,2% (13/24) | 0,32 |
| Renal | 14,3% (17/119) | 13,1% (8/61) | 21,7% (5/23) | 0,33 | 0 (0/11) | 16,7% (4/24) | 0,15 |
| Reoperación por hemorragia | 7,6% (9/119) | 8,2% (5/61) | 4,3% (1/23) | 0,54 | 9,1% (1/11) | 8,3% (2/24) | 0,94 |
| Posquirúrgica | 66,4% (79/119) | 67,2% (41/61) | 52,2% (12/23) | 0,2 | 72,7% (8/11) | 75% (18/24) | 0,89 |
| Mortalidad | 18,5% (22/119) | 13,1% (8/61) | 26,16% (6/23) | 0,15 | 18,2% (2/11) | 25% (6/24) | 0,66 |
CEC: circulación extracorpórea.
Se realizó una evaluación ecocardiográfica de la IT residual tras la cirugía a todos los pacientes dados de alta. La IT era leve o ausente en todos los casos de sustitución valvular, así que comparamos la regurgitación moderada y grave entre los grupos de reparación. La insuficiencia era moderada en 5 casos tratados con anuloplastia sin anillo (5 de 53 supervivientes, el 9,4%) frente a 1 caso tratado con anuloplastia con anillo (1 de 17 supervivientes, el 5,8%), sin diferencias significativas (p=0,51). La insuficiencia era grave en 1 caso de reparación con anillo (1/17 [5,8%]), no se encontró ningún caso en el grupo reparación sin anillo (p=0,1).
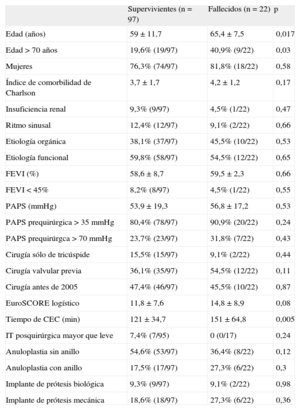
El análisis univariable de la mortalidad perioperatoria (tabla 3) muestra que los únicos factores asociados estadísticamente al resultado muerte fueron la edad (65,4±7,5 frente a 59±11,7 años; p=0,017), la edad > 70 años y el tiempo de circulación extracorpórea (151±64,8 frente a 121±34,7min; p=0,005). No se encontraron diferencias significativas en cuanto a mortalidad perioperatoria en relación con el tipo de intervención realizada. El posterior análisis multivariable incluyó, además de las variables edad y tiempo de circulación extracorpórea, al EuroSCORE logístico, y se asociaron de manera significativa a la mortalidad perioperatoria la edad (OR=1,08; IC95%, 1,01-1,15; p=0,02) y el tiempo de circulación extracorpórea (OR=1,02; IC95%, 1,01-1,03; p=0,007). No se asoció significativamente el EuroSCORE logístico (OR=1,02; IC95%, 0,94-1,1; p=0,66).
Análisis univariable de la mortalidad perioperatoria
| Supervivientes (n=97) | Fallecidos (n=22) | p | |
| Edad (años) | 59±11,7 | 65,4±7,5 | 0,017 |
| Edad >70 años | 19,6% (19/97) | 40,9% (9/22) | 0,03 |
| Mujeres | 76,3% (74/97) | 81,8% (18/22) | 0,58 |
| Índice de comorbilidad de Charlson | 3,7±1,7 | 4,2±1,2 | 0,17 |
| Insuficiencia renal | 9,3% (9/97) | 4,5% (1/22) | 0,47 |
| Ritmo sinusal | 12,4% (12/97) | 9,1% (2/22) | 0,66 |
| Etiología orgánica | 38,1% (37/97) | 45,5% (10/22) | 0,53 |
| Etiología funcional | 59,8% (58/97) | 54,5% (12/22) | 0,65 |
| FEVI (%) | 58,6±8,7 | 59,5±2,3 | 0,66 |
| FEVI <45% | 8,2% (8/97) | 4,5% (1/22) | 0,55 |
| PAPS (mmHg) | 53,9±19,3 | 56,8±17,2 | 0,53 |
| PAPS prequirúrgica >35 mmHg | 80,4% (78/97) | 90,9% (20/22) | 0,24 |
| PAPS prequirúrgca > 70 mmHg | 23,7% (23/97) | 31,8% (7/22) | 0,43 |
| Cirugía sólo de tricúspide | 15,5% (15/97) | 9,1% (2/22) | 0,44 |
| Cirugía valvular previa | 36,1% (35/97) | 54,5% (12/22) | 0,11 |
| Cirugía antes de 2005 | 47,4% (46/97) | 45,5% (10/22) | 0,87 |
| EuroSCORE logístico | 11,8±7,6 | 14,8±8,9 | 0,08 |
| Tiempo de CEC (min) | 121±34,7 | 151±64,8 | 0,005 |
| IT posquirúrgica mayor que leve | 7,4% (7/95) | 0 (0/17) | 0,24 |
| Anuloplastia sin anillo | 54,6% (53/97) | 36,4% (8/22) | 0,12 |
| Anuloplastia con anillo | 17,5% (17/97) | 27,3% (6/22) | 0,3 |
| Implante de prótesis biológica | 9,3% (9/97) | 9,1% (2/22) | 0,98 |
| Implante de prótesis mecánica | 18,6% (18/97) | 27,3% (6/22) | 0,36 |
CEC: circulación extracorpórea; FEVI: fracción de eyección del ventrículo izquierdo; IT: insuficiencia tricuspídea; PAPS: presión arterial pulmonar sistólica.
Tras el alta domiciliaria posquirúrgica, se evaluó la evolución de la IT en 74 de los 97 supervivientes (76,3%) en el seguimiento ecocardiográfico (mediana, 29 [intervalo intercuartílico, 10,5-73,5] meses). Constituyeron el grupo con seguimiento ecocardiográfico 38 pacientes tratados con anuloplastia sin anillo (mediana de seguimiento, 39 [11-86] meses), 11 con anuloplastia con anillo (29 [10,5-73,5] meses), 8 con prótesis biológica (14 [8-32] meses) y 17 con prótesis mecánica (52 [22,5-118,5] meses). Sufrieron IT grave 13 pacientes; de estos, 11 pertenecían al grupo de anuloplastia sin anillo (el 28,9% de los pacientes con seguimiento en este grupo) y 2, al de anuloplastia con anillo (el 18,2% de este grupo). Así, el 26,5% de los supervivientes tratados mediante reparación sufrieron nueva IT grave.
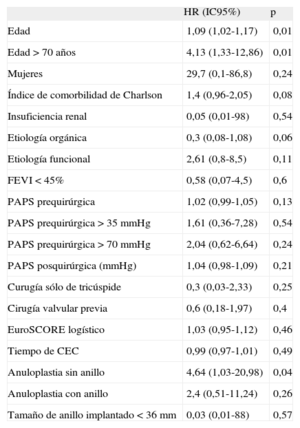
La tabla 4 recoge el análisis univariable de la IT grave en el seguimiento. Se asociaron estadísticamente a esta la edad (p=0,01), la edad > 70 años (p=0,01) y la anuloplastia sin anillo (p=0,04).
Análisis univariable de la insuficiencia tricuspídea grave durante el seguimiento
| HR (IC95%) | p | |
| Edad | 1,09 (1,02-1,17) | 0,01 |
| Edad > 70 años | 4,13 (1,33-12,86) | 0,01 |
| Mujeres | 29,7 (0,1-86,8) | 0,24 |
| Índice de comorbilidad de Charlson | 1,4 (0,96-2,05) | 0,08 |
| Insuficiencia renal | 0,05 (0,01-98) | 0,54 |
| Etiología orgánica | 0,3 (0,08-1,08) | 0,06 |
| Etiología funcional | 2,61 (0,8-8,5) | 0,11 |
| FEVI < 45% | 0,58 (0,07-4,5) | 0,6 |
| PAPS prequirúrgica | 1,02 (0,99-1,05) | 0,13 |
| PAPS prequirúrgica > 35mmHg | 1,61 (0,36-7,28) | 0,54 |
| PAPS prequirúrgica > 70mmHg | 2,04 (0,62-6,64) | 0,24 |
| PAPS posquirúrgica (mmHg) | 1,04 (0,98-1,09) | 0,21 |
| Curugía sólo de tricúspide | 0,3 (0,03-2,33) | 0,25 |
| Cirugía valvular previa | 0,6 (0,18-1,97) | 0,4 |
| EuroSCORE logístico | 1,03 (0,95-1,12) | 0,46 |
| Tiempo de CEC | 0,99 (0,97-1,01) | 0,49 |
| Anuloplastia sin anillo | 4,64 (1,03-20,98) | 0,04 |
| Anuloplastia con anillo | 2,4 (0,51-11,24) | 0,26 |
| Tamaño de anillo implantado < 36mm | 0,03 (0,01-88) | 0,57 |
CEC: circulación extracorpórea; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; PAPS: presión arterial pulmonar sistólica.
Se realizó un seguimiento clínico que incluyó al 97,9% (95 pacientes) de los supervivientes al periodo perioperatorio, con una mediana de 41 [24-89] meses. El 69,7% de estos pacientes superaron el año de seguimiento y el 58%, los 2 años. Dicho seguimiento se completó en 51 pacientes tratados con anuloplastia sin anillo (mediana, 45 [21-103] meses), 17 con anuloplastia con anillo (31 [8-77] meses), 9 con prótesis biológica (17 [7-29] meses) y 18 con prótesis mecánica (52 [22,5-118,5] meses).
Sólo 4 pacientes (4,2%) precisaron reintervención quirúrgica sobre la tricúspide: 2 pacientes del grupo de anuloplastia sin anillo (el 3,9% de ellas) y 2 del grupo de prótesis mecánica (el 11,1% de ellas). La indicación de la nueva cirugía fue la evolución hacia IT grave sintomática en los casos de anuloplastia sin anillo y la trombosis protésica en los de prótesis mecánica.
Se observó trombosis protésica en 4 pacientes (el 22,2% de las prótesis mecánicas); 2 pacientes sufrieron un único evento, que se trató mediante fibrinolisis con buen resultado ecocardiográfico (resolución del cuadro) y clínico, sin complicaciones embólicas. Un paciente sufrió dos episodios y el restante, tres. En estos 2 casos, tras el último evento trombótico se indicó sustitución quirúrgica con implante de prótesis biológica.
La mortalidad durante el seguimiento fue del 13,7% de los pacientes vivos al alta hospitalaria y no perdidos en el seguimiento (13 pacientes de 95). Sufrieron este evento 6 pacientes tratados con anuloplastia sin anillo (el 11,7% de ellas), 1 paciente con anuloplastia con anillo (5,9%), 1 paciente con prótesis biológica (11,1%) y 5 pacientes con prótesis mecánica (27,8%).
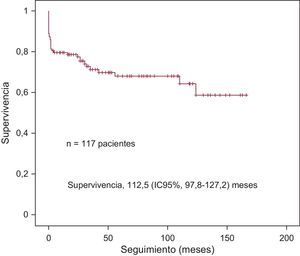
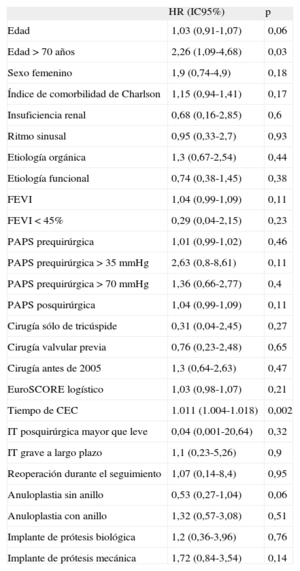
La mortalidad total (perioperatoria y durante el seguimiento) fue del 29,9% de los pacientes incluidos y no perdidos en el seguimiento (35 pacientes). La figura muestra la curva de Kaplan-Meier de la supervivencia. Mediante análisis univariable (tabla 5), se asociaron significativamente a la mortalidad total sólo la edad > 70 años (HR=2,26; IC95%, 1,09-4,68; p=0,03) y el tiempo de circulación extracorpórea (HR=1.011; IC95%, 1.004-1.018; p=0,002). Ambos se incluyeron en un análisis multivariable que mostró asociación significativa de la mortalidad total con la edad > 70 años (HR=2,33; IC95%, 1,06-5,11; p=0,03) y con el tiempo de circulación extracorpórea (HR=1,01; IC95%, 1,01-1,02; p=0,002). No encontramos diferencias significativas tras la comparación directa de la supervivencia libre de eventos entre ambos tipos de reparación (anuloplastia sin anillo, 124,6 [IC95%, 105,9-143,3] meses; anuloplastia con anillo, 35,9 [IC95%, 26,2-45,2] meses; p=0,2) y ambos tipos de sustitución (biológica, 40,9 [IC95%, 25-56,8] meses; mecánica, 86,5% [IC95%, 58,7-114,2%]; p=0,69).
Análisis univariable de la mortalidad total
| HR (IC95%) | p | |
| Edad | 1,03 (0,91-1,07) | 0,06 |
| Edad > 70 años | 2,26 (1,09-4,68) | 0,03 |
| Sexo femenino | 1,9 (0,74-4,9) | 0,18 |
| Índice de comorbilidad de Charlson | 1,15 (0,94-1,41) | 0,17 |
| Insuficiencia renal | 0,68 (0,16-2,85) | 0,6 |
| Ritmo sinusal | 0,95 (0,33-2,7) | 0,93 |
| Etiología orgánica | 1,3 (0,67-2,54) | 0,44 |
| Etiología funcional | 0,74 (0,38-1,45) | 0,38 |
| FEVI | 1,04 (0,99-1,09) | 0,11 |
| FEVI < 45% | 0,29 (0,04-2,15) | 0,23 |
| PAPS prequirúrgica | 1,01 (0,99-1,02) | 0,46 |
| PAPS prequirúrgica > 35mmHg | 2,63 (0,8-8,61) | 0,11 |
| PAPS prequirúrgica > 70mmHg | 1,36 (0,66-2,77) | 0,4 |
| PAPS posquirúrgica | 1,04 (0,99-1,09) | 0,11 |
| Cirugía sólo de tricúspide | 0,31 (0,04-2,45) | 0,27 |
| Cirugía valvular previa | 0,76 (0,23-2,48) | 0,65 |
| Cirugía antes de 2005 | 1,3 (0,64-2,63) | 0,47 |
| EuroSCORE logístico | 1,03 (0,98-1,07) | 0,21 |
| Tiempo de CEC | 1.011 (1.004-1.018) | 0,002 |
| IT posquirúrgica mayor que leve | 0,04 (0,001-20,64) | 0,32 |
| IT grave a largo plazo | 1,1 (0,23-5,26) | 0,9 |
| Reoperación durante el seguimiento | 1,07 (0,14-8,4) | 0,95 |
| Anuloplastia sin anillo | 0,53 (0,27-1,04) | 0,06 |
| Anuloplastia con anillo | 1,32 (0,57-3,08) | 0,51 |
| Implante de prótesis biológica | 1,2 (0,36-3,96) | 0,76 |
| Implante de prótesis mecánica | 1,72 (0,84-3,54) | 0,14 |
CEC: circulación extracorpórea; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; IT: insuficiencia tricuspídea; PAPS: presión arterial pulmonar sistólica.
El presente estudio muestra una mortalidad perioperatoria total del 18,5%, concordante con los resultados descritos para la cirugía valvular tricuspídea, que muestran cifras dispares entre el 0,713 y el 50%14 y generalmente se caracterizan por ser inferiores a las obtenidas en la patología valvular izquierda y la cirugía cardiaca en general15. La serie que probablemente presenta un mayor tamaño muestral sobre la enfermedad tricuspídea muestra una mortalidad perioperatoria del 10,6%16. Nuestra alta mortalidad estuvo condicionada por el elevado riesgo quirúrgico, determinado por varios factores: EuroSCORE logístico medio de 12,3±7,4, escasas intervenciones aisladas sobre la tricúspide (14,3%), elevado porcentaje de pacientes en los que fue preciso el implante de prótesis mitral y aórtica (31,9%) y exceso de procedimientos que eran segunda intervención quirúrgica valvular (39,5%). En este último caso, la IT grave aparece tardíamente en la historia natural de una valvulopatía izquierda en la que, a pesar de su corrección quirúrgica, se desarrolla finalmente una valvulopatía tricuspídea grave que no se había corregido por no ser grave o no se había identificado como orgánica, y están ampliamente descritos los malos resultados de la posterior cirugía valvular tricuspídea cuando es necesaria14,17,18. En este sentido, el hecho de que la intervención sólo de válvula tricúspide no se asociase significativamente con una menor mortalidad perioperatoria podría deberse a que la mayoría de estos pacientes ya habían sido sometidos a cirugía valvular previamente. Del mismo modo, esta asociación entre cirugía valvular previa e intervención sólo tricuspídea pudo evitar que la reoperación se asociara a una mayor mortalidad perioperatoria. El EuroSCORE logístico rozó pero no alcanzó la asociación con la mortalidad perioperatoria, lo cual probablemente indique baja potencia del estudio para señalar dicha asociación.
Nuestros resultados de mortalidad perioperatoria no superan a los que ofrece la que es, según nuestro conocimiento, la mayor serie española que aborda los resultados de la cirugía sobre la válvula tricúspide, publicada por Bernal et al6; esta presenta una mortalidad perioperatoria del 7,6% de los 328 pacientes operados entre 1974 y 2005. Dicho trabajo muestra una población sólo parcialmente comparable a la nuestra, debido a que hasta en el 28% de los pacientes la lesión predominante era estenosis, y la etiología era reumática en todos los casos. En cuanto a las características basales de la serie de Bernal et al la edad media fue casi 9 años inferior, el porcentaje de pacientes ya sometidos a cirugía cardiaca previamente fue el 12,7% menor, el porcentaje de pacientes que recibió prótesis mitral fue el 26,3% menor y el porcentaje de pacientes que precisó prótesis aórtica fue el 12,2% menor. Los porcentajes de reparación mitral y aórtica fueron superiores. Esta menor comorbilidad se reflejó en un tiempo medio de circulación extracorpórea de 19,3min menos. Así, estos datos señalan a un posible cambio en nuestro medio de la epidemiología de la valvulopatía tricuspídea, y actualmente los pacientes llegarían a la cirugía con mayor edad y una valvulopatía más evolucionada que se asocia con mayor frecuencia a polivalvulopatía grave y cirugía valvular previa, todo lo cual implica peores resultados quirúrgicos.
Mediante análisis multivariable, la mortalidad perioperatoria únicamente se asoció a la edad y al tiempo de circulación extracorpórea. Como medio para optimizar dicha mortalidad, se ha publicado la utilidad de indicar la cirugía cuando el paciente se encuentra en clase funcional de la New York Heart Association ≤ III19.
Seguimiento ecocardiográfico y clínicoEl seguimiento mostró IT grave en el 26,5% de los pacientes tratados mediante reparación. Esto concuerda con los resultados obtenidos por otras series tras la reparación17,20. La asociación mediante análisis univariable de la anuloplastia sin anillo con la aparición de IT grave nos lleva, como a trabajos previos20–22, a concluir que, en cuanto a la evolución de la IT en el seguimiento, los resultados de la reparación sin anillo fueron inferiores a los de la anuloplastia con anillo, y se propone como posible mecanismo que el anillo protésico protege de la dilatación del anillo valvular21. La asociación entre la anuloplastia sin anillo y la gravedad de la IT condicionó además la necesidad de reoperación. La reintervención tricuspídea tras reparación valvular previa se ha asociado a mal pronóstico en el postoperatorio y a largo plazo5.
Al establecer una comparación de la mortalidad entre ambos grupos de reparación, observamos una tendencia hacia mayor mortalidad perioperatoria en el grupo de anuloplastia con anillo, a cambio de una tendencia a mayor mortalidad durante el seguimiento en el grupo de anuloplastia sin anillo, todo ello sin diferencias significativas. Que el seguimiento fuera mayor en el grupo de anuloplastia sin anillo pudo condicionar esta tendencia hacia la mayor mortalidad. Disponemos de escasos trabajos, generalmente retrospectivos, que comparen la supervivencia a largo plazo según el tipo de reparación, y los resultados ofrecidos son contradictorios, a favor de la reparación con anillo en algún caso21 y sin diferencias significativas en otros23,24.
Los resultados ecocardiográficos en el postoperatorio de ambos tipos de sustitución valvular fueron excelentes. Durante el seguimiento no se observó caso alguno de dehiscencia en el grupo de prótesis biológica. Sin embargo, la trombosis protésica, complicación asociada a la prótesis mecánica, tuvo elevada incidencia (22,2%). Esto condicionó la necesidad de reoperación en el 11,1% de los pacientes tratados mediante prótesis mecánica, mientras que la necesidad de reintervención fue nula en el grupo de las prótesis biológicas. Estos resultados podrían estar condicionados por el desigual seguimiento, mayor para el grupo de las prótesis mecánicas, y quizá por eso los citados porcentajes de trombosis y dehiscencia protésica contrastan con los presentados en el metaanálisis de Rizzoli et al25. En este trabajo, la trombosis y la dehiscencia protésica se mostraron en proporción semejante, lo que condiciona una tasa de reoperación similar para las prótesis biológicas y mecánicas.
En cuanto a mortalidad perioperatoria y tras el seguimiento, los resultados del grupo de prótesis biológica mejoraron los del grupo de prótesis mecánica, aunque las diferencias no alcanzaron significación estadística. Respecto a la supervivencia a largo plazo tras la sustitución valvular tricuspídea, la bibliografía aporta una vez más datos contradictorios, en unos casos a favor de las prótesis mecánicas19,26, pero la mayoría no encuentra diferencias significativas, como ocurre además en dos metaanálisis que han abordado el tema25,27. Se han descrito como factores asociados a buen resultado a largo plazo tras cirugía de la válvula tricúspide los siguientes: clase New York Heart Association prequirúrgica < IV7,19 y la ausencia de signos ecocardiográficos de insuficiencia cardiaca derecha precoz como la disminución de fracción de acortamiento del anillo tricuspídeo28 o la seudonormalización del RIMP (right index of myocardial performance)19. También se ha propuesto que la indicación del tratamiento quirúrgico de la válvula tricúspide concomitante a la corrección valvular izquierda podría realizarse según el tamaño del anillo tricuspídeo, y no sólo en función de la presencia o el grado de la IT, lo cual podría mejorar la historia natural de la enfermedad valvular13,28.
LimitacionesEste trabajo presenta las limitaciones inherentes a todo estudio observacional retrospectivo. El tamaño relativamente pequeño de la muestra y sus características heterogéneas en cuanto a la etiología de la valvulopatía tricuspídea y la concomitancia de polivalvulopatía dificultan la generalización de los resultados obtenidos. El seguimiento ecocardiográfico a largo plazo no se pudo completar en el 23,7% de los pacientes. Los dos grupos de reparación y de sustitución valvular tuvieron periodos de seguimiento distintos, lo que limita su comparación directa. No disponemos de datos sobre la función ventricular derecha, lo cual puede haber condicionado los resultados.
CONCLUSIONESEl tratamiento quirúrgico de la IT grave presenta en nuestro medio una elevada mortalidad perioperatoria condicionada por un perfil de paciente anciano, con enfermedad polivalvular y cirugía valvular previa. El tratamiento con anuloplastia sin anillo se asoció a aparición de nueva IT grave durante el seguimiento. El implante de prótesis mecánica condicionó, respecto al implante de prótesis biológica, mayor morbilidad en el seguimiento debido a la alta incidencia de trombosis protésica. No se encontraron diferencias significativas en la mortalidad total según el tipo de reparación o sustitución valvular.
CONFLICTO DE INTERESESNinguno.