Los supervivientes a una muerte súbita extrahospitalaria constituyen un grupo de pacientes cada vez más numeroso en las unidades de cuidados intensivos cardiológicos. Nuestro objetivo es caracterizar a estos pacientes y determinar su pronóstico vital y funcional desde una perspectiva actualizada.
MétodosRegistro prospectivo multicéntrico de los pacientes ingresados en cinco unidades de cuidados intensivos cardiológicos con el diagnóstico de muerte súbita extrahospitalaria recuperada entre enero de 2010 y enero de 2012. Se registraron datos clínicos, características de la parada cardiaca, curso hospitalario, así como el estado vital y la situación neurológica al alta y a los 6 meses.
ResultadosSe incluyó a 204 pacientes. En un 64% de los casos se identificó un primer ritmo desfibrilable. El tiempo hasta la recuperación de la circulación espontánea fue de 29±18min. En un 86% se llegó a un diagnóstico etiológico. Un 44% de los pacientes fue dado de alta sin secuelas neurológicas, mientras que el 40% murió en la fase hospitalaria. A los 6 meses, el 79% de los supervivientes al alta permanecían vivos y neurológicamente indemnes o con mínimas secuelas. Un tiempo corto de reanimación, un primer ritmo desfibrilable, un pH al ingreso > 7,1, la ausencia de shock y la aplicación de hipotermia son las variables independientes asociadas a un buen pronóstico neurológico.
ConclusionesLa mitad de los pacientes recuperados de una muerte súbita extrahospitalaria tenían buen pronóstico neurológico al alta. Un 79% de los supervivientes permanecían vivos y neurológicamente indemnes a los 6 meses de seguimiento.
Palabras clave
En España se estima que cada año se producen entre 24.000 y 50.000 paradas cardiacas extrahospitalarias1; de las cuales, en adultos, un 90% podrían corresponder a muertes súbitas cardiacas2. De hecho, la muerte súbita es la forma más frecuente de fallecimiento de los pacientes con cardiopatía isquémica, que es primera manifestación de la enfermedad hasta en un 20% de los casos3.
Su estrecha relación con la enfermedad coronaria hace que la muerte súbita cardiaca frecuentemente se atienda en las unidades de cuidados intensivos cardiológicos (UCC). A pesar de que el número de ingresos por muerte súbita no es cuantitativamente muy importante, el impacto asistencial de estos pacientes es muy relevante4. Las complicaciones cardiológicas, pero fundamentalmente las neurológicas, condicionan largas estancias hospitalarias y un pobre pronóstico vital y funcional5.
Hay gran heterogeneidad de resultados en cuanto a supervivencia y estado funcional al alta hospitalaria5–9. La dificultad para la estratificación neurológica precoz y los malos resultados hasta épocas recientes han contribuido a empobrecer el pronóstico de estos pacientes alimentando el fenómeno conocido como «profecía autocumplida»7.
En nuestro medio hay escasos datos respecto a la muerte súbita extrahospitalaria (MSE) una vez que los pacientes ingresan en el hospital. Las series actuales publicadas son de un solo centro4,8, retrospectivas8, se basan en la tasa de recuperación de la circulación espontánea1 o incluyen la muerte súbita intrahospitalaria9. Por otro lado, se desconoce el impacto en la supervivencia y el pronóstico neurológico que ha tenido la aparición de nuevos algoritmos de reanimación cardiopulmonar (RCP)10, así como la generalización del desfibrilador semiautomático externo (DESA), unos cuidados tras la reanimación protocolizados11, la hipotermia terapéutica12 y la mayor disponibilidad del intervencionismo coronario13. El objetivo de este estudio es describir el problema, caracterizar a estos pacientes y su manejo y conocer el pronóstico neurológico a corto y medio plazo desde una perspectiva actualizada.
MÉTODOSPacientesSe incluyó en un registro prospectivo entre el 1 de enero de 2010 y el 31 de enero de 2012 a todos los pacientes que sobrevivieron a una MSE ingresados en cinco UCC de hospitales universitarios de Cataluña (Hospital Universitario de Bellvitge, Hospital Universitario Vall d’Hebron, Hospital Universitario Germans Trias i Pujol, Hospital Universitario de la Santa Creu i Sant Pau y Hospital Universitario Josep Trueta). Se excluyó a los pacientes con una causa no cardiológica identificada o sin información completa disponible sobre la parada cardiaca. Se recogieron todos los datos relacionados con la parada cardiaca procedentes del servicio de emergencias médicas (lugar de parada, primer ritmo registrado, tiempos y personal de reanimación, uso de DESA o desfibriladores no automáticos y valoración del estado neurológico por escala de Glasgow). Se consideró ritmo desfibrilable tanto su documentación electrocardiográfica como la evidencia de desfibrilación en caso de haberse utilizado un DESA. Asimismo se interrogó a los familiares o testigos sobre las circunstancias de la parada cardiaca y los tiempos transcurridos.
Durante su estancia hospitalaria, se registraron los antecedentes cardiológicos, el primer electrocardiograma y el pH, las constantes vitales, el porcentaje de intubación orotraqueal/traqueotomía, los resultados de pruebas complementarias, los días de intubación y estancia hospitalaria, el estado neurológico y la mortalidad. De los pacientes con síndrome coronario agudo con elevación persistente del segmento ST, se recogieron los tiempos y el procedimiento de reperfusión coronaria urgente y el territorio afectado, y de los pacientes sometidos a coronariografía, la arteria causante del evento.
El tratamiento se dejó a discreción del médico tratante, pero todos los centros disponían del documento de consenso de ILCOR (International Liaison Committee on Resuscitation14). Se empleó hipotermia terapéutica con todos los pacientes comatosos tras parada cardiaca secundaria a fibrilación ventricular o ritmo desfibrilable y que no presentaran criterios de exclusión (coma no hipóxico, embarazo, hipotensión o hipoxemia refractaria, esperanza de vida < 6 meses o hemorragia activa no controlable). Dicha técnica se aplicó según la disponibilidad de los centros y a criterio del médico tratante. Se registró la mortalidad hospitalaria.
Evaluación del estado neurológicoPara la evaluación del estado neurológico al alta, se utilizaron las categorías de Glasgow-Pittsburgh14: cerebral performance category (CPC) 1 (sin secuelas), CPC 2 (discapacidad leve, es independiente, no precisa institucionalización), CPC 3 (discapacidad grave, no es independiente, precisa institucionalización), CPC 4 (estado vegetativo persistente) y CPC 5 (muerte). Al igual que en trabajos previos15, se consideró buena evolución neurológica las dos primeras y mala evolución neurológica o muerte las tres últimas.
SeguimientoSe realizó a los 6 meses en visita médica o entrevista telefónica. Se determinó el estado vital y el estado neurológico aplicando la escala de Glasgow-Pittsburgh.
Centralización de los datosTodos los datos se introdujeron de forma cooperativa y sincrónica utilizando una plataforma web (Zoho Creator®, Zoho Corporation Pvt. Ltd.). Se obtuvo el consentimiento informado para el uso de los datos y la confidencialidad de estos se garantizó según la Ley de Protección de Datos.
Análisis estadísticoLos resultados se presentan como media ± desviación estándar para las variables continuas distribuidas normalmente, medianas para las variables continuas de distribución no gaussiana y porcentajes para las variables categóricas. Se compararon las características de los pacientes con buen y mal pronóstico utilizando la prueba de la χ2 o la exacta de Fisher para las variables categóricas. Las variables cuantitativas se analizaron mediante la prueba de la t de Student, en caso de distribución normal, o la de la U de Mann-Whitney en caso de distribución no normal. Con el fin de valorar el efecto independiente de diversos predictores recogidos al ingreso en la incidencia de buen pronóstico neurológico al alta, se construyó un modelo de regresión logística incluyendo las variables que en el análisis univariable mostraron un valor de p<0,15 (0,10-0,20) además de las que, en virtud de la literatura médica previa, aportan información pronóstica16. Las variables se introdujeron en bloque en el modelo. El nivel de significación se fijó en p < 0,05. Todos los análisis estadísticos se realizaron con el paquete estadístico SPSS 15.0 para Windows (SPSS Inc.; Chicago, Illinois, Estados Unidos).
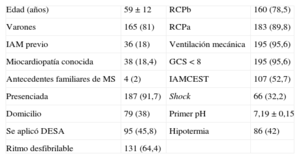
RESULTADOSEntre el 1 de enero de 2010 y el 31 de enero de 2012, se registraron 204 pacientes con MSE recuperada ingresados en las cinco UCC. Las características generales de la muestra se resumen en la tabla 1.
Características generales de la muestra y cadena de supervivencia
| Edad (años) | 59 ± 12 | RCPb | 160 (78,5) |
| Varones | 165 (81) | RCPa | 183 (89,8) |
| IAM previo | 36 (18) | Ventilación mecánica | 195 (95,6) |
| Miocardiopatía conocida | 38 (18,4) | GCS < 8 | 195 (95,6) |
| Antecedentes familiares de MS | 4 (2) | IAMCEST | 107 (52,7) |
| Presenciada | 187 (91,7) | Shock | 66 (32,2) |
| Domicilio | 79 (38) | Primer pH | 7,19 ± 0,15 |
| Se aplicó DESA | 95 (45,8) | Hipotermia | 86 (42) |
| Ritmo desfibrilable | 131 (64,4) |
DESA: desfibrilador semiautomático externo; GCS: escala de coma Glasgow; IAM: infarto agudo de miocardio; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; MS: muerte súbita; RCPa: reanimación cardiopulmonar avanzada; RCPb: reanimación cardiopulmonar básica.
Los datos expresan n (%) o media ± desviación estándar.
A pesar de que mayoritariamente (92%) las paradas cardiorrespiratorias fueron presenciadas, sólo el 29% de los testigos no sanitarios iniciaron maniobras de reanimación. Los tiempos de intervención se describen en la tabla 2. El 78,5% de los pacientes recibieron RCP básica. En un 46% de los pacientes se utilizó un DESA como parte de la RCP básica, pero sólo en un 7% de los casos lo empleó personal no sanitario.
Tiempos de intervención
| Tiempo | |
| PCR-inicio RCP (min) | 6±8 |
| Duración RCPb (min) | 11±9 |
| PCR-RCPa (min) | 16±12 |
| PCR-ROSC (min) | 29±18 |
| ROSC-hospital (min) | 79±76 |
| ROSC-hipotermia (min) | 175±102 |
| Inicio de hipotermia-temperatura objetivo (33°C) (min) | 210±133 |
| Duración de hipotermia (horas) | 23±5 |
PCR: parada cardiorrespiratoria; RCP: reanimación cardiopulmonar; RCPa: reanimación cardiopulmonar avanzada; RCPb: reanimación cardiopulmonar básica; ROSC: recuperación de la circulación espontánea.
Los datos expresan media±desviación estándar.
En un 89,8% se practicó RCP avanzada. En un 64,4% de los pacientes se identificó un ritmo desfibrilable. El sistema de emergencias médicas practicó la RCP avanzada en el 93% de los pacientes, y el resto recibió la RCP avanzada en un entorno sanitario.
A su llegada a la UCC, el 95,6% de los pacientes permanecían en coma espontáneo o farmacológico y un 32% presentaba criterios clínicos de shock. De los 195 pacientes comatosos a su llegada a la UCC, se aplicó hipotermia terapéutica a 86 (44%).
Etiología de la muerte súbita y curso hospitalarioLas pruebas complementarias realizadas para discernir el diagnóstico etiológico fueron: ecocardiografía reglada a todos los pacientes, coronariografía a 133 (64%), test de flecainida a 5 (todos negativos), estudio electrofisiológico a 4 (en 1 paciente se identificó y se ablacionó una vía accesoria; en otro se indujo taquicardia ventricular, y 2 fueron negativos) y finalmente a sólo 1 paciente se le realizó una resonancia magnética cardiaca, que no fue concluyente.
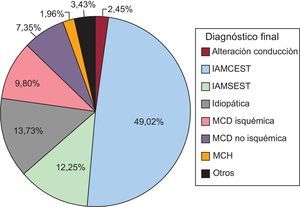
La causa más frecuente de MSE fue la cardiopatía isquémica (71,1%) en sus diferentes expresiones: miocardiopatía dilatada isquémica, infarto agudo de miocardio sin elevación del segmento ST y la más predominante, en un 49% del total de pacientes, el infarto agudo de miocardio con elevación del segmento ST (IAMCEST). Se consideró que la causa era miocardiopatía dilatada no isquémica en el 7,4% de los casos y miocardiopatía hipertrófica en el 2%. Se diagnosticó 1 síndrome de Wolf-Parkinson-White, 1 síndrome aórtico agudo y 1 caso de vasospasmo (0,5% cada uno). Finalmente no se llegó a un diagnóstico etiológico de la MSE en 28 pacientes (13,7%). Los diagnósticos finales se representan en la figura 1.
De los pacientes sin IAMCEST, el 30,2% tenía una miocardiopatía conocida y sólo uno de ellos era portador de un desfibrilador automático implantable que funcionó mal. La incidencia de antecedentes familiares de muerte súbita fue muy baja (4%).
Recibió tratamiento de reperfusión el 89% de los pacientes con IAMCEST (intervencionismo coronario percutáneo primario el 79,6% y trombolisis el 9,3%), con un tiempo síntomas-balón de 178±5min. La localización más frecuente de los IAMCEST fue la anterior (56,4%), y se identificó más frecuentemente como arteria causal la descendente anterior (57,5%).
Los pacientes presentaban marcadores de complejidad, como un tiempo medio de intubación de 6 días, una tasa de traqueotomía del 17% o una estancia hospitalaria media de 24 días.
Supervivencia y evolución del estado neurológicoDe los 204 pacientes registrados, 90 (44,1%) fueron dados de alta neurológicamente indemnes (CPC 1); 12 pacientes (5,8%) tenían leve déficit neurológico (CPC 2); en 9 casos (4,4%) las secuelas neurológicas eran graves y condicionaban estado de dependencia (CPC 3) y 10 (5%) pacientes quedaron en estado vegetativo persistente (CPC 4). La mortalidad hospitalaria fue del 40,7% (83 pacientes). Las causas de muerte más frecuentes fueron las complicaciones neurológicas (50,6%), seguidas del shock cardiogénico (18%) y las infecciones (17%).
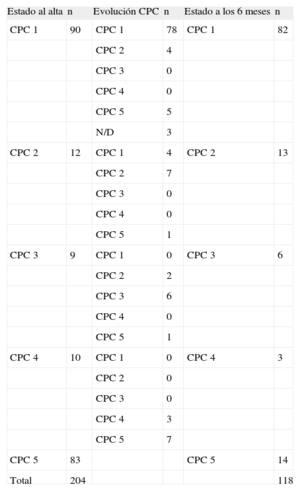
De los 121 pacientes supervivientes, se obtuvo información del seguimiento de 118 (97,5%), con un tiempo medio de seguimiento de 270 días. A los 6 meses, 82 pacientes (69,5%) permanecían en CPC 1; en CPC 2, 13 (11%); en CPC 3, 6 (5%), y en CPC 4, 3 (2,5%); 14 pacientes (11,9%) murieron durante el seguimiento. De estos 14 pacientes, se conoció la causa de la muerte de 8 (en 3 casos, deterioro neurológico; en 2, insuficiencia cardiaca; en 2, recurrencia de la muerte súbita, y en 1, complicación infecciosa). Se implantaron 19 desfibriladores automáticos. El CPC al alta y a los 6 meses y su evolución se describen en la tabla 3.
Evolución del estado neurológico
| Estado al alta | n | Evolución CPC | n | Estado a los 6 meses | n |
| CPC 1 | 90 | CPC 1 | 78 | CPC 1 | 82 |
| CPC 2 | 4 | ||||
| CPC 3 | 0 | ||||
| CPC 4 | 0 | ||||
| CPC 5 | 5 | ||||
| N/D | 3 | ||||
| CPC 2 | 12 | CPC 1 | 4 | CPC 2 | 13 |
| CPC 2 | 7 | ||||
| CPC 3 | 0 | ||||
| CPC 4 | 0 | ||||
| CPC 5 | 1 | ||||
| CPC 3 | 9 | CPC 1 | 0 | CPC 3 | 6 |
| CPC 2 | 2 | ||||
| CPC 3 | 6 | ||||
| CPC 4 | 0 | ||||
| CPC 5 | 1 | ||||
| CPC 4 | 10 | CPC 1 | 0 | CPC 4 | 3 |
| CPC 2 | 0 | ||||
| CPC 3 | 0 | ||||
| CPC 4 | 3 | ||||
| CPC 5 | 7 | ||||
| CPC 5 | 83 | CPC 5 | 14 | ||
| Total | 204 | 118 |
CPC: cerebral performance category; N/D: información del seguimiento no disponible.
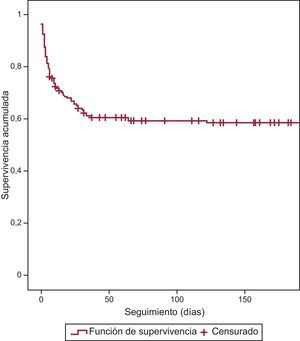
De los 102 pacientes que estaban en CPC 1 o 2 al alta, 93 (91%) se mantenían en CPC 1 o 2 a los 6 meses, mientras que sólo 2 (10%) de los 19 pacientes que fueron dados de alta en categoría CPC 3 o 4 mejoraron a CPC 2. Mientras la mortalidad de los CPC 1-2 fue del 5,8%, la del grupo CPC 3-4 fue del 42%. La mortalidad de estos pacientes se concentra en el primer mes, y después presenta un pronóstico vital bueno. En resumen, tras el seguimiento del total de 204 pacientes, 95 (el 46,5%) se encontraban vivos y neurológicamente indemnes o con mínimas secuelas y 97 (47,5%) habían fallecido.
No se encontraron diferencias significativas en la categoría CPC entre los diferentes centros, ni al alta ni durante el seguimiento. La supervivencia acumulada se representa en la figura 2.
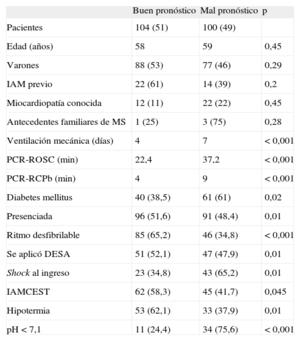
Predictores de buen pronósticoCon el fin de identificar factores predictores de buen pronóstico vital y funcional al alta, se dividió la población en dos grupos: los de buen pronóstico (categorías CPC 1-2) y los de mal pronóstico (CPC 3-5). Se realizó un análisis univariable, cuyo resultado se describe en la tabla 4.
Predictores pronósticos. Análisis univariable
| Buen pronóstico | Mal pronóstico | p | |
| Pacientes | 104 (51) | 100 (49) | |
| Edad (años) | 58 | 59 | 0,45 |
| Varones | 88 (53) | 77 (46) | 0,29 |
| IAM previo | 22 (61) | 14 (39) | 0,2 |
| Miocardiopatía conocida | 12 (11) | 22 (22) | 0,45 |
| Antecedentes familiares de MS | 1 (25) | 3 (75) | 0,28 |
| Ventilación mecánica (días) | 4 | 7 | < 0,001 |
| PCR-ROSC (min) | 22,4 | 37,2 | < 0,001 |
| PCR-RCPb (min) | 4 | 9 | < 0,001 |
| Diabetes mellitus | 40 (38,5) | 61 (61) | 0,02 |
| Presenciada | 96 (51,6) | 91 (48,4) | 0,01 |
| Ritmo desfibrilable | 85 (65,2) | 46 (34,8) | < 0,001 |
| Se aplicó DESA | 51 (52,1) | 47 (47,9) | 0,01 |
| Shock al ingreso | 23 (34,8) | 43 (65,2) | 0,01 |
| IAMCEST | 62 (58,3) | 45 (41,7) | 0,045 |
| Hipotermia | 53 (62,1) | 33 (37,9) | 0,01 |
| pH < 7,1 | 11 (24,4) | 34 (75,6) | < 0,001 |
DESA: desfibrilador semiautomático externo; IAM: infarto agudo de miocardio; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; MS: muerte súbita; PCR: parada cardiorrespiratoria; RCPb: reanimación cardiopulmonar básica; ROSC: recuperación de la circulación espontánea.
Los datos expresan n (%).
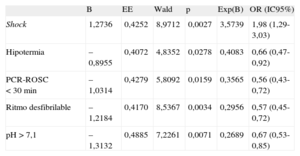
Con base en las variables disponibles al ingreso que en el análisis univariable mostraron un valor de p<0,15, se construyó un modelo multivariable, que mostró que un primer ritmo desfibrilable, un tiempo de recuperación de la circulación espontánea < 30min, un pH al ingreso > 7,1, la ausencia de shock y el uso de hipotermia terapéutica fueron los factores independientes asociados a un buen pronóstico neurológico (tabla 5).
Predictores pronósticos. Análisis multivariable (n = 126)
| B | EE | Wald | p | Exp(B) | OR (IC95%) | |
| Shock | 1,2736 | 0,4252 | 8,9712 | 0,0027 | 3,5739 | 1,98 (1,29-3,03) |
| Hipotermia | –0,8955 | 0,4072 | 4,8352 | 0,0278 | 0,4083 | 0,66 (0,47-0,92) |
| PCR-ROSC < 30 min | –1,0314 | 0,4279 | 5,8092 | 0,0159 | 0,3565 | 0,56 (0,43-0,72) |
| Ritmo desfibrilable | –1,2184 | 0,4170 | 8,5367 | 0,0034 | 0,2956 | 0,57 (0,45-0,72) |
| pH > 7,1 | –1,3132 | 0,4885 | 7,2261 | 0,0071 | 0,2689 | 0,67 (0,53-0,85) |
EE: error estándar; IC95%: intervalo de confianza del 95%; OR: odds ratio; PCR-ROSC: tiempo desde la parada cardiaca hasta la recuperación de la circulación espontánea.
En el presente artículo se describen por primera vez en nuestro país las características clínicas y el pronóstico de una cohorte prospectiva multicéntrica de supervivientes a una MSE ingresados en UCC. A pesar de la gravedad de estos pacientes a su ingreso, un 50% de los pacientes recuperados de MSE tenían buen pronóstico neurológico al alta. A los 6 meses, el 79% de los supervivientes permanecían vivos y neurológicamente indemnes o con mínimas secuelas. Estos esperanzadores resultados contrastan con los obtenidos por otros grupos en población similar.
La series más largas publicadas hasta la fecha en España, con características similares a las del presente estudio, declaran tasas de supervivencia al alta libre de secuelas neurológicas significativas de un 26-35%4,8,9. Ciertos factores podrían explicar, al menos en parte, los buenos resultados: la mejora en la cadena de supervivencia, la aplicación de hipotermia moderada, el tratamiento de reperfusión coronaria y la protocolización de cuidados tras parada cardiaca en la UCC.
En primer lugar, las comunidades con programas de desfibrilación temprana han mostrado supervivencias superiores17. En este sentido, en nuestra población, respecto a las series citadas, se han registrado unos tiempos de respuesta cortos y amplio empleo de DESA por los equipos de emergencias básicos, hechos que se han relacionado con mejoras pronósticas18. Aunque ni el tiempo de respuesta del Sistema de Emergencias ni el uso de DESA fueron predictores independientes de buen pronóstico, sí que contribuyen al tiempo total de parada y la duración y la calidad de la reanimación, resumida en el pH inicial19, que resultó ser un predictor independiente de buen pronóstico.
Dos aspectos relacionados con la cadena de supervivencia constituyen oportunidades de mejora. En primer lugar, la baja tasa de inicio de maniobras por testigos y la escasa utilización de DESA por personal no sanitario, que podrían mejorar con la educación en RCP, el acceso a la desfibrilación pública o sistemas basados en ayuda telefónica20. En segúndo lugar, el largo tiempo de transporte desde la recuperación de la circulación espontánea hasta la llegada al hospital, tiempo en el que se podrían comenzar medidas para el control del síndrome tras parada cardiaca21, así como implementar medidas para acortar dichos tiempos.
Otro de los factores que han podido contribuir a los buenos resultados es la elevada utilización de hipotermia. En nuestra serie, el 44% de los pacientes en coma recibieron hipotermia moderada, tratamiento que se ha demostrado que mejora el pronóstico vital y funcional de los supervivientes a una parada cardiaca extrahospitalaria22. Aunque se trata de una población algo más seleccionada (todos los pacientes con ritmos desfibrilables), la única serie española publicada de hipotermia tras parada cardiaca recuperada presentó una tasa de supervivencia libre de secuelas neurológicas del 44%, similar a la descrita por nosotros23.
En tercer lugar, la elevada incidencia de IAMCEST en nuestra serie y el óptimo tratamiento de este podrían haber contribuido también a los resultados obtenidos. En la serie de Escorial-Hernández, sólo el 40% de los pacientes recibieron tratamiento de reperfusión8. Por el contrario, en nuestro estudio 9/10 pacientes con IAMCEST recibieron tratamiento de reperfusión, circunstancia que se ha asociado a mejora pronóstica en supervivientes a una muerte súbita13. No obstante, probablemente la falta de potencia de nuestro estudio ha impedido demostrar que el tratamiento de reperfusión fuera una variable independiente de buen pronóstico.
En cuanto a la etiología de la muerte súbita, la importancia de la cardiopatía isquémica en nuestra serie es notoria. De modo similar a estudios previos, la enfermedad coronaria explicó 7/10 muertes súbitas24. Cabe destacar en este sentido que en el 13,7% de los casos no se llegó a un diagnóstico etiológico al alta. Se ha señalado que la sistematización de un protocolo de estudio para estos pacientes podría aportar mayor rendimiento diagnóstico25.
En nuestro estudio, a pesar de no tener un protocolo común, compartimos, además de una forma de manejo sistemático, un documento general sobre el tratamiento de estos pacientes. Sunde et al. publicaron que la protocolización y la sistematización de cuidados mejoraron la tasa de supervivientes indemnes neurológicamente al alta desde un 26 a un 56%26, datos que por otra parte son similares a los obtenidos en el presente trabajo. Respecto al pronóstico neurológico, uno de los factores que ha llevado a la abstención terapéutica y el fenómeno de la profecía autocumplida en estos pacientes es la posibilidad de contribuir a aumentar el número de pacientes con déficit neurológicos graves o estado vegetativo permanente7. En el presente estudio, sólo 19 pacientes fueron dados de alta con CPC 3-4, con pronóstico muy desfavorable, ya que a los 6 meses 8 de ellos habían fallecido. Sin embargo, el 85% de los supervivientes al alta estaban en buen estado neurológico, hecho que aumentó (92%) a los 6 meses. Dichos resultados reflejan, de manera similar que trabajos previos, que la evolución de los pacientes neurológicamente preservados tras el alta hospitalaria es excelente27.
En este sentido, la aplicación de los nuevos algoritmos de la cadena de supervivencia y la utilización de un protocolo de hipotermia han modificado los que hasta ahora eran marcadores pronósticos28. Por ello, son necesarios estudios que aporten información en este nuevo escenario. En nuestro registro, los marcadores de mejor pronóstico (primer ritmo desfibrilable, menor tiempo de recuperación de la circulación espontánea, mejor situación hemodinámica expresada por pH > 7,1, menor incidencia de shock cardiogénico y la utilización de hipotermia terapéutica) son expresión de la mejora en la cadena de supervivencia desde la atención extrahospitalaria a los cuidados hospitalarios. No obstante, un importante punto de mejora es la escasa realización de maniobras de reanimación básicas por los testigos no sanitarios de una MSE.
LimitacionesA pesar de la fortaleza que confiere ser un registro prospectivo de todos los pacientes recuperados de MSE, a nuestro juicio la limitación más importante es la dificultad de conseguir información precisa referente a los tiempos de parada, el inicio de maniobras de reanimación y su duración, ya que no se han podido medir directamente, sino a través de los informes de los servicios de emergencias extrahospitalarias y del interrogatorio a los familiares/testigos. En segundo lugar, el manejo de los pacientes no siguió un protocolo común en los cinco centros, aunque sí basado en un documento consultivo común. Por otro lado, el seguimiento no presencial de la mayoría de los pacientes y el empleo de la clasificación CPC no permiten un análisis preciso de estado neurológico; sin embargo, esta metodología está recomendada por varios documentos de consenso14. Por último, al tratarse de un registro desde la UCC, los pacientes fallecidos antes de llegar al hospital y los que ingresan en otras áreas asistenciales (cuidados intensivos, reanimación, etc.) no están representados, y por ello las conclusiones no son extrapolables a la población general.
CONCLUSIONESEn nuestra serie, la enfermedad coronaria explicó el 70% de las muertes súbitas. La mitad de los pacientes recuperados de MSE ingresados en las UCC tenían buen pronóstico vital y neurológico al alta y a los 6 meses, pese a presentar datos de gravedad a su llegada. La mayoría de las muertes durante el seguimiento ocurrieron precozmente y en los pacientes neurológicamente más deteriorados. Las mejoras en la atención inicial a la parada cardiaca y un manejo sistemático y protocolizado del síndrome posparada cardiaca pueden haber contribuido a los buenos resultados. Son necesarios programas de educación sanitaria que permitan incrementar la realización de maniobras de RCP básicas por personal no sanitario testigo de una MSE.
AGRADECIMIENTOSA los Dres. Ángel Loma-Osorio y Coloma Tirón por su apoyo y revisión crítica del artículo.
CONFLICTO DE INTERESESNinguno.