Palabras clave
INTRODUCCIÓN
La comunicación interventricular (CIV) aislada o formando parte de una lesión más compleja se observa en el 20% de los niños con alguna cardiopatía1. En la CIV aislada se produce el cierre espontáneo en la mayoría de los casos. En pocos casos se requiere tratamiento con diuréticos, digital o inhibidores de la enzima de conversión de la angiotensina (IECA) y sólo una minoría requiere tratamiento quirúrgico con circulación extracorpórea. O'Laughlin y Mullins publicaron en 1988 el primer caso de cierre percutáneo de la CIV utilizando el dispositivo de doble paraguas de Bard2. Desde entonces se han publicado pocos casos con diversos dispositivos, como el Clamshell3, dispositivo de Sideris4 y, últimamente, el nuevo dispositivo Amplatzer (AGA, Medical Corporation, Estados Unidos)5-8. En nuestro país también se ha utilizado este último dispositivo en el cierre de una comunicación interventricular en el contexto de un infarto de miocardio9. La seguridad y eficacia del dispositivo han despertado un gran interés en el cierre percutáneo de la CIV, incluso a una edad temprana, aunque se recomienda esta técnica en niños cuyo peso sea mayor de 7 kg.
CASOS CLÍNICOS
Pacientes
En la tabla 1 presentamos las características generales de los pacientes. La edad media fue de 11,25 años (intervalo, 0,6-26) y el peso promedio fue 30,9 kg (intervalo, 7,2-57).
Caso 1
Niña con truncus arteriosus tipo I (TA-I). Además de la CIV subarterial, había otra CIV muscular apical de 9 mm. A los 28 días de vida se decidió realizar un banding de arteria pulmonar para controlar la insuficiencia cardíaca. A los 6 meses de edad, a fin de evitar una ventriculotomía derecha extensa o una ventriculotomía izquierda apical en la cirugía correctora, se realizó el cierre percutáneo de la CIV apical con un dispositivo Amplatzer para cierre de CIV (DA) de 6 mm implantado por vía transyugular (fig. 1). El control por ecocardiografía mostró el DA en posición correcta (fig. 2A). Tras el cierre percutáneo de la CIV hubo una mejoría clínica, y 1 mes más tarde se hizo la reparación quirúrgica del truncus arteriosus con bioprótesis de Contegra y cierre de CIV subarterial, además de la retirada del banding de la arteria pulmonar, mostrando una salida de bomba extracorpórea sin incidencias y un postoperatorio favorable; la paciente fue extubada 20 h después.
Fig. 1. Caso 1. A: ventriculografía izquierda. B: captura de la guía (flecha) introducida desde vena femoral. Catéter-lazo (asterisco) introducido por vena yugular interna derecha. C: ventriculografía izquierda, comunicación interventricular (CIV) ocluida por Amplatzer que aún está sujeto por catéter de liberación (flecha). D: Amplatzer (flecha) ya libera do que ocluye completamente la CIV. VD: ventrículo derecho; VI: ventrículo izquierdo.
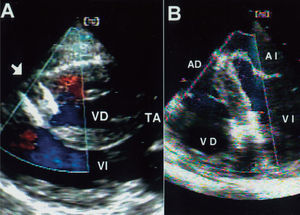
Fig. 2. A: ecocardiografía transtorácica, corte paraesternal de eje largo (caso 1). Obsérvese el Amplatzer, aún no liberado, que ocluye la comunicación interventricular (CIV) muscular apical. Obsérvese la pared libre del ventrículo derecho hipertrófica, el catéter liberador en cavidad del ventrículo derecho y la CIV subaórtica adyacente al truncus arteriosus (TA). B: ecocardiografía transesofágica, corte de 4 cámaras, en la que se observa el Amplatzer que ocluye la CIV muscular apical (caso 4).
Caso 2
Paciente con diagnóstico prenatal de dextrocardia, situs inversus, transposición de grandes arterias congénitamente corregida (L-TGA) y bloqueo cardíaco completo, con una frecuencia ventricular de 60 lat/min durante la gestación. En período neonatal se descubrió una comunicación interventricular perimembranosa. A las 2 semanas de vida le fue implantado un marcapasos endocavitario bicameral permanente. Durante el seguimiento clínico durante años sucesivos se juzgó que la CIV de septo perimembranoso era pequeña, aunque a lo largo de la infancia el hiperaflujo pulmonar fue en aumento, y desarrolló una insuficiencia de la válvula tricúspide (válvula auriculoventricular sistémica) ligera-moderada, por lo que recibía tratamiento con IECA y diuréticos. A los 8 años de edad, se decidió el cierre de la CIV con un DA de 6 mm para evitar, en lo posible, la sobrecarga de volumen del ventrículo derecho (ventrículo sistémico) y así tratar indirectamente la insuficiencia de la válvula tricúspide de una cardiopatía anatómicamente compleja. Tras el cierre percutáneo, ha tenido buena evolución y se ha podido suspender los diuréticos.
Caso 3
Niña con ventrículo derecho de doble salida (VDDS) que en el período neonatal requirió una fístula de Blalock-Taussig por la estenosis pulmonar valvular e infundibular. A los 2 años se realizó la corrección completa, fuera de nuestro país, por petición de los padres. Allí se realizó el cierre de la CIV, la ampliación del tracto de salida del ventrículo derecho y una valvulotomía pulmonar con parche transanular. Tras la cirugía, se detectó una pequeña CIV residual periparche interventricular con 2 mínimas CIV en el ápex ventricular, con gradiente infundibular de 45 mmHg. A los 5 años, el gradiente infundibular había aumentado hasta 80 mmHg y también se confirmó una CIV residual que se consideró que era de tamaño pequeño. A los 7 años, el mismo grupo quirúrgico realizó una cirugía cardíaca en la que se llevó a cabo una infundibulectomía del tracto de salida del ventrículo derecho, sin cerrar la CIV residual de la primera cirugía por considerarla de reducido tamaño. Tras la última cirugía, la paciente presentó signos de fallo cardíaco biventricular, por lo que se la trató con diuréticos, digoxina y vasodilatadores. Seis meses más tarde, con un QP/QS de 2,9, se cerró percutáneamente la CIV residual con un DA de 10 mm. Tras el cierre hubo una mejoría clínica, por lo que se suspendió la medicación.
Caso 4
Adulto con CIV muscular de septo trabeculado en grado funcional II que presentaba cardiomegalia con un índice cardiotorácico del 63% e hiperaflujo pulmonar en la radiografía del tórax, así como un QP/QS de 1,93/1. Tras el cierre de la CIV con DA de 8 mm refirió mejoría en su condición física.
Técnica
En todos los casos se practicó después de obtener el consentimiento informado. Los pacientes fueron sometidos a anestesia general. Se hizo un ecocardiograma transesofágico antes del cateterismo terapéutico y se dejó la sonda para control ecocardiográfico durante el procedimiento. En los 4 casos utilizamos el dispositivo Amplatzer para CIV muscular. En términos generales, seguimos las técnicas ya descritas para el cierre de la CIV muscular6 y perimembranosa7, con las siguientes variaciones:
- El diámetro de la CIV se midió con la ecocardiografía transesofágica y la angiografía en vez del método con balón.
- Caso 1: para evitar el circuito arteriovenoso, modificamos la técnica haciendo un circuito venovenoso. Para ello, por vía venosa femoral y en forma anterógrada, avanzamos hasta el ventrículo izquierdo después de cruzar el foramen oval. Desde allí avanzamos la guía, cruzando la CIV, hasta el ventrículo derecho y luego a la aurícula derecha. La guía se capturó y exteriorizó con un catéter-lazo introducido por la vena yugular derecha, completándose el circuito venovenoso. Por la vena yugular derecha, se introdujo una vaina de 6 Fr de 180°, y por ella, el DA de 6 mm.
- Caso 2: la CIV perimembranosa se atravesó desde el ventrículo izquierdo con una guía de intercambio (fig. 3); ésta se dejó en la arteria pulmonar derecha y allí fue capturada con una catéter-lazo introducido por la vena femoral. El acceso con la vaina de Mullins se realizó desde vena femoral, dejándose la punta terminal en la aorta ascendente. La retirada gradual y cuidadosa de la vaina permitió la expansión del primer disco en el tracto de salida del ventrículo izquierdo una vez pasada la válvula aórtica hasta adaptar el disco a la CIV.
Fig. 3. Caso 2. A: angiografía de la comunicación interventricular (CIV) desde el ventrículo derecho anatómico con catéter (flecha) introducido desde la aorta. Los asteriscos negros señalan electrodos del marcapasos bicameral. B: Amplatzer desplegado en la CIV. C: liberación del dispositivo, catéter liberador (flecha). D: la aortografía demuestra la competencia valvular aórtica.
- Casos 3 y 4: una vez realizado el circuito arterio-venoso con la guía (vena yugular-arteria femoral), se avanzó la vaina de Mullins hacia la cavidad del ventrículo izquierdo, con el extremo orientado hacia el tracto de salida del ventrículo izquierdo; allí se abrió el primer disco del DA, retirando vaina y dispositivo hasta apoyarlo en la pared septal de la CIV. En todos se realizó anticoagulación con heparina intravenosa durante el cateterismo (100 U/kg), y posteriormente se pautó aspirina en dosis de 5 mg/kg/día durante 6 meses. Se administraron 3 dosis de cefazolina, una durante el procedimiento y las restantes cada 8 h. El seguimiento de los pacientes (promedio, 7 meses/paciente) se hizo en la consulta externa. Tanto en la exploración física como en la ecocardiografía (fig. 2B), no observamos evidencia de CIV residual. Tampoco observamos complicaciones como insuficiencia aórtica, nueva lesión valvular o agravamiento de la preexistente, hemólisis, embolia sistémica o endocarditis infecciosa.
DISCUSIÓN
El paso cualitativo de poner a punto la técnica percutánea de cierre de la CIV por DA se plantea como una evolución lógica de los grupos de cardiología intervencionista que ya tienen experiencia en el cierre de la comunicación interauricular ostium secundum. Aunque conceptualmente el cerrado de CIV es muy similar al cerrado de CIA, entre ambas técnicas existen diferencias importantes, como: a) dificultad para localizar y precisar el tamaño de la CIV, y b) necesidad de establecer el circuito veno-arterial con guía de intercambio, que permita avanzar de forma estable y segura el catéter-guía, para transportar el dispositivo adecuado hasta el lugar de la implantación en la CIV. Para ello se han de establecer básicamente dos estrategias, según se localice anatómicamente la CIV. La CIV apical o de septo trabeculado se cruza desde la aorta por el ventrículo izquierdo, y una vez el catéter se encuentra en el ventrículo derecho, se deja flotar la guía, para capturarla con el catéter-lazo en la arteria pulmonar desde la vena yugular. Sin embargo, en las CIV de septo perimembranoso, el circuito venoarterial se realiza desde la aorta-ventrículo izquierdo a través de la CIV hacia el ventrículo derecho con captura de la guía de intercambio en arteria pulmonar, que se exterioriza por la vena femoral. En el caso 1 modificamos esta técnica y establecimos un circuito venovenoso debido a que en una niña pequeña evitamos utilizar la vaina de Mullins de 6 Fr por la arteria femoral; esto pudo hacerse por vía venosa femoral gracias a la presencia de un foramen oval permeable. El paso de la CIV suele ser más sencillo de lo esperado; por otra parte, la captura de la guía de intercambio por catéter-lazo ha de ser una maniobra poco traumática. Se recomienda capturar la guía con catéter-lazo en la arteria pulmonar, pero puede capturarse en la aurícula derecha, como en nuestro caso de truncus arteriosus. La medida por catéter-balón de la CIV es una maniobra adicional que puede desplazar la guía y aporta poca información. Nuestra preferencia es ajustar los diámetros del dispositivo al diámetro obtenido por ecocardiografía y ventriculografía a fin de ajustar el diámetro del dispositivo al diámetro de la CIV.
El catéter-guía, una vez cruzada la CIV, es aconsejable ubicarlo lo más distalmente posible de la CIV con el fin de evitar una desubicación del catéter-guía en el ventrículo izquierdo durante la maniobra transportadora del dispositivo. Se recomienda7 que, en la CIV de septo perimembranoso, el catéter-guía se ubique en el ápex del ventrículo izquierdo, para asegurar la maniobra de apertura y no pinzar la válvula aórtica con el disco ventricular izquierdo; sin embargo, hemos observado que esta maniobra puede realizarse de modo diferente, ubicando el catéter-guía en la aorta y retirándolo lentamente hasta el tracto de salida del ventrículo izquierdo con la ayuda de ecocardiografía transesofágica, mientras que en la CIV apical y de septo trabeculado, la parte distal del catéter-guía ha de situarse en el ventrículo izquierdo lo más distante posible de la CIV.
En 2 de nuestros pacientes, el procedimiento ha sido complementario al tratamiento quirúrgico. En el caso 1, la presencia de 2 CIV aconsejó primero la realización del banding pulmonar y luego el cerrado por dispositivo de la CIV apical. De este modo se evitó la ventriculotomía apical izquierda que hubiera sido necesaria además de la cirugía de la reparación completa de truncus arteriosus, junto con la CIV subarterial. En el caso 3, evitamos una cuarta cirugía cardíaca.
La indicación de cierre primario en el caso 2, con un QP/QS de 1,8, se realizó porque se trataba de una L-TGA que ya empezaba a tener fallo del ventrículo derecho (sistémico) que se manifestaba por la insuficiencia tricuspídea.
El caso 4 era un paciente que había llevado una vida normal, salvo una intolerancia a hacer grandes esfuerzos. Tenía, además, signos radiológicos de hiperaflujo pulmonar con un QP/QS de 1,9/1. Tras el cierre percutáneo presentó mejoría clínica y mejoró la tolerancia a grandes esfuerzos. Aunque se trata de un solo caso, el cierre percutáneo podría ser una indicación en los pacientes en los que el cierre espontáneo de la CIV es ya poco probable (adolescentes y adultos). Uno de nuestros pacientes tenía un bloqueo auriculoventricular completo y llevaba un marcapasos definitivo desde el nacimiento. En el resto no observamos defectos de conducción tras la implantación del dispositivo, aunque se ha observado bloqueo auriculoventricular8 transitorio en el 2,8% de los casos y completo en el 1,9%.
Aunque sólo uno de nuestros casos era una CIV perimembranosa, no observamos interferencia con la válvula aórtica; si bien esta complicación no se ha observado con el dispositivo de Amplatzer, sí se ha apreciado con otros dispositivos1.
COMENTARIO
A pesar de que nuestra experiencia inicial es aún escasa, encontramos que el cierre primario de la CIV llevado a cabo cuidadosamente no tiene complicaciones. El cierre de la CIV se puede realizar en los pacientes en los que la cirugía tiene un riesgo muy alto, lo que evita una nueva cirugía o, en otros casos, disminuye el riesgo de cirugías muy complejas. En pacientes muy poco sintomáticos y con muy poca probabilidad de cierre espontáneo de la CIV, el cierre percutáneo podría convertirse en una alternativa.
Correspondencia: Dr. C. Mortera.
Cardio-Hemodinámica. Hospital Sant Joan de Déu.
Pg. de Sant Joan de Déu, 2. 08950 Esplugues de Llobregat. Barcelona. España.
Correo electrónico: cmortera@hsjdbcn.org