Palabras clave
INTRODUCCION
Durante los últimos meses se ha publicado una cantidad importante de artículos en el campo de las arritmias y la electrofisiología cardiaca. Como en años precedentes, buena parte del esfuerzo investigador está relacionado con la fibrilación auricular, probablemente por su prevalencia, su elevada morbimortalidad y la dificultad de su tratamiento, que representa un reto sanitario importante e incide de forma apreciable en el gasto sanitario. Las cuestiones relacionadas con los dispositivos implantables (especialmente desfibriladores y dispositivos de terapia de resincronización) ocupan también un lugar importante en la literatura científica de este último año. Revisaremos algunos de los estudios más relevantes aparecidos en los últimos meses, clasificándolos en varios grupos: genética y enfermedades hereditarias, bradiarritmias y marcapasos, terapia de resincronización, desfibriladores implantables, fibrilación auricular (FA), síncope, estratificación de riesgo en prevención primaria de muerte súbita y nuevas guías de práctica clínica.
GENÉTICA Y ENFERMEDADES HEREDITARIAS
En el 2006 se publicaron varios estudios genéticos que inciden en la relación de la displasia arritmogénica del ventrículo derecho (DAVD) con mutaciones de los genes que codifican las proteínas de los desmosomas cardiacos: plakofilina-2, plakoglobina, desmoplakina y desmogleína-2. Así, en una población de pacientes holandeses se encontraron mutaciones en el gen de la plakofilina-2 en casi la mitad de los casos con criterios clínicos de DAVD1, mientras un grupo investigador londinense hallaba mutaciones en el gen de esta proteína en el 11% de los individuos afectados2. Por su parte, Pilichou et al3 encontraron mutaciones de la desmogleína-2 en el 10% de una población italiana portadora de la enfermedad. Estos datos indican que se puede encontrar una alta tasa de diagnósticos genéticos positivos en los pacientes con DAVD y plantean el papel cada vez más relevante de la información genética en el diagnóstico y el tratamiento clínico de los pacientes con enfermedades cardiacas potencialmente hereditarias.
Gollob et al4 han encontrado mutaciones somáticas del gen de la conexina 40 (proteína involucrada en la activación eléctrica coordinada de los miocitos auriculares) en 4 de 15 pacientes con FA idiopática, lo que plantea cuestiones muy interesantes sobre el origen genético de esta arritmia en algunos casos.
Por otro lado, es conocido que en el desarrollo de la miocardiopatía hipertrófica participan alteraciones en al menos 12 genes, cuya prevalencia es distinta según la población que se estudie. Así, se ha encontrado que las mutaciones en el gen de la cadena pesada de la betamiosina cardiaca (gen MYH7b) se hallan en menos del 5% de las familias españolas con miocardiopatía hipertrófica, en contraste con lo que ocurre con otras poblaciones caucásicas, en las que las alteraciones de este gen son las más frecuentes y se dan en hasta el 30% de los pacientes estudiados5. El estudio genético de la miocardiopatía hipertrófica es prometedor y probablemente incida en la disminución de la gran heterogeneidad en el tratamiento de esta enfermedad, en especial si tenemos en cuenta el riesgo de muerte súbita que conlleva6.
Finalmente, en ausencia de información genética, las pruebas farmacológicas también pueden resultar útiles en el diagnóstico de algunas canalopatías. Así, Vyas et al7 estudian el valor diagnóstico de la administración controlada de adrenalina en el diagnóstico del síndrome de QT largo (SQTL). La respuesta de individuos normales a la administración del fármaco consiste en un acortamiento de la duración del intervalo QT, pero en el SQTL tipo 1 (SQTL-1) se observa una respuesta paradójica. Los autores estudian el efecto de una perfusión de adrenalina en dosis progresivamente crecientes en 147 pacientes con genotipo conocido y observan una respuesta paradójica (definida como un incremento de la duración del intervalo QT > 30 ms) en el 92% de 40 pacientes con SQTL-1, comparado con un 18% de los individuos sin alteración genética. La sensibilidad del test para el diagnóstico de esta entidad fue del 92,5%, con una especificidad del 86%. Los autores concluyen que esta prueba ofrece una buena precisión diagnóstica para desenmascarar los casos dudosos de SQTL-1.
BRADIARRITMIAS Y MARCAPASOS
Healey et al8 presentan un metaanálisis de 5 estudios aleatorizados que comparan la estimulación auricular monocameral o bicameral aurícula ventricular (AV) frente a la monocameral ventricular en pacientes con indicación de marcapasos definitivo. Se incluyó a más de 5.000 pacientes en el análisis, que no mostró diferencias significativas entre los dos modos de estimulación en cuanto a la mortalidad global o los ingresos por insuficiencia cardiaca. Por el contrario, la incidencia de FA e ictus se redujo de forma significativa con la estimulación auricular monocameral o bicameral AV, especialmente en los pacientes con disfunción sinusal. El metaanálisis confirma, a grandes rasgos, los resultados de los principales estudios individuales. Los autores comentan en la discusión que la incorporación de nuevos algoritmos que permiten respetar la conducción AV propia del paciente o la estimulación en modo AAI cuando sea posible podrían modificar estos resultados en algunos subgrupos de pacientes, ya que evitarían el potencial efecto deletéreo de la estimulación ventricular derecha.
RESINCRONIZACION
La estimulación biventricular sigue consolidando su papel en el tratamiento de pacientes con insuficiencia cardiaca avanzada y asincronía ventricular. El estudio CARE-HF, cuyos resultados se publicaron en abril de 2005, incluyó a 813 pacientes con insuficiencia cardiaca en clase funcional III-IV de la NYHA con fracción de eyección ≤ 35% y una duración del complejo QRS > 150 ms o entre 120 y 150 ms, pero con criterios ecocardiográficos de asincronía. El estudio mostró una reducción en el objetivo primario (muerte u hospitalización por evento cardiovascular) en un seguimiento medio de 29,4 meses. Los investigadores del estudio han publicado recientemente los resultados de una extensión adicional de 8 meses del período de seguimiento9. La terapia de resincronización redujo la mortalidad por cualquier causa un 40% (del 12,2 al 7,9% anual), manteniéndose el beneficio observado en el período de observación inicial. La muerte súbita presentó también una reducción significativa en los pacientes con terapia de resincronización, pese a que el dispositivo utilizado en el estudio era un estimulador biventricular sin desfibrilador asociado. Por otro lado, la persistencia del beneficio observado con el dispositivo durante un tiempo más prolongado implica una reducción de los costes estimados de la terapia, lo que mejora la relación coste-beneficio de ésta.
Otro estudio publicado durante el año 2006 es el HOBYPACE10, cuyos resultados indican que la estimulación biventricular puede también ser útil en pacientes con disfunción ventricular (diámetro telediastólico≥ 60 mm y fracción de eyección del ventrículo izquierdo ≤40%) y necesidad de estimulación ventricular permanente por bloqueo AV. En total, 33 pacientes que cumplían los criterios de inclusión fueron aleatorizados para recibir estimulación monocameral (ápex del ventrículo derecho) o biventricular de forma ciega y cruzada en períodos de 3 meses, y al final de cada período se evaluaron los parámetros de función ventricular, capacidad de ejercicio y calidad de vida. Comparada con la monocameral, la estimulación biventricular redujo los diámetros ventriculares de forma significativa y mejoró la fracción de eyección (de 28,5 ± 11,2 a 34,8 ± 8,9%; p < 0,001), el consumo pico de oxígeno, la clase funcional y la puntuación de calidad de vida. El efecto de la estimulación biventricular fue similar para los pacientes en ritmo sinusal y en FA crónica. Los autores concluyen que se debe considerar la estimulación biventricular en estos pacientes.
DESFIBRILADORES IMPLANTABLES
La administración de terapias de choque inapropiadas debidas a episodios de taquiarritmia supraventricular constituye un problema de los desfibriladores implantables que no ha sido totalmente resuelto. Los choques del dispositivo crean ansiedad en los pacientes, disminuyen su calidad de vida, consumen batería y pueden ser proarrítmicos, por lo que la discriminación correcta entre taquicardias ventriculares y supraventriculares es muy importante. Teóricamente, los modelos bicamerales con electrodo auricular podrían discriminar el tipo de taquicardia mejor que los dispositivos unicamerales, cuya única información proviene del electrodo ventricular. Sin embargo, este hecho no ha sido comprobado de manera concluyente en la literatura científica. El estudio «Detect supraventricular tachycardia»11 se inició con la idea de demostrar este supuesto. Para ello, se aleatorizó a 400 pacientes con indicación de desfibrilador a recibir un modelo monocameral o bicameral y se programaron los diversos algoritmos de discriminación de una forma optimizada. El estudio mostró una disminución significativa de la tasa de detección inadecuada del 40 al 31%, lo que supuso una reducción de un 25% en el número de terapias inapropiadas. Sin embargo, las terapias de choque no disminuyeron en los pacientes con un desfibrilador bicameral, probablemente porque se tendió a programar menos terapias de sobrestimulación en este grupo. Por tanto, el beneficio clínico obtenido al añadir un electrodo auricular resultó modesto globalmente en este estudio.
Otra opción utilizada a menudo para evitar terapias inapropiadas del desfibrilador es la utilización de fármacos antiarrítmicos de clase III, que pueden reducir los episodios de FA en pacientes con cardiopatía estructural. Algunos estudios han indicado que la administración de amiodarona podría empeorar el umbral de desfibrilación, pero esta información no ha sido validada en un estudio prospectivo y aleatorizado en pacientes con desfibriladores modernos. El estudio OPTIC se diseñó para comparar la eficacia de la amiodarona y el sotalol con el tratamiento convencional con bloqueadores beta en cuanto a la incidencia de choques por cualquier causa en portadores de desfibrilador. Además, recientemente se ha publicado un subestudio sobre las modificaciones en los umbrales de desfibrilación con el tratamiento antiarrítmico12. La administración de amiodarona produjo una pequeña elevación estadísticamente significativa del umbral cuando se comparó con el grupo que recibió bloqueadores beta, pero el incremento fue pequeño (de 8,53 ± 4,29 a 9,82 ± 5,84 J) y sin repercusión clínica, por lo que los autores concluyen que, con los dispositivos modernos de desfibrilación, no es necesario, en general, practicar una prueba de desfibrilación cuando se inicia la terapia con amiodarona.
Otro subestudio publicado en el año 2006 evalúa la relación entre episodios de arritmia ventricular tratados por el desfibrilador y muerte súbita. Se basa en los datos del estudio DEFINITE, diseñado para evaluar la eficacia del desfibrilador implantable en la prevención primaria de muerte arrítmica en pacientes con miocardiopatía dilatada no isquémica. El resultado del estudio global mostró una reducción significativa de la muerte súbita y una tendencia hacia una menor mortalidad global en el grupo de pacientes aleatorizados a recibir el dispositivo comparado con el grupo de tratamiento convencional13. En el subestudio se han utilizado los datos para evaluar si la aparición de una arritmia ventricular tratada mediante choque en un paciente portador de desfibrilador podría haber resultado en la muerte súbita del paciente en caso de que no llevara el dispositivo14. Para ello se compara el número de choques apropiados en el grupo aleatorizado a desfibrilador con el número de muertes súbitas en el grupo de tratamiento convencional, y se observa una diferencia significativa entre ambas cifras. El número de choques es casi el doble que el de eventos de muerte súbita en el grupo de tratamiento convencional (33 frente a 15, respectivamente) y es similar a la suma de eventos de muerte súbita y síncope en los pacientes sin desfibrilador. Esto demuestra que una arritmia ventricular terminada por un choque del desfibrilador no siempre implicaría la muerte arrítmica del paciente en caso de que no hubiese llevado implantado el dispositivo, pues en aproximadamente la mitad de los casos la arritmia termina de manera espontánea pese a ser sincopal.
Por otro lado, Abello et al15 demuestran que el desarrollo de síncope en el seguimiento tras el implante de un desfibrilador por una taquicardia ventricular sincopal puede llegar a ser del 46%, frente a apenas un 2% cuando la indicación es una taquicardia ventricular no sincopal. Estos resultados pueden tener implicaciones relevantes en la práctica habitual de restricción de la conducción de vehículos durante al menos 6 meses a los portadores de un desfibrilador para prevención secundaria de una taquicardia ventricular, en especial si se tiene en cuenta que en este estudio el tiempo mediano tras el implante hasta la primera recurrencia de taquicardia ventricular sincopal fue superior a un año y con frecuencia tras haber presentado el paciente una recurrencia no sincopal previa.
Finalmente, en el Congreso de la Sociedad Americana de Electrofisiología (Heart Rhythm 2006) se ha presentado los resultados del SMASH VT Study16. En este estudio, 126 pacientes con infarto previo e indicación de desfibrilador por prevención secundaria fueron aleatorizados a efectuar o no una ablación profiláctica del sustrato de taquicardia ventricular previamente al implante del desfibrilador. En un seguimiento de 2 años, el porcentaje de pacientes que recibieron terapias adecuadas del dispositivo se redujo a la mitad en el grupo de ablación, y también fue importante y significativa la reducción del número de choques.
Fibrilación auricular
Las publicaciones sobre técnicas, resultados y complicaciones de la ablación siguen acaparando buena parte de la literatura de investigación clínica en el campo de la FA. Pappone et al17 han publicado los primeros resultados en ablación de FA con una técnica de navegación magnética que permite efectuar el mapeo y la ablación de forma remota a través de un sistema robótico controlado a distancia. El procedimiento fue eficaz y sin complicaciones en 38 de 40 pacientes, y parece tener una curva de aprendizaje más rápida que la de otras técnicas de ablación. Frente a la utilización de un procedimiento estándar para todos los pacientes, Oral et al18 presentan un esquema escalonado de ablación en 153 pacientes consecutivos con FA paroxística. La técnica se basa en cartografiar la aurícula izquierda durante FA espontánea o inducida y eliminar o aislar primeramente los focos de alta frecuencia en las venas pulmonares. Si la FA sigue siendo inducible, se eliminan a continuación las áreas con electrogramas fragmentados en la aurícula izquierda, el seno coronario y/o la vena cava superior. El proceso termina cuando no hay ectopia espontánea y la FA deja de ser inducible, basalmente o con infusión de isoproterenol. Con esta técnica, los autores consiguen un ritmo sinusal estable al año de seguimiento en ausencia de antiarrítmicos en el 77% de los pacientes, con un bajo índice de complicaciones. Como ventajas de esta aproximación, indican que se evite aplicar radiofrecuencia en áreas innecesarias y que se eliminen focos extrapulmonares que pueden ocasionar recurrencias. En este sentido, pueden ser interesantes los datos publicados por Isa-Param et al19 en Revista Española de Cardiología, que muestran una alta tasa de inducibilidad en pacientes con FA paroxística o persistente con la administración de isoproterenol y/o adenosina. Estos estudios se suman a la ya abundante literatura científica sobre ablación de la FA paroxística, procedimiento que va alcanzando su madurez como demuestra su inclusión en las guías de práctica clínica publicadas en 2006 por las sociedades Europea y Americana de Cardiología como alternativa a la terapia farmacológica para prevenir la FA recurrente en pacientes sintomáticos con aurícula izquierda normal o poco dilatada (figs. 1 y 2)20. Sin embargo, sólo recientemente empezamos a tener datos sobre la ablación de la FA crónica. En este sentido, un estudio prospectivo y aleatorizado de los grupos de Michigan y Milán21 muestra que la ablación circunferencial de las venas pulmonares en pacientes con FA crónica es superior al tratamiento médico con amiodarona para mantener el ritmo sinusal al año de seguimiento. La presencia de ritmo sinusal se asoció, además, a una reducción en el tamaño de la aurícula izquierda, una mejoría de la fracción de eyección ventricular izquierda y una mejor calidad de vida de los pacientes. Hay que destacar, sin embargo, que un tercio de los pacientes en el grupo de ablación recibió un segundo procedimiento por recurrencia de la arritmia o por aparición de un aleteo auricular izquierdo tras el procedimiento inicial. El grupo de Burdeos ha publicado en 2006 un estudio sobre el mecanismo de algunas recurrencias de FA tras un procedimiento inicial de ablación22. Un 17% de los pacientes con recurrencias de la arritmia presentaba un patrón «organizado» durante el estudio electrofisiológico, con electrogramas discretos aunque de cadencia irregular. Los autores demuestran que, en estos casos, la activación auricular se mantiene por focos o circuitos localizados espacialmente, que se pueden cartografiar y eliminar con radiofrecuencia. En algunos casos incluso se pudo registrar con el catéter de ablación una actividad eléctrica compleja y continua durante casi todo el ciclo de la arritmia, con paso a ritmo sinusal al aplicar radiofrecuencia en esa área. Esto indica la presencia de una reentrada local o un rotor como causa del mantenimiento de la FA en estos pacientes. El estudio es interesante porque señala que, en algunos casos de recurrencia, la ablación de una zona concreta y reducida puede ser eficaz para eliminar definitivamente la FA. En este sentido, los datos experimentales de las arritmias fibrilatorias continúan mostrando que estas arritmias no representan una desorganización completa, encontrándose áreas localizadas estables de frecuencia dominante rápida23.
Fig. 1. Desconexión eléctrica de las venas pulmonares guiada mediante el sistema de navegación no fluoroscópica Ensite-NavX en un paciente con fibrilación auricular. Se muestran en dos proyecciones, oblicua anterior derecha (izquierda) y oblicua anterior izquierda (derecha), la reconstrucción anatómica de la aurícula izquierda (gris) y de las venas pulmonares derechas (verdes) e izquierdas (azules) y la disposición y relación de un catéter multipolar circular y con polos proximales en su cuerpo (amarillo) en el interior de la vena pulmonar inferior izquierda, del catéter de ablación (blanco) en la aurícula izquierda y de un catéter bipolar de referencia situado en la aurícula derecha (rojo). Los círculos rojos representan posiciones previas del catéter de ablación donde se aplicó radiofrecuencia en torno a los ostia de las 4 venas pulmonares.
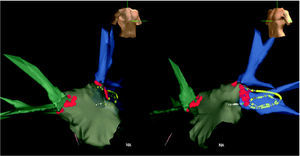
Fig. 2. Desconexión eléctrica de las venas pulmonares guiada mediante el sistema de navegación no fluoroscópica Ensite-NavX en el mismo paciente con fibrilación auricular de la figura anterior. Se muestran ahora dos proyecciones, lateral izquierda (izquierda) y oblicua anterior derecha forzada (derecha), en las que se ha retirado la pared más cercana auricular, dejando ver una visión endocárdica («endoscópica») del ostia de las venas pulmonares derechas (izquierda) e izquierdas (derecha). La representación de los catéteres y las lesiones de radiofrecuencia es la misma que la representada en la figura 1.
La terapia antitrombótica continúa siendo un aspecto esencial en el tratamiento de los pacientes con FA. La búsqueda de alternativas a la anticoagulación oral con dicumarínicos para pacientes con alto riesgo embólico no ha dado, por el momento, resultados clínicos. En este sentido, en junio de 2006 se publicaron los resultados preliminares que han llevado a la suspensión del estudio ACTIVE A, que comparaba la anticoagulación oral convencional con la doble antiagregación (ácido acetilsalicílico [AAS] + clopidogrel) en pacientes con FA y algún factor de riesgo para embolias24. Los eventos embólicos fueron claramente superiores en el grupo de antiagregación (riesgo anual del 5,60 frente al 3,93% de los pacientes anticoagulados), lo que ha motivado la terminación prematura del estudio. También se han presentado datos interesantes sobre la anticoagulación después de un procedimiento de ablación de FA. Oral et al25 publican su experiencia en complicaciones embólicas en 755 pacientes consecutivos con FA paroxística o crónica a los que se practicó una ablación circunferencial de las venas pulmonares o el procedimiento escalonado descrito previamente18. Por protocolo, los pacientes recibieron anticoagulación oral los 3 primeros meses posprocedimiento, dejando luego a criterio del médico su interrupción. De hecho, la anticoagulación fue suspendida en el 79% de los pacientes que no tenían ningún factor de riesgo embólico y en el 68% de los que tenían algún factor. Se registraron 7 eventos embólicos en los primeros días posprocedimiento y otros 2 tardíos (0,3%) durante un seguimiento de 2 años. Los autores concluyen que la retirada del tratamiento anticoagulante después de una ablación efectiva parece segura en los pacientes sin factores de riesgo embólico y en la mayoría de los que tienen factores de riesgo, aunque el carácter retrospectivo del estudio no permite extraer conclusiones en el subgrupo de pacientes > 65 años o con antecedentes de ictus.
Síncope
La búsqueda de terapias efectivas para los pacientes con síncope vasovagal recurrente sigue despertando interés en la literatura científica. Van Dijk et al26 presentan los resultados del estudio PC-Trial, diseñado para evaluar la efectividad de las maniobras de contracción muscular isométrica en la prevención del síncope neuromediado. Para ello, 223 pacientes con síncope vasovagal recurrente precedido de pródromos fueron aleatorizados para recibir terapia convencional o entrenamiento en maniobras de contracción muscular para abortar el síncope cuando presentaban los
síntomas premonitorios. El grupo que recibió entrenamiento presentó menos recurrencias sincopales (reducción relativa del riesgo del 36%), y este efecto fue independiente de otras variables clínicas en el análisis multivariable. Los autores concluyen que el entrenamiento del paciente en estas maniobras es un método eficaz y barato para el tratamiento del síncope vasovagal con síntomas prodrómicos. Por su parte, Sheldon et al27 presentan un estudio aleatorizado y controlado sobre el tratamiento con metoprolol en 208 pacientes con síncope vasovagal recurrente y prueba de basculación positiva. El tratamiento con metoprolol no tuvo un beneficio significativo sobre la recurrencia sincopal en la población global. El subgrupo de pacientes con prueba basculante positiva durante la infusión de isoproterenol tampoco mostró beneficio significativo. El resultado añade un fármaco más a la larga lista de terapias que han sido propuestas para el tratamiento del síncope vasovagal basándose en estudios observacionales, pero que se muestran ineficaces en estudios controlados y aleatorizados.
ESTRATIFICACION DE RIESGO EN PREVENCION PRIMARIA DE MUERTE SUBITA
Dentro de los procedimientos no invasivos de estratificación de riesgo en prevención primaria, la microalternancia de la onda T (MA-T) es el que está ofreciendo resultados más interesantes. Recientemente se ha comprobado en registros de Holter que la inestabilidad de la repolarización aumenta en los minutos previos al desarrollo espontáneo de una arritmia ventricular sostenida28. A más largo plazo, el valor predictivo para ausencia de eventos arrítmicos de un resultado negativo parece bastante elevado, lo que permitiría seleccionar a subgrupos de bajo riesgo en la población potencialmente candidata a recibir un desfibrilador, evitando de esta forma implantes innecesarios. Chow et al29 publican un estudio sobre 768 pacientes con cardiopatía isquémica y fracción de eyección del ventrículo izquierdo ≤ 35% a los que se determinó la MA-T, que fue clasificada en negativa o no negativa. En el análisis multivariable, la presencia de alternancia no negativa fue un predictor independiente de mortalidad total y arrítmica, con un aumento del riesgo relativo a más del doble. Además, la mortalidad arrítmica fue similar en los pacientes con microalternancia negativa y en el grupo portador de desfibrilador implantable, lo que indica que el dispositivo no ofrece un beneficio en esta población. Los resultados fueron similares en el subgrupo de pacientes con fracción de eyección del ventrículo izquierdo ≤ 30%. En otro estudio prospectivo y multicéntrico se incluyó a 549 pacientes con fracción de eyección deprimida (≤40%), la mitad de ellos de etiología isquémica. El 34% de los pacientes presentaba una prueba de alternancia normal, con una supervivencia del 97,5% a los 2 años para este subgrupo. Los resultados fueron similares para la etiología isquémica o no isquémica de la disfunción ventricular y permiten concluir a los autores que una prueba de alternancia negativa permite seleccionar a un grupo de pacientes de buen pronóstico que probablemente no obtengan beneficio adicional con el implante de un desfibrilador. Estos resultados y otros obtenidos en estudios más reducidos han motivado la inclusión de esta técnica como recomendación de clase IIa para la estratificación de riesgo de pacientes susceptibles de presentar muerte súbita en las guías de práctica clínica para el tratamiento de las arritmias ventriculares de las sociedades Americana y Europea de Cardiología, recientemente publicadas30.
GUIAS DE PRACTICA CLINICA
En la segunda mitad de 2006 se publicaron las guías más recientes de práctica clínica en las arritmias ventriculares y la muerte súbita y en la FA, recomendadas por las sociedades Europea y Americanas de Cardiología20,30. Son dos documentos extensos que abordan y actualizan todos los aspectos de diagnóstico y tratamiento en relación con los dos tipos de arritmia. Se pueden encontrar en la página web de la Revista Española de Cardiología a través de los enlaces situados en «Guías de Práctica Clínica». Entre las recomendaciones más relevantes podemos citar que actualmente se considera que hay una indicación de clase I para el implante de un desfibrilador automático en los pacientes con disfunción ventricular izquierda isquémica crónica (fracción de eyección ≤ 30-40%) o no isquémica (fracción de eyección ≤ 30-35%) asociada con insuficiencia cardiaca (grado funcional de la New York Heart Association [NYHA] II o III) a pesar del tratamiento médico optimizado y que presentan una expectativa de vida superior a un año. Esta recomendación pasa a ser de tipo IIa y IIb, respectivamente, cuando la disfunción ventricular izquierda (fracción de eyección ≤30-35%) isquémica crónica y no isquémica se asocian con un grado funcional I de la NYHA con un tratamiento médico optimizado. En cuanto a las guías de la FA, merece la pena reseñar la nueva orientación que se da a las recomendaciones para la profilaxis tromboembólica, que divide los factores de riesgo en 3 grupos (tabla 1) y considera opcional la anticoagulación oral para los pacientes que no presentan factores de alto riesgo o con hasta uno de ellos moderado.
Correspondencia:
Dr. A. García Alberola.
Unidad de Arritmias y Electrofisiología Cardiaca.
Hospital Virgen de la Arrixaca.
Ctra. Madrid-Cartagena. 30120 El Palmar. Murcia. España.
Correo electrónico: arcadi@secardiologia.es