Palabras clave
CARDIOPATÍA ISQUÉMICA
Este último año ha sido particularmente fructífero en lo que se refiere a la enfermedad coronaria del anciano, destacándose la publicación de los excelentes documentos de consenso sobre el síndrome coronario agudo (SCA) del anciano publicados por la American Heart Association (AHA)1,2 y de varios artículos que, finalmente, aportan datos sobre el tratamiento con dosis altas de estatinas en pacientes de edad avanzada3-5.
Síndrome coronario agudo
Como la consideración de un paciente como anciano es una cuestión subjetiva, la AHA ha recomendado categorizar la edad en 4 grupos: < 65, 65-74, 75-84 y ≥ 85 años1. En los estudios en los que el número de pacientes no haga recomendable la elaboración de subgrupos, la recomendación sería poner un único punto de corte en 75 años, una posible cifra para considerar a un paciente como anciano. Pese a todas las limitaciones conocidas, como la diferencia entre edad biológica-cronológica y la importancia de la presencia de comorbilidad, es importante que usemos los mismos valores para poder comparar los resultados de los distintos estudios.
El 83% de las muertes por enfermedad coronaria se producen en personas con 65 o más años y el 30%, en personas con más de 85 años6. La mortalidad intrahospitalaria de los pacientes con SCA (con y sin elevación del segmento ST) es unas 10 veces superior en individuos ≥ 85 años que en los ≤ 65 años. Pese a ello, son pocos los ensayos clínicos recientes en los que se ha descrito el efecto de los tratamientos en pacientes de edad avanzada. En la mayoría se sigue excluyendo a los pacientes ≥ 75 años, bien de forma explicita (lo más frecuente), bien mediante la inclusión de criterios de selección tan restrictivos que, en la práctica, imposibilitan la inclusión de la gran mayoría de ancianos. De hecho, los pacientes incluidos en los ensayos de SCA son más jóvenes, son con más frecuencia varones y tienen menos insuficiencia renal y cardiaca que los no incluidos. Incluso los ancianos que forman parte de los ensayos están muy seleccionados y presentan menos comorbilidad, menos factores de riesgo y una mejor situación hemodinámica y función renal que los no incluidos1.
La edad es un importante factor pronóstico en el SCA y las complicaciones tras éste (reinfarto, sangrado e insuficiencia cardiaca) también son más frecuentes en ancianos. Sin embargo, en los estudios se ha demostrado de forma repetida la infrautilización de fármacos cardiovasculares y tratamiento invasivo en los ancianos. Las razones de esta paradoja estriban en la escasez de datos procedentes de ensayos clínicos realizados en pacientes de edad avanzada y en la incertidumbre respecto a la relación riesgo-beneficio de algunos tratamientos en pacientes ancianos con comorbilidad. Aunque son los pacientes de más riesgo y, en concreto los ancianos, los que más se benefician de una estrategia invasiva y agresiva, la elevada incidencia de sangrado mayor (del 17% en pacientes ≥ 75 años) y la frecuente aparición de insuficiencia renal tras la coronariografía inclinan con demasiada frecuencia la balanza hacia una estrategia más conservadora en los ancianos2,7.
El tipo de SCA y sus síntomas varían en función de la edad. En pacientes ≥ 75 años, el infarto de miocardio con elevación del segmento ST constituye menos del 30% de los SCA. El registro americano de infarto de miocardio (National Registry of Myocardial Infarction [NRMI]) ha mostrado que la mayoría (60%) de los pacientes ≥ 85 años no presenta dolor torácico cuando experimentan un infarto de miocardio, mientras que esto es excepcional en los pacientes < 65 años (23%)8. Incluso en pacientes con infarto de miocardio con elevación del segmento ST (IAMCEST), la frecuencia de dolor torácico en > 85 años no llega al 57%. Estos datos confirman que la disnea (el 49% en el registro GRACE) puede ser igual de frecuente que el dolor torácico en los ancianos con infarto. Además de esta presentación atípica, las dificultades de comunicación que con frecuencia presentan los ancianos (por deterioro cognitivo, hipoacusia o menor agudeza visual) dificultan el diagnóstico de SCA, lo que obliga a mantener un alto grado de sospecha1.
Dada la gran escasez de datos en pacientes muy ancianos, es particularmente relevante la reciente publicación de un estudio del registro CRUSADE (Can Rapid risk stratification of Unstable angina patients Supress ADverse outcomes with Early implementation of the American College of Cardiology/American Heart Association Guidelines)9, en el que se compara a 5.557 pacientes con SCA sin elevación del segmento ST y edad ≥ 90 años con 46.270 pacientes con 75-89 años. En este estudio se ha confirmado que, tal y como sucede en pacientes más jóvenes10, el cumplimiento de las guías de práctica clínica (desarrolladas a partir de información obtenida en pacientes de menos edad) se asocia con una menor mortalidad en pacientes nonagenarios y centenarios. Sin embargo, el estudio pone de manifiesto que los pacientes muy ancianos eran ingresados en servicios de cardiología con menos frecuencia (el 33 frente al 48%) y recibían menos los tratamientos recomendados por las guías (fig. 1). Para muchos de los tratamientos recomendados, incluida la coronariografía precoz, la contraindicación citada con más frecuencia era la edad. Esto es paradójico, ya que los datos de publicación más recientes parecen indicar que los pacientes más ancianos son los que más se benefician de tratamientos agresivos, como pueden ser los inhibidores de la glucoproteína IIb/IIIa11, pese al aumento de sangrado que se produce con la edad. En el caso de los ancianos, es importante recordar la necesidad de ajustar la dosis de los inhibidores de la glucoproteína IIb/IIIa a la función renal estimada mediante el aclaramiento de creatinina, ya que estos fármacos se sobredosifican con frecuencia en los ancianos.
Fig. 1. Tratamiento intrahospitalario en pacientes sin contraindicaciones en el registro CRUSADE (Can Rapid risk stratification of Unstable angina patients Supress ADverse outcomes with Early implementation of the American College of Cardiology/American Heart Association Guidelines). Tratamiento médico e intervencionismo coronario percutáneo (angioplastia) en las primeras 24 h. Coronariografía en las primeras 48 h. Cirugía de revascularización coronaria (cirugía) y cualquier revacularización durante todo el ingreso. Tomada de Skolnick et al9.
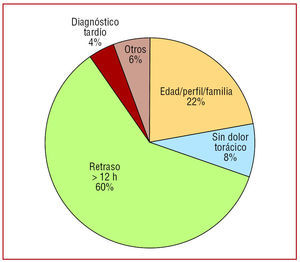
Hay un claro beneficio de las terapias de reperfusión en ancianos de hasta 85 años con infarto agudo de miocardio con elevación del segmento ST2. Los ancianos tienen con más frecuencia contraindicaciones absolutas o relativas para la reperfusión; sin embargo, aun cuando no las tienen, reciben tratamiento de reperfusión con menos frecuencia por diversas causas, la principal de las cuales es el retraso desde el inicio de los síntomas, que aumenta con la edad (fig. 2)12,13. El registro TRIANA (TRatamiento del Infarto Agudo de miocardio eN Ancianos), realizado en 410 pacientes ≥ 75 años atendidos en hospitales con programa de angioplastia primaria, mostró que el 42% no recibió tratamiento de reperfusión, el 35% fue tratado con trombolisis y sólo el 22% lo fue con angioplastia primaria14.
Fig. 2. Causas de tratamiento conservador en el estudio MIMORE89 (Myocardial Infarction Management: Observation and Registry in Elderly Patients Aged ≥ 89 Years). Tomada de Martínez-Selles et al12,13.
Ya hemos mencionado que la mortalidad es unas 10 veces superior en pacientes ≥ 85 años que en los ≤ 65 años. Aunque el riego de ictus también se incrementa con la edad, lo hace de una forma más gradual, sin llegar a contribuir de forma importante a la mortalidad. En el registro PPRIMM75 (Pronóstico del PRimer Infarto de Miocardio en Mayores de 75 Años)15, la mortalidad intrahospitalaria fue del 30%, con una tasa de ictus del 3%. La rotura cardiaca sí fue frecuente y osciló entre el 17% en los pacientes que recibieron fibrinolisis, el 8% en los tratados de forma conservadora y el 5% en los que recibieron angioplastia primaria. Sin embargo, la causa más frecuente de muerte en el anciano con IAMCEST es la insuficiencia cardiaca/shock cardiogénico por fallo de bomba, que se incrementa de forma exponencial con la edad (fig. 3).
Fig. 3. Porcentaje de muertes por insuficiencia cardiaca/shock cardiogénico sobre el total de muertes en pacientes con infarto agudo de miocardio con elevación del segmento ST en función de la edad media de los estudios. Datos del estudio de Pontremoli, de Leone et al16, PPRIMM75 (Pronóstico del PRimer Infarto de Miocardio en Mayores de 75 Años), de Bueno et al15 y MIMORE89 (Myocardial Infarction Management: Observation and Registry in Elderly Patients Aged ≥ 89 Years), de Martínez-Selles et al12,13.
Respecto a la mejor terapia de reperfusión en el anciano, los datos del Senior PAMI, estudio con 481 pacientes ≥ 70 años, fueron presentados en 2005 en el Transcatheter Cardiovascular Therapeutics, pero todavía no se han publicado. En este estudio no se mostraron diferencias relevantes entre ambas estrategias de reperfusión, con una tendencia a que los pacientes de 70-80 años tratados con angioplastia primaria tuvieran menos eventos y una evolución prácticamente idéntica en los mayores de 80 años tratados con angioplastia primaria o fibrinolisis. Los resultados del ensayo clínico TRIANA, actualmente en marcha, posiblemente arrojen más luz sobre la terapia de reperfusión óptima para el anciano.
En el año 2007, nuevos estudios han alertado acerca del riesgo más elevado que presentan los ancianos en los que se realiza cirugía de revascularización coronaria, particularmente en el caso de las mujeres y los ancianos con enfermedad vascular periférica, insuficiencia renal o puntuaciones altas en el EuroSCORE17-19. En un novedoso estudio se han relacionado también estas dos últimas variables con el desarrollo de fibrilación auricular tras la cirugía de revascularización coronaria en pacientes ≥ 65 años20.
Estatinas
En los clásicos estudios de prevención secundaria, como Cholesterol and Recurrent Events (CARE), Scandinavian Simvastatin Survival Study (4S), y Long-term Intervention with Pravastatin in Ischemic Disease (LIPID), se excluyó de forma sistemática a los pacientes de edad avanzada, con un límite superior de edad de 69-74 años. El Heart Protection Study (HPS) subió el límite de edad a los 80 años y el Pravastatin in Elderly Individuals at Risk of Vascular Disease (PROSPER) se realizó exclusivamente en ancianos (≥ 70 años)2. Respecto a este último estudio, es importante señalar que Sattar et al21 han publicado recientemente un análisis que muestra un escaso valor de la proteína C reactiva (PCR), tanto en la predicción del riesgo como en la respuesta al tratamiento con estatinas en ancianos21. En el estudio Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering (MIRACL) se mostró que un tratamiento con atorvastatina 80 mg iniciado a las 24-96 h del ingreso reducía los eventos cardiovasculares a las 16 semanas. En un subanálisis de este estudio recientemente publicado se ha concluido que el beneficio de este tratamiento intensivo precoz es superior en los pacientes ≥ 65 años que en los < 65 años22.
En todos los trabajos previamente mencionados se mostró el efecto protector de las estatinas; pese a ello, la prescripción de estatinas tras un infarto de miocardio se reduce con la edad23 (fig. 4). Más recientemente, los estudios se han centrado en comparar un tratamiento intensivo con dosis altas de estatinas con el tratamiento hasta entonces considerado estándar. El Pravastatin or Atorvastatin Evaluation and Infection Therapy (PROVE-IT) mostró un claro beneficio del tratamiento con 80 mg diarios de atorvastatina respecto a 40 mg de pravastatina, que fue más pronunciado en los pacientes ≥ 70 años. Sin embargo, el escaso número de pacientes ancianos y la preocupación por los efectos secundarios y el coste del tratamiento intensivo en la edad avanzada habían limitado, hasta ahora, la generalización del tratamiento intensivo en los ancianos. Durante el año 2007 se han publicado 3 importantes estudios centrados en la terapia intensiva en ancianos. En el ensayo SAGE (Study Assessing Goals in the Elderly)4 se siguió durante 12 meses a 893 pacientes con enfermedad coronaria y edades comprendidas entre los 65 y los 85 años, y se mostró un beneficio, no sólo en los eventos cardiovasculares, sino también en la mortalidad total, para los pacientes tratados con 80 mg diarios de atorvastatina respecto a los que recibieron 40 mg de pravastatina. Este año se ha publicado también un subanálisis del TNT (Treating to New Targets), realizado en 3.809 pacientes ≥ 65 años con enfermedad coronaria3. En este estudio se comparó el tratamiento con 10 mg diarios de atorvastatina con 80 mg diarios, y se mostró una reducción de eventos cardiovasculares en los pacientes que recibieron la dosis superior. Aunque los resultados de estos estudios parecen aconsejar de forma clara la generalización de la terapia intensiva en ancianos con cardiopatía isquémica, en un tercer estudio publicado también este año se han mostrado datos discordantes. Choudhry et al5 analizaron una cohorte retrospectiva no aleatorizada de 18.311 pacientes ≥ 65 años dados de alta tras un SCA y no consiguieron mostrar un beneficio del tratamiento intensivo respecto al uso de estatinas en dosis más bajas.
Fig. 4. Porcentaje de prescripción de estatinas tras un infarto agudo de miocardio en función de la edad, según el estudio de Berger et al23.
Podemos resumir que hay una gran escasez de datos acerca de la cardiopatía isquémica del anciano que sólo se solucionará mediante la eliminación de criterios de exclusión por la edad o criterios que dificulten de forma desproporcionada la inclusión de pacientes mayores con comorbilidad. Debemos categorizar la edad en 4 grupos: < 65, 65-74, 75-84 y ≥ 85 años o, alternativamente, < 75 y ≥ 75 años. Es recomendable realizar un tratamiento agresivo de la enfermedad coronaria en el anciano, aunque hay que individualizar cada caso.
ARRITMIAS
Los 2 temas de mayor actualidad en la arritmología del paciente anciano son la fibrilación auricular (FA) y el uso de desfibriladores automáticos implantables (DAI) para la prevención de la muerte súbita.
Fibrilación auricular
La prevalencia de FA en la población general es del 0,4-1%24, alcanza el 5% en sujetos ≥ 65 años y afecta a cerca del 10% en las personas > 80 años25. En España se han publicado recientemente, en Revista Española de Cardiología, los datos del estudio PREV-ICTUS, que son concordantes con lo ya mencionado; sobre 7.108 sujetos ≥ 60 años, la prevalencia de FA fue del 8,5%, y aumentó del 4,2% en sujetos de 60-64 años al 16,5% en los ≥ 80 años26. Se estima que en el año 2050 habrá 5,6 millones de personas con FA en Estados Unidos, y que el 50% de ellas tendrá más de 80 años24. La terapia de la FA se centra en la elección del tratamiento antitrombótico y en la decisión sobre el control de la respuesta ventricular o el mantenimiento del ritmo sinusal; ambos aspectos están poco definidos en los pacientes ancianos.
Tratamiento antitrombótico
Los pacientes con FA sin valvulopatía mitral tienen un riesgo de ictus isquémico que es 5 veces mayor que el de sujetos sin FA; este riesgo de ictus aumenta con la edad, de manera que el riesgo anual de ictus atribuido a la FA es del 1,5% en pacientes de 50-59 años, y hasta del 24% en los de 80-89 años24. El tratamiento con anticoagulantes orales (ACO) ha demostrado disminuir el riesgo de ictus en sujetos con FA27, pero los pacientes ancianos están escasamente representados en dichos estudios. Esto es importante, ya que el riesgo de ictus isquémico aumenta con la edad, pero también lo hace el riesgo de hemorragias. Las últimas guías de práctica clínica sobre FA de las sociedades Europea y Americana de Cardiología28 consideran la edad ≥ 75 años como factor de riesgo moderado de tromboembolia, y en presencia de al menos dos factores de riesgo moderado recomiendan iniciar tratamiento con ACO. Aclaran que los sujetos ≥ 75 años con riesgo de hemorragias (sin contraindicación para ACO) pueden ser tratados para mantener un INR de 1,6-2,5.
Se han evaluado diversas estrategias antitrombóticas como alternativa a los ACO. En un estudio reciente en el que se incluyó a 75 pacientes de 80-89 años con FA no se demostró un beneficio en cuanto a la reducción de eventos en los pacientes tratados con warfarina, en comparación con el tratamiento con aspirina, aunque el estudio no tenía potencia suficiente para detectar dichas diferencias29. Sin embargo, el tratamiento con aspirina produjo significativamente más efectos adversos (sobre todo gastrointestinales). En el estudio español NASPEAF se demostró que, en pacientes con FA, el tratamiento con el antiagregante triflusal combinado con una anticoagulación moderada (con INR 1,4-2,4) reducía significativamente el número de eventos en comparación con la anticoagulación habitual30. Este año se ha publicado un subanálisis de dicho estudio sobre los pacientes ≥ 75 años31. En comparación con los pacientes más jóvenes, los ancianos tuvieron mayores tasas de eventos (accidente isquémico transitorio o ictus isquémico o hemorrágico fatal y no fatal, embolismos sistémicos, infarto de miocardio, muerte súbita o muerte por hemorragia) y mayores tasas de sangrados graves durante el tratamiento anticoagulante. Pero, sobre todo, cabe destacar que, en los pacientes ancianos, el tratamiento combinado también redujo la tasa de eventos en comparación con el tratamiento anticoagulante, y produjo menor sangrado intracraneal y menor mortalidad por hemorragias, aunque ocasionó más hemorragias gástricas no fatales. Están pendientes de publicación los resultados del estudio BAFTA, en el que se aleatorizó a más de 1.000 pacientes ≥ 75 años con FA para recibir tratamiento con aspirina o warfarina32.
Complicaciones hemorrágicas
Como ya hemos mencionado, el riesgo de sangrado en pacientes tratados con ACO se incrementa con la edad, pero los datos han sido contradictorios y con escasos pacientes ancianos, sobre todo > 80 años. En 2 estudios observacionales con un gran número de pacientes ancianos se ha objetivado que la interacción entre edad y sangrado es incluso mayor de lo que se creía. En el estudio ATRIA se incluyó a 13.559 sujetos con FA (3.818 de ellos ≥ 80 años) y se separaron 4 grupos etarios (< 60, 60-69, 70-79 y ≥ 80 años). Las tasas de sangrado mayor aumentaron con la edad, tanto en los que tomaban ACO (incremento del riesgo en cada grupo etario de 1,2; intervalo de confianza [IC] del 95%, 1,0-1,4) como en los que no los tomaban (incremento del riesgo en cada grupo etario de 1,5; IC del 95%, 1,3-1,8)33. Más espectaculares son los resultados de un registro americano en el que se incluyó a 472 pacientes (el 32% ≥ 80 años)34. La incidencia acumulada de hemorragias mayores fue 13,1 por 100 pacientes-año en los pacientes ≥ 80 años y 4,7 por 100 pacientes-año en los < 80 años (p = 0,009). El riesgo de sangrado se relacionó con tener una edad ≥ 80 años, un INR ≥ 4 y con los primeros 90 días del inicio del tratamiento con ACO.
Para optimizar la indicación de ACO en pacientes con FA se han ideado modelos de riesgo de sangrado. Recientemente se ha diseñado un modelo que engloba los publicados con anterioridad, que ha sido denominado HEMORR2HAGES (enfermedad hepática o renal, abuso de etanol, malignidad, edad ≥ 75 años, disminución del número de plaquetas, riesgo de resangrado, hipertensión no controlada, anemia, factores genéticos, riesgo de caídas e ictus previo) y validado en una población de 3.791 sujetos35. En una población todavía mayor (26.345 sujetos con FA > 65 años dados de alta en tratamiento con ACO) se han establecido como variables que incrementan el riesgo de sangrado la diabetes, la anemia, la edad ≥ 70 años, el sangrado remoto, el sangrado reciente, el abuso de alcohol, el sexo femenino y el uso de antiagregantes36. Estos modelos son útiles, pero no resuelven el problema, ya que algunos de los factores que incrementan el riesgo de sangrado (como la edad o tener un ictus previo) también aumentan el riesgo embólico.
Control del ritmo o la respuesta ventricular
En los ensayos clínicos no se ha demostrado superioridad de la estrategia de mantenimiento del ritmo sinusal (control del ritmo) con fármacos antiarrítmicos frente a un control de la respuesta ventricular37,38. La estrategia de control del ritmo no reduce el riesgo embólico, por lo que no debe suprimirse el tratamiento antitrombótico. Por tanto, según los síntomas, el control de la frecuencia cardiaca puede ser una estrategia inicial válida en pacientes ancianos para controlar los síntomas y prevenir la taquimiocardiopatía. Sin embargo, en el estudio SAFE-T se ha observado que la estrategia basada en el control del ritmo frente al control de la frecuencia mejora la calidad de vida y la capacidad de realizar esfuerzo (la edad media era de 67 años)39. Si se opta por la estrategia del control del ritmo, puede ser útil la información de un estudio publicado en Revista Española de Cardiología, en el cual se realizó cardioversión eléctrica (previo tratamiento con amiodarona) en 295 sujetos con FA persistente (edad media de 69 años)40. Se consiguió restaurar el ritmo sinusal en el 92,5% de ellos; pero, al año, sólo un 45% de los sujetos se mantuvo en ritmo sinusal. Las variables que se relacionaron con la recurrencia de FA fueron la duración de la FA superior a un año, la dilatación del ventrículo izquierdo y las cardioversiones previas. Sin embargo, la edad no se relacionó con un menor mantenimiento del ritmo sinusal.
Por último, para aquellos casos en los que el tratamiento médico es ineficaz y la FA es mal tolerada, se dispone de medidas de tratamiento invasivo. Por un lado, la ablación del nódulo auriculoventricular con implantación de marcapasos es una alternativa válida que permite controlar la respuesta ventricular, pero que precisa el mantenimiento del tratamiento antitrombótico y no ha demostrado reducir la mortalidad41. Sobre esta alternativa no hay publicaciones recientes. Por otro lado, hoy día disponemos de diversas técnicas de ablación de la FA centradas principalmente en aislar las venas pulmonares. Sobre este aspecto hay muchas novedades, pero por el momento no se ha evaluado en pacientes > 75 años.
Fibrilación auricular perioperatoria
La FA es la complicación arrítmica más frecuente de la cirugía cardiaca y ocurre en un 20-40% de las cirugías de revascularización coronaria42. En un estudio realizado en Turquía en 426 pacientes > 65 años en los que se llevó a cabo revascularización quirúrgica, la incidencia de FA postoperatoria fue del 21,4% y, entre otros, la edad fue un factor de riesgo de desarrollar FA en el postoperatorio20. Estos datos coinciden con los de un registro americano de 19.083 pacientes intervenidos para revascularización quirúrgica, con una incidencia de FA postoperatoria del 21,5%, en el que la edad también fue un factor independiente de riesgo de FA43.
Muerte súbita y desfibirilador automático implantable
La muerte súbita origina más de 300.000 muertes anuales en Estados Unidos44; los datos en Europa son similares45. La incidencia de muerte súbita aumenta en relación con la edad (en paralelo con el incremento de la prevalencia de insuficiencia cardiaca), y puede observarse un decremento relativo a partir de los 80 años, al predominar otras causas de muerte46. En ensayos clínicos recientes se ha demostrado la eficacia de los DAI frente al tratamiento médico en la prevención primaria y secundaria de la muerte súbita. Las últimas guías de práctica clínica sobre arritmias ventriculares y muerte súbita de las sociedades Europea y Americana de Cardiología mencionan que los pacientes ancianos con arritmias ventriculares deben ser tratados de la misma manera que los individuos jóvenes47. Sin embargo, ninguno de los ensayos clínicos mencionados se centró específicamente en la eficacia de los DAI en los pacientes más ancianos. La edad de los sujetos incluidos oscilaba entre los 50 y los 70 años, mientras que en número de sujetos con 80 o más años era muy escaso, de tal forma que no está claro que el beneficio observado en la supervivencia en sujetos de mediana edad o «ancianos jóvenes» pueda extenderse a los más ancianos. En este sentido, en un registro de 2.467 pacientes «reales» (es decir, fuera de ensayos clínicos) en los que se implantó un DAI en Ontario se observó que los pacientes > 65 años tenían mayor morbilidad asociada y una mayor mortalidad en el seguimiento que los < 65 años48. Así, se refleja que es importante tener en cuenta la comorbilidad en pacientes ancianos en los que se indica un DAI. En cuanto al uso DAI para la prevención primaria de muerte súbita en ancianos, recientemente se ha publicado un subestudio del MADIT-II en el que se comparó a los sujetos < 75 años frente a los 204 pacientes (121 recibieron DAI) ≥ 75 años49. Estos últimos tenían mayor incidencia de FA, insuficiencia renal y complejo QRS ancho, y recibían con menos frecuencia tratamiento con bloqueadores beta y estatinas. En el seguimiento, la mortalidad de los pacientes ≥ 75 años fue hasta un 80% superior. Sin embargo, los pacientes de ambos grupos etarios asignados a DAI tuvieron una reducción similar de la mortalidad total; los de 75 años o más tuvieron un riesgo relativo (RR) de 0,56 (IC del 95%, 0,29-1,08; p = 0,08) en un seguimiento medio de 17,2 meses y los de menos de 75 años, un RR = 0,63 (IC del 95%, 0,45-0,88; p = 0,01) después de 20,8 meses. Los autores concluyen que, en pacientes ancianos adecuadamente seleccionados, no hay diferencias en cuanto a la efectividad del DAI en la prevención primaria. Estos datos contrastan con los de un metaanálisis recientemente publicado de los 3 principales estudios de DAI en la prevención secundaria de muerte súbita (AVID, CIDS y CASH)50. En los pacientes < 75 años, el DAI redujo significativamente la mortalidad global (RR = 0,69; IC del 95%, 0,56-0,85; p < 0,0001) y la arrítmica (RR = 0,44, IC del 95%, 0,32-0,62; p < 0,0001). En cambio, no se observó ningún beneficio en los ≥ 75 años (RR = 1,06; IC del 95%, 0,69-1,64; p = 0,79 para mortalidad global y RR = 0,90; IC del 95%, 0,42-1,95; p = 0,79 para mortalidad arrítmica). Durante el seguimiento la mortalidad fue superior en los sujetos ≥ 75 años, que tuvieron una mayor mortalidad de causa no cardiológica y por insuficiencia cardiaca y, sin embargo, una mortalidad arrítmica similar. Un 20% de los pacientes ancianos murió en el primer año, un 75% de causas no arrítmicas, lo cual podría explicar la ausencia de beneficio del DAI en estos pacientes. Los autores concluyen que la falta de indicación de un DAI no puede basarse solamente en la edad; sin embargo, debe valorarse con cuidado el riesgo de mortalidad no arrítmica de los pacientes ancianos e individualizar la indicación en cada caso. Además, refieren que las diferencias con los resultados del MADIT II, mencionadas previamente, pueden deberse a que en la prevención secundaria la urgencia es mayor y, por tanto, la selección de los pacientes es menor que en los estudios de prevención primaria.
En definitiva, los resultados de los ensayos clínicos sobre el efecto beneficioso de los DAI deben extrapolarse con precaución a los pacientes más ancianos, ya que suelen tener una mayor comorbilidad en la práctica diaria y se encuentran escasamente representados en dichos estudios. El hecho de que esté aumentando la edad de la población y que sean precisamente los ancianos los que tienen con más frecuencia insuficiencia cardiaca, y tratándose de una intervención terapéutica cara, debería plantearse la necesidad de realizar ensayos clínicos en pacientes ancianos.
HIPERTENSIÓN PULMONAR E INSUFICIENCIA CARDIACA
En este campo, los avances publicados en el último año en pacientes de edad avanzada han sido menos relevantes. La hipertensión arterial pulmonar idiopática suele afectar principalmente a mujeres jóvenes; sin embargo, se observa en la actualidad que una parte importante de los pacientes son ancianos. La sintomatología, la severidad hemodinámica y la disfunción ventricular derecha suelen ser superponibles a las de los pacientes jóvenes. En el caso de la presión capilar pulmonar (PCP), suele ser superior a la del grupo joven y, en ocasiones, no cumple los criterios establecidos para el diagnóstico de hipertensión arterial pulmonar (PCP > 15 mmHg). Cuando presentan PCP baja, el pronóstico es peor que en el grupo joven51.
En un informe epidemiológico realizado en Estados Unidos se señala que la proporción de pacientes < 65 años con hipertensión pulmonar está creciendo, sobre la base de las hospitalizaciones y las muertes. La insuficiencia cardiaca contribuye en buena parte a ello52. Además, la hipertensión pulmonar que acompaña a la insuficiencia cardiaca, sea con función sistólica deprimida o conservada, aumenta la mortalidad a corto y a largo plazo53,54. La incidencia de insuficiencia cardiaca diastólica aislada está creciendo en la población senil y conlleva mal pronóstico55. En ciertas áreas de España, la insuficiencia cardiaca por disfunción diastólica llega a ser la más frecuente56. Esta tendencia se hace más marcada en la población octogenaria57. Lamentablemente, seguimos sin disponer de tratamientos que mejoren la supervivencia de los pacientes con insuficiencia cardiaca y fracción de eyección normal, la forma de presentación más frecuente en el anciano.
Los beneficios del tratamiento con bloqueadores beta e inhibidores de la enzima de conversión de angiotensina (IECA) en la población senil con insuficiencia cardiaca sistólica se han confirman de forma clara y se relacionan con la dosis óptima alcanzada. En el caso de los bloqueadores beta, los pacientes que no los toleran tienen peor pronóstico58. También se recomiendan, en la mayoría de los pacientes, los inhibidores de la aldosterona y, en el caso de intolerancia a los IECA o en pacientes que no reciban inhibidores de la aldosterona, los antagonistas de los receptores de angiotensina II (ARA-II). En los pacientes ancianos es fundamental vigilar con frecuencia las concentraciones de potasio por la posibilidad de hiperpotasemia. En el caso de las estatinas, su eficacia está por probar en los pacientes con insuficiencia cardiaca59, pero los resultados de los ensayos clínicos que actualmente están en marcha (GISSI Heart failure y CORONA) ayudarán a despejar esta incógnita.
Otras alternativas terapéuticas, como la resincronización cardiaca, han mostrado beneficio en la edad senil, extendiéndose más allá de los 80 años, en función de la mejoría clínica, funcional y de remodelación inversa. Además muestran los mismos beneficios sobre la muerte súbita por insuficiencia cardiaca60. Estos avances en el tratamiento de la insuficiencia cardiaca han trasladado el momento del trasplante cardiaco, en particular en el caso de las mujeres, a edades más avanzadas61. La población de 61-70 años se beneficia de esta modalidad de tratamiento final de la insuficiencia cardiaca62. Muchos centros de trasplante en España aceptan ya a candidatos a trasplante hasta los 70 años, tras una selección adecuada y una cuidadosa evaluación.
VALVULOPATÍAS
Los avances más relevantes publicados este año en ancianos se centran en el tratamiento percutáneo de la estenosis aórtica severa (verdadera epidemia del anciano) y la insuficiencia mitral (también habitual en pacientes ancianos, que con frecuencia tienen comorbilidad que contraindica la cirugía). Sin embargo, la cirugía sigue siendo el tratamiento de elección de la mayoría de las enfermedades valvulares y sólo se ha validado el tratamiento percutáneo como primera elección en la estenosis pulmonar, la estenosis aórtica congénita y la estenosis mitral con anatomía favorable63.
Tratamiento percutáneo de la estenosis aórtica
La valvuloplastia aórtica (VPAo) se inició a comienzos de la década de 1980. En primer lugar fue indicada en la estenosis aórtica (EAo) congénita y, con posterioridad, Cribier et al64 la recomendaron en el tratamiento de la EAo severa sintomática degenerativa del anciano. Este tratamiento llenó un vacío terapéutico ya que, en aquellas fechas, el tratamiento quirúrgico de este tipo de pacientes no estaba muy extendido65. Por desgracia, se demostró que la realización de una VPAo no incidía en la historia natural de la EAo severa sintomática66. Además, no carecía de morbimortalidad y, finalmente, la reestenosis en un plazo de 6-12 meses era la regla. Es verdad que se producía una mejoría de los síntomas, pero de una duración también limitada64,67,68.
Desde finales del siglo pasado, muchos autores involucrados en el tratamiento no invasivo de las enfermedades valvulares comenzaron a considerar la implantación valvular percutánea como un tratamiento posible, con unas características menos agresivas que la cirugía y, probablemente, mucho más efectivo que la simple dilatación con un balón. El primer autor en hacer realidad este sueño fue Bonhoeffer69. Este investigador, tras múltiples ensayos en animales, diseñó una prótesis mediante el aislamiento de una válvula de la vena yugular, que suturó a un stent vascular. Con posterioridad, válvula y stent se montaron manualmente en un balón, que al inflarse implantaba la válvula. Esta prótesis fue implantada en un conducto valvulado disfuncionante entre el ventrículo derecho y la arteria pulmonar. Tras la colocación de la prótesis quedó cierto grado de estenosis, pero la insuficiencia pulmonar se resolvió. Cribier et al70 realizaron su primera implantación de válvula aórtica percutánea en 2002, en un paciente con EAo severa sintomática no subsidiario de tratamiento quirúrgico, justamente 17 años después de su primera valvuloplastia aórtica. Se trata de una válvula biológica tricúspide de pericardio, cosida a un stent de acero inoxidable que, a su vez, está recubierto por polietilen tereftalato (PET). Esta prótesis se monta sobre un balón que, al inflarse, coloca la prótesis en el anillo aórtico, quedando la válvula nativa aplastada por el stent y adosada a la pared. Previamente a la implantación de la prótesis se debe realizar una valvuloplastia con balón, para fracturar los depósitos de calcio valvular, de manera que la prótesis pueda atravesar la válvula y ajustarse con más facilidad a la pared. El stent que sustenta la prótesis queda adosado a la pared aórtica, pero en medio de ambos continúa estando la válvula nativa. Los diseños actuales de la válvula de Cribier, que es la más empleada, aunque no la única, son demasiado voluminosos. En la actualidad, hay al menos 13 diseños prótesis percutáneas aórticas. Las más empleadas son la Cribier-Edward y la Cor-Valve71. El gran perfil de la válvula de Cribier llevó a que, en un principio, la vía de acceso empleada fuera la anterógrada, que precisa una punción transeptal y es técnicamente muy engorrosa, por lo que en la práctica ya ha sido abandonada. La segunda vía de acceso es la retrógrada, que es la más sencilla técnicamente72,73. Dado lo voluminoso de la prótesis, es necesaria la disección quirúrgica de la arteria femoral, para permitir colocar un introductor de 8 mm de diámetro. Por último, el acceso transapical se ha empezado a utilizar en 200574,75. Este trabajo debe ser realizado por un equipo integrado por el cirujano cardiaco, el hemodinamista, el anestesista y el ecocardiografista. Se abre el ápex del ventrículo izquierdo, para permitir el paso de la prótesis sin problemas. Para evaluar la posición correcta de la válvula, que es el punto más crucial de la técnica, se utiliza la fluoroscopia, que visualiza el calcio valvular, la angiografía y el ecocardiograma (al igual que en las otras vías de acceso). El lugar más adecuado para realizar esta técnica es el quirófano. En Alemania hay un grupo multidisciplinario que subraya la ventaja de poder cambiar rápidamente al tratamiento quirúrgico convencional si es preciso75. Walther y Mohr76, cirujanos que forman parte de dicho equipo multidisciplinario, dan una lección de modestia y modernidad. Subrayan que sólo se opera a un tercio de los pacientes ancianos portadores de EAo severa sintomática, que la EAo severa sintomática del anciano supone el 10-30% del trabajo del cirujano cardiaco, que la implantación percutánea de la válvula aórtica evita la esternotomía, la parada cardiaca y la entrada en bomba, y también el trauma posquirúrgico, y disminuye el riesgo. Concluyen que, aunque la cirugía sigue siendo el tratamiento de elección en la EAo severa sintomática, los éxitos que se están teniendo en la implantación percutánea hacen que los cirujanos necesiten tomar parte en este campo.
La información más reciente disponible acerca de las prótesis aórticas percutáneas es la presentada en el Congreso Europeo de Cardiología de septiembre de 2007. Se han implantado ya 450 válvulas de Cribier-Edward y 250 de Core-Valve. La vía de acceso anterógrada ya se ha desechado, la retrógrada continúa y la transapical va en aumento. Tras la implantación de la prótesis se alcanzan áreas valvulares de 1,7 cm2, el gradiente desaparece y la fracción de eyección aumenta. El procedimiento no produce oclusión de las coronarias. La mortalidad a los 30 días es del 8-12% y está claramente influida por la curva de aprendizaje. A los 4 años de seguimiento no se observa migración ni disfunción valvulares. En un estudio de la experiencia mundial de la válvula de Cribier- Edward (Europa, Canadá y Estados Unidos), se analizó a 432 pacientes. La vía anterógrada se utilizó en el 14%, la retrógrada en el 50% y la transapical en el 37%. Teniendo en cuenta que esta última comenzó a emplearse en 2005, parece que su utilidad se está consolidando. Se consideran criterios de inclusión la EAo severa sintomática degenerativa en mayores de 70 años, con un área valvular de 0,8 cm2 o menos, una clase funcional ≥ II de la New York Heart Association (NYHA), alto riesgo quirúrgico y una medida del anillo aórtico > 16-25 mm.
Reparación percutánea de la válvula mitral
El tratamiento de las insuficiencias valvulares ha sido un reto fascinante para el cardiólogo intervencionista. Las válvulas auriculoventriculares tienen una anatomía mucho más compleja y, aunque la estenosis se ha abordado con balón de forma efectiva (sobre todo en la estenosis mitral con anatomía favorable), la insuficiencia parecía de muy difícil abordaje. Alfieri et al77 desarrollaron en 2001 una técnica quirúrgica de reparación de la insuficiencia mitral mediante la sutura de la parte media de ambas valvas y la transformación del orificio mitral en uno doble en forma de «8», y por tanto, reduciéndolo de tamaño. Esta técnica se puede llevar a cabo percutáneamente mediante 2 tipos de dispositivos: uno utiliza una grapa metálica78,79 y el otro da puntos de sutura. Algunos grupos han tratado ya a más de 70 pacientes con el método de la grapa, con buenos resultados78.
Otra técnica de reparación percutánea mitral consiste en la utilización del seno coronario como soporte para la realización de una anuloplastia79. El seno coronario corre paralelo al anillo mitral. Si se introduce en su interior un catéter capaz de ejercer una acción constrictora sobre el seno coronario, dicha fuerza puede transmitirse al anillo mitral y reducir su diámetro80,81. En la actualidad, este dispositivo tiene varias limitaciones. Por un lado, el seno coronario exhibe una anatomía muy variada y ocasionalmente se sitúa alejado del anillo mitral. Además, la arteria circunfleja discurre próxima al seno coronario y el «catéter constrictor» puede dañarla82. Claramente, esta aproximación terapéutica debe ser mejorada para que sea más efectiva y menos peligrosa.
Podríamos resumir este apartado diciendo que, por fortuna, el tratamiento percutáneo de las valvulopatías del anciano no ha quedado confinado a la mera dilatación con un balón. En la actualidad, las prótesis pulmonar y aórtica percutáneas son una realidad, aunque deban de ser mejoradas. El tratamiento percutáneo de la insuficiencia mitral está menos desarrollado, pero la técnica de Alfieri por vía percutánea parece ser efectiva.
Correspondencia: Dr. M. Martínez-Sellés.
Servicio de Cardiología. Hospital Universitario Gregorio Marañón.
Dr. Esquerdo, 46. 28007 Madrid. España.
Correo electrónico: mmselles@secardiologia.es