Palabras clave
La enfermedad coronaria es una causa importante de mortalidad entre las mujeres (la primera causa en los EE.UU.) y, además, el pronóstico después de un infarto de miocardio o de una cirugía de derivación coronaria es significativamente peor en las mujeres que en los varones. Por este motivo, ha existido un interés considerable en cualquier posibilidad terapéutica que pudiera proporcionar cardioprotección, y en este sentido se estudió la hormonoterapia.
VEROSIMILITUD BIOLÓGICA
Los mecanismos biológicos que sugieren un beneficio del tratamiento con estrógenos son convincentes pero, a veces, contradictorios. Así, por ejemplo, se sabe que los estrógenos ejercen un efecto positivo sobre la concentración de lípidos y lipoproteínas, provocando una disminución del 10-15% del colesterol de las LDL y un aumento similar del colesterol de las HDL. No obstante, la terapia oral con estrógenos tiene un efecto desfavorable en la concentración de triglicéridos. También ejercen una acción beneficiosa en la coagulación y la fibrinólisis pero, paradójicamente, producen a menudo un incremento de la trombosis en venas profundas y embolia pulmonar. Además, aunque disminuyen la concentración de homocisteína, elevan la concentración plasmática de la proteína C reactiva, importante marcador de inflamación. También se ha descrito que los estrógenos disminuyen la respuesta inflamatoria de la aterosclerosis, reducen la proliferación de células musculares lisas vasculares y favorecen la vasodilatación dependiente de endotelio. Asimismo, existen evidencias recientes que demuestran que pueden actuar como factores angiogénicos. Sin embargo, la verosimilitud biológica por sí sola únicamente genera hipótesis, pero no es una evidencia por sí misma de cardioprotección.
ESTUDIOS OBSERVACIONALES
Los datos procedentes de los estudios observacionales identificaron casi uniformemente que los estrógenos tenían un efecto cardioprotector. En un metaanálisis de estos estudios se observó una reducción del 35-50% del riesgo coronario asociado a la terapia estrogénica y, aunque existen menos estudios que analicen la respuesta de la asociación de estrógenos con progestágenos, también sugieren un efecto beneficioso1. Sin embargo, estos datos deben ser tomados con cautela y teniendo en cuenta que existen factores que pueden distorsionar la interpretación de los resultados obtenidos en los estudios observacionales2.
Entre estos factores cabe destacar, en primer lugar, el sesgo de la selección. En este sentido, conviene recordar que las mujeres fumadoras, hipertensas, diabéticas, obesas, con angina de pecho, insuficiencia cardíaca, vasculopatía periférica o aquellas que han tenido un infarto de miocardio previo o un accidente cerebrovascular, no han sido consideradas hasta el momento como candidatas para la terapia con estrógenos. Es difícil saber hasta qué punto los resultados favorables obtenidos se deben a la terapia hormonal, cuando la población de estudio está seleccionada por tener pocos factores de riesgo coronario o episodios cardiovasculares previos. Otro factor que puede influir en los resultados es el que se deriva del sesgo de cumplimiento. En varios ensayos clínicos, el análisis, tanto de varones como de mujeres del grupo placebo, demostró que los pacientes que siguieron correctamente el tratamiento con placebo presentaron una tasa de episodios coronarios un 40-60% menor que el grupo que no lo siguió de manera correcta, lo que obviamente sugiere que la adhesión al tratamiento es un marcador de otros comportamientos saludables. El tercer aspecto que hay que tener presente a la hora de interpretar los resultados de los estudios observacionales es el de la aparición de efectos adversos precoces. Así, en un estudio transversal, las mujeres que han interrumpido el tratamiento debido a la aparición de efectos adversos no son captadas como usuarias. En conjunto, y teniendo en cuenta estos factores, los datos observacionales que consideran el efecto de una terapia o de una intervención tienden a sobrevalorar el beneficio y a infravalorar el riesgo.
Un reciente metaanálisis del estudio observacional citado anteriormente, que se adaptó al nivel socioeconómico, la educación y los factores de riesgo mayores, no pudo demostrar la protección cardíaca, con un riesgo relativo del 1,07 para las usuarias de hormonas3. Esto, obviamente, refleja que las mujeres que utilizan hormonoterapia se diferencian de las no tratadas en muchos aspectos, incluyendo el estado de la salud en general, conocimiento de la salud, nivel socioeconómico, atributos del riesgo coronario, etcétera
Asimismo, una revisión científica publicada recientemente por los Servicios de Prevención de los EE.UU. examinó los datos publicados de ensayos clínicos y observacionales, y resumió los efectos de la hormonoterapia de la siguiente manera4: los beneficios incluyeron la prevención de fractura por osteoporosis y el cáncer colorrectal; no había certeza en cuanto a la prevención de la demencia; y los perjucios incluyeron un incremento en el riesgo de enfermedad coronaria, accidente cerebrovascular, tromboembolia venosa, colecistitis y cáncer de mama (con el uso de hormonas durante cinco o más años).
RESULTADOS DE LOS ENSAYOS CLÍNICOS ALEATORIZADOS
El estudio clínico PEPI (Post-menopausal Estrogen Progestin Intervention Trial) fue diseñado para investigar el efecto de la intervención con estrógenos y progestágenos en el riesgo cardiovascular en mujeres sanas tras la menopausia. La hipótesis del estudio fue que la administración de estrógenos disminuye el riesgo de coronariopatía porque tiene un efecto favorable en los factores de riesgo. Las pacientes fueron aleatorizadas a recibir uno de los siguientes tratamientos: a) 0,625 mg diarios de estrógeno equino conjugado; b) la misma dosis de estrógenos combinada con acetato de medroxiprogesterona administradas de manera cíclica; c) las mismas dosis de estrógenos y acetato de medroxiprogesterona administrados de manera continua, y d) la misma dosis de estrógenos combinados con progesterona micronizada y administrados de manera cíclica. Estos grupos de tratamiento se compararon con un grupo placebo. Los resultados de este estudio demostraron un efecto beneficioso en la concentración de HDL, LDL y fibrinógeno en todos los regímenes hormonales, asociado a una elevación de la concentración de triglicéridos. El efecto más beneficioso en la concentración de HDL se obtuvo con la administración de estrógenos sin oposición o con la combinación de estrógenos y progesterona micronizada. La administración de acetato de medroxiprogesterona se asoció a un aumento transitorio de la glucosa sanguínea, pero ninguno de los tratamientos tuvo efecto en la presión arterial ni en la concentración de insulina. Asimismo, ningún tratamiento indujo un aumento de peso de las pacientes, comparado con placebo. Es importante señalar que se observaron efectos adversos significativos en las mujeres que tenían el útero intacto y recibían estrógenos sin progestágenos, pues tuvieron una incidencia del 10% anual de hiperplasia endometrial atípica o adenomatosa (un precursor inequívoco de cáncer endometrial). Estos datos han cambiado la práctica clínica y, hoy día, las mujeres con útero intacto deben recibir los estrógenos en asociación con progesterona. Así pues, como se deriva del estudio PEPI, los estrógenos en asociación con progesterona micronizada constituyen la mejor combinación para obtener un perfil de riesgo favorable en mujeres con útero intacto; en el caso de mujeres histerectomizadas, se recomienda la administración de estrógenos sin oposición.
A partir de la experiencia adquirida, se ha ido caracterizando el riesgo no cardíaco del tratamiento hormonal sustitutorio. Los datos disponibles han permitido saber que, además de la hiperplasia endometrial atípica o adenomatosa asociada al tratamiento con estrógenos, la hormonoterapia aumenta entre 2 y 4 veces el riesgo relativo de tromboembolia venosa, un 40% el de enfermedad de vesícula biliar y, en los tratamientos crónicos de 5-10 años de duración, puede aumentar el riesgo de padecer cáncer de mama entre 4 y 5 veces.
No fue hasta 1998, con la publicación de los resultados del estudio HERS (the Heart and Estrogen/progestin Replacement Study), cuando salieron a la luz los datos obtenidos del primer gran ensayo clínico aleatorizado, doble ciego y controlado con placebo, que demostraron los efectos de la terapia con estrógenos y progestágenos en mujeres menopáusicas con enfermedad coronaria.
El estudio HERS incluyó a 2.763 mujeres menopáusicas hasta los 80 años de edad, que tenían el útero intacto y que presentaban historia de enfermedad coronaria definida por infarto de miocardio previo, cirugía cardíaca de derivación, angioplastia o estenosis igual o superior al 50% de al menos una arteria coronaria, si el modo de presentación era únicamente angina de pecho. Las pacientes fueron aleatorizadas a recibir una cápsula diaria que contenía 0,625 mg de estrógeno conjugado y 2,5 mg de acetato de medroxiprogesterona, o una cápsula de placebo. Las variables principales del estudio fueron la combinación del infarto de miocardio no fatal o la muerte por enfermedad coronaria, y se consideraron diversas variables secundarias (revascularización coronaria, hospitalización por angina inestable, hospitalización por insuficiencia cardíaca congestiva, enfermedad arterial periférica, etc.).
Durante el seguimiento se produjeron los cambios previstos en el perfil lipoproteico: los datos al año demostraron una mayor reducción del colesterol de las LDL con estrógenos y progestágenos que con placebo y un aumento del colesterol y HDL. También se documentó el anticipado y no deseado aumento en la concentración de triglicéridos con la hormonoterapia (fig. 1).
Fig. 1. Cambios en el perfil lipoproteico producidos en las mujeres posmenopáusicas incluidas en el estudio HERS. Como estaba previsto, después de un año de tratamiento con hormonoterapia oral se produjo una reducción significativa de la concentración de LDL y un aumento de las HDL y los triglicéridos sanguíneos.
Sin embargo, al final del ensayo no hubo diferencias significativas en la mortalidad por causa coronaria o en la incidencia de infarto no fatal. Un análisis retrospectivo puso de manifiesto que la terapia hormonal durante el primer año estaba asociada con un riesgo relativo para episodios coronarios de 1,52; este riesgo fue neutro en el segundo año y pareció demostrar una tendencia beneficiosa en los años 3-5. Los investigadores concluyeron que, tras 4 años de terapia, no se había reducido el riesgo global de coronariopatía. Más bien existía una tendencia hacia un aumento temprano de la tasa de episodios cardiovasculares, se triplicaba el riesgo de tromboembolia venosa y aumentaba en un 40% el riesgo de padecer enfermedad de vesícula biliar. Es importante señalar, no obstante, que en este ensayo clínico no se estudió el tratamiento con estrógenos sin progestágenos y no se investigó cuál era el efecto de la hormonoterapia en mujeres sin cardiopatía. En resumen, las recomendaciones que se derivan del estudio HERS son: a) no se debe iniciar la terapia hormonal para la prevención secundaria de cardiopatía isquémica, y b) en el caso de las pacientes que lleven varios años de tratamiento, puede ser apropiado continuar con la terapia, dada la posibilidad de un beneficio tardío.
¿Qué sucede con otros ensayos clínicos posteriores al estudio HERS? En un reducido ensayo aleatorizado procedente del Reino Unido, PHASE (the Papworth Hormone-replacement therapy Survival Enquiry) se utilizó hormonoterapia transdérmica comparada con placebo en 255 mujeres menopáusicas con cardiopatía isquémica. El estudio se complicó con diversas interrupciones. A los 4 años de seguimiento se observó un aumento no significativo de riesgo cardiovascular, la mayoría al inicio del estudio, y de tromboembolia venosa5.
Existen datos recientes, bastante preocupantes, procedentes de mujeres menopáusicas sanas de la US Women's Health Iniciative (WHI). En este caso se trata de un amplio estudio que incluye a más de 160.000 mujeres menopáusicas con edades comprendidas entre los 50 y 79 años, y aborda varios aspectos de salud menopáusica, principalmente en una cohorte observacional. En un subgrupo de 27.000 mujeres, los investigadores analizaron en un ensayo aleatorizado y controlado con placebo el efecto de la terapia hormonal (estrógenos solos en mujeres histerectomizadas o estrógenos con progesterona en mujeres con el útero intacto) en contraposición con placebo. En el año 2000, el Comité de Monitorización y de Seguridad de Datos obligó a los investigadores a enviar a cada una de las 27.000 mujeres incluidas en el estudio un escrito informándoles sobre el imprevisto aumento de episodios cardiovasculares tempranos (infartos de miocardio y accidentes cerebrovasculares) en los dos grupos que recibían tratamiento hormonal. La información no estaba incluida en los documentos de consentimiento informado. Este hecho afectó a menos del 1% de las pacientes y, debido a la posibilidad de algún beneficio tardío, el Comité de Monitorización y Seguridad de Datos recomendó la continuación del estudio. Estos episodios sucedieron añadidos al aumento anticipado de tromboembolia venosa. De nuevo en el año 2001, y por orden del Comité, se notificó a las pacientes que el pequeño aumento del riesgo cardiovascular persistía en los datos de los años 3-4 y otra vez el Comité recomendó continuar con el ensayo6.
El estudio ERA (Estrogen Replacement and Atherosclerosis) fue un ensayo angiográfico diseñado con el objetivo de investigar si la terapia hormonal (estrógenos o estrógenos en combinación con progestágenos) es beneficiosa en la progresión y regresión angiográfica en las mujeres con enfermedad coronaria documentada, como se desprendía de los datos observacionales. Se practicó un angiograma al inicio del ensayo y al final de una media de 3,1 años de seguimiento. No hubo diferencias en lo que respecta a la progresión o regresión angiográfica. Una vez más, el ensayo fue negativo.
Otros dos estudios intermedios aportan datos contradictorios sobre el beneficio de la terapia hormonal en la progresión de la aterosclerosis subclínica. El ensayo alemán PHOREA (Postmenopausal HOrmone REplacement against Atherosclerosis) analizó el efecto del estradiol combinado con gestodeno en mujeres con un aumento del grosor de la íntima-media de la carótida determinado por ecografía. Aunque el tratamiento se asoció a una disminución significativa de las LDL, el fibrinógeno y la FSH, no hubo diferencias en la progresión de la aterosclerosis subclínica medida por ecografía carotídea al final del estudio7. Por otro lado, el ensayo estadounidense EPAT (Estrogen in the Prevention of Atherosclerosis Trial) se centró en el papel del estradiol en mujeres menopáusicas sanas con una concentración de LDL superior a 130 mg/dl. Cuando las LDL sobrepasaban los 160 mg/dl, el tratamiento hormonal se combinaba con un liporreductor. El seguimiento de las pacientes se realizó por exámenes de ultrasonido carotídeo seriados. Al final de este estudio, y contrariamente a lo obtenido en el estudio europeo, hubo una disminución en la progresión de la aterosclerosis carotídea subclínica, pero sólo en las pacientes que no recibieron terapia con estatinas. En el grupo al que se administraron estatinas, la hormonoterapia no proporcionó ningún beneficio adicional8.
El estudio WEST (Women's Estrogen for Stroke Trial) abordó el papel del 17-beta-estradiol en el pronóstico de las mujeres menopáusicas (edad media de 71 años) que habían padecido un ictus reciente o un episodio isquémico transitorio. Los estrógenos no redujeron el riesgo de muerte o de accidente cerebrovascular recurrente no fatal, pero aumentaron el riesgo de accidente cerebrovascular fatal y empeoraron los signos neurológicos y déficit funcionales de los ictus no fatales. Los investigadores del estudio concluyeron que el estradiol está contraindicado en la prevención secundaria de la enfermedad cerebrovascular9.
En las figuras 2a y b, preparadas en la primavera del año 2002, se expone un resumen de los ensayos clínicos de prevención secundaria y de prevención primaria, respectivamente, y los beneficios y riesgos obtenidos en cada uno de ellos.
Fig. 2. Resumen de los beneficios y riesgos obtenidos en los principales ensayos clínicos de prevención secundaria (a) y de prevención primaria (b) que han analizado el efecto de la terapia hormonal oral o transdérmica sobre la incidencia de enfermedad cardiovascular e ictus.
ENSAYOS CLÍNICOS COMUNICADOS RECIENTEMENTE: VERANO DE 2002
El HERS II (the Heart and Estrogen/progestin Replacement Study follow-up)10 fue un estudio observacional, sin enmascaramiento, en el que se llevó a cabo un seguimiento de la mayoría de las participantes en el estudio HERS por un período adicional de 2,7 años, manteniendo a las pacientes con su tratamiento original. El objetivo era conocer si la tendencia a la reducción del riesgo coronario en los últimos años observado en el estudio HERS persistiría tras un seguimiento adicional. HERS II contó con el 93% de las participantes supervivientes del HERS, y aproximadamente la mitad de las pacientes continuó con el tratamiento del estudio original. Sin embargo, después de una media de 6,8 años de seguimiento total, este régimen de estrógenos y progestágenos no redujo el riesgo de episodios cardiovasculares en mujeres con enfermedad coronaria establecida. Incluso después de corregir por posibles factores de confusión y otros factores, como el uso de estatinas, no hubo diferencias en el pronóstico. Tampoco se alteraron los resultados cuando se realizó el análisis en función del tratamiento recibido en vez de según la intención de tratamiento. En vista de este resultado nulo, deben enfatizarse los riesgos concomitantes: la aparición de tromboembolia venosa se duplicó, predominantemente en los años iniciales, y el porcentaje de enfermedad de la vesícula biliar que requirió cirugía aumentó en casi un 50%. Por tanto, los investigadores concluyeron que este tratamiento de estrógenos-progestágenos no proporciona ningún beneficio en mujeres mayores con enfermedad coronaria establecida y puede ser perjudicial.
La Women's Health Iniciative (WHI), siguiendo el consejo del Comité de Monitorización y de Seguridad de Datos, interrumpió el grupo de tratamiento con estrógenos y progestágenos del ensayo aleatorizado en julio de 2002, después de un seguimiento medio de 5,2 años11. El tratamiento se interrumpió por el aumento del riesgo de cáncer de mama invasivo, que sobrepasaba los límites de finalización del ensayo previamente establecidos, y el aumento del riesgo global, que fue superior al beneficio. El seguimiento de estas pacientes continuará en un estudio de tipo observacional. Por otro lado, continúa la parte del ensayo aleatorizado dedicado a la terapia con estrógenos únicamente.
Debido a que la relación beneficio/riesgo de la terapia con estrógenos y progestágenos en mujeres menopáusicas predominantemente saludables es desfavorable desde un punto de vista poblacional, no puede recomendarse para promover la salud y prevenir la enfermedad. Sin embargo, es importante destacar que la mayoría de las mujeres en el estudio WHI no experimentó ningún episodio adverso, es decir, el riesgo individual de perjuicio es pequeño. Por ejemplo, el tratamiento combinado de 2.000 mujeres durante 5 años induciría un exceso de 7 episodios coronarios, 8 accidentes cerebrovasculares, 8 casos de cáncer de mama invasivo y 8 casos de embolia pulmonar. En contraste con estas cifras, habría 6 casos menos de cáncer colorrectal y 5 casos menos de fractura de cadera. Merece la pena resaltar que los episodios coronarios, los accidentes cerebrovasculares, el cáncer de mama y la embolia pulmonar contribuyeron por igual al perjuicio.
Se debe mencionar al grupo de mujeres que no fueron incluidas en el estudio HERS ni en la WHI, y que son las mujeres menopáusicas muy sintomáticas. Sería improbable que se ofrecieran voluntariamente a participar, dado el 50% de probabilidad de aleatorización a placebo. En estas mujeres, en su mayoría jóvenes, los síntomas, la calidad de vida y otros beneficios posibles de la terapia hormonal pueden perfectamente superar a los perjuicios, aunque esto no ha sido probado en una evaluación científica sólida.
POTENCIALES ALTERNATIVAS A LA TERAPIA HORMONAL «CLÁSICA»: LOS MODULADORES SELECTIVOS DE LOS RECEPTORES DE ESTRÓGENOS
El interés de los investigadores se ha centrado, más recientemente, en los moduladores selectivos de los receptores de estrógenos. Se trata de preparaciones no hormonales con efectos antagonistas de los estrógenos en la mama y el útero y con efectos agonistas de los estrógenos en el hueso y en los factores de riesgo cardiovascular. El raloxifeno, único principio activo que está incluido en ensayos clínicos actualmente en marcha, tiene licencia en los EE.UU. para la prevención y el tratamiento de la osteoporosis, y puede tener efectos favorables en la mama y el sistema cardiovascular. Su efecto sobre el perfil lipoproteico se resume en la figura 312. Los datos disponibles demuestran que se trata de una terapia con una seguridad clínica notable y, aunque el riesgo de tromboembolia venosa es similar al que se asocia a la terapia hormonal, tiene la gran ventaja de no producir hemorragias ni proliferación endometriales y de no aumentar el dolor mamario ni el riesgo de cáncer de mama. Los sofocos y los calambres en las piernas son similares a los observados en el grupo placebo.
Fig. 3. Efecto del tratamiento con raloxifeno, un modulador de los receptores de estrógenos, sobre el perfil lipoproteico en mujeres posmenopáusicas a los 6 meses de seguimiento. Obsérvese que en este caso no se produjo un aumento de la concentración de triglicéridos asociado al tratamiento, como ocurría con la terapia hormonal clásica, pero tampoco hubo efecto sobre las HDL (tomada de Walsh BW et al12).
El estudio MORE (Multiple Outcomes of Raloxifene Evaluation) analizó de forma aleatoria a mujeres con osteoporosis y riesgo de fracturas, pero no seleccionadas por tener riesgo de cáncer de mama o enfermedad coronaria. El análisis de los datos del ensayo puso de manifiesto una reducción del cáncer de mama invasivo en el grupo tratado con raloxifeno comparado con el grupo placebo. La magnitudad del posible efecto beneficioso ha sido tal que el Instituto Nacional de la Salud de los EE.UU. ha decidido emprender un estudio comparativo entre el raloxifeno y el tamoxifeno en la prevención del cáncer de mama en mujeres con riesgo elevado de padecerlo. En la figura 4 se observa la reducción que ejerció este fármaco sobre la incidencia de cáncer de mama entre las pacientes que recibieron raloxifeno después de 4 años de seguimiento13.
Fig. 4. Efecto del raloxifeno sobre la incidencia de cáncer de mama invasivo en mujeres posmenopáusicas después de 4 años de tratamiento, según los resultados del estudio MORE. Contrariamente a lo que se ha descrito para la terapia hormonal clásica, el raloxifeno no sólo previno el aumento de la tasa de cáncer de mama, sino que tuvo un drástico efecto reductor (tomada de Cauley JA et al13).
Debido al éxito de estos resultados, decidimos emprender el estudio RUTH (Raloxifene Use in The Heart), que incluye de forma aleatoria a más de 10.000 mujeres menopáusicas de 26 países, con el fin de evaluar el efecto del raloxifeno sobre el corazón. Las variables principales del estudio incluyen la muerte por causa coronaria, el infarto de miocardio no fatal, la hospitalización por síndrome coronario agudo y el cáncer de mama invasivo. El ensayo RUTH fue diseñado para estudiar tanto a mujeres con enfermedad coronaria documentada, como aquellas con alto riesgo de sufrir algún episodio coronario. Se caracteriza por tener un sistema de puntuación que asigna un número determinado a la existencia de episodios coronarios previos y ciertos factores de riesgo14. La puntuación crece a medida que se acumulan estos factores y así, por ejemplo, haber tenido un infarto de miocardio previo equivale a 4 puntos, mientras que la diabetes equivale a 3 puntos. Otros factores de riesgo que puntúan son la edad, el tabaquismo, la hipertensión, la hiperlipemia, etc. Para entrar en el estudio RUTH se precisa un mínimo de 4 puntos; las características basales de las participantes en el estudio se describen en un manuscrito pendiente de publicación15.
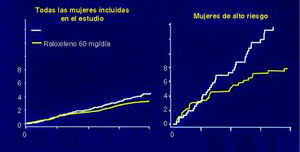
El sistema de puntuación del estudio RUTH se aplicó para analizar a las pacientes con osteoporosis que habían sido incluidas en el estudio MORE, para identificar de manera retrospectiva a aquellas en gran riesgo de sufrir episodios coronarios. Las mujeres con un elevado riesgo cardiovascular se benefician significativamente del tratamiento con raloxifeno en cuanto al porcentaje de episodios cardiovasculares ocurridos durante el seguimiento (fig. 5), algo que no pudo observarse cuando se analizó la totalidad de la población del estudio16. Significativamente, no hubo ningún aumento prematuro de los episodios cardiovasculares en las pacientes del estudio MORE con alto riesgo cardiovascular tratadas con raloxifeno.
Fig. 5. Incidencia de episodios cardiovasculares durante el seguimiento de pacientes posmenopáusicas aleatorizadas a recibir raloxifeno o placebo, según resultados del estudio MORE. Cuando se considera el subgrupo de mujeres sin riesgo cardiovascular (izqda.) no se observa un efecto protector asociado al tratamiento. Por el contrario, entre las pacientes con factores de riesgo cardiovascular (dcha.) el tratamiento con raloxifeno redujo significativamente la tasa de episodios cardiovasculares durante el seguimiento (tomada de Barrett-Connor E et al16).
RECOMENDACIONES SOBRE TERAPIA HORMONAL EN LA MENOPAUSIA PARA LA PREVENCIÓN DE LA ENFERMEDAD CARDIOVASCULAR
Las recomendaciones de la American Heart Association del año 200117 sobre la terapia hormonal en la menopausia reflejan los resultados obtenidos en los recientes ensayos clínicos. Si bien las guías previas de práctica clínica en la enfermedad coronaria del American College of Cardiology y de la American Heart Association (AHA) aconsejaban la terapia hormonal como hipolipemiante de elección en pacientes coronarias menopáusicas, y estas recomendaciones también se hicieron por parte del National Cholesterol Education Program Adult Treatment Panel II (NCEP II), las nuevas directrices aconsejan la administración de estatinas, que han demostrado una clara ventaja en los ensayos clínicos en mujeres, sin que se observen los riesgos asociados a la hormonoterapia. La recomendación actual de la AHA es que el inicio de la hormonoterapia no está indicado para la prevención secundaria de la enfermedad coronaria. En aquellos casos en los que una paciente con enfermedad cardiovascular haya recibido el tratamiento durante un período previo prolongado, la decisión de continuar o interrumpir la terapia debe basarse en los beneficios no coronarios establecidos y en los riesgos y preferencias de las pacientes. Por otro lado, si se hospitaliza a una paciente por un síndrome coronario agudo o cualquier otra enfermedad o tratamiento quirúrgico asociado, con una inmovilización mientras recibe terapia hormonal, debe considerarse la interrupción del tratamiento o la profilaxis del tromboembolismo venoso17.
Las recomendaciones clínicas de la AHA sobre el uso de hormonoterapia para la prevención primaria se encuentran a la espera de los resultados de los ensayos clínicos que están actualmente en marcha. Hoy día, los datos a favor de la administración de terapia hormonal para la prevención primaria de la enfermedad coronaria son todavía insuficientes y la iniciación o continuación de la hormonoterapia debe basarse, en las mujeres sanas, en los beneficios y riesgos no coronarios establecidos, en los posibles beneficios y riesgos coronarios y en las preferencias individuales.
Las recomendaciones de la AHA del año 2002 aparecerán próximamente. Una publicación reciente del Instituto Nacional de la Salud de los EE.UU.18 presenta una completa revisión basada en la evidencia sobre la salud de la mujer y la menopausia.
Basado en una ponencia del X Simposio Internacional de Cardiopatía Isquémica celebrado en Bilbao, España, el 22-24 de mayo de 2002. Actualizado en octubre de 2002.
Correspondencia: Dra. N.K. Wenger.
Department of Medicine (Cardiology).
Emory University School of Medicine.
69 Jesse Hill Jr. Drive, SE. Atlanta, GA 30303. EE.UU.