Palabras clave
INTRODUCCIÓN
El campo de las arritmias y de la electrofisiología cardiaca ha continuado experimentando numerosos avances en el pasado año. En este artículo se comentan algunos de los más relevantes, tanto para el cardiólogo clínico como para el electrofisiólogo, seleccionados por su repercusión clínica y por aportar mejoras significativas para la realización y los resultados de los procedimientos invasivos en esta materia (fig. 1).
Figura 1. Búsqueda en PubMed con los artículos publicados el último año. La fibrilación auricular tiene el mayor número de ellos.
El artículo se ha dividido en seis apartados:
1. Arritmología clínica y síncope, incluye la reciente publicación de las nuevas guías de síncope.
2. Arritmias ventriculares, ablación, síndrome de Brugada, síndromes genéticos.
3. Arritmias supraventriculares, ablación, fibrilación auricular (FA), uno de los campos que ha experimentado un mayor avance.
4. Desfibrilador implantable.
5. Terapia de resincronización cardiaca (TRC).
6. Sistemas de monitorización.
De cada estudio destacado se muestra un resumen, según lo expuesto en forma oral si se ha comunicado en los congresos más recientes o, en su caso, de lo publicado en revistas científicas. Dado que algunos de ellos no han sido publicados todavía en su versión completa, en estos casos la información debe interpretarse como preliminar. La sección de electrofisiología de la Sociedad Española de Cardiología dispone de un blog de actualizaciones bibliográficas cuya visita se recomienda (www.arritmias.org).
ARRITMOLOGÍA CLÍNICA Y SÍNCOPE
A finales de 2009 se publicaron las nuevas guías de síncope1, completamente reelaboradas y con muchos nuevos aspectos. El primero de ellos es la definición del síncope en el contexto de otras enfermedades que producen pérdida de conciencia. El segundo es que incluyen muchos más datos epidemiológicos con distribución y etiología por edades. Las nuevas guías incluyen también una nueva estrategia diagnóstica con una exhaustiva estratificación del riesgo y valoran la utilidad de la monitorización prolongada en estos pacientes.
La utilidad y metodología del test de mesa basculante continúa siendo objeto de frecuentes publicaciones. En una de ellas, publicada por Flevari et al2, se indica que la realización del test con clorimipramina puede ser útil en algunos casos, por su actuación a diferentes niveles en el sistema nervioso central. Esto no significa que deba reemplazar a otros fármacos en los protocolos, sino que se podría seleccionar uno específico según las características clínicas del síncope, por ejemplo, la nitroglicerina si predomina el factor ortostático, el isoproterenol si predomina el estímulo adrenérgico y quizá la clorimipramina en ausencia de trigger o con sospecha de trigger en el sistema nervioso central.
El electrocardiograma simple sigue siendo una herramienta fundamental en la valoración clínica de las arritmias cardiacas, como acreditan Bazan et al3 en su artículo, al revisar su experiencia en 87 pacientes sometidos a ablación de taquicardia auricular. En el ECG, identificar una onda P con una duración > 110 ms con una melladura en la onda P en pacientes de edad < 50 años, sin cardiopatía de base, se asocia a un origen de la taquicardia auricular en las venas pulmonares, lo que tiene trascendencia de cara a planificar el procedimiento de ablación en estos pacientes.
ARRITMIAS VENTRICULARES, ABLACIÓN, SÍNDROME DE BRUGADA, SÍNDROMES GENÉTICOS
El síndrome de Brugada continúa ocupando un puesto relevante por el número de publicaciones en este año. Así, una excelente revisión del síndrome de Brugada publicada en esta misma Revista4, en la que se hace una puesta al día integral de aspectos epidemiológicos, electrocardiográficos genéticos, mecanismos iónicos, clínicos, estratificación de riesgo y tratamiento. Otros autores han demostrado que pacientes con FA de reciente comienzo pueden tener un síndrome de Brugada latente que, además, puede preceder el inicio de arritmias ventriculares malignas5.
El diagnóstico electrocardiográfico aún ocupa artículos como el de Richter et al6, en el que se valora la capacidad diagnóstica de V3 para el síndrome de Brugada, y se concluye que no aporta información y que los pacientes con una sola derivación precordial derecha diagnóstica tienen un perfil clínico y de riesgo similar al de los que tienen más de una derivación anormal. Esto es una información adicional que modifica el consenso actual, que requiere la elevación típica en más de una derivación electrocardiográfica precordial derecha. En el estudio genético se realizó un compendio internacional de mutaciones en el canal de sodio SCN5A7, y se han encontrado hasta 200 nuevas mutaciones en un 21% de los pacientes con síndrome de Brugada frente a un 2-5% en controles. Asimismo, García-Castro et al8 realizaron un estudio del espectro mutacional del gen SCN5A en pacientes españoles con síndrome de Brugada, y han encontrado nuevas mutaciones.
La muerte súbita en las miocardiopatías y canalopatías es aún objeto de gran atención. En un estudio de Gimeno et al9 se revisan las características de esta muerte súbita en familias con cardiopatías hereditarias. Para ello, se documentaron 152 casos de muerte súbita y se revisaron todos los datos. Los varones predominaron claramente y la muerte súbita ocurrió con más frecuencia en el ejercicio o actividad cotidiana en las miocardiopatías y en el reposo/sueño en las canalopatías, como el síndrome de Brugada.
El síndrome de QT largo ha sido objeto de estudios como el FAMI-LION10. Kapplinger et al analizaron la prevalencia de mutaciones de los primeros 2.500 pacientes consecutivos remitidos para la prueba genética FAMILION, en busca de mutaciones en 5 de los genes SQTL: KCNQ1 (LQT1), KCNH2 (LQT2), SCN5A (LQT3), KCNE1 (LQT5) y KCNE2 (LQT6). En total, 903 casos (36%) tuvieron una posible mutación causante de SQTL, ausente en > 2.600 alelos de referencia. Aproximadamente 1/3 de las mutaciones más recientemente detectadas siguen siendo noveles. Aunque los datos de control de la población señalan que la gran mayoría de estas mutaciones son patógenas, la interpretación de los expertos de los resultados de pruebas genéticas seguirá siendo fundamental para el uso clínico efectivo.
La ablación de la taquicardia ventricular (TV) es una técnica imprescindible y muy eficaz para el tratamiento de TV de múltiples orígenes y mecanismos diversos, así como para el control de pacientes con taquicardias recurrentes, no controlables con tratamiento médico11. Viana-Tejedor et al12 publicaron su experiencia positiva de ablación de TV en un grupo de 33 pacientes ancianos con cardiopatía estructural. Los buenos resultados y la tasa muy baja de complicaciones nos aconsejan valorar esta alternativa, aun en pacientes de edad avanzada, ya que se pueden beneficiar enormemente de ella. Kuck et al13 publicaron también el estudio multicéntrico VTACH sobre la ablación por catéter de la TV estable antes de la implantación de desfibrilador. Tras 2 años, las estimaciones de la supervivencia libre de arritmias ventriculares fueron del 47% en el grupo de ablación y el 29% en el grupo control (hazard ratio [HR] = 0,61; intervalo de confianza [IC] del 95%, 0,37-0,99; p = 0,045). La ablación profiláctica antes de la implantación de desfibrilador, según esta experiencia clínica, parece prolongar el tiempo hasta la recurrencia.
La ablación epicárdica puede ser necesaria en aproximadamente un 10-30% de los casos con TV tras infarto de miocardio y en 1/3 de los pacientes con TV en el seno de una miocardiopatía dilatada no isquémica. Sacher et al14 analizaron la seguridad y las complicaciones a medio plazo tras abordaje epicárdico. De un total de 913 procedimientos de ablación de TV entre los años 2001 y 2007, el 17% requirió abordaje epicárdico, el 86% de ellos tras abordaje endocárdico fallido. El 71% de los sujetos no presentaron recurrencias de la TV tras un seguimiento medio de 2 años. El abordaje epicárdico es necesario para el tratamiento de un número significativo de pacientes con TV.
ARRITMIAS SUPRAVENTRICULARES, ABLACIÓN, FIBRILACIÓN AURICULAR
Guías clínicas, registros y consensos
Simultáneamente a su presentación en el Congreso Europeo de Cardiología 2010, se publicaron las nuevas guías del manejo de la fibrilación auricular15. Incluyen importantes cambios, como la nueva propuesta de estratificación de riesgo CHA2DS2-VASc y la inclusión de la dronedarona en el esquema de decisión de tratamiento.
También se ha publicado el Registro Español de Ablación con Catéter16. En él participaron 55 centros con un total de 7.741 procedimientos; media, 141 ± 97 procedimientos/centro. Los tres sustratos más frecuentes fueron la taquicardia intranodal (n = 2.302; 31%), el istmo cavotricuspídeo (n = 1.720; 22%) y las vías accesorias (n = 1.658; 21%). El cuarto sustrato abordado (n = 829; 11%) fue la FA, que mostró un incremento del 18% respecto al registro de 2007. La tasa general de éxito fue del 93%; las complicaciones mayores, del 1,7%, y la mortalidad, del 0,03%.
La fibrilación auricular
Este año se han producido significativos avances en el tratamiento de la FA (fig. 2). La progresión de FA paroxística a persistente sigue despertando gran interés, según el análisis realizado por De Vos et al17. El análisis multivariable mostró que la insuficiencia cardiaca, la edad, el evento cerebrovascular, la enfermedad pulmonar y la hipertensión fueron los únicos predictores independientes de progresión. Utilizando el coeficiente de regresión, se calculó la puntuación del índice HATCH (iniciales en inglés de las enfermedades nombradas). Un 50% de los pacientes con puntuación de HATCH > 5 progresaron a FA persistente en comparación con sólo el 6% de los pacientes con puntuación 0.
Figura 2. Principales ensayos clínicos publicados este año referentes al tratamiento de la fibrilación auricular.
Los aspectos genéticos de la FA siguen produciendo interés. Gudbjartsson et al18 informan que una nueva variante genética en el gen ZFHX3 tiene mayor riesgo de FA en europeos. Más de un tercio de los europeos llevan una copia de la variante, y tienen un riesgo 20% mayor de FA y evento embólico que los individuos sin esta. La aplicación clínica de estos hallazgos requiere nuevas investigaciones.
Nuevos tratamientos para la fibrilación auricular
Entre los nuevos fármacos antiarrítmicos (FAA) en desarrollo, el vernakalant bloquea selectivamente los canales de potasio IKur presentes en las aurículas pero no en los ventrículos. El vernakalant también inhibe la corriente INa. Se necesitan estudios adicionales antes de que el fármaco esté disponible.
La ranolazina es un inhibidor de la INa (corriente tardía de sodio) e IKr (corriente rectificada). Este medicamento es un antianginoso aprobado, pero espera ensayos clínicos controlados como agente antiarrítmico19.
La dronedarona es un nuevo FAA con propiedades electrofisiológicas similares a la amiodarona y con menos efectos secundarios20. Los datos se basan en la evaluación de los resultados de múltiples ensayos en pacientes con FA. El estudio ATHENA, con 4.628 pacientes, es el mayor ensayo realizado hasta la fecha con un FAA. El estudio alcanzó su objetivo principal al demostrar que la dronedarona añadida al tratamiento estándar reducía un 24% (p < 0,001) la variable de análisis combinada de riesgo de hospitalización por causas cardiovasculares o muerte, en comparación con placebo.
Este año se publicó el estudio DIONYSOS, en el que se comparó la dronedarona con la amiodarona21. El objetivo primario se alcanzó en el 75% de los pacientes tratados con dronedarona y en el 59% de los que recibieron amiodarona, en 12 meses de seguimiento. La dronedarona se toleró mejor, y hubo menor tasa de abandonos por menos efectos adversos, aunque los pacientes tuvieron más recurrencias que con la amiodarona. Actualmente está todavía en marcha el estudio ARTEMIS, cuya idea fue tratar a todos los pacientes con FA persistente mediante dosis de carga de amiodarona durante meses y luego realizar el cambio a dronedarona o no. La hipótesis principal será la recurrencia de la FA, pero en realidad los problemas de seguridad son los protagonistas: bradicardia, prolongación del PR y QT y la interacción INR.
Hay nuevos datos que señalan que podría haber un papel para el bloqueador del receptor de la angiotensina irbesartán en la prevención y el desarrollo de insuficiencia cardiaca en pacientes con FA. El irbesartán no logró reducir el objetivo primario compuesto de infarto cerebral, infarto de miocardio y muerte vascular, pero sí redujo el secundario de hospitalizaciones por insuficiencia cardiaca. Los resultados del estudio ACTIVE I se presentaron durante la sesión de la Sociedad Europea de Cardiología 2009.
Control de la frecuencia cardiaca. El estudio RACE II
El ensayo RACE-2 evaluó un control farmacológico (bloqueadores beta, digoxina, antagonistas del calcio) moderado o estricto en 614 pacientes con FA crónica22. Se considera moderado: < 110 lpm en reposo, y estricto, < 80 lpm en reposo o < 110 lpm durante el ejercicio moderado. Los objetivos primarios fueron la muerte por causas cardiovasculares, hospitalización por insuficiencia cardiaca e incidencia de tromboembolias. Tres años de seguimiento demostraron igual eficacia de ambas estrategias en cuanto al objetivo primario (el 12,9 y el 14,9%; p < 0,001). Los beneficios clínicos potenciales de controlar estrictamente la frecuencia, si se logran, pueden ser compensados por los efectos adversos de los FAA. Los pacientes en el grupo leve tuvieron 10 veces más probabilidades de lograr su objetivo de frecuencia cardiaca sólo con bloqueadores beta (p < 0,001), mientras que los estrictos recibieron doble o triple terapia de FAA.
Prevención de la embolia en la fibrilación auricular con nuevos anticoagulantes
El objetivo del ensayo EXPLORE-Xa de fase 2 fue evaluar el tratamiento con 3 dosis de betrixabán, inhibidor oral directo del factor Xa, en comparación con warfarina en 508 pacientes con FA no valvular23. Los resultados con betrixabán fueron similares al tratamiento con warfarina. El apixabán es un inhibidor oral del factor Xa. El estudio AVERROES incluyó a 5.600 pacientes con todo tipo de FA, intolerantes o no aptos para la warfarina, aleatorizados a 5 mg de apixabán o entre 81 y 324 mg de ácido acetilsalicílico. El ensayo reveló una reducción clínicamente importante en la embolia sistémica y del accidente cerebrovascular con apixabán.
El estudio RE-LY24 compara el dabigatrán (inhibidor directo de la trombina) con la warfarina en 18.113 pacientes con FA. Se utilizaron dos dosificaciones fijas de dabigatrán (110 y 150 mg) dos veces al día frente a warfarina según INR, y se demostró un beneficio equivalente entre la dosis de 110 mg y la warfarina. A la dosis de 150 mg dos veces al día, el dabigatrán demuestra superioridad respecto a la prevención de eventos embólicos, con un perfil de seguridad similar a la warfarina.
Prevención de la embolia en la fibrilación auricular con otras ayudas: genotipificación y dispositivo oclusor de la orejuela
Se han comunicado los resultados del estudio MM-WES25. El protocolo de este ensayo incluyó el análisis genético de 896 pacientes para aislar los genes CYP2C9 y VKORC1, ya que se han definido polimorfismos en ambos que, en teoría, conllevarían cambios individuales en sensibilidad o resistencia a la warfarina. La aplicación de la genotipificación para determinar la dosis ajustada de warfarina puede resultar en una disminución total de la tasa de hospitalización por eventos adversos de aproximadamente un 30%.
En el manejo de pacientes con FA no valvular se publicó el estudio PROTECT-AF, que valora el tratamiento con oclusión de la orejuela izquierda mediante dispositivo percutáneo WATCHMAN en pacientes con complicaciones con el tratamiento anticoagulante26. Su diseño es un doble brazo aleatorizado a grupo dispositivo (463 pacientes) o a grupo control (244 pacientes). El ictus hemorrágico fue sensiblemente inferior en el grupo de dispositivo, sin mostrarse inferior en mortalidad o embolias. Actualmente, en España el único oclusor de orejuela comercializado es el Amplatzer Cardiac Plug® (fig. 3).
Figura 3. Dispositivo oclusor de orejuela Amplatzer Cardiac plug .
Ablación de la fibrilación auricular
La ablación de la FA ha evolucionado, con lo que se han mejorado indicaciones y resultados en los últimos años, como resumía Pappone en su Editorial de REVISTA ESPAÑOLA DE CARDIOLOGÍA27. En él se analizaba la estrategía de ablación circular amplia para la FA paroxística, mientras que en pacientes con fibrilación persistente hay menos consenso y se emplean lesiones lineales y estrategias escalonadas. En un registro multicéntrico internacional se presentó una actualización sobre métodos, eficacia y seguridad de la ablación de FA28, con datos de 20.825 procedimientos de ablación en más de 16.000 pacientes durante un periodo de 4 años. La tasa de éxito total con o sin el uso de FAA fue del 80%. La tasa total de complicaciones fue del 4,5%. En cuanto a la técnica de ablación, el aislamiento de venas pulmonares (VP) fue el objetivo en el 75% de los procedimientos, que puso de manifiesto que el aislamiento de VP es el objetivo más importante.
Un estudio29 evaluó los resultados clínicos de 153 pacientes consecutivos, sometidos a ablación de FA persistente, utilizando un enfoque escalonado. La ablación fue eficaz en la terminación de la FA en 130 (85%) pacientes. La FA recurrió en sólo 6 de los 130 pacientes (5%) en los que se interrumpió por la ablación y en 9 de los 23 pacientes (39%) que requirieron cardioversión. Otros autores han demostrado, en pacientes con FA persistente de larga duración a quienes se realizó ablación, que la aurícula derecha es la causa de la FA en aproximadamente una quinta parte de los casos persistentes de larga duración. Hay que tener en cuenta que la reconducción por las VP ocurre tras la ablación y es la causa de muchas recurrencias, lo que ha sido objeto también de muchos estudios experimentales y en humanos30.
Se comunicaron los primeros resultados del estudio multicéntrico STOP-AF23, que incluyó a 245 pacientes con FA paroxística con el objetivo primario de comparar la crioablación con catéter-balón con los fármacos convencionales. El 70% de los pacientes tras crioablación estaban libres de arritmia en comparación con sólo el 7% de los pacientes tratados con fármacos. La crioablación con catéter-balón es efectiva y posible en la mayoría de los pacientes. Se pueden dar casos de estenosis de las VP y parálisis frénica, reversibles en su mayoría.
Ya se han hecho públicos los primeros datos del estudio piloto CABANA23 (ablación comparada con los FAA para el tratamiento de la FA). Se incluyó a pacientes que presentaban FA persistente y factores de riesgo cardiovascular adicionales, como diabetes mellitus, enfermedad coronaria, hipertensión, insuficiencia cardiaca o fracción de eyección del ventrículo izquierdo (FEVI) < 35%. Tras 12 meses de seguimiento clínico, el análisis de los resultados mostró ausencia de FA en el 65% de los casos tras crioablación en comparación con el 41% de los pacientes tratados con fármacos (p = 0,003).
El estudio ThermoCool AF31, recientemente publicado, demostró la superioridad de la ablación con aislamiento de VP respecto a FAA en el tratamiento de pacientes con FA sintomática en quienes había fallado al menos un antiarrítmico. Se incluyó a un total de 167 pacientes que habían experimentado al menos tres episodios de FA en los últimos 6 meses. Después de 9 meses, el 66% de los pacientes en el grupo de ablación y sólo el 16% de los pacientes en el grupo de tratamiento con FAA tuvieron éxito con el tratamiento.
Según los resultados de un nuevo estudio, el tratamiento de la FA con ablación reduce el riesgo de Alzheimer y demencia32. Los mismos investigadores habían establecido previamente un vínculo entre la enfermedad de Alzheimer, la demencia y la FA33.
Nuevas tecnologías para la ablación de la fibrilación auricular
Hay dos sistemas diferentes de navegación remota disponibles en nuestro país: la navegación magnética de Stereotaxis y la navegación robotizada Sensei de Hansen-Medical. La falta de un catéter magnético de punta irrigada adecuado ha limitado el papel de la ablación de la FA por control remoto magnético. En un artículo reciente del grupo de Kuck34, se analizan los resultados de un catéter irrigado y un rediseño en 56 pacientes. Aunque con el catéter inicial se observa carbonización frecuente (61%) y complicaciones (11%), con el rediseño del catéter mejora el perfil de seguridad y eficacia. También se ha desarrollado un nuevo sistema de navegación remota, el sistema CGCI de Magnetecs, de campos magnéticos para posicionar los catéteres, que parece permitirá un montaje más cómodo y una movilización del catéter más rápida y precisa.
Se sigue desarrollando la crioablación de VP mediante balón, prueba de ello es el artículo de Claudia Herrera35, que utiliza ecocardiograma transesofágico para controlar la posición del balón y la oclusión completa de la VP. Al final del procedimiento se demostró el aislamiento eléctrico en 109 de 111 venas ocluidas y sólo en 1 de 12 venas no ocluidas. El aislamiento con éxito con criobalón requiere un contacto adecuado en todo el ostium.
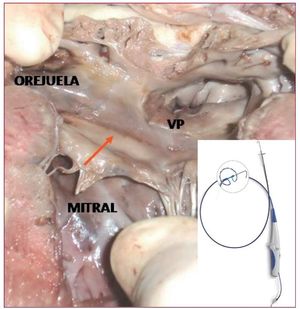
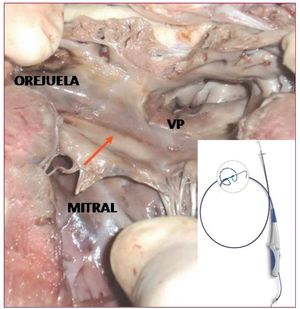
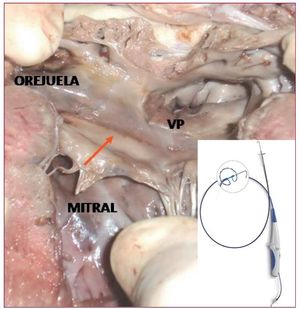
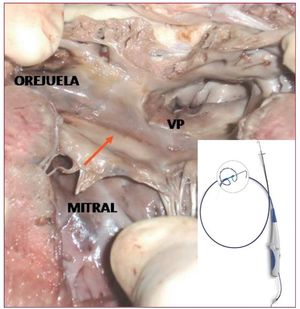
Asimismo, hay nuevos sistemas de ablación con catéter circular multielectrodo que permiten lesiones en arcos antrales. El PVAC® es un catéter de ablación circular decapolar que permite mediante RF crear lesiones continuas (fig. 4). En un estudio prospectivo de 50 pacientes con FA persistente, el procedimiento duró 155 min y el aislamiento completo se logró en todos los casos. La ablación con catéter circular puede reducir los tiempos totales de procedimiento al simplificarlo36.
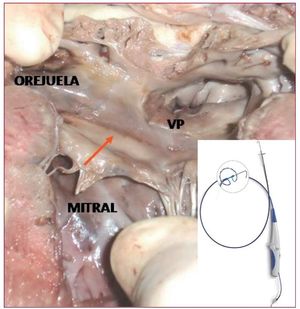
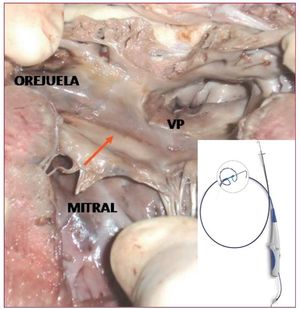
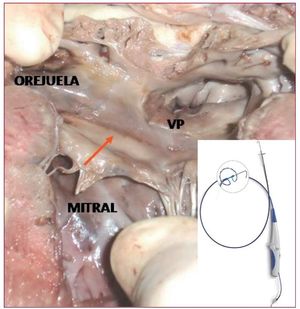
Figura 4. Lesión continua realizada con el catéter PVAC en el antro de las venas pulmonares (VP) de un corazón de cerdo en un modelo experimental.
Wazni et al37 han publicado su experiencia con el sistema robótico de Hansen para la ablación de la FA, que demostró reducción de fluoroscopia. No hay diferencia con respecto a las recurrencias frente al abordaje convencional.
Para finales de 2010 se dispondrá de la tecnología Ensite-Contact. Este nuevo sistema permite visualizar el contacto eléctrico que existe entre la punta del catéter de ablación y el tejido cardiaco. Las mediciones se basan en el cálculo de impedancias y así poder hacer lesiones más precisas y eficaces. En su fase inicial, se probó ya en diversos hospitales españoles este año (fig. 5).
Figura 5. Ablación de fibrilación auricular con el nuevo sistema Contact de control de presión con medida de impedancias. Cuando los valores de referencia de la impedancia aseguran un buen contacto, la punta del catéter se ilumina en verde.
Control de la seguridad de la ablación en aurícula izquierda
Arana-Rueda38 ha estudiado la relación particular del esófago con la aurícula izquierda. Entre las complicaciones, la fístula esofágica es muy rara pero de alta letalidad. Por este motivo se han desarrollado sistemas de monitorización de la temperatura esofágica. En un artículo de Rillig39, con control de temperatura esofágica, se describió hasta un 14,3% de pacientes con lesiones esofágicas (6 de 42 pacientes). El sistema de monitor, a pesar de emplearse potencias bajas en la pared posterior auricular izquierda, detectó un aumento significativo de la temperatura esofágica > 39 °C en el 79,5% de los pacientes.
DESFIBRILADOR IMPLANTABLE
Registros, guías y consensos
Se publicó el Registro español de desfibrilador40. Este año se ha informado de un total de 3.486 implantes, cifra que se estima en un 84,7% del número total real anual en España (90/millón). La tasa de primoimplantes fue del 78,1%; la mayoría, varones, con una media de edad de 62 años y con disfunción ventricular. La cardiopatía subyacente más frecuente fue isquémica, y la prevención primaria continúa aumentando, lo que supone un 57% de los primoimplantes. En cuanto al tipo de dispositivo, el 48,1% son monocamerales; el 23,8%, bicamerales, y el 28,1%, resincronizadores.
La Sociedad Europea de Cardiología ha publicado una declaración de consenso, en la que recomiendan ciertas restricciones y precauciones para los conductores de los vehículos a motor con desfibriladores automáticos41. El documento establece una distinción entre conductores de grandes camiones y otros vehículos profesionales y conductores de coches normales y motocicletas y reconoce menos riesgos en los conductores con desfibrilador para prevención primaria. Por lo tanto, la restricción debe ser menos estricta en estos que en los pacientes implantados para prevención secundaria.
También se publicó una declaración de Consenso de la EHRA sobre la gestión de dispositivos electrónicos implantables cardiovasculares en pacientes en el final de su vida o si solicitan la suspensión del tratamiento42. La sentencia definitiva debe realizarla el paciente (o su representante legal) después de una comunicación cuidadosa acerca de las consecuencias de la desactivación, respetando su autonomía.
Utilización e indicaciones del desfibrilador
Este año comenzaron a estar disponibles los nuevos cables de desfibrilación IS-4 con las conexiones de bobinas y electrodos de sensado-estimulación integradas en una única conexión, lo cual facilitará el implante y recambio de estos dispositivos.
Recientemente se ha publicado que la infrautilización de los desfibriladores tras revascularización coronaria es mayor en mujeres y ancianos43, según ha mostrado un estudio de 13 años de seguimiento. Otro ensayo aleatorizado y controlado no ha demostrado beneficio en la supervivencia para el desfibrilador como terapia en las primeras semanas después de un infarto de miocardio. En el estudio IRIS44, en casi 900 pacientes con infarto de miocardio, la mortalidad total no se vio afectada por la terapia de desfibrilación en comparación con el tratamiento médico. Tras una media de unos 3 años, la proporción de riesgo de muerte de los pacientes con desfibrilador en comparación con el grupo control fue 1,04 (p = 0,78). La población IRIS y los resultados son similares a los del estudio DINAMIT, publicado en 2004 y que es la base para la actual orientación contra la implantación temprana tras el infarto.
Programación de la terapia del desfibrilador automático
La programación de la terapia antitaquicárdica en pacientes con desfibrilador es un tema importante, que sigue siendo objeto de múltiples estudios y modificaciones de algoritmos de los desfibriladores. Gasparini et al45 publicaron el estudio RELEVANT, en el que un desfibrilador biventricular simplificado con intervalos fijos de detección largos reduce las intervenciones del desfibrilador y las hospitalizaciones de insuficiencia cardiaca en pacientes con miocardiopatía no isquémica en prevención primaria. También Gasparini46 publicó un estudio prospectivo aleatorizado que comparó la eficacia de la estimulación antitaquicárdica biventricular con la derecha para terminar episodios de TV; en ambas fueron efectivas de forma similar, con tendencia a menor aceleración de la arritmia con estimulación biventricular en isquémicos.
La programación es importante y se deben evitar los choques lo máximo posible. Según los resultados de un estudio47, al programar ciertas variables, frecuencia de corte y duración más larga de detección, entre otros, se obtuvo una reducción de choques de un 17-28%. Los resultados se basan en datos de observación de una gran cohorte de 88.804 pacientes.
También un grupo español publicó el estudio REMEDIO48. Su objetivo fue determinar si las terapias inapropiadas podrían reducirse mediante el uso de un criterio de discriminación de morfología (Wavelet; Medtronic, Inc.). Los criterios de discriminación de Wave-let como único discriminador pueden reducir significativamente el tratamiento inapropiado para supraventriculares, por lo que se aconseja su uso.
Y es que todos los datos acaban confirmando que una programación más estratégica de los DAI reduciría significativamente la morbimortalidad. Este año también nos lo ha recordado Sweeney49 en un estudio para probar la hipótesis de que el riesgo de mortalidad en los pacientes con desfibrilador está influida por las interacciones entre el tipo de ritmo y el tipo de terapia eléctrica. Se probó esta hipótesis en un conjunto de datos único compuesto de cuatro ensayos clínicos que aplicaron ampliamente ATP para suprimir las crisis. Como se esperaba, el tratamiento con estimulación antitaquicárdica para la TV fue muy efectivo, terminando el 92% de los episodios, y ligeramente menos eficaz para la TV rápida, terminando el 68% de estos episodios. Se comprobó que los episodios de arritmias ventriculares conllevaban un aumento del 20% del riesgo relativo de muerte por cada episodio de choque, mientras que la terminada con estimulación no aumentó el riesgo de mortalidad.
Medtronic ha comercializado un nuevo desfibrilador con algoritmos adicionales que reduce drásticamente la incidencia de choques inapropiados. La tecnología SmartShock® incluye seis algoritmos que discriminan las arritmias potencialmente letales del resto de los eventos arrítmicos y no arrítmicos, Wavelet + PRLogicR, discriminadores de supraventriculares en la zona de fibrilación, confirmación+, discriminador de onda T, discriminación y alerta de ruido de cable y alerta de integridad del cable. Al parecer, con todos ellos se pueden reducir las descargas inapropiadas hasta una cifra tan baja como el 2%.
Resonancia y desfibrilador automático
Buendía et al50 publicaron un artículo sobre la resonancia magnética en pacientes portadores de dispositivos de estimulación cardiaca. Se estima que cada paciente tiene una probabilidad superior al 50% de precisar una resonancia posteriormente a lo largo de su vida. De forma prospectiva evaluaron a 33 pacientes, en los que se consideró imprescindible realizar la resonancia. No apreciaron complicaciones clínicas y se detectaron 2 casos de fallo temporal de la telemetría, 2 errores de detección y una respuesta de seguridad. No hubo alteraciones permanentes de ningún dispositivo.
Desfibriladores implantables subcutáneos
Se publicaron los resultados de 55 pacientes portadores de un desfibrilador íntegramente subcutáneo tras 1 mes de seguimiento51; 53 completaron un estudio electrofisiológico y el dispositivo detectó correctamente las 137 fibrilaciones ventriculares inducidas. Tras un seguimiento de 10 meses, el dispositivo detectó y trató correctamente 12 episodios espontáneos de fibrilación ventricular. No hubo problemas de fractura de electrodo, pero sí de migración y desplazamiento, por lo que hubo que hacer correcciones posteriores en estos pacientes. Se está llevando a cabo un ensayo no aleatorizado, multicéntrico e internacional en 330 pacientes; habrá que esperar a que termine para analizar los resultados.
TERAPIA DE RESINCRONIZACIÓN CARDIACA
Registros, guías y consensos
Se publicó la encuesta europea sobre terapia de resincronización cardiaca (TRC)52. Una cuarta parte de los pacientes tenían FA, un cuarto tenía un dispositivo anterior y un 20% tenía QRS estrecho < 130 ms. La encuesta también señala que en Europa la resincronización está infrautilizada en las mujeres y en los pacientes ancianos. Simultáneamente con su presentación en el Congreso Europeo de Cardiología 2010 se publicó una actualización sobre la terapia con dispositivos en la insuficiencia cardiaca. Los cambios que incluye están basados en los resultados de los últimos estudios, como MADIT-CRT y REVERSE que comentaremos a continuación53,54. Previamente, un panel asesor de la FDA recomendó por unanimidad que las indicaciones para TRC se amplíen para incluir la insuficiencia cardiaca leve. Las nuevas indicaciones propuestas son: pacientes en clase funcional NYHA II (en pacientes isquémicos clase I), con FEVI < 30% y QRS > 130 ms. Otro requisito es que los pacientes elegibles tengan BRIHH.
Indicaciones del resincronizador
Han comenzado a implantarse en nuestro país electrodos de estimulación ventricular izquierda con cuatro electrodos, lo que permite programar diferentes configuraciones de estimulación, y reducir así umbrales y estimulación frénica (fig. 6).
Figura 6. Electrodo cuatripolar para estimulación ventricular izquierda que permite seleccionar múltiples sitios distintos y alejados entre sí, lo que nos proporciona mejores umbrales y menor estimulación frénica.
Existe una fuerte asociación entre un remodelado inverso y la evolución clínica. Por esto, la intervención precoz con TRC podría retrasar la progresión de la enfermedad. El estudio REVERSE incluyó a 610 pacientes, en su mayoría con NYHA II. Su objetivo, el porcentaje de pacientes que empeoraron, no fue significativamente diferente con resincronización o sin ella. Sin embargo, la TRC se asoció con una reducción significativa del volumen sistólico final. El subanálisis de los datos europeos de 262 pacientes seguidos durante 24 meses55 ofrece importantes perspectivas adicionales sobre el papel de la TRC en pacientes con síntomas leves de insuficiencia cardiaca. Como en el estudio principal, debían tener QRS > 120 ms y FEVI < 40%. Tras 24 meses, el 19% del TRC ON frente al 34% de los pacientes con TRC OFF empeoraron (p < 0,01). Por lo tanto, estos resultados proporcionan datos adicionales para apoyar el uso de la TRC en retrasar la progresión de la insuficiencia cardiaca. Como con cualquier subanálisis, existe la clara posibilidad de sobrestimar o subestimar el tamaño del efecto.
Fundamental fue la publicación del estudio MADIT-CRT54. En estos pacientes con indicación de desfibrilador para prevención primaria se aleatorizó la adición de resincronización, lo que redujo un tercio el riesgo de muerte o insuficiencia cardiaca, el objetivo primario, sobre todo por la reducción del 41% en el riesgo de insuficiencia cardiaca, independientemente de la etiología, isquémica o no isquémica. Este estudio proporcionó evidencia de que la TRC preventiva disminuye el riesgo de insuficiencia cardiaca en pacientes con síntomas mínimos, pero con un complejo QRS ancho. Un análisis de subgrupos preespecificados demostró que el beneficio de la TRC para el objetivo primario fue impulsado por la reducción del riesgo del 52% (p = 0,001) en pacientes con duración del QRS > 150 ms. También hubo una interacción significativa por sexo: las mujeres muestran mayor beneficio que los varones (p = 0,01).
Otro estudio demostró que la estimulación biventricular puede ser potencialmente útil para evitar los efectos deletéreos de la estimulación derecha. En un ensayo de Yu et al56, en 177 pacientes con indicación de marcapasos por disfunción sinusal o bloqueo auriculoventricular y FEVI > 45%, se implantó un marcapasos biventricular, y se los aleatorizó a estimulación derecha o biventricular. Después de 1 año, en sólo 1 paciente biventricular pero en 8 con estimulación derecha se redujo la FEVI por debajo del 45% (p = 0,02). Un patrón similar se observó para el volumen sistólico final ventricular izquierdo.
Implante, resultados y optimización del dispositivo de resincronización
En un análisis de seguimiento del estudio MADIT-CRT en 799 pacientes, la tasa de muerte o insuficiencia cardiaca-hospitalización aumentó significativamente en los pacientes con electrodo ventrícular izquierdo implantado cerca del vértice del corazón, en comparación con localizaciones medias o basales. La colocación apical del electrodo puede hacer que la resincronización sea menos eficaz.
Sitges et al57 estudiaron a 57 pacientes con regurgitación mitral funcional sometidos a TRC para identificar los mejores candidatos para el procedimiento; 30 pacientes respondieron clínicamente a la TRC. La reducción media de la insuficiencia mitral con TRC fue del 18% aguda y el 38% después de 12 meses.
Diversos ensayos clínicos han demostrado que aproximadamente 2/3 de los pacientes a los que se implanta un dispositivo con TRC responden favorablemente. Sin embargo, no es infrecuente observar una respuesta favorable mucho mayor en algunos casos, si bien las variables antes y tras el implante que puedan ser predictoras de dicha respuesta no son bien conocidas. Rickard et al58 observan que un 13,7% (32 pacientes) de un total de 233 sujetos de la cohorte retrospectiva son superrespondedores. Estos pacientes eran mayoritariamente mujeres, con bloqueo de rama izquierda, con menores volúmenes ventriculares izquierdos y menores valores de BNP preimplante. El análisis demuestra igualmente una tendencia a la asociación con miocardiopatía no isquémica, posiciones medioventriculares del electrodo ventrícular izquierdo y QRS estimulados más estrechos con la mejor respuesta. La mortalidad fue menor en el subgrupo de superrespondedores respecto al resto de la cohorte analizada (el 9,4 y el 43,2%) durante un seguimiento de más de 5 años.
La optimización de la programación de los retrasos VV y AV en TRC puede ser importante en algunos pacientes, pero requiere mucho tiempo y, en ocasiones, no se realiza habitualmente. El objetivo del estudio realizado por Tamborero et al59 fue comparar la respuesta hemodinámica aguda obtenida por diferentes métodos de programación VV. Demostraron que la consecución de los QRS más estrechos obtiene una respuesta hemodinámica adecuada, además de simplificada, por lo que se propone como alternativa.
SISTEMAS DE MONITORIZACIÓN
Monitorización remota
Uno de los temas motivo de múltiples comunicaciones este año es la monitorización remota de los dispositivos implantables. La monitorización remota permite a los pacientes transmitir datos desde la comodidad de sus hogares (fig. 7). Las ventajas de esta tecnología son evidentes y sin duda constituyen el futuro. Los datos obtenidos a través del monitor a distancia son fiables; además, el control remoto ha demostrado que disminuye la carga de tiempo del personal médico y de los pacientes.
Figura 7. Episodio de taquicardia ventricular interrumpido con un choque, como se mostraría en la pantalla de nuestro ordenador con el paciente en su domicilio, en un paciente con sistema de monitorización remota Care-Link .
Dispositivos implantables de monitorización
Este año han aparecido varias publicaciones relevantes en este campo. Una de ellas es un documento de EHRA sobre indicaciones para el uso de los sistemas diagnósticos implantables internos y externos60. En él se han recogido puntos clave, como tener en cuenta que la evaluación clínica completa, con frecuencia, permite establecer un mecanismo de síncope y que se debe excluir a aquellos con indicación clara de desfibrilador o marcapasos.
Los resultados de un estudio interesante, el Xpect61, también se publicaron este año. Se realizó un seguimiento prospectivo de 247 pacientes. De 206 registros Holter disponibles para el análisis, el 37% contenía por lo menos un episodio de FA. Basándose en estos hallazgos, el monitor implantable tenía una precisión total en el diagnóstico de FA del 98,5%. La monitorización continua y precisa del ritmo puede ayudar a descubrir las verdaderas incidencia y duración de los episodios sintomáticos y asintomáticos de FA y establecer un nuevo estándar para comparar la eficacia de diferentes estrategias de tratamiento.
CONFLICTO DE INTERESES
Los autores declaran no tener ningún conflicto de intereses.
Abreviaturas
FA: fibrilación auricular.
FAA: fármacos antiarrítmicos.
FEVI: fracción de eyección del ventrículo izquierdo.
TRC: terapia de resincronización cardiaca.
TV: taquicardia ventricular.
VP: venas pulmonares.
*Autor para correspondencia:
Sección de Electrofisiología y Arritmias, Cardiología, Hospital Ramón y Cajal, Ctra. de Colmenar Viejo, km 9,100, 28034 Madrid, España.
Correo electrónico:antoniomadri@gmail.com (A. Hernández-Madrid).