La insuficiencia tricuspídea (IT) de grado moderado a grave no es una valvulopatía infrecuente, y las formas moderadas o graves se dan en hasta un 4% de la población anciana1. Se ha identificado que estas formas clínicamente importantes de IT son un factor independiente predictivo de peor supervivencia a largo plazo1,2. Sin embargo, las opciones de tratamiento para estos pacientes son limitadas, ya que a lo largo de los años ha persistido una mortalidad quirúrgica elevada3,4. Dados estos resultados, del total de 1,6 millones de pacientes con IT de moderada a grave de Estados Unidos, cada año se trata con una intervención quirúrgica solo al 0,5%5. Para poder abordar esta amplia necesidad clínica insatisfecha, varios dispositivos percutáneos están actualmente en desarrollo o ya en fase de pruebas clínicas6.
La mayor parte de tales dispositivos se centran en reducir la dilatación del anillo o en reparar las valvas. Sin embargo, muchos de los pacientes identificados y remitidos actualmente al tratamiento no son aptos para estos abordajes, puesto que presentan un remodelado grave del ventrículo derecho, con una dilatación sustancial y un desplazamiento de los músculos papilares que causa una tensión en las valvas y una gran brecha de coaptación7. En presencia de estas características anatómicas extremas, los sistemas de modificación anular y reparación de las valvas tienen una eficacia limitada y pueden dar lugar a una insuficiencia residual importante. Para superar estas limitaciones técnicas, se están desarrollando sistemas percutáneos de reemplazo de la válvula tricúspide ortotópicos y heterotópicos, con objeto de ampliar el arsenal de soluciones técnicas y de intervención para tratar la IT grave en situaciones anatómicas extremas y difíciles.
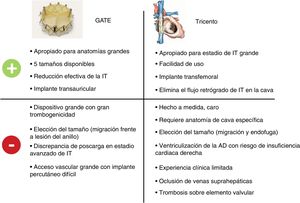
En 2 artículos recientes publicados en Revista Española de Cardiología, los autores presentan su experiencia más reciente con 2 dispositivos que son apropiados específicamente para tratar las fases más avanzadas de la IT con una anatomía alterada (figura 1).
Íñiguez-Romo et al.8 describen su experiencia con el dispositivo Tricento (TNV AG; Muri, Suiza), una bioprótesis valvular utilizada para tratar una IT masiva en una mujer de 81 años. De forma resumida, el dispositivo es una estructura de stent de nitinol cubierto con pericardio, que se extiende de la vena cava superior a la vena cava inferior (VCI) y lleva una válvula de pericardio porcino bicúspide lateral en su parte media, que permite el flujo hacia la aurícula derecha. El sistema Tricento sigue el concepto de implante de válvula cava (CAVI), cuyo objetivo es proteger los órganos vulnerables reduciendo al mínimo el flujo retrógrado de IT hacia el sistema venoso9. Además de la primera experiencia en el ser humano descrita por Toggweiler et al.10 y la reciente descripción de 2 casos adicionales (con un total de 18 intervenciones realizadas en todo el mundo), Íñiguez-Romo et al. presentan en la Revista el primer implante del dispositivo realizado con éxito en España, con un diseño de la intervención especialmente sencillo y unos resultados clínicos prometedores, que confirman que la intervención es segura y factible en los estadios avanzados de la IT11. Deben cumplirse unos criterios anatómicos específicos para permitir el implante, y es posible que esto limite un uso más amplio del dispositivo: el diámetro de la vena cava debe ser de entre 16 y 42mm y las conexiones de las venas suprahepáticas con la VCI deben estar a una distancia mínima de 1cm de la aurícula derecha. Además, el dispositivo debe hacerse a medida en un proceso de fabricación de 4 semanas, lo cual aumenta los costes y las limitaciones de uso en un contexto de tratamiento agudo. Al igual que ocurre con todas las intervenciones de CAVI, la posición heterotópica de la válvula da lugar a una ventriculización de la aurícula derecha que puede conducir a una disfunción progresiva del corazón derecho. Este es el motivo de que el uso de esta técnica solo pueda considerarse en contextos paliativos. Sin embargo, los resultados tanto clínicos como ecocardiográficos del dispositivo CAVI Tricento hasta 1 año son prometedores, lo cual hace necesaria una evaluación más amplia de esta técnica. Ahora, las perspectivas aportadas por Íñiguez-Romo et al. constituyen unos primeros pasos importantes para esclarecer mejor el potencial de este dispositivo.
Estévez-Loureiro et al.12 presentan su experiencia con el sistema GATE (NaviGate CSI; Lake Forest, Estados Unidos), una válvula autoexpandible para el reemplazo ortotópico de la válvula tricúspide. Los autores trataron a una mujer de 76 años con insuficiencia cardiaca derecha previa y una IT grave. El dispositivo consta de un stent de nitinol de forma cónica con dispositivos de fijación ventriculares para el anclaje y aletas auriculares cubiertas de un tejido de microfibra de poliéster para el sellado hermético. El stent tiene una válvula de pericardio equino de 3 valvas. En el caso presentado, el dispositivo se implantó empleando una vía de acceso transauricular a través del cuarto espacio intercostal. La vía transyugular se ha abandonado en gran parte debido al tamaño (42 Fr) del sistema de aplicación, que es algo antiguo. Los autores resaltan la viabilidad del implante en anatomías difíciles, con lo que se consigue una abolición persistente de la IT a los 3 meses de seguimiento. Los autores utilizaron un tamaño de la válvula implantada un 4% superior al anatómico, que facilitaba un anclaje estable sin causar mayor daño al anillo tricuspídeo. Durante la experiencia inicial con el dispositivo, se recomendó cierto grado de aumento del tamaño respecto al anatómico, pero posteriormente se prefirió el uso del tamaño nominal para reducir al mínimo el riesgo de causar daño al anillo tricuspídeo frágil; esto se consideró viable sin que aumentara la tasa de desplazamientos de la válvula a causa de la menor presión en el corazón derecho13. Sin embargo, recientemente se ha descrito un caso de migración de la válvula tras el implante del GATE, lo cual pone de relieve que aún no se han abordado plenamente los problemas relativos al tamaño óptimo de las válvulas percutáneas14. Otro problema actualmente comentado del reemplazo ortotópico en estos pacientes en un estadio avanzado es la posible discrepancia de poscarga tras la reducción absoluta de la IT, que finalmente pueda conducir a una insuficiencia cardiaca derecha aguda con agravamiento del estado clínico del paciente e insuficiencia cardiaca derecha fulminante. Así pues, el papel futuro del reemplazo en las fases avanzadas de la IT deberá ser evaluado con mayor detalle y, en este caso, tras 40 implantes realizados en todo el mundo, Estévez-Loureiro et al. aportan una perspectiva adicional de gran valor.
Debe felicitarse a los autores de ambos artículos no solo por aportar datos y experiencias adicionales en este campo novedoso, sino también por realizar con éxito estas intervenciones innovadoras y difíciles para ayudar a pacientes que las necesitan.
Hay varios problemas pendientes de abordar en el desarrollo de los dispositivos antes comentados y de otras técnicas de reemplazo en estudio:
Los dispositivos actuales son frecuentemente voluminosos y pesados, lo que hace necesario el uso de introductores y vainas de gran tamaño. Esta característica técnica puede provocar que haya un número no desdeñable de complicaciones vasculares; además, el perfil voluminoso de los dispositivos actuales puede ser propenso a un aumento de la trombogenicidad (que se agrava también por las presiones inferiores existentes en el lado derecho). Esto se complica como consecuencia de la necesidad de una anticoagulación agresiva que podría conducir a eventos hemorrágicos graves en estos pacientes frágiles.
La técnica de implante, en especial por lo que respecta al tamaño del dispositivo deberá perfeccionarse para alcanzar un equilibrio entre el riesgo de migración de la válvula y el riesgo de dañar el anillo tricuspídeo, al tiempo que se consigue un sellado suficiente de la prótesis. En una parte significativa de los pacientes hay también un cable de marcapasos venoso a través de la válvula tricúspide, y no se ha evaluado la viabilidad de un implante valvular en presencia de este cable. Dado que el aparato valvular tricuspídeo es significativamente más frágil que las estructuras valvulares del lado izquierdo del corazón y, puesto que las presiones son significativamente inferiores, apenas puede aprovecharse la experiencia obtenida en intervenciones de reemplazo de otras válvulas, y es necesario llevar a cabo el desarrollo desde el principio para esta nueva posición de implante. Además, el riesgo de bloqueo auriculoventricular requiere una evaluación más detallada.
En la actualidad, los pacientes remitidos para este tipo de tratamiento se encuentran a menudo en fases muy avanzadas de la IT, lo que ocasiona un deterioro de las estructuras anatómicas con cavidades ventriculares enormes y anillos dilatados. En estos pacientes, los dispositivos de reemplazo son con frecuencia la última opción. Sin embargo, es probable que estas técnicas den resultados aún mejores en anatomías más conservadas en fases más tempranas de la enfermedad. Además, el tratamiento con una válvula ortotópica o heterotópica para mitigar los síntomas de una insuficiencia ventricular derecha avanzada puede causar incluso una discrepancia aguda de la poscarga, que daría lugar a un mayor agravamiento de la función ventricular derecha.
En conclusión, es necesario un mayor desarrollo y la realización de pruebas clínicas, a lo cual contribuyen en gran manera los autores con la presentación de casos en esta publicación. También es necesario aumentar la concienciación de los profesionales de la asistencia sanitaria y de los pacientes respecto a las fases iniciales de la IT grave, con objeto de permitir un tratamiento en un momento cuidadosamente elegido con estos nuevos enfoques percutáneos prometedores.
CONFLICTO DE INTERESESA. Latib ha sido consultor de Medtronic y Abbott Vascular. Los demás autores no tienen nada que declarar.