La estenosis valvular aórtica severa degenerativa tiene mal pronóstico con tratamiento médico. Se ha demostrado que la cirugía de sustitución valvular es un tratamiento muy eficaz y seguro en los pacientes sometidos a él. Sin embargo, son muchos los pacientes que, por diferentes razones (edad, comorbilidades graves, riesgo quirúrgico excesivo, etc.), nunca llegan a ser operados. En estos pacientes se ha propuesto una terapia alternativa mediante la implantación transcatéter de prótesis valvular aórtica. Están disponibles dos modelos de prótesis transcatéter (Edwards y Medtronic CoreValve). El modelo Edwards se implanta por vía transfemoral y transapical; la Medtronic CoreValve ha tenido como vía de acceso la transfemoral con alguna experiencia por vía transapical. Con ambos modelos se han observado buenos resultados, progresivamente mejores, en registros individuales y multicéntricos. Los resultados pendientes del estudio aleatorizado PARTNER determinarán el verdadero papel de la prótesis transcatéter en diferentes contextos. Nuevos modelos (Direct Flow, Sadra Lotus, HLT) están en diferentes estadios de evaluación clínica, dispuestos a incrementar el arsenal de esta nueva tecnología que, sin duda, tendrá un impacto muy importante en el tratamiento de la estenosis valvular aórtica severa degenerativa.
La historia de la implantación transcatéter de prótesis valvulares cardiacas la inició H. Andersen en 1992 en un modelo porcino1. Bonhoffer2 implantó la primera válvula pulmonar en humanos en 2000. Estos dos investigadores habían comenzado la experiencia en la implantación transcatéter de prótesis valvulares creando un modelo de stent en cuyo interior habían cosido una válvula. La primera experiencia de implantación percutánea de prótesis valvular aórtica en humanos la realizó Cribier en 2002 por vía anterógrada, pasando por la válvula mitral después de una punción transeptal3.
NECESIDAD DE ESTA ESTRATEGIA TERAPÉUTICASe acepta que la estenosis aórtica severa es indicación de sustitución valvular mediante cirugía4. El pronóstico de los pacientes con estenosis aórtica sintomática con tratamiento médico es malo, y los tratamientos percutáneos existentes hasta ahora mediante valvuloplastia aórtica han mostrado un efecto beneficioso muy escaso en la mayoría de los casos5. Un número importante de pacientes con estenosis aórtica severa sintomática no son operados mediante sustitución valvular aórtica por comorbilidades graves que comportan un alto riesgo quirúrgico6,7.
La estenosis valvular aórtica es actualmente la enfermedad valvular más prevalente en el mundo occidental, con una incidencia por encima del 4% en personas mayores de 75 años, y esta incidencia aumentará con el incremento de la esperanza de vida. La cirugía de sustitución valvular aórtica tiene una mortalidad quirúrgica media de un 3-8%, pero puede ser mayor dependiendo de las comorbilidades y otras características del paciente y el centro8-10. Para ayudar a predecir el riesgo quirúrgico, se han desarrollado diferentes escalas; las más utilizadas son EuroSCORE y STS11,12. A pesar de los muy buenos resultados clínicos de la cirugía de sustitución valvular aórtica, en muchos pacientes muy añosos nunca se realiza cirugía de sustitución valvular aórtica debido al alto riesgo quirúrgico.
Una encuesta del Euro Heart demostró que no se opera al 33% de los pacientes con estenosis aórtica severa sintomática6. A este grupo de pacientes hay que añadir otro superior al 20% que tiene estenosis aórtica severa pero aún no sufre síntomas; cada día hay más evidencia de que estos pacientes tienen mejor pronóstico si se los opera13. El American College of Cardiology recomienda la cirugía de sustitución valvular aórtica para algunos pacientes asintomáticos con estenosis aórtica severa: los que tienen una respuesta anormal al esfuerzo, aquellos con signos de progresión rápida de la estenosis y los que tienen una estenosis severísima14.
Estos son algunos de los argumentos que demuestran la necesidad de la prótesis valvular aórtica transcatéter: pacientes con comorbilidades graves que contraindican o implican un altísimo riesgo para la cirugía de sustitución valvular aórtica y pacientes con estenosis aórtica muy severa aún asintomáticos y en los que se ha demostrado un mejor pronóstico cuando se sustituye la válvula estenosada.
En los años ochenta se intentó en estos pacientes el tratamiento percutáneo mediante valvuloplastia aórtica, pero se demostró que esta estrategia terapéutica, además de conllevar un riesgo no despreciable, tenía una alta tasa de reestenosis y no cambiaba el curso clínico de estos pacientes15-18. La implantación transcatéter de prótesis valvular aórtica aparece como una alternativa atractiva para el tratamiento de estos grupos de pacientes.
Como precedente a la implantación percutánea de prótesis valvular aórtica, apareció en los años ochenta la valvuloplastia, cuyo beneficio resultó ser insuficiente y poco duradero en la mayoría de los casos19. Actualmente las indicaciones de valvuloplastia aórtica percutánea serían las destinadas a pacientes en situación clínica desesperada, demasiado inestables para someterse a cirugía de sustitución o como puente a la implantación percutánea de prótesis valvular aórtica o cirugía de sustitución15. Por lo tanto, hay argumentos a favor de la implementación de la prótesis valvular aórtica percutánea con el objetivo de hacer llegar un tratamiento eficaz a los pacientes con estenosis aórtica severa sintomática y comorbilidad importante, que hacen que la cirugía de sustitución valvular aórtica esté contraindicada o sea de muy alto riesgo.
TECNOLOGÍAS ACTUALMENTE DISPONIBLESEn la actualidad se dispone, para utilización clínica en Europa, España y la mayor parte de los países del arco occidental, de dos modelos de prótesis valvular aórtica percutánea conceptualmente diferentes, pero con una misma finalidad funcional: a) la prótesis balón expandible de Edwards- SAPIEN, y b) la prótesis autoexpandible de Medtronic CoreValve.
La prótesis Edwards-SAPIEN ha pasado por diferentes modificaciones hasta llegar al modelo actualmente disponible para uso clínico: la prótesis Edwards-SAPIEN XT con el sistema de transporte y liberación XT. El primer modelo utilizado en humanos en 2002 (la prótesis de Cribier-Edwards) tenía un stent de acero inoxidable al que estaban cosidas tres valvas de pericardio equino. El tercio inferior del stent estaba cubierto con una falda que sellaba el anillo aórtico para evitar la regurgitación perivalvular3. Solamente estaba disponible en un tamaño (23mm) y las primeras implantaciones se realizaron por vía anterógrada después de una punción transeptal20.
El siguiente modelo, denominado Edwards- SAPIEN, introdujo algunas modificaciones: el stent seguía siendo de acero inoxidable, pero la falda tenía más extensión para reducir aún más el riesgo de regurgitación perivalvular. Las valvas estaban construidas de pericardio bovino y estaba disponible en dos tamaños (23 y 26mm). Webb introdujo la implantación por vía arterial retrógrada21 utilizando como dispositivo de transporte y liberación de la válvula el sistema Retroflex, con capacidad de modificar el ángulo de avance para facilitar el paso por el cayado aórtico y la introducción en el ventrículo izquierdo. Han aparecido dos modelos más del sistema Retroflex, que mejoran sus características y facilitan el transporte de la prótesis, sobre todo en el caso del Retroflex III. Para su implantación percutánea, estas válvulas requieren introductores de 22 Fr para la válvula de 23mm y 24 Fr para la de 26mm.
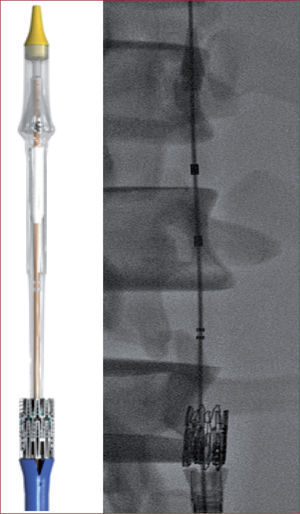
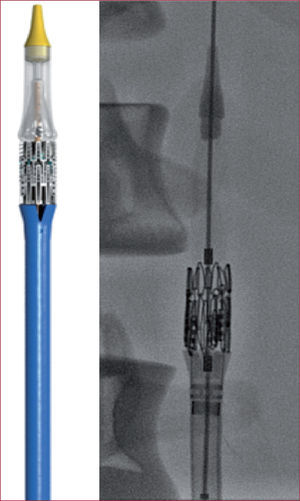
Recientemente ha aparecido un nuevo modelo, el Edwards-SAPIEN XT, que introduce importantes cambios en la prótesis valvular y el sistema de transporte y liberación. La válvula, además de pequeños cambios en el diseño de los struts, está construida en una nueva aleación de cromo y cobalto que permite reducir su perfil manteniendo sus características mecánicas. Sin embargo, los cambios más atractivos residen en el sistema de transporte y liberación denominado Novaflex que, utilizando una forma muy ingeniosa de montaje de la válvula proximal al balón (después de avanzarlo a la aorta descendente se monta en el balón), permite reducir el perfil para adaptarse a un introductor de 18 Fr para la válvula de 23mm y 19 Fr para la de 26mm (figs. 1 y 2).
La válvula autoexpandible Medtronic CoreValve está construida a partir de un tubo de aleación de níquel y titanio cortado con láser. Las características de esta aleación permiten que el stent pueda ser comprimido a baja temperatura e introducido en una vaina de bajo perfil, compatible con un introductor de 18 Fr. Una vez transportado al plano valvular aórtico y retirada la vaina compresora, el stent al que va unida la válvula adquiere su forma predeterminada. La válvula Medtronic Core es más larga y tiene una especial forma de embudo que favorece el anclaje de la parte más proximal en la aorta ascendente. Aunque los struts del stent valvular traspasan los ostium de las coronarias, la gran apertura entre struts no dificulta el flujo coronario. El perfil de esta válvula ha ido disminuyendo progresivamente, de 25 Fr en el modelo original, pasando por 21 Fr hasta llegar a los 18 Fr del modelo actual.
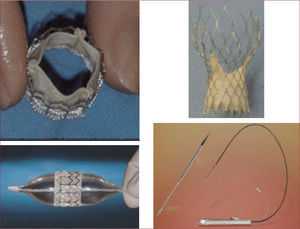
Los métodos de implantación de estas dos prótesis valvulares son bastante diferentes y han sido descritos previamente20,21 (fig. 3). Resumidamente, ambas prótesis requieren la valvuloplastia aórtica con balón para permitir el acceso de la prótesis al ventrículo izquierdo sin grandes dificultades. Para su definitiva implantación, la válvula Edwards- SAPIEN utiliza un balón que al inflarse impacta la prótesis en el plano valvular, mientras se sobrestimula el corazón a 180–220 lat/min para evitar el movimiento de la prótesis. La prótesis Edwards- SAPIEN se ha implantado por vía transfemoral y transapical.
En el caso de la Medtronic CoreValve, la retirada de la vaina que comprime el stent al que va unida la válvula permite implantarla sin utilizar sobrestimulación. La prótesis Medtronic CoreValve se ha implantado preferentemente por vía transfemoral. Se han practicado algunos accesos a través de la subclavia en pacientes con enfermedad importante del eje iliofemoral. Por su diseño y su concepción, esta prótesis no se ha implantado por vía transapical.
RESULTADOS CLÍNICOSPrótesis valvular con balón expandible (vía transfemoral)La primera experiencia en humanos la realizó Cribier en 2002 en Rouen, implantando una prótesis de Cribier-Edwards en un paciente con estenosis aórtica severa, edema pulmonar sin respuesta al tratamiento médico y graves comorbilidades que contraindicaban la sustitución valvular quirúrgica3. La prótesis valvular aórtica se implantó con éxito por vía anterógrada después de punción transeptal. La situación cardiaca del paciente mejoró espectacularmente, pero este sufrió múltiples complicaciones graves extracardiacas y falleció 17 semanas después de la implantación. La ecocardiografía demostró un funcionamiento normal de la prótesis, con excelente comportamiento hemodinámico.
Esta primera experiencia abrió las puertas a la exploración del comportamiento técnico y clínico en la implantación transcatéter de prótesis valvular aórtica. Las siguientes experiencias por vía anterógrada evidenciaron tres cosas: a) la dificultad técnica del procedimiento por vía anterógrada; b) el excelente comportamiento hemodinámico de la válvula, y c) la necesidad de explorar otra variante de esta técnica por vía retrógrada que simplifique el procedimiento20.
En 2006, Webb describió por primera vez la técnica de implantación de prótesis valvular aórtica por vía femoral retrógrada utilizando el sistema Retroflex en 18 pacientes. Se realizó con éxito en 14 pacientes y no hubo mortalidad durante el procedimiento. Se comprobó que el procedimiento era más adecuado que el que utilizaba la vía anterógrada, aunque se evidenciaron algunas dificultades a tener en cuenta: dificultad en las vías de acceso por el perfil grande de los introductores; dificultad en encontrar la referencia más adecuada para el posicionamiento y la implantación de la prótesis, y la existencia de regurgitación perivalvular tras la implantación, sobre todo cuando únicamente estaba disponible la válvula de 23mm21.
Un año después se comunicó la ampliación de esta experiencia en implantación de prótesis de Edwards por vía retrógrada en 50 pacientes con estenosis aórtica severa y alto riesgo para sustitución valvular quirúrgica. Se observó éxito de implantación de la prótesis en el 86% y una mortalidad intraprocedimiento del 2 y el 12% a los 30 días. La regurgitación perivalvular fue frecuente, pero ligera y bien tolerada clínicamente. Se observó una mejoría significativa en la función ventricular y la clase funcional. La mejoría funcional se mantuvo en el seguimiento al año y no se observó deterioro de la función de la prótesis. Se observó un aumento significativo del éxito del procedimiento y una disminución de la mortalidad en los últimos 25 casos respecto a los primeros 25.
Estas experiencias iniciales por vía retrógrada se consolidaron en estudios observacionales multicéntricos en Europa (REVIVE II) y Estados Unidos (REVIVAL), en los que se observó un éxito del procedimiento que se acerca al 90%, una disminución importante de las complicaciones vasculares y un excelente comportamiento hemodinámico de la prótesis.
A finales de 2007 se aprobó la válvula Edwards- SAPIEN para su uso comercial en Europa y otros países del arco occidental, excepto Estados Unidos, y se pusieron en marcha estudios observacionales de experiencia clínica (PARTNER EU y SOURCE). El estudio PARTNER EU recopiló en nueve centros europeos los resultados de 61 pacientes con estenosis aórtica severa y comorbilidades importantes cuyo EuroSCORE logístico era superior al 20%. La media de edad era 83±5 años y la del área valvular, 0,6±0,2cm2. El EuroSCORE fue 25%±11%. El éxito técnico del procedimiento (implantación de la prótesis con éxito con insuficiencia aórtica<2) fue del 91%. Las complicaciones más frecuentes fueron las vasculares (26%). A los 30 días, la mortalidad era del 8%; la incidencia de accidentes cerebrovasculares, del 3% y la implantación de marcapasos, menos del 2%. Al año, la supervivencia era del 78%; la supervivencia libre de accidentes cerebrovasculares, del 93% y la supervivencia libre de infarto, del 97%. Se observó una mejoría muy importante del gradiente transvalvular, el área valvular, la función ventricular y la clase funcional.
El SOURCE es un estudio observacional tras comercialización más amplio, en el que 34 centros europeos incluyeron a 463 pacientes con estenosis aórtica severa tratados por vía transfemoral y con graves comorbilidades que contraindicaban o hacían de alto riesgo el tratamiento quirúrgico. El éxito inmediato del procedimiento fue del 95,6%, no hubo ningún caso de embolización de la válvula, se observó mala aposición en el 1,7% de los casos; la oclusión coronaria ocurrió en el 0,7%; la insuficiencia aórtica>2, en el 3,2%, y la implantación de marcapasos, en el 6,7% de los pacientes. A los 30 días, la supervivencia era del 93,7%. Entre los pacientes con complicaciones vasculares, la supervivencia a los 30 días era del 88,6%22.
Prótesis expandible con balón. Acceso transapicalLicthtenstein et al informaron sobre la experiencia inicial en 7 pacientes con estenosis aórtica severa, graves comorbilidades y malos accesos vasculares. En estos 7 pacientes, la válvula se implantó a través de una mínima incisión en el hemitórax izquierdo a nivel del ápex y punción en el ápex del ventrículo izquierdo sin circulación extracorpórea. No hubo mortalidad durante el procedimiento23. A los 6 meses no se observó disfunción valvular24. Walther et al publicaron un año después su experiencia inicial en 30 pacientes. La válvula se pudo implantar con éxito en 29 y se tuvo que reconvertir a un paciente a sustitución valvular por esternotomía25. Se comprobó que había una vía alternativa eficaz a la vía transfemoral en pacientes con mal acceso vascular. Este mismo autor recogió la experiencia de 4 centros que trataron a 59 pacientes con un EuroSCORE medio de 24%±14% a los que se intentó implantar una prótesis Edwards-SAPIEN. Se pudo implantar la prótesis por vía transapical en 53 pacientes y en 4, por esternotomía. Fallecieron 8 pacientes (13,6%) en el hospital y no se observó disfunción de la prótesis26.
Fuera de Europa, se recogió la experiencia de cuatro centros americanos en la implantación transapical de la válvula Edwards-SAPIEN. Se intentó la implantación transapical en 40 pacientes y se consiguió en 35. La mortalidad a los 30 días era del 17,5%. En un seguimiento medio de 143 días, 6 pacientes más fallecieron y las curvas de Kaplan- Meier aportan una supervivencia del 81,8%±6,2% a 1 mes y el 71,7%±7,7% a los 3 meses27.
En el registro PARTNER EU, se incluyó a 69 pacientes con estenosis aórtica severa sintomática y graves comorbilidades, con acceso vascular pobre y alto riesgo quirúrgico (EuroSCORE medio, 33,8%±14,7%). El éxito técnico del dispositivo fue del 91%. A los 30 días la mortalidad era del 18,8%; la incidencia de accidente cerebrovascular, del 2,9%; la necesidad de cirugía urgente, del 2,9%, y la de implantación de marcapasos permanente, del 4,4%. La supervivencia a 1 año fue del 50%. Hubo una mejoría importante de la clase funcional en la mayoría de los pacientes.
En el registro SOURCE se han evaluado los resultados de 575 pacientes con estenosis aórtica severa con un EuroSCORE medio del 29,2% a los que se implantó una prótesis valvular Edwards-SAPIEN por vía transapical. El éxito del procedimiento fue del 92,8%. Hubo una conversión a cirugía convencional en el 3,5% de los pacientes, insuficiencia aórtica severa en el 5,9% y mala aposición valvular en el 1,4%. A los 30 días la mortalidad era del 10,3%; la incidencia de accidente cerebrovascular, del 2,9% y se había implantado marcapasos permanente al 7,3%22.
Registro Edwards de implantación transfemoral en EspañaSe han analizado de forma retrospectiva los resultados de 212 pacientes tratados en 11 centros españoles (anexo) mediante implantación transfemoral de prótesis valvular balón expandible (Edwards-SAPIEN). La media de edad era 81±2,6 años; el EuroSCORE, del 20,6%±12,5%; el 37% tenía enfermedad coronaria asociada y el 17%, enfermedad mitral. En el 65% de los pacientes se accedió a través de exposición quirúrgica de la arteria femoral y en el resto, por acceso percutáneo.
Centros participantes en el Registro transfemoral de prótesis de Edwards
| Hospital Clínico San Carlos (Eulogio García, Rosana Hernández) | Madrid | 43 |
| Policlínica Guipúzcoa (Mariano Larman) | San Sebastián | 34 |
| Hospital Virgen de la Arraixaca (Mariano Valdés) | Murcia | 32 |
| Complexo Hospitalario Universitario de A Coruña (Nicolás Vázquez) | A Coruña | 28 |
| Hospital Vall d'Hebron (Juan Ángel, Bruno García) | Barcelona | 15 |
| Hospital La Paz (Raúl Moreno) | Madrid | 14 |
| Hospital Meixoeiro (Andrés Iñiguez) | Vigo | 13 |
El éxito del procedimiento fue del 90%. En el 1% hubo migración de la prótesis; en otro 1%, oclusión coronaria; en el 5%, regurgitación aórtica>2; en el 5%, implantación de marcapasos permanente, y en el 3%, accidente cerebrovascular. Un 10% de los pacientes en los que se intentó la implantación fallecieron en el hospital. Después de un seguimiento medio de 240±203 días, se observó una mortalidad cardiaca del 8%.
Prótesis valvular autoexpandibleLos resultados de la prótesis valvular aórtica autoexpandible (Medtronic CoreValve) han ido evolucionando con los diferentes modelos aparecidos, que requerían la utilización de introductores con perfiles de 25, 21 y 18 Fr, respectivamente. Con el modelo de 25 Fr se trató únicamente a 10 pacientes y la mortalidad a 30 días fue del 40%28. Los resultados mejoraron espectacularmente con los dispositivos de 21 y 18 Fr. En un informe de 86 pacientes, 20 tratados con dispositivo de 21 Fr y 36 con el de 18 Fr, el éxito medio del dispositivo fue del 88% y el del procedimiento, del 78%. La mortalidad en el procedimiento fue del 6% y a los 30 días se incrementó al 12%. Combinando los eventos adversos de muerte, infarto de miocardio y accidente cerebrovascular, la incidencia alcanzó el 22% al mes de seguimiento29.
Posteriormente se ha comunicado la experiencia de un solo centro (Hatrtzentrum Seigburg) con la prótesis Medtronic CoreValve en 450 pacientes. El EuroSCORE logístico era superior al 20% en el 90% de los pacientes. La mortalidad ha ido disminuyendo paulatinamente hasta una media del 5% en los últimos 2 años. El resto de las complicaciones intrahospitalarias también disminuyó, excepto la necesidad de implantación de marcapasos, que se ha estabilizado en el 39%; la mortalidad a los 30 días de los últimos 2 años ha sido del 6% y la incidencia de accidente cerebrovascular, del 1,6%. La supervivencia al año ha sido del 60% con el dispositivo de 25 Fr, del 79% con el de 21 Fr y del 84% con el de 18 Fr.
NOVEDADES Y PERSPECTIVAS TECNOLÓGICASEdwards-SAPIEN XT y sistema de liberación NovaflexRecientemente se ha comercializado un nuevo modelo (Edwards-SAPIEN XT) con un nuevo sistema de liberación (Novaflex) que ha reducido el perfil necesario para el acceso transfemoral a 18 Fr para la válvula de 23mm y 19 Fr para la válvula de 26mm.
En los primeros 32 pacientes en los que hemos tenido la oportunidad de utilizar esta nueva válvula, el éxito del dispositivo ha sido del 100%; la mortalidad hospitalaria, del 3%; los accidentes cerebrovasculares, el 3%; hubo un 9% de complicaciones vasculares que requirieron cirugía o transfusión (2/3 debido a un mal funcionamiento del dispositivo percutáneo de cierre vascular). Aún es pronto para ofrecer datos concluyentes de las ventajas que este nuevo modelo tiene respecto al anterior, pero las primeras observaciones son muy prometedoras. La válvula Edwards-SAPIEN XT con el sistema de liberación Novaflex permite el acceso y el cierre transfemoral totalmente percutáneo en un porcentaje muy importante (probablemente superior al 80%) de los pacientes tributarios de implantación de prótesis valvular aórtica transcatéter.
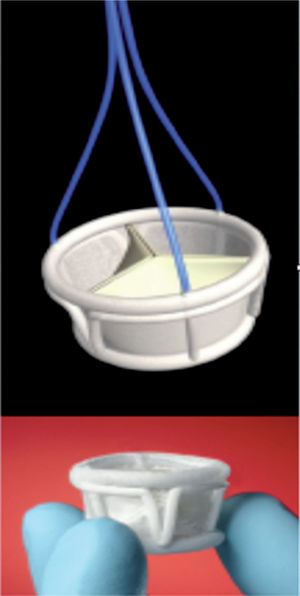
Direct FlowEsta prótesis valvular aórtica para implantación transcatéter se encuentra en periodo de evaluación clínica. Es una prótesis sin soporte metálico. Las valvas están elaboradas a partir de pericardio bovino con tratamiento contra la calcificación. El soporte se construye in situ rellenando con un polímero dos anillos que fijan la prótesis al anillo valvular aórtico (fig. 4). Existen dos tamaños, de 23 y 25mm. Se ha evaluado en 31 pacientes en la Universidad de Hamburgo y en el Helios Hartzentrum, en Seigburg. Se intentó la implantación transfemoral en 31 pacientes y se consiguió en 22, aunque solamente 18 fueron dados de alta con la prótesis implantada. A los 30 días, 4 pacientes más fallecieron. Actualmente, la prótesis está en periodo de rediseño para tratar de incrementar su fuerza radial.
Sadra LotusEsta prótesis está diseñada para una implantación fácil y predecible, y es autocentrable y recuperable. Está construida de pericardio bovino con un mecanismo de liberación todavía muy complejo; se ha evaluado en un número de pacientes pequeño y actualmente se está a la búsqueda de un mecanismo de liberación de la prótesis más sencillo y seguro (fig. 5).
Otras tecnologías que se encuentran en evaluación preclínica o en el inicio de la evaluación clínica son: Sorin Perceval, 3F Endurance Valve, LPI Repositionable, Lutter Valve, Heart leaflet Technologies, Aortech y Aortx valves.
PERSPECTIVAS CLÍNICASLas indicaciones actualmente aceptadas para la implantación transcatéter de una prótesis valvular aórtica incluyen a pacientes con estenosis aórtica severa sintomática degenerativa que no son candidatos para sustitución valvular quirúrgica o tienen un riesgo quirúrgico excesivo, establecido en los límites de un EuroSCORE logístico del 20%. ¿Cómo se ha llegado a este punto de corte? Van Gelrdop et al, en un artículo aparecido en 2009, analizaron en un grupo de 179 pacientes con estenosis aórtica sintomática las razones en las que se basaba la elección de tratamiento: cirugía convencional, implantación transcatéter o tratamiento médico conservador. El 46% de los pacientes recibió tratamiento quirúrgico o transcatéter y el 54%, tratamiento médico conservador. Las razones para el tratamiento médico fueron: riesgo estimado excesivo (34%); estimación de la gravedad de los síntomas ligera o moderada (33%); preferencia del paciente (19%); periodo de evaluación de la gravedad (5%), otras razones no aclaradas. A los 2 años de seguimiento, la supervivencia era del 90% en el grupo de implantación de prótesis por vía quirúrgica o transcatéter y el 69% en el grupo de tratamiento médico conservador30.
En el próximo congreso Transcateter Cardiovascular Terapeutics (TCT), que se celebrará en Washington en septiembre de 2010, se presentarán los resultados de un brazo del estudio PARTNER en el que se comparan los resultados de pacientes con estenosis aórtica severa sintomática no tributarios de reemplazo valvular aórtico convencional que fueron aleatorizados a tratamiento médico (incluida valvuloplastia aórtica con balón) o a implantación percutánea de prótesis aórtica. Los resultados de este estudio, incluido el análisis de costes, determinarán el papel de la implantación percutánea de prótesis valvular aórtica en pacientes no tributarios de sustitución valvular aórtica quirúrgica convencional.
El estudio PARTNER tiene otros tres brazos en los que se compararán los resultados de pacientes con estenosis aórtica severa y alto riesgo quirúrgico que serán aleatorizados a sustitución valvular quirúrgica convencional, implantación valvular por vía transapical o implantación valvular por vía transfemoral. El reclutamiento de los pacientes ya ha finalizado y pronto sabremos cuál es el tratamiento de elección en el grupo de pacientes con estenosis aórtica severa y alto riesgo quirúrgico. Mientras tanto, ya se han implantado más de 12.000 válvulas transcatéter y los resultados clínicos mejoran cada día.
Superada una primera etapa en la que los dispositivos eran obviamente mejorables y los pacientes elegidos tenían altísimo riesgo («dispositivos de primera generación para tratar a pacientes de última generación»), las mejoras tecnológicas y en la selección de pacientes están haciendo el procedimiento de implantación de prótesis valvular aórtica transcatéter más predecible y con mejores resultados inmediatos. Es importante analizar cuidadosamente los resultados de esta técnica, separando claramente los atribuibles a la técnica y el funcionamiento de la válvula de los inherentes a las comorbilidades de estos pacientes en alto riesgo31.
¿Qué factores determinarán la posibilidad de mover la indicación de esta tecnología a pacientes de menor riesgo? En primer lugar, la consolidación de buenos resultados inmediatos y la constatación de la durabilidad de al menos 10 años. Es importante también continuar por el camino de la mejora tecnológica que facilite el procedimiento y lo haga más predecible, con una previsión de éxito inmediato superior al 95% sin complicaciones vasculares importantes ni alteración grave del sistema de conducción.
CONCLUSIONESEn resumen, estamos ante una tecnología y una estrategia terapéutica que, desde la primera experiencia publicada en nuestro país realizada hace 2 años, se han ido consolidando por vía transfemoral y transapical, y experiencias aisladas por vía subclavia con las dos tecnologías comercializadas actualmente (balón expandible Edwards-SAPIEN y autoexpandible Medtronic Core) y alguna experiencia, como tratamiento de prótesis biológica disfuncional, hasta alcanzar una cifra de implantes que se acerca al millar32-36.
Las indicaciones clínicas actuales están dirigidas a los pacientes con estenosis aórtica severa sintomática que no son candidatos para cirugía convencional o tienen alto riesgo quirúrgico. Los resultados inmediatos y a medio plazo están mejorando constantemente. Conviene analizar los resultados a largo plazo teniendo en cuenta las comorbilidades que acompañan a estos pacientes. El futuro del espectro de esta tecnología dependerá de la consolidación de los resultados, la constatación de la durabilidad y la mejora tecnológica y la confirmación de estudios recientes que indican un mejor pronóstico en pacientes con estenosis aórtica muy severa cuando se recambia la válvula mientras aún están asintomáticos37.
CONFLICTO DE INTERESESLos autores declaran no tener ningún conflicto de intereses.