Palabras clave
INTRODUCCIÓN
Desde que en 1979 se utilizó por primera vez la ecocardiografía de estrés (EE) para inducir isquemia1, su utilización en la práctica clínica ha ido en constante aumento y en la actualidad está claramente establecido su papel en el diagnóstico y la evaluación de la cardiopatía isquémica.
Sin embargo, los estudios que evalúan la seguridad de la técnica aún son escasos y con resultados bastante discordantes2-5. Incluso muchas de las publicaciones iniciales acerca de la seguridad de la técnica pueden no ser aplicables en la actualidad6 pues, por un lado, los pacientes explorados hoy por la ecocardiografía de estrés son mucho más complejos que antes, al haberse expandido las indicaciones desde la búsqueda inicial de la isquemia a la valoración de viabilidad miocárdica en pacientes con mala función ventricular o identificación del territorio isquémico en pacientes con enfermedad multivaso revascularizados. Por otro lado, los protocolos actuales son más agresivos que los inicialmente descritos, y se desconoce la influencia que estos cambios pueden haber tenido en la seguridad de la técnica (protocolos mixtos, dosis altas de dobutamina, administración de atropina y, sobre todo, nuevos criterios de interrupción de la prueba).
Finalmente, es cuestionable si los resultados acerca de la seguridad de una serie de un centro con gran experiencia pueden ser extrapolados a la actividad cotidiana de centros más pequeños y con una actividad más limitada. Es probable que muchas complicaciones no se publiquen por diversos sesgos que posiblemente se acumulen en los centros con menor experiencia en la EE y/o en las técnicas de publicación.
En nuestro medio no tenemos datos publicados acerca de la seguridad de la EE, por lo que diseñamos este registro retrospectivo con la experiencia de 29 centros con la finalidad de conocer la experiencia y seguridad de la técnica en nuestro medio.
MÉTODOS
En el marco del estudio multicéntrico europeo Stress Echo Horror Poll se recogieron los datos de 29 hospitales de la península Ibérica, 23 españoles y 6 portugueses, que participaron en el estudio (tabla 1).
El cuestionario fue enviado a los 32 hospitales españoles que, en una encuesta previa practicada por la Sección de Ecocardiografía y otras técnicas de la Imagen, habían comunicado que practicaban EE. De los 32 centros, completaron el cuestionario 23 (72%), otros cuatro (12%) respondieron que no practicaban EE, y cinco (16%) no contestaron. A estos centros españoles se adhirieron 6 hospitales portugueses.
Se recogieron los datos de toda la actividad de ecocardiografía de estrés de los hospitales, desde su inicio en la práctica de EE hasta septiembre de 1999, fecha de terminación de la encuesta.
Hasta esa fecha, estos hospitales habían realizado 22.105 exploraciones: 10.975 ecocardiografías de estrés con ejercicio sobre tapiz rodante (EEE), 2.969 ecocardiografías de estrés con dobutamina a dosis bajas (<= 10 µg/kg/min) (EEDb), 6.832 ecocardiografias con dobutamina a dosis altas (EEDa), 1.276 ecocardiografias de estrés con dipiridamol (EEDp), 41 ecocardiografías de estrés con «estimulación» y 12 con adenosina.
En cada cuestionario, además de solicitar datos acerca de la actividad general de la EE, se pedían diversos datos de la historia clínica de los pacientes que habían presentado complicaciones: edad, sexo, antecedentes clínicos, electrocardiograma basal, movimiento parietal en la ecocardiografía basal, terapia antiisquémica durante el test, modalidad de ecocardiograma de estrés, tipo de complicaciones y tratamiento de las mismas.
Únicamente se contabilizaron las complicaciones graves, con peligro potencial de muerte o que precisaron posterior hospitalización. Se definieron como taquicardia ventricular sostenida las rachas de taquicardia ventricular de más de 30 latidos.
El análisis estadístico se realizó mediante un estudio descriptivo de las variables analizadas. Las variables cuantitativas continuas se expresan como media y desviación estándar; las variables cualitativas como número de casos y el porcentaje respecto al total. El cálculo de los percentiles se realizó con el método de Haverage.
RESULTADOS
Características de los centros
De los 29 hospitales, todos los centros practican EED, pero sólo 17 (59%) realizan EEE y 11 (38%) EEDp. Como actividad principal, 21 centros realizan EED (72%), 8 (28%) EEE y ninguno la EEDp.
Hasta el momento de responder a la encuesta, la media del número total de EE realizadas por centro era de 762, y la mediana de 356. Cuatro centros habían realizado menos de 200 EE, once de 200 a 400, seis de 400 a 600 y otros ocho más de 600.
Si valoramos la actividad por año (número de EE por año) observamos que la media era de 199, y la mediana, de 123 EE realizadas por centro y año. Si dividimos a los centros según el número de exploraciones anuales aconsejadas por la Sección de Ecocardiografía y otras técnicas de la Imagen7 para adquirir la formación y mantener la acreditación en la práctica de EE, observamos que se realizan más de 200 EE al año sólo en 9 centros, y más de 400 EE sólo en cuatro.
En cuanto al tiempo de experiencia en la práctica de EE de los centros que aportaron sus datos, en 6 centros era de un año, en cinco de 2 años, en otros cinco de 3 años y en 13 de más de 3 años.
Complicaciones
Se registraron 26 complicaciones graves (tabla 2). La única complicación mortal fue debida a una fibrilación ventricular no reanimada a pesar de las maniobras habituales.
Entre los 9.801 EED aparecieron 21 complicaciones (0,21%, una complicación seria por cada 466 exploraciones): 14 arritmias (9 taquicardias ventriculares sostenidas, 3 fibrilaciones ventriculares, una de las cuales fue la que terminó en muerte y 2 bloqueos auriculoventriculares completos), 4 infartos agudos de miocardio, una rotura ventricular, un accidente isquémico transitorio y una hipotensión severa sintomática. Todas las complicaciones aparecieron con la dobutamina a dosis altas, siendo el porcentaje total de complicaciones entre las 6.832 EEDa de un 0,30%, el de arritmias graves de un 0,21% y el de infarto de un 0,04%.
Entre las 10.975 EEE aparecieron cuatro complicaciones (0,03%, una por cada 2.743 exploraciones): 2 arritmias (una fibrilación ventricular y una taquicardia ventricular sostenida), un infarto agudo de miocardio y una rotura ventricular.
Entre los 1.231 EEDp sólo apareció una única complicación (0,08%), que fue un infarto agudo de miocardio.
Cuando analizamos los datos clínicos observamos que, salvo un IAM en una mujer, las 25 complicaciones restantes (96%) aparecieron en varones. Trece de las complicaciones aparecieron en pacientes ingresados y 12 en enfermos ambulatorios (en otro caso se desconoce), aunque al ignorar el número total de pruebas realizadas en cada situación no podemos llevar a cabo un análisis estadístico. En cuanto a sus antecedentes cardiológicos, 16 habían tenido un infarto agudo de miocardio (siete reciente, nueve crónico), ocho tenían angina y dos, dolor torácico atípico. El electrocardiograma basal era normal en 7 casos y anormal en 19 (ondas «q» en 14, alteraciones ST en tres, bloqueo rama izquierda en dos). El ecocardiograma basal era normal en 18 casos (69%) y existían anomalías segmentarias de la contractilidad en los otros 8 casos (31%).
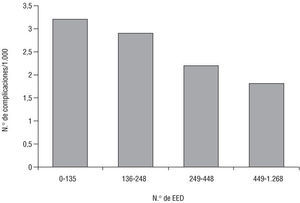
En relación con la terapia farmacológica durante la realización del ecocardiograma de estrés, 14 pacientes recibían medicación (dos con bloqueadores beta, ocho con antagonistas del calcio y 13 con nitratos) y nueve no tomaban ningún medicamento; en 3 casos este dato se desconocía. Cuando analizamos la relación entre la experiencia (número de ecos practicadas) y la frecuencia de complicaciones, dividiendo a los centros en cuartiles según el número de EED practicadas, observamos una clara tendencia a la disminución del número de complicaciones con el incremento de actividad (fig. 1).
Fig. 1. Tasa de complicaciones por cada 1.000 EED practicadas, según la actividad de los centros (divididos en cuartiles según nú-mero de exploraciones realizadas).
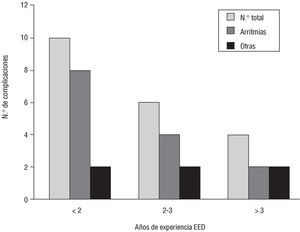
Cuando analizamos el tiempo transcurrido entre el inicio en la actividad en EEE y la aparición de las 20 complicaciones presentadas durante la EED en las que conocemos este intervalo, observamos que 10 (50%) complicaciones se presentaron con menos de 2 años de experiencia, siendo las arritmias las únicas complicaciones que tuvieron una evidente distribución temporal, pues el 57% (8 de 14) tuvieron lugar en los primeros 2 años (fig. 2).
Fig. 2. Número total de complicaciones, arritmias y «otras complicaciones» no arrítmicas según los años de experiencia en ecocardiografía de estrés con dobutamina.
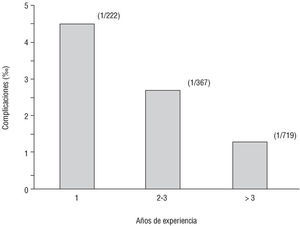
La frecuencia de complicaciones con la EED en relación con el tiempo de actividad fue de una por cada 222 exploraciones en los centros con un año de experiencia (4,5‰), mientras que en los centros con 2-3 años y más de 3 años se presentaron cada 367 (2,7‰) y 719 (1,3‰) exploraciones (fig. 3).
Fig. 3. Tasa de complicaciones por cada 1.000 exploraciones según los años de experiencia. Entre paréntesis, número de pruebas realizadas por cada complicación.
La tasa de complicaciones en la EED en relación con el tiempo de actividad fue del 4,5‰ en los centros con un año de experiencia (una complicación por cada 222 exploraciones), mientras que en los centros con 2-3 años y más de 3 años fue del 2,7‰ y del 1,3% (una complicación cada 367 y 719 exploraciones, respectivamente) (fig. 3).
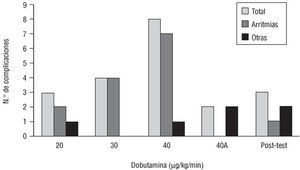
La relación entre la dosis de dobutamina y el número de complicaciones queda reflejada en la figura 4. Después de terminar el test se produjeron 3 complicaciones: una fibrilación ventricular, un infarto agudo de miocardio y un accidente cerebrovascular.
Fig. 4. Relación del número total de complicaciones, arritmias y otras complicaciones no arrítmicas con la dosis de dobutamina.
DISCUSIÓN
En nuestro conocimiento, éste es el primer estudio que se publica en España acerca de la seguridad de la ecocardiografía transtorácica de estrés, pues únicamente se han publicado datos aislados relativos a las complicaciones de la ecocardiografía transesofágica de estrés8. Se han recogido las 26 complicaciones serias que se han presentado en 22.105 ecocardiogramas de estrés realizados en 29 hospitales de la Península Ibérica.
En comparación con otros estudios publicados en lengua anglosajona, tiene algunas características diferenciales: es el más amplio, recoge el mayor número de exploraciones y complicaciones, abarca todas las variedades del eco de estrés, está realizado sobre una muestra no seleccionada (incluye todo tipo de pacientes e indicaciones) y es multicéntrico, ya que recoge la experiencia de muchos centros con relativa baja actividad (mucho más representativa de la realidad de nuestro medio que las amplias series de un único centro).
Así, Secknus6 aporta datos acerca de 3.011 exploraciones, Mertes2 de 1.118, Poldermans3 de 1.734, Mathias4 de 4.033, Geleijnse9 de 102, Cornel10 de 318, Smart11 de 232, Hiro12, en un estudio también retrospectivo, aporta datos de 732 pacientes, y Picano13 en uno multicéntrico en el que colaboran 24 centros aporta datos de 2.949. El registro italiano Test-Eco-Dobutamina14, en un estudio similar al nuestro, aporta datos de 3.041 exploraciones realizadas en 63 centros. Nuestro estudio, con 22.105 exploraciones es, por tanto, el más amplio de los publicados hasta el momento.
Dado que es un estudio retrospectivo, creímos oportuno recoger sólo las complicaciones severas (presentes en las bases de datos de todos los centros colaboradores), más fáciles de tabular en un estudio de estas características.
Analizaremos las complicaciones de la ecocardiografía de estrés según la modalidad empleada.
En cuanto al EEE, no hay estudios acerca de su seguridad, pues siempre se ha asumido que la tasa de complicaciones debería ser similar a la de la ergometría convencional. Así ha ocurrido en nuestro estudio, pues se presentaron cuatro complicaciones graves (1/2.743 exploraciones), lo que, en efecto, supone una frecuencia similar a la ya relatada para la ergometría (una muerte y cinco complicaciones serias por cada 10.000 exploraciones)15.
En cuanto a la EED, tiene una importancia crucial destacar que no encontramos ninguna complicación entre las 2.969 EEDb realizadas con dosis bajas (<= 10 µg/kg/min) para la valoración de viabilidad. Creemos que este hecho debería aumentar nuestra tranquilidad cuando sentamos la indicación de una EEDb para valorar la viabilidad miocárdica en un paciente isquémico con mala función ventricular.
Sin embargo, entre los 6.832 EEDa encontramos 21 complicaciones (0,31%), es decir, una complicación por cada 325 exploraciones. Esta cifra es similar a la de Secknus (1/300)6, ligeramente superior a la de Mathias (1/400)4, e inferior a la de Picano (1/210)13. Nuestros resultados, como los de otros autores, sólo difieren sustancialmente de los de Poldermans3, en el sentido de que éste presenta un considerable mayor número de complicaciones (1/80). Esto puede ser debido a la mayor agresividad de su protocolo, pues sólo interrumpe la EEDa si las alteraciones de la contractilidad son extensas y severas.
Si bien se ha descrito ya un fallecimiento durante una EEDp debido a una hipotensión severa16, nuestro estudio aporta el conocimiento de la primera complicación mortal publicada como consecuencia de una EED. Se trataba de un varón de 76 años, con antecedentes de un infarto de miocardio 15 días antes, en el que se practicó una EEDa para estratificación de riesgo, realizándose el test sin interrumpir la medicación con nitratos y bloqueadores beta. Cuando estaba con la dosis de 20 µg/kg/min presentó una fibrilación ventricular con posterior asistolia que no obedeció a las maniobras habituales de reanimación.
Por otro lado, hay que tener en cuenta que las dos roturas ventriculares no acabaron en fallecimiento probablemente debido a que ocurrieron en centros con servicio de cirugía cardíaca, a la que fueron sometidos con carácter inmediato. Sin embargo, en un metaanálisis de 28 centros17 que abarcó 2.246 exploraciones no se describió tampoco ninguna muerte.
Las arritmias fueron las complicaciones más frecuentes durante la EED (0,21%). Durante la EEDa se presentaron 3 fibrilaciones ventriculares (0,04%) y 9 taquicardias ventriculares sostenidas (0,13%), proporciones similares a las descritas con anterioridad. Así, el porcentaje de fibrilación ventricular se sitúa entre el 0,02 de Mathias4 y el 0,07 de Picano13, y es sensiblemente menor que el 0,17 de Poldermans3 debido probablemente a la mayor agresividad de su protocolo, que sólo interrumpe el ecocardiograma si las alteraciones segmentarias de la contractilidad son severas y extensas. En cuanto a las taquicardias ventriculares sostenidas, nuestro porcentaje se encuentra también en la línea de las diversas publicaciones: 0,10% de Picano13, 0,19% de Mathias4 y lejos del 0,7% de Poldermans3.
Mucho se ha especulado a propósito de la etiopatogenia de las arritmias graves durante la EED. Parece existir acuerdo acerca de la ausencia de predictores clínicos, salvo la misma existencia previa de arritmias5. Ni la presencia de anomalías segmentarias en la contractilidad, la función ventricular basal, la inducción de isquemia (aparición de nuevas anomalías segmentarias en la contractilidad) y la adición de atropina se han podido relacionar de manera independiente con la inducción de arritmias. En algunos estudios, la mala función ventricular se había asociado con la inducción de arritmias18, pero ha quedado claro en los análisis multivariantes10 que la mala función ventricular se relaciona con las arritmias únicamente en el sentido de ser un buen marcador de la existencia previa de arritmias. Algunos autores han encontrado una asociación entre la presencia de arritmias y el sexo masculino18. En nuestro caso, aunque desconocemos el porcentaje de pruebas realizadas en varones y mujeres, es de destacar que todas las arritmias se presentaron en varones.
Sorprendentemente, en la mayoría de los estudios tampoco se ha encontrado relación entre las arritmias y la dosis de dobutamina administrada, a pesar de que se ha relacionado la inducción de las arritmias con el efecto estimulante β o la inducción de hipopotasemia plasmática, hechos que deberían ser más intensos con una dosis más elevada de fármaco administrada.
Sin embargo, de nuestro estudio parece inferirse una cierta relación entre la dosis de dobutamina y la presencia de arritmias, pues el número de arritmias aumentó con la dosis de dobutamina a pesar de que, necesariamente, el número de pacientes que alcanzaron la dosis máxima debería ser menor (interrupción a dosis inferiores por isquemia, otros efectos secundarios, etc.). Por desgracia no se pueden extraer conclusiones, pues únicamente conocemos la dosis de dobutamina administrada en los casos de las complicaciones, y no el porcentaje de pacientes que recibieron cada dosis, por lo que no podemos realizar un análisis estadístico.
Aunque se han publicado bloqueos auriculoventriculares transitorios de primer y segundo grado durante la EED2,19, nunca habían sido comunicados bloqueos auriculoventriculares completos. La presencia de bloqueos auriculoventriculares transitorios de II grado ha sido atribuida fundamentalmente a la inducción de isquemia, aunque no se pueden descartar mecanismos accesorios vagales a través del reflejo de Bezold-Jarisch.
En nuestro estudio, uno se presentó en un varón de 62 años con sospecha de angina, electrocardiograma basal normal, en tratamiento con antagonistas del calcio y nitratos (no interrumpidos durante el test), y que a dosis de 40 µg/kg/min presentó un bloqueo auriculoventricular completo transitorio junto con una respuesta isquémica positiva, precisando atropina y bloqueadores beta. El otro tuvo lugar en un varón de 75 años, con dolor torácico atípico y electrocardiograma basal anormal (con anomalías del ST-T), sin tratamiento, y que a dosis de 40 µg/kg/min de dobutamina presentó un bloqueo completo que cedió con atropina.
En el caso de infarto de miocardio, se presentaron seis: cuatro con EED, uno con EEE y otro con EEDp. La proporción de infartos durante el EED (0,06%) se encuentra entre los valores previamente relatados de un 0,02%5 y 0,07%13, si bien nuestro estudio es el que más infartos describe en valor absoluto. De los 4 infartos, tres se presentaron con 40 µg/kg/min y uno con dosis de 20 µg/kg/min. En 2 pacientes existían antecedentes de infarto reciente, en otro angina y uno estaba siendo explorado por dolor torácico atípico. En la etiología de los infartos, han sido implicados diversos mecanismos que van desde el espasmo coronario hasta fenómenos de trombosis coronaria debidos a activación plaquetaria secundaria a la dobutamina4.
En cuanto a la hipotensión, se ha descrito como efecto secundario en muy distintas proporciones según los criterios aplicados para definirla (descenso de más de 20 mmHg o de 40 mmHg con respecto a la presión arterial basal, cifra absoluta inferior a 100 mmHg, presencia de síntomas, etc.). En la actualidad parece que a este efecto secundario se le da menos importancia y sólo se utiliza como criterio para interrumpir la prueba si la hipotensión es severa (> 40 mmHg) y sintomática, por lo que el porcentaje de pruebas interrumpidas por este motivo se ha reducido de manera muy significativa6, coincidiendo con otros autores en que la hipotensión severa sintomática es muy rara20. Si bien se ha comunicado un fallecimiento secundario a una hipotensión durante una EEDp14, en nuestro estudio se presentó en un solo caso y fue secundario a un EED.
Es de destacar que tres complicaciones (2 infartos y un accidente cerebrovascular) ocurrieron, al igual que en otros estudios4,6,13, después de terminar el test. Esto debe tener necesariamente implicaciones a la hora de planear la realización de ecocardiograma de estrés en pacientes ambulatorios y se aconseja que permanezcan en el área del laboratorio de ecocardiografía hasta una hora después de terminado el test con una vía venosa disponible. En la etiopatogenia de este fenómeno se ha sugerido que, aunque la vida media plasmática de la dobutamina es corta, tiene efectos biológicos, como la isquemia o el vasospasmo, que pueden durar horas. El efecto α-1 podría producir una vasoconstricción coronaria paradójicamente exacerbada por la administración de bloqueadores beta. Por otro lado, la activación plaquetaria podría traducirse tardíamente en un fenómeno trombótico con repercusiones clínicas retrasadas. Así, en nuestro caso, tanto el infarto como el accidente cerebrovascular podrían ser explicados por este mecanismo.
Si bien la mayoría de los autores están de acuerdo en que las complicaciones serias durante la ecocardiografía de estrés son impredecibles, nosotros encontramos una relación entre la experiencia del centro y el número de complicaciones. Esta relación, aunque lógica, nunca había sido descrita. En principio parece que «la falta de reconocimiento» de la aparición de nuevas anomalías segmentarias en la contractilidad debería ser el hecho relacionado con la experiencia. Por esto, no tiene fácil explicación que fueran precisamente las arritmias las complicaciones que se relacionaron con la experiencia si tenemos en cuenta que, según estudios previos, la inducción de isquemia (y de nuevas anomalías segmentarias en la contractilidad) no se relaciona con la aparición de arritmias.
CONCLUSIONES
La ecocardiografía de estrés es una técnica relativamente segura, pero no inofensiva. En la valoración de isquemia, la EEE debería ser la técnica de elección cuando sea posible, pues es mucho más segura que la EED.
Dado que existe una relación entre experiencia y número de complicaciones, parece lógico adquirir un adecuado entrenamiento antes de comenzar a realizar la prueba.
No debemos olvidar que un número significativo de las complicaciones (15%) aparece una vez terminado el test, por lo que se debe protocolizar un tiempo adecuado de vigilancia en el área del laboratorio de ecocardiografía.
Por último, la EED debe ser realizada por personal entrenado en las maniobras de resucitación.
AGRADECIMIENTO
Agradecemos la colaboracion del Dr. Varga (Instituto Fisiologia Clínica, Pisa, Italia), Dra. Mesa (Hospital Reina Sofía, Córdoba), Dr. Lacamba (Hospital Lozano Blesa, Zaragoza), Dr. Miró (Hospital La Fe, Valencia), Dr. Negrín (Hospital Dr. Negrín, Gran Canaria), Dr. Evangelista (Hospital Vall d'Hebron, Barcelona), Dr. Alonso (Hospital Txagorritxu, Vitoria), Dr. Placer (Hospital Miguel Servet, Zaragoza), Dr. Paré (Hospital Clínico de Barcelona, Barcelona), Dres. Alcalá y Rodríguez Padial (Hospital Virgen de la Salud, Toledo), Dr. Borrás y Dr. Carreras (Hospital de la Santa Creu i Sant Pau, Barcelona), Dr. San Román (Hospital Clínico de Valladolid, Valladolid), Dr. Villegas (Hospital Virgen de la Arrixaca, Murcia), Dr. González-Juanatey (Hospital Xeral de Lugo, Lugo), Dr. Peteiro (Hospital Juan Canalejo, La Coruña), Dr. Calvo (Hospital Meixoeiro, Vigo), Dra. Laraudogoitia (Hospital de Galdakao, Vizcaya), Dr. Alcaraz (Hospital Universitario, Alicante), Dr. Fernández (Hospital Policlínico, Vigo), Dr. Mora (Hospital Universitario Dr. Peset, Valencia), Dra. Caetano (Hospital San Bernardo, Setubal), Dr. Torres (Hospital General San Antonio, Oporto), Dr. Lourenco (Hospital Señora da Olivera, Guimara~es), Dr. Macedo (Hospital San Juan, Oporto), Dr. Barba (Clínica Universitaria Navarra), Dra. Moreno (Hospital Gregorio Marañón, Madrid), Dr. Marín y Dr. Morena (Hospital General, Elche).
Correspondencia: Dr. M.A. Rodríguez. Servicio de Cardiología. Hospital de León. Altos de Nava, s/n. 24071 León. Correo electrónico: faroucc@infocarlo.es Recibido el 5 de julio del 2000. Aceptado para su publicación el 19 de febrero del 2001.