El edoxabán se ha estudiado extensamente en ensayos de fase III, tanto en fibrilación auricular no valvular (ensayo ENGAGE AF-TIMI 48) como en estudios de prevención de la tromboembolia venosa recurrente (estudio HOKUSAI-VTE) y de prevención tras cirugía ortopédica (estudio STARs). Asimismo, se han publicado recientemente distintos subanálisis de los ensayos fundamentales sobre los subtipos de accidente cerebrovascular y embolia periférica en pacientes tratados con amiodarona y pacientes de edad, que merecen ser analizados.
Palabras clave
El ENGAGE AF-TIMI 481 es un estudio internacional, aleatorizado, con doble enmascaramiento y de no inferioridad que comparó 2 regímenes de edoxabán una vez al día con el tratamiento con warfarina con buen control de anticoagulación. El objetivo final primario de eficacia fue el accidente cerebrovascular (ACV) o la embolia sistémica (ES) y el objetivo de seguridad principal fue el sangrado mayor. Se asignó aleatoriamente a 21.105 pacientes con fibrilación auricular no valvular (FANV) y con una puntuación CHADS2 ≥ 2 a edoxabán 60 mg una vez al día (régimen de dosis alta) o 30 mg una vez al día (régimen de dosis baja), con un ajuste de dosis para la warfarina (international normalized ratio [INR] 2,0-3,0). La puntuación media del esquema de riesgo CHADS2 fue 2,8. Los pacientes de este estudio eran, por lo tanto, de riesgo de ACV o ES moderado-alto.
Las características demográficas y clínicas basales de los grupos de tratamiento estaban bien equilibradas, y la mediana de la duración de la exposición al tratamiento fue 907 días, excepto interrupciones. La mediana de seguimiento fue de 1.022 días (2,8 años). Los criterios para la reducción de la dosis fueron el tratamiento concomitante con un potente inhibidor de glucoproteína P (GP-P) (verapamilo, quinidina o dronedarona), peso corporal < 60 kg o aclaramiento de creatinina (AclCr) 30-50 ml/min. Para los pacientes de la estrategia de edoxabán 60 mg, la dosis se redujo a 30 mg una vez al día, y para los del grupo de dosis baja, se redujo de 30 a 15 mg una vez al día con doble enmascaramiento.
Un total de 5.330 pacientes (25,3%) recibieron una dosis reducida de edoxabán o placebo correspondiente en la aleatorización. Después de la aleatorización, se redujo la dosis a otro 7,1% de los pacientes. Hubo significativamente menos interrupciones del fármaco en los grupos de pacientes tratados con edoxabán que con warfarina (p < 0,001 para ambas comparaciones). La mediana de tiempo en rango terapéutico (TTR) del grupo de warfarina fue del 68,4% [intervalo intercuartílico, 56,5-77,4%], lo que indica que los pacientes del grupo de warfarina recibieron un tratamiento óptimo que se comportó como un comparador activo eficaz para el edoxabán. Al final del ensayo, los pacientes hicieron la transición al tratamiento anticoagulante oral en abierto mediante un plan de transición detallado2, monitorización frecuente y evaluación del INR durante 30 días.
El resultado de eficacia primaria de ACV a través de un análisis por intención de tratar modificado (mITT) ocurrió con una tasa del 1,50% por año en el grupo de warfarina bien controlada, el 1,18% al año en el grupo de edoxabán a dosis alta de 60 mg una vez al día (p < 0,001 para no inferioridad; p = 0,02 para superioridad) y el 1,61% al año en el grupo de dosis baja de edoxabán de 30 mg una vez al día (p = 0,005 para no inferioridad; sin diferencias significativas para superioridad).
En el análisis de superioridad hubo una tendencia favorable a la dosis alta de edoxabán (1,57%) frente a la warfarina (1,80%; p = 0,08 para superioridad), mientras que la tendencia era desfavorable para el grupo de dosis baja de edoxabán (2,04%) comparada con la warfarina (p = 0,10 para superioridad). Las tasas de ACV hemorrágico en los grupos de dosis alta y dosis baja de edoxabán (el 0,26 y el 0,16% respectivamente) fueron de manera estadísticamente significativa menores que con warfarina (0,47%; p < 0,001).
Con respecto al ACV isquémico, el grupo de dosis alta de edoxabán (1,25%) no fue significativamente diferente del de warfarina (el 1,25%; p = 0,97), mientras que el grupo de dosis baja de edoxabán (1,77%) tuvo una tasa significativamente mayor que el grupo de warfarina (p < 0,001).
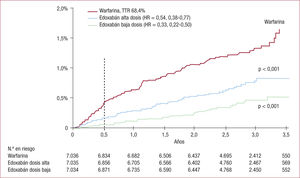
Entre los pacientes con dosis reducidas, no hubo diferencias en los eventos primarios en comparación con los pacientes sin reducción de dosis reducida en el grupo de dosis alta (p = 0,97 para la interacción) o el grupo de dosis baja de edoxabán (p = 0,74 para la interacción). Además, la tasa de muertes de causa cardiovascular fue del 3,17% en el grupo de warfarina y significativamente menor en el grupo de dosis alta de edoxabán (2,74%; hazard ratio [HR] = 0,86; intervalo de confianza del 95% [IC95%], 0,77-0,97; p = 0,013) y el grupo de dosis baja de edoxabán (2,71%; HR = 0,85; IC95%, 0,76-0,96; p = 0,008). No se observaron diferencias en la tasa de infarto de miocardio entre edoxabán a dosis altas y warfarina (el 0,70 frente al 0,75%; HR = 0,94; IC95%, 0,74-1,19; p = 0,60) o entre dosis bajas de edoxabán y warfarina (el 0,89 frente al 0,75%; HR = 1,19; IC95%, 0,95-1,49; p = 0,13), lo que indica que el riesgo de infarto de miocardio no fue alto durante el tratamiento con edoxabán (figura 1).
Curvas de Kaplan-Meier para el objetivo primario de eficacia del estudio ENGAGE AF-TIMI 48. Reproducido con permiso de Giugliano et al1 © 2016 Massachusetts Medical Society.
Desde el punto de vista de la seguridad, el estudio ENGAGE AF-TIMI 48 mostró una reducción estadísticamente significativa de la tasa de sangrado mayor entre el régimen de dosis alta de edoxabán (2,75%) y el régimen de dosis baja (1,61%) en comparación con la warfarina bien controlada (3,43%; p < 0,001 para ambos grupos).
Con respecto a la hemorragia intracraneal, las tasas fueron significativamente menores con el régimen de dosis alta (0,39%) y los grupos de tratamiento con dosis baja (0,26%) que en el grupo tratado con warfarina (0,85%; p < 0,001 para ambas comparaciones).
Ambos regímenes de edoxabán también presentaron tasas significativamente menores de sangrado mortal, sangrado con compromiso vital o sangrado no mayor clínicamente relevante (CRNM) y sangrado manifiesto que con warfarina (p ≤ 0,01 para todas las comparaciones).
En comparación con warfarina (0,82%), el grupo de dosis baja de edoxabán tuvo una tasa significativamente menor de hemorragia digestiva (1,23%; p < 0,001 en comparación con warfarina), mientras que se observó una tasa significativamente más alta en el grupo de dosis alta de edoxabán (1,51%; p = 0,03 frente a warfarina). Respecto a los pacientes con dosis reducida, la tasa de sangrado mayor fue significativamente menor que entre los pacientes con dosis alta de edoxabán (p = 0,02 para la interacción) y en los grupos de dosis bajas (p < 0,01 para la interacción) (figura 2).
Curvas de Kaplan-Meier para el objetivo primario de seguridad del ensayo ENGAGE AF-TIMI 48. Reproducido con permiso de Giugliano et al1 © 2016 Massachusetts Medical Society.
Además, tanto los grupos de dosis alta como los de dosis baja de edoxabán tuvieron una frecuencia de eventos adversos relacionados con el fármaco similar a la del grupo de warfarina. En materia de seguridad hepática, los grupos de dosis alta y dosis baja de edoxabán tuvieron frecuencias de elevación de aspartato aminotransferasa (AST) o alanina aminotransferasa (ALT) ≥ 3 veces y bilirrubina total ≥ 2 veces el límite superior normal, similares a las del grupo de warfarina.
También se observó un patrón similar con la frecuencia adjudicada de lesión hepatocelular o colestasis y los pacientes que cumplían los criterios de la ley de Hy. Por lo tanto, el tratamiento con dosis altas o dosis bajas de edoxabán no se asoció con eventos adversos hepáticos en pacientes con FANV.
En general, los resultados de eficacia y seguridad con edoxabán en el estudio ENGAGE AF-TIMI 48 mostraron que el edoxabán no es inferior a la warfarina para la prevención de ACV y ES en los pacientes con FANV y se asocia con un riesgo significativamente menor de hemorragia y muerte por causa cardiovascular.
En posteriores análisis3 se ha confirmado además que el edoxabán parece mostrar mayor eficacia en los pacientes sin tratamiento previo tratados con warfarina que en los pacientes que ya tenían experiencia con este fármaco. El edoxabán reduce de manera significativa el sangrado mayor comparado con la warfarina independientemente de la exposición previa a ella.
La amiodarona es uno de los fármacos antiarrítmicos más frecuentemente utilizados para pacientes con fibrilación auricular a pesar de sus conocidos efectos secundarios e interacciones farmacológicas. En este sentido, dada la enorme cantidad de datos del ensayo ENGAGE-TIMI 48, se realizó un análisis de sus subgrupos para comprobar el perfil de eficacia y seguridad del edoxabán en los pacientes tratados con amiodarona4. En el momento de la aleatorización, 2.492 pacientes (11,8%) recibían tratamiento con amiodarona. Los pacientes aleatorizados a la dosis baja de edoxabán tratados con amiodarona presentaron una reducción significativa de eventos isquémicos frente a warfarina cuando se compararon con los que no estaban tratados con amiodarona, conservando la seguridad. La amiodarona no tuvo efecto alguno en la eficacia y la seguridad en los pacientes aleatorizados a la dosis alta de edoxabán.
Un análisis del ENGAGE-TIMI 48 estratificó a los 21.105 pacientes del ensayo por categorías de edad y tratamiento5 para comprobar la eficacia y la seguridad de edoxabán: < 65 (n = 5.497), 65-74 (n = 7.134) y ≥ 75 años (n = 8.474). Independientemente del tratamiento, el riesgo de sangrado mayor e ictus/embolia sistémica se incrementó con la edad (p < 0,001), pero más marcadamente el sangrado mayor. Ambos regímenes de edoxabán tuvieron un efecto similar en todas las categorías de edad: dosis alta de edoxabán frente a warfarina: < 65 años, HR = 0,94; 65-74, HR = 0,89, y ≥ 75, HR = 0,83; dosis baja de edoxabán frente a warfarina: < 65 años, HR = 1,42; 65-74, HR = 1,0, y ≥ 75, HR = 1,12 (diferencias no significativas en ambos).
Cuando se comparó el edoxabán con la warfarina, el mayor impactó se vio en la reducción del riesgo absoluto de sangrado mayor, incluido el sangrado intracraneal. El beneficio del tratamiento con edoxabán concordó en todas las categorías de edad (para la interacción, diferencia no significativa) con ambos regímenes, y se llegó a la conclusión de que la eficacia y seguridad del edoxabán en comparación con la warfarina es constante con independencia de la edad y el beneficio absoluto del fármaco es mayor en el anciano que, a la sazón, presenta un riesgo mucho mayor de sangrado con la edad.
Prevención de la tromboembolia venosa recurrenteEl estudio Hokusai-VTE6 es el mayor estudio internacional realizado en tromboembolia venosa (TEV) recurrente sintomática aguda, con 8.292 pacientes con trombosis venosa profunda, embolia pulmonar o ambas. El diseño del estudio fue aleatorizado, a doble ciego, con doble enmascaramiento de grupos paralelos, con diseño de no inferioridad, una duración de tratamiento flexible de 3-12 meses y un análisis primario de los pacientes a los 12 meses. El ensayo comparó la eficacia y la seguridad de un tratamiento inicial con una heparina de bajo peso molecular (enoxaparina) seguida de edoxabán 60 mg una vez al día frente al tratamiento estándar (tratamiento inicial con enoxaparina, continuado con warfarina [INR 2,0-3,0]) en el tratamiento de la TEV sintomática.
El objetivo primario de eficacia fue la TEV sintomática recurrente y el objetivo de seguridad principal, hemorragia mayor o CRMN. Los pacientes del grupo de edoxabán cualificados para una reducción de dosis (AclCr 30-50 ml/min, peso corporal ≤ 60 kg o la administración concomitante de inhibidores potentes de la GP-P) pasaron a edoxabán 30 mg una vez al día a doble ciego.
En la aleatorización, aproximadamente el 17% de los pacientes de cada grupo de tratamiento fueron a la reducción de dosis y aproximadamente el 65% de los pacientes habían sufrido un evento índice de TEV no provocado, lo que comporta un riesgo de recurrencias muy elevado.
Las características basales de los pacientes en cada grupo de tratamiento fueron similares. Aproximadamente el 40% de los pacientes asignados al azar habían sufrido embolia pulmonar (EP): en el 46% la EP había sido extensa (definida como afección de múltiples lóbulos, con un 25% o más de la vasculatura total) y se clasificó al 42% de los pacientes de trombosis venosa profunda (TVP) extensa (definida como un evento en el que el sitio más próximo fue la vena femoral o la vena iliaca común).
La duración del tratamiento fue flexible: el 40% de los pacientes recibieron tratamiento durante 12 meses, mientras que el 61% lo recibió durante 6 meses. En el grupo de warfarina, la media del TTR fue del 63,5%, lo que indica que estos pacientes estaban relativamente bien controlados en el estudio.
El ensayo demostró que edoxabán 60 mg una vez al día después del tratamiento inicial con heparina frente al tratamiento estándar no es inferior al tratamiento recibido por el grupo de pacientes aleatorizados a warfarina con TTR bien controlado y causó significativamente menos hemorragias en una amplia variedad de pacientes con TEV.
La tasa de TEV recurrente sintomática fue del 3,2% por año en el grupo de edoxabán, comparado con el 3,5% al año en el grupo de tratamiento estándar (p < 0,001 para no inferioridad) (figura 3).
Curvas de Kaplan-Meier para el objetivo primario de eficacia del estudio Hokusai-VTE. Tromboembolia venosa (TEV) recurrente adjudicada: compuesto de trombosis venosa profunda o embolia pulmonar mortal o no mortal en todo el estudio. Reproducido con permiso de Büller et al6 © 2016 Massachusetts Medical Society.
El edoxabán 60 mg una vez al día también se asoció de manera significativa con menos eventos hemorrágicos mayores o CRNM en comparación con el tratamiento estándar (el 8,5 frente al 10,3% por año; p = 0,004 para superioridad) (figura 4).
Curvas de Kaplan-Meier del objetivo principal de seguridad. Incidencia adjudicada de hemorragia no mayor clínicamente relevante (NMCR), definida como el compuesto de sangrado mayor o sangrado no mayor clínicamente relevante. Reproducido con permiso de Büller et al6 © 2016 Massachusetts Medical Society.
El edoxabán fue efectivo en una amplia variedad de pacientes con TVP y EP durante un tiempo de tratamiento flexible de 3-12 meses. Comparadas con las tasas de recurrencia de TVP, en el análisis general de los pacientes tratados con edoxabán o warfarina durante 3-12 meses, las tasas de recurrencia, en concreto de los tratados durante 12 meses (análisis realizado en tratamiento), fueron más bajas con edoxabán (el 3,2 frente al 1,6% por año) y warfarina (el 3,5 frente al 1,9% por año), lo que demuestra que no es inferior a la warfarina (p < 0,001 para no inferioridad).
Con respecto a los pacientes con un evento índice de TVP, se observó TEV recurrente en aproximadamente el 3,4 y el 3,3% de los grupos de edoxabán y warfarina (HR = 1,02; IC95%, 0,75-1,38).
En pacientes con un evento índice de PE, se produjo TEV recurrente en el 2,8 y el 3,9% de los grupos de edoxabán y warfarina respectivamente, aunque la diferencia no fue estadísticamente significativa (HR = 0,75; IC95%, 0,50-1,06).
El edoxabán también ha mostrado con firmeza su eficacia frente a la warfarina (el 3,3 y el 6,2% por año) en el subgrupo de pacientes de PE con evidencia de disfunción ventricular derecha y cifras de NT-pro-BNP > 500 pg/ml, apoyado por un análisis en un subgrupo grande de pacientes evaluados mediante tomografía computarizada (n = 1.002).
Entre los pacientes que recibían la dosis reducida de edoxabán 30 mg una vez al día, las tasas de recurrencia de TEV, sangrado mayor o sangrado CRNM fueron menores en el grupo de edoxabán que en el de warfarina, lo que indica que una dosis específica en función de las características del paciente mantiene tanto la eficacia como la seguridad. La tasa de eventos adversos graves que condujeron a la interrupción del tratamiento fue similar en los grupos de edoxabán y warfarina.
Con relación a la seguridad hepática, el grupo de edoxabán tuvo una frecuencia similar de ALT ≥ 3 veces o ≥ 5 veces el límite superior de la normalidad, ALT o AST ≥ 3 veces y bilirrubina total ≥ 2 veces el límite superior de la normalidad, así como pacientes que cumplían los criterios de la ley de Hy en comparación con el grupo de warfarina. Por lo tanto, el tratamiento con edoxabán no se asoció con eventos adversos hepáticos en pacientes con TEV sintomática.
Además, un análisis post-hoc preespecificado de pacientes con antecedentes de cáncer o cáncer activo aleatorizados en un subgrupo de pacientes grande (n = 771) (9,3%) del total de pacientes del estudio evaluó la eficacia y la seguridad del edoxabán7.
El 3,7% de los pacientes del grupo de edoxabán frente al 7,1% de los pacientes que recibieron warfarina sufrieron TEV recurrente. En el 12,4% de los pacientes del grupo de edoxabán se produjo hemorragia mayor o CRNM, frente al 18,8% del grupo de warfarina.
Este análisis indicó que el edoxabán es tan eficaz (y posiblemente más) que la warfarina en pacientes con TEV y podría reducir las hemorragias en estos pacientes. El estudio tuvo una duración de tratamiento flexible para simular la práctica clínica habitual tanto como fuera posible, y demostró que el tratamiento con edoxabán es eficaz y bien tolerado, con menor riesgo de sangrado que el tratamiento estándar con warfarina en un amplio espectro de pacientes agudos con VET sintomática.
Prevención de la tromboembolia venosa tras cirugía ortopédicaUn programa clínico integral de fase III, aleatorizado, a doble ciego, con doble simulación, que comprende los estudios STARS E-38, STARS J-59 y STARS J-410 con edoxabán estableció su eficacia y su seguridad en la prevención del TEV tras cirugía ortopédica.
El estudio STARS E-3 en pacientes sometidos a cirugía de reemplazo total de rodilla7 aleatorizó a 716 pacientes a edoxabán 30 mg una vez al día o enoxaparina 20 mg subcutánea cada 12 h durante 11-14 días. El objetivo primario de eficacia fue la ocurrencia de TEV sintomática: el 13,9% de los pacientes del grupo de enoxaparina presentaron TEV frente al 7,4% de los pacientes que recibieron edoxabán, lo que demuestra la no inferioridad del edoxabán (p < 0,001) y la superioridad (p = 0,010) frente al tratamiento de enoxaparina.
Ocurrieron hemorragias mayores en el 1,1% del grupo de edoxabán y el 0,3% del de enoxaparina (p = 0,373 frente a edoxabán) y hemorragias mayores o hemorragias CRNM en el 6,2% del de edoxabán y el 3,7% del de enoxaparina (p = 0,129 frente a edoxabán).
El estudio STARS E-38, por lo tanto, demostró que el edoxabán es superior a la enoxaparina en la prevención del TEV tras cirugía de reemplazo total de rodilla, sin un aumento significativo en las tasas de sangrado.
El estudio STARS J-59 tenía un diseño similar al del STARS E-3, pero se llevó a cabo en 610 pacientes sometidos a cirugía de reemplazo total de cadera. Se produjo TEV en el 6,9% de los pacientes que recibieron enoxaparina y el 2,4% de los que recibieron edoxabán, y se demostró que el edoxabán es no inferior (p < 0,001) y sí superior (p = 0,0157) a la enoxaparina.
La hemorragia mayor o CRNM ocurrió en el 2,6% de los pacientes que recibieron edoxabán y el 3,7% del grupo de enoxaparina (p = 0,475 frente a edoxabán), mientras que sufrieron hemorragia mayor el 0,7% del grupo de edoxabán y el 2,0% del de enoxaparina. El ensayo STARS J-5, por lo tanto, demostró que el edoxabán es superior a la enoxaparina en la prevención del TEV tras cirugía de reemplazo total de cadera y se asoció con similar riesgo de hemorragia.
Finalmente, en el ensayo STARS J-410, multicéntrico, abierto y de seguridad en pacientes japoneses sometidos a cirugía por fractura de cadera, se aleatorizó a los pacientes a edoxabán 30 mg una vez al día o enoxaparina subcutánea 2.000 UI/12 h durante 11-14 días.
La incidencia de hemorragia mayor o mayor CRNM fue del 3,4% en el grupo de edoxabán y el 6,9% en el de enoxaparina, mientras que se produjo cualquier evento de sangrado en el 25,4 y el 17,2% respectivamente.
Hubo un episodio de hemorragia mayor en cada grupo y la tasa de eventos tromboembólicos asintomáticos fue del 6,5% en el grupo de edoxabán y el 3,7% en el de enoxaparina, sin que se observaran eventos sintomáticos. El edoxabán, por lo tanto, ha mostrado eficacia y seguridad similares a las de enoxaparina en pacientes japoneses sometidos a cirugía de fractura de cadera.
En general, el programa STARS demostró que el edoxabán es más efectivo que la enoxaparina en la prevención del TEV tras la cirugía de reemplazo de cadera o rodilla y se asocia con similar riesgo de sangrado. Los estudios STARS apoyaron la aprobación regulatoria de edoxabán 30 mg una vez al día para la prevención del TEV tras cirugía ortopédica en Japón en 2011.
Análisis pormenorizado del ensayo engage AF-TIMI 48 ICTUSEs de especial interés abordar el análisis preespecificado de los subtipos de eventos cerebrovasculares del ensayo ENGAGE AF-TIMI 4811.
El objetivo primario era el total de ictus (isquémicos y hemorrágicos), definidos como un comienzo abrupto de déficit neurológico focal por infarto o hemorragia con síntomas que perduren más de 24 h o muerte en menos de 24 h. Neurólogos independientes que no conocían el grupo de tratamiento de los pacientes adjudicaron los eventos cerebrovasculares.
Los pacientes aleatorizados a la dosis alta de edoxabán presentaron menor número de ictus en el análisis en tratamiento (HR = 0,80; IC95%, 0,65-0,98) que los tratados con warfarina (TTR, 68,4%). Los pacientes del grupo tratado con la dosis baja de edoxabán presentaron cifras similares (HR = 1,10 frente a warfarina; IC95%, 0,91-1,32).
El número de ictus isquémicos y transitorios fue similar en el grupo de dosis alta de edoxabán (el 1,76% por año) y warfarina (el 1,73% por año; p = 0,81), pero más frecuentes con dosis bajas de edoxabán (el 2,48% por año; p < 0,001). Ambos regímenes de edoxabán redujeron significativamente los ictus hemorrágicos (figura 5) y otros subtipos de hemorragias intracraneales.
Curvas de Kaplan-Meier para el ictus hemorrágico. Análisis por intención de tratar en los 3 brazos de tratamiento durante todo el periodo del estudio. Las tasas de ictus hemorrágico de warfarina, edoxabán a alta dosis y edoxabán a baja dosis fueron del 0,39, el 0,17 y el 0,06%. Reproducido con permiso de Giugliano et al11.
El subanálisis concluye que, para los pacientes con FANV, edoxabán una vez al día es tan efectivo como la warfarina en la prevención de todo tipo de ictus, con reducciones significativas en varios subtipos de ictus hemorrágico. Los eventos isquémicos se reducen de modo similar con las dosis altas de edoxabán y warfarina, mientras que las dosis bajas de edoxabán son menos efectivas que la warfarina.
En las gráficas se señala el porcentaje de ictus isquémicos en el análisis por intención de tratar en los diferentes grupos de tratamiento y la superposición de este tipo de ictus a los 30 días de la aleatorización (figura 6).
Curvas de Kaplan-Meier para el ictus isquémico en las 3 ramas de tratamiento por intención de tratar. En la parte superior del gráfico se señala el ictus isquémico en los primeros 30 días tras la aleatorización. Reproducido con permiso de Giugliano et al11.
En el análisis por intención de tratar modificado (figura 7), se observa la no inferioridad tanto del régimen de dosis alta como del de dosis baja frente a la warfarina, con un límite para la no inferioridad de 1,38.
Todos los ictus por grupo de tratamiento. El análisis en tratamiento se realizó por intención de tratar modificada (mITT) sobre todos los pacientes que tomaron al menos una dosis del fármaco del estudio, contando los eventos que ocurrieron mientras los pacientes estaban en tratamiento más 3 días después de interrumpirlo. El intervalo de censura se incrementó por tiempo durante las interrupciones de más de 4 días. Reproducido con permiso de Giugliano et al11. IC95%: intervalo de confianza del 95%; TTR: tiempo en rango terapéutico.
En la figura 8 se presenta el análisis de todos los pacientes aleatorizados en el ensayo por intención de tratar, es decir, contando los eventos entre la aleatorización y la última visita, y se observa que las estrategias de tratamiento con edoxabán no superan el límite de no inferioridad.
Análisis por intención de tratar de todos los ictus por grupo de tratamiento. Reproducido con permiso de Giugliano et al11. IC97,5%: intervalo de confianza del 97,5%; TTR: tiempo en rango terapéutico.
La ES es mucho menos frecuente que el ictus, a pesar de lo cual se asocia a una morbimortalidad significativa en los pacientes con FANV. Aunque el número de eventos es demasiado pequeño para encontrar diferencias significativas en el riesgo de ES entre warfarina y edoxabán, es interesante analizarlo en el ensayo ENGAGE AF-TIMI 4812.
De los 1.016 pacientes del ensayo ENGAGE AF-TIMI 48 que sufrieron un evento, 949 (93,4%) tuvieron un ictus; 58 (5,7%), ES y 9 (0,9%), ambos. Los pacientes que sufrieron ES, comparados con los que tuvieron un ictus, eran mayores (media, 78 frente a 74 años; p = 0,005) y tenían mayor probabilidad de FA permanente (el 72 frente al 55%; p = 0,02), alteración de la función renal de grado moderado (AclCr 50 ml/min; el 42 frente al 27%; p = 0,01) o tratamiento previo con un fármaco antagonista de la vitamina K (AVK) (el 80 frente al 57%; p < 0,001).
En un modelo multivariable, los factores independientes predictores de ES fueron: la disminución del AclCr (por cada 10 ml/min de disminución, HR = 1,30; IC95%, 1,12-1,50; p < 0,001), FA permanente (HR = 2,97; IC95%, 1,33-6,63; p = 0,008) y tratamiento previo con un AVK (HR = 86; IC95%, 1,04-3,30; p = 0,04).
En cuanto a la localización y la gravedad del ES, hubo un total de 73 ES, incluidos 6 eventos recurrentes; la mayoría ocurrió en las extremidades (n = 62 [85%]) —el 82% en las extremidades inferiores y el 15% en las superiores—; el 10% tuvo localización abdominal o mesentérica; el 4%, renal y el 1%, en otras localizaciones (figura 9).
Localización de las embolias en los diferentes territorios vasculares. Reproducido con permiso de Ceder et al12.
Resultaron mortales 9 embolias (13%); el 52% de las embolias fueron no mortales y el 41% requirió tratamiento percutáneo o quirúrgico para restablecer el flujo sanguíneo.
Eficacia relativa del edoxabán frente a la warfarinaEn el grupo de warfarina, el TTR fue del 68,4% (56,5%-77,4%). Hubo 23 ES (0,12%/año), frente a 15 en el grupo de dosis de 60 mg de edoxabán (0,08%/año; HR = 0,65; IC95%, 0,34-1,24; p = 0,19) y 29 en el grupo de dosis baja de edoxabán (0,15%/año; HR = 1,24; IC95%, 0,72-2,15; p = 0,43).
El grupo de dosis alta de edoxabán presentó un número significativamente menor de ES que el grupo de dosis baja (HR = 0,52; IC95%, 0,28-0,97; p = 0,04). En el grupo de warfarina, 4 ES (17%) fueron mortales en comparación con ninguno en el grupo de dosis alta de edoxabán y 5 (17%) en el grupo de dosis baja de edoxabán.
En un metanálisis de los 4 ensayos controlados de fase III en FANV13, los anticoagulantes orales directos redujeron el riesgo de ES en un 37% (IC95%, 0,43-0,91; p = 0,01).
Conflicto de interesesI. Lekuona ha dado conferencias remuneradas sobre anticoagulantes orales directos para Boehringer, Bayer, Pfizer-Squibb y Daiichi Sankyo.