Palabras clave
SITUACIÓN ACTUAL DE LA RECONSTRUCCIÓN MITRAL
Numerosas publicaciones han mostrado claramente la superioridad de la reparación mitral respecto al recambio valvular debido a su menor mortalidad hospitalaria y tardía, la tasa de accidentes tromboembólicos y el número de reoperaciones. El único factor limitante de la reconstrucción mitral es la presencia de lesiones no reparables. Sin embargo, las nuevas técnicas quirúrgicas han aumentado significativamente la tasa de reparaciones que, en el caso de las insuficiencias no reumáticas, es cercana al 100%, lo que ha resultado en una tendencia progresiva hacia indicaciones cada vez más tempranas. Este cambio también se ha debido a las numerosas publicaciones de la Clínica Mayo que demuestran que la evolución de la insuficiencia mitral no es tan lenta y benigna como se pensaba. El número de muertes súbitas1, la progresión de las lesiones que hacen su reparación más difícil2 y la incidencia de fibrilación auricular3 llevaron a que estos autores recomendaran la necesidad de adelantar el momento quirúrgico. De hecho, pacientes totalmente asintomáticos son actualmente sometidos a cirugía con tal de que tengan una insuficiencia severa y una probabilidad de reparación cercana al 100%4. Este alto índice de reparación valvular ha sido posible gracias al trabajo en equipo del cardiólogo y del cirujano, que utilizan una terminología común para describir exactamente la localización anatómica de las lesiones5, y a la ecocardiografía preoperatoria transtorácica y sobre todo transesofágica, que permite un análisis anatómico preciso (fig. 1). Actualmente es posible planear exactamente antes de la cirugía todas y cada una de las técnicas reparadoras necesarias para obtener un perfecto resultado6. Sin embargo, esta actitud agresiva conlleva una gran responsabilidad ya que tenemos que asegurar al paciente no sólo un buen resultado inmediato sino también a largo plazo.
Fig. 1. Diagrama de los planos ecocardiográficos usados por el cardiólogo y el cirujano para localizar cada una de las lesiones mitrales. Cada parte del velo y la cuerda es identificada por el músculo papilar que le soporta (anterior 1, posterior 2). LAX: eje largo; 4 ch: eje de 4 cámaras; 2 ch: eje de 2 cámaras; RV: ventrículo derecho.
La estabilidad de toda reconstrucción mitral depende de la etiología y la calidad de la reparación quirúrgica. Como toda cirugía de las cardiopatías adquiridas, la reparación mitral, aunque no cura la enfermedad subyacente, lentifica su progresión, mejora la situación hemodinámica y, consecuentemente, la calidad de vida del enfermo. En el caso de las lesiones reumáticas, la edad del paciente es el factor más importante. En el enfermo joven la probabilidad de reparación es alta pero su durabilidad está limitada por la fibrosis progresiva característica de la enfermedad reumática7. En el enfermo mayor, la posibilidad de reparación se reduce aproximadamente al 50% pero su durabilidad es buena8. En los países industrializados, las lesiones degenerativas son las más frecuentes, con una probabilidad de reparación superior al 80% de los casos. Sin embargo, dada la alteración de la matriz extracelular, la durabilidad de la reconstrucción está ligada al grado de reducción quirúrgica del estrés mecánico de todos los elementos del aparato mitral. Las insuficiencias funcionales, principalmente las isquémicas, son fáciles de reparar con una simple anuloplastia, pero la incidencia de recurrencia alcanza casi el 30%9.
OBJETIVO ACTUAL DE LA RECONSTRUCCIÓN MITRAL
Inicialmente se pensaba que el éxito de una reparación mitral se limitaba a conseguir una válvula funcionalmente suficiente. Actualmente el objetivo es más ambicioso. Una buena reconstrucción requiere no sólo ausencia de regurgitación, sino también una reparación anatómica de todos los elementos del complejo mitral. El objetivo es la reducción al mínimo del estrés mecánico en un tejido severamente alterado.
Estudios recientes han demostrado que la inducción experimental de alteraciones geométricas en uno de los elementos del aparato mitral resulta en un aumento significativo del estrés mecánico sobre toda la estructura valvular. Por ejemplo, la nueva técnica de análisis virtual de la válvula mitral (finite element modeling) ha mostrado claramente que durante el ciclo cardíaco la válvula mitral normal está sometida a un estrés mecánico mínimo, lo que explica la longevidad de un tejido tan delicado durante millones de ciclos. Este estrés aumenta muy significativamente cuando se introducen pequeños cambios anatómicos. Por ejemplo, Kunzelman et al10 han demostrado que una dilatación del anillo mitral, aunque no alcanza a producir insuficiencia valvular, duplica el estrés mecánico en los velos y trígonos fibrosos. La reducción de esta dilatación con un anillo flexible revierte el estrés a valores normales (lo que no ocurre con un anillo rígido). En el animal de experimentación, la sonomicrometría, que consiste en la implantación quirúrgica de pequeños cristales ultrasónicos (1-2 mm) en el anillo mitral, los músculos papilares y el ventrículo izquierdo, permite la reconstrucción tridimensional del complejo mitral con una extrema resolución temporoespacial, a una frecuencia de 200 imágenes por segundo11 (fig. 2). Esta técnica no sólo ha confirmado los estudios clásicos de Tsakiris et al12 y Ormiston et al13, que mostraron los cambios continuos del área mitral, sino también que el anillo no está en un plano único sino que tiene una forma en silla de montar. Esta configuración geométrica de paraboloides hiperbólicos, bien conocida y utilizada por los arquitectos, cumple una función de reducción muy significativa del estrés mecánico en los velos mitrales14. La implicación clínica de estos hallazgos es que la implantación de un anillo rígido impone una configuración del anillo fija, constante y en un plano (fig. 3). La curvatura o convexidad normal de los velos es también importante en relación con el estrés mecánico. Tanto la reducción como el aumento de la curvatura normal de los velos mitrales cambian el grado de estrés en éstos. Estos datos explican la espiral evolutiva de la insuficiencia mitral mixomatosa. El aumento del estrés mecánico en un tejido anormal produce una dilatación anular que incrementa el estrés en los velos que se abomban aumentando aun más su tensión. Por lo tanto, toda reconstrucción mitral requiere: a) una anuloplastia que evite la dilatación progresiva del anillo, permita sus cambios continuos y mantenga la configuración en silla de montar, y b) una reparación geométrica de los velos que retorne su área lo más cerca posible a la normal.
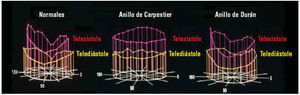
Fig. 2. Curvas de los cambios observados con sonomicrometría durante el ciclo cardíaco en una oveja normal. Annulus: área del anillo mitral; CIV: contracción isovolumétrica; PAo: presión de la aorta ascendente; papilar: distancia interpapilar; PVI: presión del ventrículo izquierdo; RIV: relajación isovolumétrica; velo mitral: distancia entre bordes libres de los velos.
Fig. 3. Imágenes ecocardiográficas del anillo mitral que muestran su forma en silla de montar (normal) y tras la implantación de un anillo rígido (Carpentier) y flexible (Durán). Con permiso de Yamaura Y et al. J Heart Valve Dis 1995;4:618-22.
La importancia de mantener o restituir la geometría normal de la válvula mitral es aun más evidente en las insuficiencias mitrales funcionales de origen isquémico o por miocardiopatía donde la insuficiencia es debida a la deformación geométrica de un aparato mitral normal. En estos casos, el anillo mitral está dilatado de forma no homogénea. Es decir, el diámetro anteroposterior del anillo está selectivamente aumentado debido a un desplazamiento apicolateral del músculo papilar posterior. En estos casos, el problema no es mitral sino ventricular. Este hallazgo cuestiona el concepto clásico de la válvula mitral como una estructura independiente del ventrículo izquierdo y que, por lo tanto, puede ser recambiada o reparada ignorando su efecto en la función del ventrículo. La válvula mitral debe ser considerada como parte integral del ventrículo. Este concepto integral de la unidad mitroventricular es aparente en la conocida necesidad de conservar el aparato subvalvular en el recambio mitral y explica la menor mortalidad hospitalaria de la reparación, que es aproximadamente un tercio de la mortalidad tras el recambio mitral, de acuerdo con la base de datos de la Society of Thoracic Surgeons. Esta diferencia, mayor cuanto más deteriorada sea la función ventricular15, realza la importancia de la conservación del aparato mitral en los enfermos con cardiopatías avanzadas.
NUEVAS TÉCNICAS QUIRÚRGICAS
La reconstrucción mitral exige en cada enfermo un análisis ecocardiográfico preoperatorio exacto de todas las lesiones anatómicas del aparato valvular mitral. Cada una de las lesiones debe ser corregida incluso cuando, aparentemente, una lesión determinada parece poder ser ignorada. En este caso, la distorsión geométrica residual condicionará una recurrencia tardía de la insuficiencia. Por lo tanto, en la mayoría de los casos es necesario aplicar técnicas quirúrgicas específicas en todas las zonas del aparato mitral, es decir annulus, velos, cuerdas tendinosas y músculos papilares.
Reconstrucción de los velos valvulares
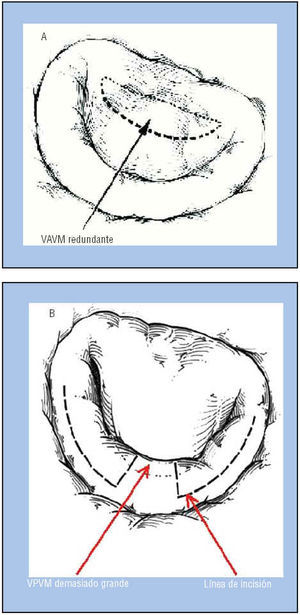
Todas las insuficiencias mitrales orgánicas presentan lesiones de los velos valvulares. Mientras el área de los velos está severamente reducida por la retracción fibrosa presente en las lesiones reumáticas, las lesiones mixomatosas siempre presentan un exceso de tejido valvular. En ambos casos es necesario aplicar técnicas reconstructivas que aumenten o reduzcan el área de los velos16. La altura o distancia entre el borde libre del velo anterior y posterior, y sus correspondientes inserciones en el anillo mitral, son medidas en diástole en el estudio ecocardiográfico intraoperatorio. En un estudio transesofágico en 100 enfermos con válvula mitral normal hemos obtenido una serie de parámetros geométricos normales17. Las alturas normales de los velos anterior y posterior son de aproximadamete 27 mm y 15 mm, respectivamente. Típicamente en las lesiones reumáticas ambos velos están retraídos. En estos casos practicamos una extensión del velo anterior con un parche de pericardio autólogo tratado durante 10 min en glutaraldehído. La mayoría de las lesiones degenerativas presenta una gran redundancia de tejido en ambos velos acompañada de prolapso del velo posterior. Cuando la altura del velo anterior es superior a 30 mm, acortamos el velo mediante una incisión y resutura paralela a su inserción que reduce la altura del velo en 5 mm. En caso de una mayor elongación del velo anterior es necesaria una resección de la base del velo (fig. 4A). Cuando el velo posterior está elongado por encima de 15 mm, además de practicar la conocida resección cuadrangular del segmento central del velo, practicamos una incisión y resutura todo a lo largo de la base del velo (sliding plasty) (fig. 4B). En resumen, actualmente es posible planear preoperatoriamente exactamente la cantidad de tejido valvular idóneo en cada enfermo mitral. Estas técnicas han conseguido prácticamente hacer desaparecer el hallazgo postoperatorio de movimiento anterior sistólico, antes frecuente en estos pacientes.
Fig. 4. Técnica de la reducción del velo mitral anterior (A) y posterior (B). VAVM: velo anterior de la válvula mitral; VPVM: velo posterior de la válvula mitral. Con permiso de Duran CMG16.
Reconstrucción de cuerdas tendinosas
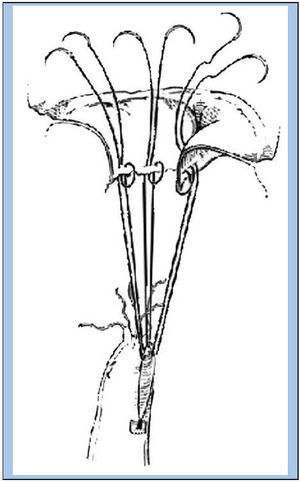
La mayoría de las insuficiencias mitrales de origen degenerativo presentan un prolapso del velo posterior y menos frecuentemente de ambos velos. Hasta hace poco, la cirugía del prolapso mitral con o sin rotura de cuerdas se limitaba a la resección cuadrangular del segmento prolapsado. El prolapso del velo anterior es aún considerado en muchos centros como contraindicación a la reparación debido a la dificultad técnica de practicar una transposición de cuerdas tendinosas. Actualmente, la construcción de neocuerdas con suturas tipo Goretex ha simplificado esta cirugía, que no se limita a la sustitución de cuerdas rotas sino también a cuerdas elongadas o muy adelgazadas18. La superficie de estas neocuerdas se recubre rápidamente con una envoltura de tejido fibroso que no reduce su movilidad pero las mantiene intactas durante un seguimiento superior a los 15 años (fig. 5).
Fig. 5. Implantación de neocuerdas. Cuando el número de neocuerdas es elevado, se utiliza un soporte único en el músculo papilar. Con permiso de Duran CMG y Pekar F18.
Anuloplastia mitral
Actualmente hay una gran variedad de anuloplastias. Las antiguas anuloplastias que inducían una plicatura del anillo mitral con una sutura en ambas comisuras han sido abandonadas. Estas anuloplastias, al no proteger la totalidad del anillo valvular, han resultado ser poco estables a la larga. La descripción hecha por Carpentier de un anillo protésico rígido que permitía una reducción selectiva de todo el anillo abrió el campo de la reparación mitral moderna19. Desde entonces, se ha desarrollado una serie de prótesis que básicamente pueden ser clasificadas como rígidas o flexibles y totales o parciales. Las prótesis rígidas y monoplanares han sido desplazadas debido a los numerosos trabajos experimentales y clínicos que han demostrado que el perímetro del anillo mitral cambia de tamaño y forma continuamente durante el ciclo cardíaco. El reciente hallazgo de que estos cambios se producen de forma tridimensional con un anillo en forma de silla de montar ha dado origen a nuevas prótesis tridimensionales pero rígidas. Estos diseños ignoran de nuevo los cambios continuos de esta estructura. De hecho, prácticamente todas las nuevas prótesis ya son flexibles o semirrígidas.
Todas las prótesis han estado basadas en la observación de que la dilatación patológica del anillo mitral no es homogénea, sino que se limita fundamentalmente al segmento posterior. El segmento anterior del anillo, al ser fibroso, se consideraba inextensible. Este principio se utilizó no sólo como método para la selección del tamaño de prótesis adecuado, sino también para el diseño de prótesis parciales que solamente reducen y sostienen el anillo posterior20. Estos tipos de anuloplastia reducen el tiempo quirúrgico y permiten conservar los cambios fisiológicos que ocurren en el área intertrigonal. Recientemente hemos demostrado con sonomicrometría en un modelo ovino que la distancia intertrigonal cambia en un 12% durante el ciclo cardíaco21. Este hallazgo, que cuestiona el principio de la inmovilidad del annulus normal, ha sido confirmado recientemente por un estudio necrópsico en controles y en enfermos con cardiopatía isquémica y miocardiopatía dilatada que mostró una dilatación del área intertrigonal de hasta el 40%22. Todos estos datos, junto con los estudios experimentales del grupo de Stanford, permiten concluir que la prótesis mitral ideal debe: a) prevenir la dilatación del área intertrigonal; b) reducir la dilatación, y c) restaurar su forma en silla de montar23. Solamente un anillo flexible y completo cumple con todas estas características.
INSUFICIENCIA MITRAL FUNCIONAL
Las insuficiencias mitrales funcionales son actualmente el caballo de batalla no sólo de la cirugía mitral, sino también del tratamiento quirúrgico de la insuficiencia cardíaca. El continuo aumento del número de enfermos, que ha llegado a ser equiparado a una epidemia24, es debido al envejecimiento de la población y al éxito de la revascularización percutánea postinfarto. La presencia de insuficiencia mitral isquémica es de aproximadamente el 20%25 y duplica la mortalidad postinfarto26 incluso en enfermos con insuficiencias poco severas (grado 1-2+) donde la supervivencia a 5 años es del 49%27. El mecanismo causante de la insuficiencia es el desplazamiento apical de los velos (tethering) que impide su coaptación. Esta fijación de unos velos perfectamente normales es secundaria al desplazamiento lateral y apical de los músculos papilares, a su vez secundario al aumento de la esfericidad del ventrículo izquierdo28. El tratamiento quirúrgico ha consistido en la reducción del anillo mitral con una prótesis pequeña que aproxima los velos permitiendo su coaptación. Los resultados de esta cirugía han mostrado una mortalidad operatoria satisfactoria, del 5% al 10%, y una mejoría en la calidad de vida del enfermo. Sin embargo, la supervivencia a los 5 años de seguimiento sigue siendo solamente del 50%29. De forma similar, la estabilidad de este tipo de reparación mitral no parece ser tan satisfactoria como en otras patologías. En una revisión de 110 enfermos operados en nuestro servicio, el 30% presentó una recurrencia de la insuficiencia mitral durante su seguimiento9. En todos ellos se había practicado con éxito una revascularización miocárdica y una anuloplastia con anillo flexible. Durante un período de seguimiento medio de 3,5 años apareció una nueva insuficiencia mitral grado 2+ en el 26% de los enfermos y de grado 3+ en el 9%. Recientemente, hemos analizado los ecocardiogramas transtóracicos preoperatorios y postoperatorios tardíos de 2 grupos de pacientes con características preoperatorias similares y con ausencia de regurgitación mitral tras la revascularización y la anuloplastia. La única diferencia entre los 2 grupos era la ausencia o presencia tardía de insuficiencia mitral significativa. No existieron diferencias entre los grupos en la fracción de eyección y el grado de insuficiencia mitral preoperatoria, ni en el tamaño de la prótesis implantada. Durante el período de seguimiento no hubo nuevos accidentes isquémicos. Los únicos datos ecocardiográficos preoperatorios que permiten diferenciar a los 2 grupos fueron un mayor grado de esfericidad ventricular30 y un mayor grado de desplazamiento lateral del músculo papilar posterior31 (fig. 6). Estos datos no invalidan la indicación actual de realizar una anuloplastia de forma simultánea con la revascularización miocárdica, ya que no aumenta la mortalidad hospitalaria y mejora la clase funcional del enfermo. Sin embargo, el número de recurrencias cuestiona la idoneidad de la anuloplastia aislada en las miocardiopatías severas. Es muy probable que sea necesaria una reconstrucción completa del aparato mitral que incluya una anuloplastia que reduzca el perímetro completo del anillo, corrija su deformación anteroposterior manteniendo su forma en silla de montar y una plastia que reaproxime los músculos papilares32.
Fig. 6. Diagrama del aparato mitral normal y con insuficiencia mitral isquémica mostrando el desplazamiento apical de los velos. Normal (A). Insuficiencia mitral isquémica (B). AI: aurícula izquierda; VI: ventrículo izquierdo; VAVM: velo anterior de la válvula mitral; VPVM: velo posterior de la válvula mitral. Con permiso de Matsunaga et al. J Heart Valve Dis [en prensa].
Aunque fuera del ámbito de este trabajo, es importante llamar la atención sobre la alta incidencia de insuficiencias tricuspídeas funcionales asociadas a la lesión mitral. Koelling et al25, en un estudio en 1.436 enfermos isquémicos, encontraron una incidencia de insuficiencia mitral del 49% y tricuspídea del 35%. Actualmente, en nuestro servicio, los enfermos que van a ser revascularizados y presentan una insuficiencia mitral y tricuspídea en la ecocardiografía transtorácica preoperatoria reciben una doble anuloplastia. Los resultados iniciales de esta doble anuloplastia en enfermos con miocardiopatía isquémica o dilatada parecen avalar esta actitud agresiva33.
CONCLUSIONES Y PERSPECTIVAS FUTURAS
Independientemente del valor diagnóstico funcional de la ecocardiografía, el estudio anatómico con ecocardiografía transesofágica es absolutamente necesario para la reconstrucción mitral. Preoperatoriamente, proporciona al cirujano información acerca del número, el tipo y la localización exacta de cada una de las lesiones. Esta información determina la probabilidad de reparación y la selección de las maniobras quirúrgicas necesarias.
Las nuevas técnicas quirúrgicas han hecho posible la reparación de la casi totalidad de las lesiones degenerativas.
Los enfermos asintomáticos con insuficiencia mitral severa de origen degenerativo deben ser operados si el estudio ecocardiográfico preoperatorio muestra un índice de reparación cercano al 100%.
Los enfermos con insuficiencia mitral funcional isquémica que van a ser revascularizados deben ser tratados con un simple anillo completo y flexible.
Las insuficiencias tricuspídeas, frecuentes en las miocardiopatías, no deben ser ignoradas.
La reconstrucción mitral aislada, es decir, sin posibilidad de revascularización, de la insuficiencia funcional en las miocardiopatías isquémicas y dilatadas es aún experimental y probablemente necesita, además de la anuloplastia, una plastia en los músculos papilares.
Correspondencia: C.M.G. Duran, MD, PhD.
International Heart Institute of Montana Foundation.
554 W Broadway, Missoula, MT 59802, USA.
Correo electrónico: duran@saintpatrick.org