La aparición de los nuevos antiagregantes orales que actúan bloqueando el receptor de adenosindifosfato P2Y12 en las plaquetas ha supuesto un importante avance en el manejo de los pacientes con síndrome coronario agudo. En el espectro general de los síndromes coronarios agudos, tanto el prasugrel como el ticagrelor se han demostrado más eficaces que el clopidogrel en reducir el riesgo de nuevos eventos cardiovasculares, aunque con un discreto aumento en el número de hemorragias. Por otro lado, los pacientes que sufren un síndrome coronario agudo tienen un perfil heterogéneo, y tanto los beneficios como los riesgos en la utilización de estos nuevos tratamientos no son uniformes. En este contexto, el objetivo de este artículo es revisar los resultados de los análisis de subgrupos que comparan la eficacia y la seguridad del prasugrel y el ticagrelor frente al clopidogrel con la intención de definir los perfiles clínicos con el balance riesgo-beneficio más propicio al manejo con los nuevos bloqueadores orales del receptor P2Y12.
Palabras clave
La terapia antiagregante oral es uno de los pilares del tratamiento de los síndromes coronarios agudos (SCA) y la prevención de nuevos eventos a largo plazo1–4. La administración combinada de ácido acetilsalicílico (AAS) y clopidogrel, un antagonista del receptor de adenosindifosfato (ADP) P2Y12, ha sido hasta hace poco el tratamiento antiplaquetario estándar para estos pacientes5. Aun siendo un fármaco con demostrada eficacia, el clopidogrel tiene importantes limitaciones, como el inicio lento en su acción y una variabilidad significativa entre unos pacientes y otros en su efecto antiagregante6. Los nuevos inhibidores del receptor P2Y12, prasugrel y ticagrelor, son más potentes, tienen menos variabilidad y un inicio de acción más rápido que el clopidogrel7–10. Las guías de práctica clínica elaboradas por la Sociedad Europea de Cardiología para el manejo de los SCA sin elevación del segmento ST (SCASEST)2 y para la revascularización coronaria4 recomiendan el uso preferencial de prasugrel o ticagrelor, y relegan el clopidogrel para los pacientes a los que no sea posible administrar uno de estos fármacos. Esta recomendación se basa en los resultados generales y significativos de dos grandes ensayos clínicos: el estudio TRITON-TIMI 38 (TRial to assess Improvement in Therapeutic outcomes by optimizing platelet inhibitiON with prasugrel-Thrombolysis In Myocardial Infarction 38)11, que comparó el prasugrel con el clopidogrel, y el estudio PLATO (PLATelet inhibition and patient Outcomes)12, que comparó el ticagrelor con el clopidogrel, ambos realizados en un amplio espectro de pacientes con SCA. Desde un punto de vista práctico, esta recomendación puede resultar demasiado general y choca con la necesidad diaria que tiene el clínico de recurrir a algún tipo de consejo o clave que le indique en qué situaciones concretas y con qué fármaco la relación riesgo-beneficio resulta más favorable para iniciar el uso de estos nuevos tratamientos13.
Aun reconociendo las limitaciones de los análisis de subgrupos dentro de un ensayo clínico aleatorizado, las implicaciones clínicas y regulatorias de estos análisis suelen ser importantes14. En este artículo se intenta revisar los resultados en los diferentes subgrupos que comparan la eficacia y la seguridad del ticagrelor y el prasugrel con las del clopidogrel en el manejo de los SCA, centrándonos en la búsqueda de los perfiles y las situaciones con el mejor balance neto a la hora de utilizar estos nuevos antiagregantes.
Diabetes mellitusLas guías clínicas para el manejo de los SCASEST consideran a los diabéticos como pacientes de alto riesgo cardiovascular y, por lo tanto, candidatos a tratamiento combinado con potentes agentes antitrombóticos2. Por otro lado, está demostrado que el efecto antiagregante de la doble terapia con AAS y clopidogrel es menor en los diabéticos que en los no diabéticos15,16, y precisamente este grupo de pacientes está necesitado de nuevas fórmulas de tratamiento antiagregante capaces de mejorar su pronóstico cardiovascular.
Cuando los diabéticos toman dosis altas de clopidogrel, 150mg diarios, se consigue una mayor inhibición de la agregación plaquetaria17, pero la eficacia clínica de esta pauta de tratamiento en los diabéticos no está comprobada. En el ensayo CURRENT/OASIS-7 (Clopidogrel optimal loading dose Usage to Reduce recurrent EveNTs/Optimal Antiplatelet Strategy for InterventionS)18 se incluyó a 25.087 pacientes, el 23,4% de ellos diabéticos, con SCA candidatos a coronariografía precoz, y se los aleatorizó a recibir una dosis alta de clopidogrel (600mg de carga y 150mg diarios durante 7 días, seguida de 75mg diarios) o una dosis estándar (300mg de carga seguida de 75mg diarios). En ese estudio, en general, no se encontraron diferencias significativas en el objetivo de valoración principal (combinación de muerte cardiovascular, infarto de miocardio e ictus a 30 días), aunque entre los pacientes tratados con intervencionismo coronario percutáneo (ICP) sí hubo una reducción significativa en esta variable combinada (el 3,9 y el 4,5%; hazard ratio [HR]=0,85; p=0,036) y una disminución en la incidencia de trombosis del stent de un 30%. Sin embargo, en el subgrupo de pacientes diabéticos tratados con ICP en ese ensayo, las diferencias no fueron significativas (el 4,9 y el 5,6%; HR=0,87; intervalo de confianza del 95% [IC95%], 0,66–1,15).
El estudio TRITON-TIMI 38 (n=13.608)11 ha comparado prasugrel con clopidogrel en pacientes con SCA. El análisis en el subgrupo de pacientes diabéticos en ese ensayo (n=3.146) se definió a priori, y mostró una reducción significativa en la incidencia de eventos cardiovasculares en los diabéticos tratados con prasugrel comparado con clopidogrel (el 12,2 y el 17,0%; HR=0,70; IC95%, 0,58–0,85) sin un incremento significativo en la tasa de sangrados mayores en este subgrupo (el 2,5 y el 2,6%; HR=1,06; IC95%, 0,66–1,09)19. Este beneficio se observó tanto en pacientes tratados con insulina (el 14,3 y el 22,2%; HR=0,63; IC95%, 0,44–0,89) como en los diabéticos no tratados con insulina (el 11,5 y el 15,3%; HR=0,74; IC95%, 0,59–0,93). En general, el beneficio clínico neto del prasugrel frente al clopidogrel (eventos cardiovasculares y eventos hemorrágicos) fue mayor para los pacientes diabéticos (el 14,6 y el 19,2%; HR=0,74; IC95%, 0,62–0,89) que para los no diabéticos (el 11,6 y el 12,3%; HR=0,92; IC95%, 0,82–1,03).
Los beneficios del ticagrelor frente al clopidogrel para los pacientes diabéticos también se estudiaron en un análisis preespecificado del estudio PLATO20. En ese estudio se incluyó a 18.624 pacientes, 4.662 de ellos diabéticos (25%), y en este subgrupo el ticagrelor mostró tendencia a reducir la incidencia combinada de eventos cardiovasculares (el 14,1 y el 16,2%; HR=0,88; IC95%, 0,76–1,03), la mortalidad total (el 7 y el 8,7%; HR=0,82; IC95%, 0,77–1,01) y la tasa de hemorragias (el 14,1 y el 14,8%; HR=0,95; IC95%, 0,81–1,12). Por otro lado, en un análisis preespecificado sobre el efecto del ticagrelor en función de la concentración de glucohemoglobina (HbA1c) en el momento de la inclusión en el estudio, el ticagrelor redujo de manera significativa la incidencia de eventos cardiovasculares (el 11,4 y el 14,2%; HR=0,80; IC95%, 0,70–0,91) y la mortalidad total (el 5,6 y el 7,4%; HR=0,78; IC95%, 0,65–0,93) entre los pacientes con cifras de HbA1c por encima del valor medio (6%) y, de nuevo, sin un incremento significativo en la tasa de hemorragias (el 12,3 y el 12,6%; HR=0,98; IC95%, 0,86–1,12).
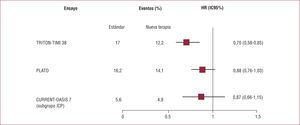
La eficacia relativa del prasugrel, el ticagrelor y las dosis altas de clopidogrel para reducir el riesgo de eventos cardiovasculares tras un SCA en los subgrupos de diabéticos incluidos en estos tres ensayos clínicos se muestra en la figura.
Análisis de las diferentes pautas de tratamiento antiagregante en el subgrupo de pacientes diabéticos (adaptado de Ferreiro et al13). HR: hazard ratio; IC95%: intervalo de confianza del 95%; ICP: intervencionismo coronario percutáneo
En torno a un tercio de los pacientes con SCA atendidos en los hospitales presentan alteraciones de la función renal significativas según los datos de los registros21. También se sabe que la insuficiencia renal crónica (IRC) es un predictor independiente de eventos cardiovasculares, asociada a mayor riesgo hemorrágico en pacientes con SCA22. Por lo tanto, la utilización adecuada de agentes antitrombóticos en pacientes con IRC es con frecuencia un asunto difícil de resolver, y las evidencias científicas en este terreno suelen ser escasas debido en parte a la pobre representación de pacientes con IRC avanzada en los ensayos clínicos sobre SCA.
Las guías europeas y estadounidenses para el manejo de los SCASEST no hacen recomendaciones específicas para el uso de clopidogrel en pacientes con IRC moderada o grave, en quienes el riesgo hemorrágico es mayor2,23. En los estudios que miden la función plaquetaria se muestra que los pacientes con IRC responden peor al clopidogrel, sobre todo aquellos con IRC moderada o grave24. En un análisis post-hoc del estudio CREDO (Clopidogrel for the Reduction of Events During Observation)25, estudio que incluyó a pacientes con o sin SCA tratados mediante ICP, se muestra una reducción significativa en el riesgo de eventos cardiovasculares con clopidogrel frente a placebo en los pacientes con función renal conservada, mientras que este beneficio no se ve en los pacientes con IRC leve (el 10,3 y el 12,8%; p=0,30) o moderada (el 17,8 y el 13,1%; p=0,24), subgrupos en los que, por otro lado, sí se documentó un incremento de sangrados con el clopidogrel. Sin embargo, entre los pacientes del estudio CURE (Clopidogrel in Unstable Angina to Prevent Recurrent Events)26, todos con SCASEST, el tratamiento con clopidogrel sí redujo la tasa de eventos cardiovasculares en comparación con placebo independientemente de que tuvieran IRC o no.
No hay muchos resultados específicamente sobre la eficacia del prasugrel en pacientes con IRC. La cantidad de metabolito activo del prasugrel en pacientes con función renal conservada, disfunción moderada o disfunción grave se analizó en un trabajo, que mostró que los pacientes con IRC de grado alto tienen una concentración del metabolito activo en sangre un 40% menor que los pacientes con función conservada, pero, pese a ello, en este estudio no se observaron diferencias en la inhibición de la agregación plaquetaria entre los tres grupos de pacientes27. En el estudio TRITON-TIMI 3811 se incluyó a 1.490 pacientes (el 10,9% del total) con aclaramiento de creatinina (ACr) < 60ml/min. En este grupo, el beneficio del prasugrel comparado con clopidogrel en la reducción de eventos cardiovasculares no alcanzó diferencias significativas (el 15,1 y el 17,5%). Dado que por el momento no tenemos datos concluyentes sobre la eficacia y la seguridad del prasugrel en la IRC, no existen recomendaciones específicas para su utilización en este tipo de pacientes.
Los beneficios clínicos del ticagrelor para los pacientes con insuficiencia renal sí quedaron demostrados en un análisis de subgrupos preespecificado del estudio PLATO28. En ese ensayo se incluyó a 3.237 pacientes con ACr < 60ml/min (el 21,3% de los 15.202 pacientes con datos de creatinina disponibles). En este subgrupo, el ticagrelor redujo significativamente la incidencia de eventos cardiovasculares (el 17,3 y el 22%; HR:=0,77; IC95%, 0,65–0,90) en comparación con el clopidogrel, y también la mortalidad (el 10 y el 14%; HR=0,72; IC95%, 0,58– 0,89), todo ello sin un incremento significativo en la tasa de sangrados mayores. En términos absolutos, los pacientes con IRC moderada del estudio PLATO presentaron una reducción en la incidencia de eventos cardiovasculares al año de seguimiento del 4,7%, frente a un 1% de los pacientes sin IRC28. Por otro lado, en los estudios de farmacocinética y farmacodinámica realizados con ticagrelor en voluntarios sanos y pacientes con IRC, se observó que las concentraciones circulantes de ticagrelor son hasta un 17% menores en los pacientes con IRC, pero de nuevo estas diferencias no afectaron al grado de inhibición plaquetaria, similar en ambos grupos29.
Estrategia de tratamiento no invasivoA pesar de que las guías de práctica clínica recomiendan una estrategia invasiva sistemáticamente con coronariografía precoz en los pacientes con SCASEST de riesgo moderado o alto, por diversos condicionantes todavía hoy a un número importante de pacientes se los maneja de forma conservadora2,30. En el estudio CURE5, publicado en 2001, se manejó a la mayor parte de los pacientes de forma conservadora (se revascularizó durante el ingreso hospitalario sólo al 21,8%), y sus resultados demostraron claramente el beneficio de la doble antiagregación para los pacientes con SCASEST, independientemente de la estrategia, invasiva o no, elegida para el tratamiento. Con ese estudio, además, se estableció la duración del tratamiento con doble antiagregación en los 12 meses que actualmente se sigue recomendando en las guías de práctica clínica.
En el estudio TRITON-TIMI 3811 se definió como criterio de inclusión la intención de tratamiento invasivo, de tal manera que se incluyó a la mayoría de los pacientes tras conocer la anatomía coronaria y tener decidido revascularizar alguna de las lesiones coronarias. Debido al particular diseño del estudio, por el momento no hay datos sobre el beneficio del prasugrel para los pacientes manejados inicialmente de forma conservadora. La eficacia clínica de este fármaco en pacientes con SCASEST manejados con tratamiento médico se está valorando en el ensayo TRILOGY-SCA31 (Targeted Platelet Inhibition to Clarify the Optimal Strategy to Medically Manage Acute Coronary Syndromes, NCT00699998), cuyos resultados se esperan para finales de 2012.
En el estudio PLATO32, el tratamiento con ticagrelor o clopidogrel se inició precozmente y al margen de la estrategia de manejo terapéutico elegida, de modo que se manejó de manera conservadora sin coronariografía precoz a 5.216 pacientes (28%). En este subgrupo, la incidencia del evento combinado de muerte cardiovascular, infarto de miocardio no fatal o ictus también fue menor entre los pacientes tratados con ticagrelor que entre los tratados con clopidogrel (el 12 y el 14,3%; HR=0,85; IC95%, 0,73–1), y también fue menor la mortalidad con ticagrelor (el 6,1 y el 8,2%; HR=0,75; IC95%, 0,61–0,93), de nuevo todo ello sin un incremento significativo en la incidencia de sangrados mayores (el 11,9 y el 10,3%; HR=1,17; IC95%, 0,98–1,39).
Cirugía de revascularización coronariaLa terapia antiplaquetaria disminuye la tasa de eventos cardiovasculares, incluido el fracaso del injerto, en los pacientes tratados con cirugía de revascularización coronaria (CABG)33. En el caso de la doble terapia antiagregante, este beneficio se ve empañado por un mayor riesgo hemorrágico, sobre todo en el periodo perioperatorio. Por este motivo, la doble antiagregación en pacientes con CABG todavía es un tratamiento controvertido y poco extendido en la práctica habitual34. Un análisis post-hoc del subgrupo de 2.072 pacientes operados con CABG del estudio CURE (el 16,5% del total) mostró una tendencia no significativa a la reducción de eventos cardiovasculares con la doble antiagregación, AAS más clopidogrel, en comparación con AAS solo (el 14,5 y el 16,2%; HR=0,89; IC95%, 0,71–1,11), pero con un exceso en la incidencia de sangrados (el 9,6 y el 7,5%; HR=1,27; IC95%, 0,96–1,69), especialmente entre los pacientes que no suspendieron el clopidogrel con al menos 5 días de antelación a la cirugía35. Por este mayor riesgo de sangrado, en las guías se recomienda interrumpir el clopidogrel al menos 5–7 días antes de la CABG siempre que sea posible2–4.
De nuevo, por el especial diseño del estudio TRITON-TIMI 38, el número de pacientes que requirieron CABG fue bajo (n=422; el 3,1% del total de pacientes del ensayo). Cabe destacar que, aunque el análisis de este subgrupo no estaba preespecificado, la mortalidad a 1 año, una vez corregida por los potenciales factores de confusión, fue menor entre los pacientes tratados con prasugrel que con clopidogrel (el 2,3 y el 8,7%; p=0,016). Por otro lado, la pérdida sanguínea por el drenaje en 12h fue mayor con prasugrel (655±580 y 503±378ml; p=0,050) y también la necesidad de transfusión de plaquetas (el 17,96 y el 9,82%; p=0,033)36.
En el estudio PLATO, el grupo de pacientes que requirieron CABG y recibieron el tratamiento antiplaquetario del estudio en los 7 días previos a la intervención también era pequeño (n=1.261; el 6,8% del total), y en ellos el ticagrelor mostró una reducción no significativa en la incidencia del evento combinado de muerte cardiovascular, infarto de miocardio no fatal e ictus en comparación con el clopidogrel (el 10,6 y el 13,1%; HR=0,84; IC95%, 0,60–1,16) y también una disminución en la mortalidad (el 9,7 y el 4,7%; HR=0,49; IC95%, 0,32–0,77), en este caso sin un incremento significativo en la incidencia de sangrados37. Este beneficio se demostró especialmente entre los pacientes que suspendieron la medicación del estudio entre el segundo y el cuarto día antes de la CABG, mientras que no se objetivaron diferencias en cuanto a la mortalidad si se suspendía el día previo.
En las guías más recientes se recomienda suspender el tratamiento con ticagrelor o clopidogrel, en la medida de lo posible, al menos 5 días antes de la CABG, y con prasugrel al menos 7 días antes2,4, y se aconseja reiniciar el tratamiento con el inhibidor plaquetario tras la CABG tan pronto como sea seguro.
Riesgo hemorrágicoEl principal problema para la utilización de estos nuevos antiplaquetarios es el riesgo de sangrado. En el estudio TRITON-TIMI 38, el uso de prasugrel se asoció a un incremento absoluto en el riesgo de hemorragias mayores según criterios TIMI y no relacionadas con CRC de un 0,6% (el 2,4 y el 1,8%; p=0,03), hemorragias que en su mayoría se observaron en la fase de seguimiento del estudio11. En el estudio PLATO, aunque no se describe un incremento significativo de las hemorragias con ticagrelor cuando se aplica la definición establecida en el estudio (el 11,6 y el 11,2%; p = 0,43), el ticagrelor se asoció también a un incremento absoluto en el riesgo de hemorragias mayores según criterios TIMI no relacionadas con CRC de un 0,6% (el 2,8 y el 2,2%; p = 0,03)12.
Por lo tanto, ambos fármacos deben utilizarse con precaución en pacientes con riesgo hemorrágico elevado. De hecho, para los pacientes con mayor riesgo hemorrágico, las guías recomiendan seguir utilizando clopidogrel en lugar de estos nuevos antiplaquetarios2. Un ejemplo común en la práctica clínica son los pacientes que precisan doble antiagregación y además un tratamiento crónico con anticoagulantes orales, como los pacientes con un SCA y fibrilación auricular o los portadores de prótesis valvulares, pacientes para los que probablemente el clopidogrel siga siendo la opción con mejor balance riesgo/beneficio38.
Enfermedad coronaria crónicaEn las guías clínicas se recomienda mantener la doble antiagregación durante 12 meses tras un SCA o tras una ICP con implantación de un stent recubierto2–4. Esta cuestión sobre la duración del doble tratamiento antiagregante adquirió gran relevancia clínica con el uso extendido de los stents farmacoactivos y tras publicarse en varios estudios observacionales que la interrupción prematura del clopidogrel es un importante factor precipitante de trombosis del stent39. Recientemente se han publicado los resultados de un estudio, con 2.701 pacientes, que evalúa los beneficios de una doble terapia antiplaquetaria con AAS y clopidogrel prolongada más allá de los 12 meses tras un SCA40. En ese trabajo, el tratamiento prolongado con doble antiagregación (media, 19,2 meses) no se tradujo en una reducción significativa de la tasa de eventos cardiovasculares. Estos datos concuerdan con los recientemente comunicados del estudio PRODIGY (PROlonging Dual-antiplatelet treatment after Grading stent-induced Intimal hyperplasia study)41, que comparó una pauta de tratamiento con AAS y clopidogrel durante 6 o 24 meses tras la implantación de un stent recubierto; no se demostraron diferencias significativas entre ambos grupos en cuanto a la incidencia de eventos cardiovasculares, pero sí una mayor tasa de sangrados en el grupo con doble antiagregación prolongada a 24 meses.
En cuanto a la duración del tratamiento con prasugrel o ticagrelor más allá de 12 meses, todavía no hay datos disponibles. A este respecto, se encuentra en marcha el ensayo PEGASUS-TIMI 54 (Prevention of Cardiovascular Events in Patients With Prior Heart Attack Using Ticagrelor Compared to Placebo on a Background of Aspirin, NCT01225562), ensayo que evalúa el beneficio de la doble antiagregación mantenida con AAS y ticagrelor (60 y 90mg dos veces al día), en comparación con AAS solo, para pacientes que han sufrido un infarto agudo de miocardio entre 1 y 3 años antes de la aleatorización y tienen riesgo elevado de sufrir otro (edad ≥ 65 años, diabetes mellitus, nefropatía, enfermedad multivaso o más de un infarto previo).
Otros subgruposTeniendo en cuenta el mayor riesgo hemorrágico asociado a la utilización del prasugrel, en el estudio TRITON-TIMI 38 se realizó una serie de análisis exploratorios post-hoc para identificar los subgrupos con beneficio clínico neto nulo o incluso negativo11. En ese análisis se comprobó la falta de beneficio neto en los pacientes de edad avanzada (≥ 75 años) y en los de bajo peso (< 60kg) y un efecto negativo para los pacientes con antecedentes de ictus o accidente isquémico cerebral transitorio. Por otro lado, un análisis exploratorio similar realizado en los pacientes del estudio PLATO muestra que el ticagrelor sí resulta beneficioso para pacientes mayores de 75 años, pacientes de bajo peso (< 60kg) o con antecedentes de ictus42,43. También debemos tener en cuenta que entre los pacientes del estudio PLATO tratados con ticagrelor se dio mayor incidencia de disnea, pausas ventriculares de más de 3 s o incrementos en las cifras de creatinina y ácido úrico12, por lo que se recomienda utilizar con cautela este fármaco en pacientes con disnea de causa no filiada, bradiarritmias o antecedentes de artritis gotosa.
La tabla resume las indicaciones preferenciales de clopidogrel, prasugrel y ticagrelor en los diferentes subgrupos de pacientes con SCA.
Indicaciones de los fármacos antagonistas del receptor de adenosindifosfato P2Y12 según diferentes subgrupos.
| Clopidogrel | Prasugrel | Ticagrelor | |
| Riesgo bajo | +++ | — | — |
| Riesgo moderado-alto+ | +++ | +++ | |
| Estrategia invasiva | ++ | +++ | +++ |
| Estrategia no invasiva | + | — | +++ |
| SCACEST | + | +++ | ++ |
| SCASEST | +++ | +++ | |
| Trombosis de stent | + | +++ | ++ |
| Diabetes mellitus | + | +++ | ++ |
| Insuficiencia renal | ++ | + | +++ |
| Ictus | ++ | — | + |
| Riesgo hemorrágico elevado | + | — | + |
| Uso de anticoagulación oral | + | — | — |
| Edad > 75 años | +++ | + | +++ |
| Peso < 60kg | ++ | + | +++ |
| CRC | + | — | +++ |
| Disnea | ++ | ++ | — |
| Bradiarritmia | ++ | ++ | — |
| Artritis gotosa | ++ | ++ | — |
—: ausencia de indicación para su uso; +: indicación baja para su uso; ++: indicación moderada para su uso; +++: de elección para su uso; CRC: cirugía de revascularización coronaria; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
Tanto el prasugrel como el ticagrelor se han demostrado más eficaces que el clopidogrel en la reducción de eventos cardiovasculares tras un SCA, aunque ambos con un ligero incremento en el riesgo de sangrados. Teniendo en cuenta la heterogeneidad de presentaciones del SCA, resulta necesario aproximarnos lo más posible a la identificación de los subgrupos en que estos nuevos antiagregantes puedan resultar más eficientes. Así, en el caso de los SCASEST manejados con angioplastia primaria, se considera que ambos fármacos son igualmente beneficiosos, como también lo son en la reducción del riesgo de trombosis del stent. Ambos son igualmente beneficiosos en los pacientes con SCA de moderado o alto riesgo, aunque por el diseño del estudio el prasugrel se recomienda sólo si se conoce la anatomía y la intervención coronaria está decidida, mientras que el ticagrelor se puede administrar a todos los pacientes independientemente de la estrategia de tratamiento elegida. Por otro lado, los análisis de subgrupos muestran que el prasugrel es más beneficioso para los pacientes diabéticos y está contraindicado para quienes tengan antecedentes de ictus, mientras que el ticagrelor es especialmente beneficioso para los pacientes con insuficiencia renal y se puede administrar a los pacientes con ictus previo. Finalmente, para pacientes con SCASEST de bajo riesgo o que precisen tratamiento anticoagulante oral (p. ej., por fibrilación auricular), el clopidogrel continúa siendo una alternativa válida.
Conflicto de interesesA. Fernández-Ortiz: consultorías (Lilly, MSD, Chiesi, Ferrer), presentaciones (Sanofi-Aventis, Bayer, Chiesi, GSK, Astra-Zeneca, Ferrer, Roche, Daiichi-Sankyo, Lilly), formación (GSK, MSD) y becas (Sanofi- Aventis).