La capacidad para responder a los ligandos de toll-like receptors (TLR) puede verse afectada por polimorfismos de un solo nucleótido en genes que codifican TLR. Estudiamos la influencia de los polimorfismos TLR2 (R753Q, R677W), TLR4 (D299G, T399I) y CD14 (C-159T) en 65 pacientes consecutivos con endocarditis infecciosa. El grupo control (n=66) estuvo formado por voluntarios sanos. Todos los polimorfismos fueron genotipados mediante análisis de restricción después de su amplificación. Se observó asociación de endocarditis con variantes de TLR2 R753Q (p<0,001) y no se encontró asociación con otros polimorfismos. Los genotipos TLR2 R753Q, codominantes (odds ratio=13,33), recesivo (odds ratio=9,12) y dominantes (odds ratio=3,65) mostraron asociación positiva con el fenotipo de endocarditis infecciosa. El polimorfismo TLR2 R753Q se asoció a una mayor susceptibilidad a sufrir endocarditis infecciosa. Son necesarios futuros estudios para validar estos resultados e identificar otros factores genéticos de riesgo.
Palabras clave
La incidencia anual de endocarditis oscila entre 15 y 60 casos por millón de habitantes1, 2. El pronóstico es malo y no ha cambiado en las últimas cuatro décadas2. Incluso con tratamiento antibiótico, la tasa de mortalidad es superior al 30% en la mayor parte de los estudios y puede llegar a ser de un 70% en determinados grupos de población de alto riesgo2. El mecanismo patogénico a través del cual se produce la infección del endocardio es multifactorial. Sin embargo, los factores hereditarios e inmunitarios pueden contribuir también a su desarrollo y han sido poco estudiados1, 3.
Los toll-like receptors (TLR) intervienen en el sistema inmunitario innato. Hasta la fecha, se han identificado 11 tipos de TLR que reconocen diferentes componentes antigénicos de los patógenos que se han conservado evolutivamente en clases específicas de microorganismos. Estos antígenos incluyen componentes de la pared celular de bacterias Gram-positivas (lipoproteínas y ácidos lipoteicoicos, detectados por TLR2) y Gram-negativas (lipopolisacárido [LPS], detectado por TLR4). En la identificación del LPS interviene el complejo del receptor de LPS del cual CD14 y TLR4 son componentes fundamentales4.
Los datos existentes indican que la capacidad de ciertos individuos para responder adecuadamente a los ligandos de TLR puede verse afectada por polimorfismos de un solo nucleótido (SNP) en los genes que codifican TLR que den lugar a alteraciones en la susceptibilidad a sufrir infecciones o procesos inflamatorios5. El polimorfismo genético TLR2 R753Q se ha relacionado con variaciones en la respuesta a estafilococo6 y el polimorfismo R677W se ha asociado con un aumento de la susceptibilidad a lepra y tuberculosis en poblaciones asiáticas7. Se han descrito dos mutaciones frecuentes del gen de TLR4: TLR4 D299G y T399I. Estas mutaciones se han relacionado con un aumento del riesgo de infecciones por bacterias Gram-negativas y shock séptico4, 8. Un polimorfismo en la región del promotor del gen CD14 se asocia a un aumento en la prevalencia de infecciones por bacterias Gram-negativas9.
Nuestra hipótesis fue que la presencia de polimorfismos en los genes que codifican estos receptores de la inmunidad innata se podía asociar a un aumento en la prevalencia de endocarditis infecciosa. Analizamos la frecuencia de los polimorfismos TLR2 (R753Q, R677W), TLR4 (D299G, T399I) y CD14 (C-159T) en pacientes con endocarditis infecciosa y en controles sanos.
MétodosPacientes y controlesSe estudió a 65 pacientes (57 varones, 8 mujeres; media±desviación estándar de edad, 63,7±11,9 [intervalo, 32-85] años) diagnosticados consecutivamente de endocarditis infecciosa según los criterios de Duke entre diciembre de 2005 y diciembre de 2008 (flujo de inclusión de pacientes: 2006, 22 pacientes; 2007, 17; 2008, 26). El grupo control (n=66) lo formaron donantes de sangre sanos (55 varones, 11 mujeres; edad, 61,7±10,2 [32-79] años). Los pacientes y los controles formaban parte de una población homogénea; todos ellos eran de raza caucásica y residentes en la misma región (Castilla y León, España). Cada participante dio su consentimiento para participar en el estudio, previamente aprobado por el comité de investigación del hospital.
Preparación del ADN genómico y cuantificaciónSe extrajeron muestras de 2 ml de sangre total en tubos con recubrimiento de ácido etilendiaminotetraacético mediante punción venosa periférica. Se extrajo el ADN genómico de las muestras de sangre total con el uso del MagNA Pure Compact Nucleic Acid Isolation Kit I (Roche; Mannheim, Alemania) siguiendo las instrucciones del fabricante.
Análisis de polimorfismos en los genesTodos los polimorfismos se genotipificaron mediante análisis de restricción tras amplificación mediante la técnica de reacción en cadena de polimerasa (PCR). Se realizaron 35 ciclos de PCR en termociclador (GeneAmp9700, Perkin-Elmer Cetus; Norwalk, Connecticut, Estados Unidos). Se sintetizaron los cebadores (VWR International Eurolab; Barcelona, España). La reacción de PCR consistió en 50 ng de ADN, 10 pm de cada cebador, 10μl de mezcla maestra de PCR (Promega; Madison, Wisconsin, Estados Unidos) y 20μl de agua.
Los cebadores de PCR de TLR2 p.R677W (rs5743706) fueron 5’CAATCCCCCCTTCAAGTTG-3’ y 5’-CAGTTCATACTTGCACCACTC-3’. El programa de termociclado consistió en 94°C durante 30 s, 58°C durante 30 s y 72°C durante 30 s (SsiI, Fermentas; Burlington, Canadá).
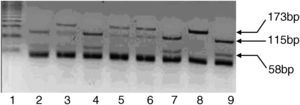
Los cebadores de PCR de TLR2 p.R753Q (rs5743708) fueron 5’-GAAGAGAACAATGATGCTGCCATTC-3’ y 5’CTAGGACTTTATCGCAGCTCTC-3’. El programa de termociclado consistió en 94°C durante 30 s, 49°C durante 30 s y 72°C durante 30 s (SsiI, Fermentas; Burlington, Canadá) (Figura 1).
Figura 1. Migración electroforética del polimorfismo del toll-like receptor 2p.R753Q.
Los cebadores de PCR de TLR4 p.D299G (rs4986790) fueron 5’-ACTTAGACTACTACCTCGGTG-3’ y 5’-GATTTGAGTTTCAATGTGGGAAAC-3’. El programa de termociclado consistió en 94°C durante 30 s, 53°C durante 30 s y 72°C durante 30 s (HphI, Fermentas; Burlington, Canadá).
Los cebadores de PCR de TLR4 p.T399I (rs4986791) fueron 5’-TCTCAAAGTGATTTTGGGACGA-3 y 5’-GTTCTCAAAGTGATTTTGGGAATG-3’. El programa de termociclado consistió en 94°C durante 30 s, 56°C durante 30 s y 72°C durante 30 s (MboI, Fermentas; Burlington, Canadá).
Los cebadores de PCR de CD14 c.-159C>T (rs2569190) fueron 5’-TCACCTCCCCACCTCTCTT-3’ y 5’-CCTGCAGAATCCTTCCTGTT-3’. El programa de termociclado consistió en 94°C durante 30 s, 59°C durante 30 s y 72°C durante 30 s (HaeIII, Roche; Mannheim, Alemania).
Análisis estadísticoTodos los análisis estadísticos se realizaron con el programa SPSS Inc. versión 15.0 (SPSS Inc.; Chicago, Illinois, Estados Unidos). La distribución de los genotipos (TLR2 R677W, TLR2 R753Q, TLR4 D299G, TLR4 T399I y C-159T CD14) se evaluó con el equilibrio de Hardy-Weinberg en pacientes y controles10. Se utilizó la prueba de la t de Student para la comparación de las variables numéricas dentro de un mismo grupo y la correlación de Pearson para la evaluación de la correlación de variables numéricas. Se utilizó la prueba de la χ2 y la prueba exacta de Fisher (cuando fue apropiado) para la comparación de los grupos. Los datos se expresaron en forma de media±desviación estándar y se aceptó como significación estadística un valor de p ≤ 0,05.
Se utilizó regresión logística para estimar el efecto del genotipo TLR2 R753Q en la probabilidad de que un paciente tuviera un fenotipo de endocarditis infecciosa en tres modelos genéticos (recesivo, codominante y dominante), según lo aplicado en estudios previos11.
ResultadosLa endocarditis fue de origen extrahospitalario en 44 pacientes (67,7%), se detectó cardiopatía previa en 39 (60%), se identificó al menos un factor de riesgo en 31 (47,7%) y las enfermedades predisponentes fueron las siguientes: diabetes mellitus, 12 (18,5%); alcoholismo, 6 (9,2%); cáncer, 4 (6,1%); insuficiencia renal crónica, 3 (4,6%), y enfermedad pulmonar obstructiva crónica, 6 (9,2%). Se aislaron gérmenes Gram-positivos como agente causal en 50 (76,9%) pacientes (el 46,1% Staphylococcus y el 30,8% Streptococcus), mientras que el agente etiológico fue un germen Gram-negativo en 5 (7,7%). No se aisló ningún microorganismo en 9 (13,8%) pacientes, y 39 pacientes (60%) requirieron tratamiento quirúrgico; la tasa de mortalidad hospitalaria fue del 30,8% (n=20).
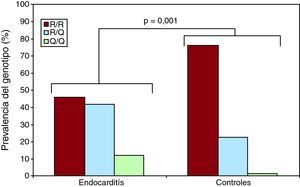
Distribución de genotipos y frecuencias alélicas en pacientes y controlesEn el análisis de los genes (Tabla 1), se observaron asociaciones significativas con endocarditis infecciosa con el TLR2 R753Q tanto para el genotipo (p=0,001) (Figura 2) como para las variantes alélicas (p=0,0001). No se observó asociación alguna con otros polimorfismos. El genotipo y las frecuencias alélicas del polimorfismo TLR2 R753Q fueron similares a las frecuencias observadas por otros grupos en poblaciones caucásicas.
Tabla 1. Distribución de los polimorfismos génicos de toll-like receptor 2 y 4 y CD14 en pacientes con endocarditis y en los controles
| Polimorfismo genético | Frecuencias genotípicas | Endocarditis (n=65) | Controles (n=66) | χ2 de Pearson | p | Frecuencias alélicas | Endocarditis | Controles | OR (IC del 95%) | χ2 | p |
| TLR2 R677W | |||||||||||
| CC | 36 (55,4) | 41 (62,2) | 1,3393 | 0,5119 | C | 95 (73,1) | 104 (78,8) | 0,731 (0,413-1,291) | 1,1696 | 0,2795 | |
| TC | 23 (35,4) | 22 (33,3) | T | 35 (26,9) | 28 (21,2) | ||||||
| TT | 6 (9,2) | 3 (4,5) | |||||||||
| TLR2 R753Q | |||||||||||
| R/R | 30 (46,1) | 50 (75,8) | 13,8662 | 0,001 | R | 87 (66,9) | 115 (87,1) | 0,299 (0,16-0,56) | 15,1335 | 0,0001 | |
| R/Q | 27 (41,6) | 15 (22,7) | Q | 43 (33,1) | 17 (12,9) | ||||||
| Q/Q | 8 (12,3) | 1 (1,5) | |||||||||
| TLR4 D299G | |||||||||||
| D/D | 53 (81,5) | 60 (90,9) | 2,6762 | 0,2624 | D | 117 (90) | 125 (94,7) | 0,504 (0,194-1,307) | 2,049 | 0,152 | |
| D/G | 11 (16,9) | 5 (7,6) | G | 13 (10) | 7 (5,3) | ||||||
| G/G | 1 (1,5) | 1 (1,5) | |||||||||
| TLR4 T399L | |||||||||||
| T/T | 60 (92,3) | 59 (89,4) | 1,0084 | 0,604 | T | 125 (96,2) | 124 (93,9) | 1,613 (0,513-5,066) | 0,6811 | 0,409 | |
| T/I | 5 (7,7) | 6 (9,1) | I | 5 (3,8) | 8 (6,1) | ||||||
| I/I | 0 (0) | 1 (1,5) | |||||||||
| CD14 C-159T | |||||||||||
| C/C | 20 (30,8) | 21 (31,8) | 0,493 | 0,7815 | C | 70 (53,8) | 75 (56,8) | 0,887 (0,545-1,443) | 0,2341 | 0,628 | |
| C/T | 30 (46,1) | 33 (50) | T | 60 (46,2) | 57 (43,2) | ||||||
| T/T | 15 (23,1) | 12 (18,2) | |||||||||
IC: intervalo de confianza; OR: odds ratio; TLR: toll-like receptor.
Los valores expresan n (%).
Figura 2. Prevalencia de los genotipos correspondientes a los grupos de endocarditis y control para el polimorfismo R753Q del toll-like receptor 2.
Se realizaron otros análisis mediante regresión logística para evaluar las variantes significativas de TLR2 R753Q. Realizando el análisis de los tres modelos genéticos, se evaluó el efecto del genotipo de mayor riesgo en comparación con el de menor riesgo y la probabilidad de presentar el fenotipo de endocarditis infecciosa (Tabla 2). Los tres modelos genéticos fueron significativos y el codominante fue el que asociaba mayor riesgo. Para los modelos recesivo y codominante, las odds ratio (OR) para los efectos del genotipo en cuanto a presentar un fenotipo de endocarditis infecciosa fueron de 9,12 y 13,33, respectivamente, mientras que para el modelo dominante fue OR=3,65.
Tabla 2. Análisis de regresión logística de las variantes genéticas de R753Q del toll-like receptor 2 asociadas a la endocarditis infecciosa (todos los pacientes, n=131)
| Variante genética y SNP de referencia | Modelo recesivo | Modelo codominante | Modelo dominante | |||
| OR (IC del 95%) | p | OR (IC del 95%) | p | OR (IC del 95%) | p | |
| TLR2 R753Q | 9,12 (1,11-75,18) | 0,04 a | 13,33 (1,59-111,92) | 0,017 b | 3,65 (1,73-7,69) | 0,001 c |
IC: intervalo de confianza; OR: odds ratio; SNP: polimorfismos de un solo nucleótido; TLR: toll-like receptor.
Se presentan las OR para el genotipo de máximo riesgo en comparación con el genotipo de mínimo riesgo.
El número de pacientes (131) refleja los genotipos disponibles. Se indican a continuación las comparaciones de genotipos específicos.
a Los valores corresponden a la comparación del genotipo QQ con la combinación de los genotipos R/Q y RR.
b Los valores corresponden a la comparación del genotipo QQ con el genotipo RR.
c Los valores corresponden a la comparación de la combinación de los genotipos R/Q y QQ con el genotipo RR.
Este es el primer estudio que muestra que el polimorfismo TLR2 R753Q se asocia a un aumento significativo en el riesgo de sufrir endocarditis infecciosa y que los genotipos codominante, recesivo y dominante se asocian al fenotipo de endocarditis infecciosa.
Se ha descrito que los SNP R677W7 y R753Q8 en el gen que codifica el TLR2 conllevan aumento del riesgo de enfermedades infecciosas.
El polimorfismo R753Q fue identificado por primera vez por Lorenz et al6. Se ha descrito también una asociación positiva con Mycobacterium tuberculosis y con la fiebre reumática aguda causada por bacterias Gram-positivas (Streptococcus betahemolítico)12. Nuestros resultados concuerdan con estudios previos. Sin embargo, en un estudio de 420 pacientes consecutivos con infecciones graves por S. aureus, Moore et al no observaron asociación alguna con este SNP13.
Por lo que respecta al SNP TLR2 R677W, en nuestro estudio no se observaron diferencias en la distribución de los genotipos o los alelos. Esto concuerda con los datos existentes en la literatura, puesto que este polimorfismo sólo se ha identificado en poblaciones asiáticas con lepra lepromatosa, y no en poblaciones caucásicas europeas7.
Los SNP TLR4 D299G y C-159T CD14 muestran una asociación positiva con varias enfermedades infecciosas como el shock séptico causado por gérmenes Gram-negativos4, 8, 9. En nuestro estudio no se observó una correlación positiva con endocarditis infecciosa, probablemente debido a que sólo el 7,7% de los pacientes presentaron endocarditis por Gram-negativos.
En resumen, observamos que el polimorfismo del TLR2 R753Q comporta un aumento en la susceptibilidad a sufrir endocarditis infecciosa. Será necesario reproducir este estudio en grupos de población con características diferentes para demostrar la validez de los resultados e identificar otros factores genéticos asociados que puedan comportar un aumento del riesgo de endocarditis infecciosa, dada la importancia de la variabilidad de la información genética.
FinanciaciónEste trabajo fue financiado por la Gerencia de Salud, Consejería de Sanidad, Junta de Castilla y León [GRS 143/A/07], por Redes Temáticas, RD06/0001/0020 y por la Obra Social Caja Burgos.
Conflicto de interesesNinguno.
Recibido 20 Diciembre 2010
Aceptado 20 Febrero 2011
Autor para correspondencia: Servicio de Cirugía Cardiaca, Instituto de Ciencias del Corazón (ICICOR), Hospital Clínico Universitario de Valladolid, Ramón y Cajal 3, 47005 Valladolid, España. jbustamantemunguira@gmail.com