Las fístulas coronarias congénitas son una cardiopatía poco frecuente que, dejada a su evolución, puede producir clínica de hipertensión pulmonar e insuficiencia cardíaca e isquemia miocárdica, aunque en un porcentaje no despreciable pueden cerrarse espontáneamente. Además, son posibles las complicaciones por endocarditis, rotura, aneurisma o trombosis. Los pacientes afectados están en su gran mayoría asintomáticos y los métodos usualmente empleados para su detección son la ecocardiografía-Doppler y la angiografía. Presentamos el caso de un varón de 10 años, asintomático, remitido para estudio de soplo cardíaco, con tres fístulas, dos de ellas originadas en la arteria coronaria izquierda que drenaban al ventrículo derecho, y otra con origen en coronaria derecha y drenaje en la arteria pulmonar.
Palabras clave
Cardiopatías congénitas
Fístula
Ecocardiografía
INTRODUCCIÓN
La fístula coronaria congénita es una anomalía relativamente inusual consistente en la comunicación entre una o ambas arterias coronarias y uno de los vasos (arterias o venas) o bien una cámara cardíaca. La mayoría drenan al ventrículo derecho, aurícula derecha, arteria pulmonar o seno coronario, siendo menos frecuente que lo hagan al ventrículo izquierdo y la aurícula izquierda.
Estos enfermos pueden presentar isquemia miocárdica provocada por el efecto de robo o bien desarrollar hipertensión pulmonar e insuficiencia cardíaca congestiva si se produce un cortocircuito de considerable magnitud, rotura o trombosis de la fístula, aneurisma de la misma y endocarditis infecciosa.
La gran mayoría de los pacientes con esta malformación suelen estar asintomáticos y habitualmente son motivo de estudio por soplo cardíaco. El electrocardiograma y la radiografía de tórax suelen ser normales aunque, en ocasiones, se observan signos de isquemia miocárdica o agrandamiento de alguna cavidad cardíaca. El estudio ecocardiográfico pone de manifiesto a menudo arterias coronarias aumentadas de tamaño, y el Doppler color ayuda a localizar el punto de entrada y salida de la fístula, además de su trayecto. La angiografía practicada con balón de oclusión en la raíz aórtica, con el fin de visualizar las coronarias, permite identificar las características anatómicas del trayecto fistuloso y puede incluso proporcionar el tratamiento si el mismo es susceptible de cierre por embolización percutánea 1,2.
CASO CLÍNICO
Varón de 10 años de edad remitido por el servicio de pediatría para estudio de soplo cardíaco. Éste ya se conocía desde los 4-5 años de edad y era continuo, de intensidad III/VI y más audible en el borde esternal izquierdo bajo. En el electrocardiograma no se apreciaban alteraciones y el niño, por lo demás, se encontraba asintomático e incluso practicaba actividades deportivas de una forma semicompetitiva. El estudio ecocardiográfico puso de manifiesto un ventrículo izquierdo de tamaño normal (43 mm de diámetro telediastólico), con fracción de acortamiento de 38%, grosor de paredes normales, ventrículo derecho de tamaño (20 mm de diámetro telediastólico) y función normales, tamaños de aurícula izquierda y de raíz aórtica también normales. Las válvulas cardíacas tenían una estructura y una movilidad normales y no se detectaban regurgitaciones valvulares patológicas. Tanto la coronaria derecha proximal como el tronco común de la coronaria izquierda se encontraban dilatados (9 y 8 mm, respectivamente) (fig. 2A). De la coronaria derecha se originaba un trayecto fistuloso de 7 mm de diámetro que discurría de manera transversal por delante de la aorta ascendente, hasta abocar al tronco de la arteria pulmonar, inmediatamente por debajo de la válvula pulmonar (figs. 1A y B). La técnica de Doppler color detectaba un flujo predominantemente diastólico a lo largo de toda la fístula, facilitando la delimitación de la misma (fig. 1C). Desde la arteria coronaria izquierda se originaban dos trayectos fistulosos, de 7 mm de diámetro máximo cada uno, con múltiples ramificaciones que drenaban al ventrículo derecho (figs. 2A y B y 3A y B), siendo también fundamental el Doppler color para su diagnóstico definitivo.
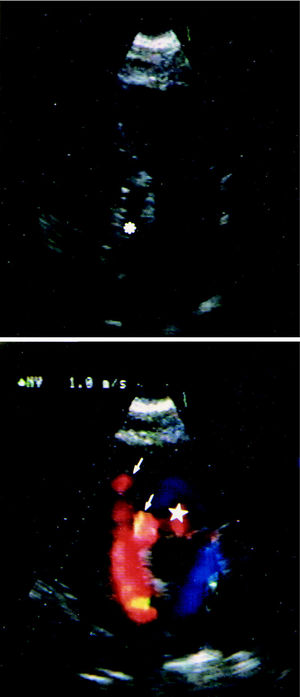
Fig. 3. A: ecocardiograma bidimensional, plano paraesternal transversal alto congelado en diástole, ligeramente modificado para apreciar un trayecto fistuloso (asterisco) también originado en la arteria coronaria izquierda, que discurre paralelo al lado derecho del tronco de la arteria pulmonar para abocar al tracto de salida del ventrículo derecho. B: por Doppler color se delimita mejor la fístula y sus abocaduras múltiples (flechas) por delante de la válvula pulmonar. Se aprecia también el flujo de regurgitación pulmonar ligera fisiológica (estrella).
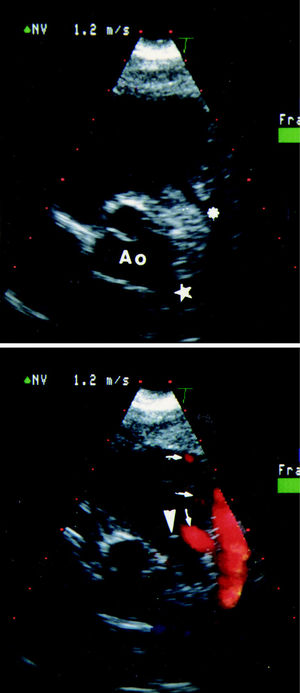
Fig. 2. A: ecocardiograma bidimensional, plano paraesternal transversal alto congelado en diástole, ligeramente modificado para observar el trayecto fistuloso (asterisco) originado en una arteria coronaria izquierda dilatada (estrella) y dirigido hacia adelante para abocar al tracto de salida del ventrículo derecho. B: por Doppler color se aprecia el flujo de la fístula codificado en rojo y sus abocaduras múltiples (flechas) inmediatamente por delante de la válvula pulmonar (punta de flecha). Ao: raíz aórtica.
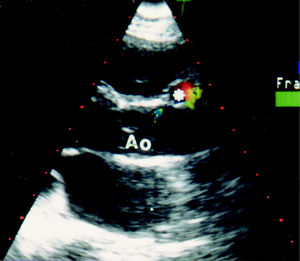
Fig. 1. Ecocardiograma bidimensional. A: plano paraesternal longitudinal en el que se detecta un trayecto fistuloso circular inmediatamente por delante de la aorta ascendente (asterisco), con flujo codificado en color en su interior. B y C: plano paraesternal transversal alto congelado en diástole, en el que se observa la fístula (asterisco) abocando al tronco de la arteria pulmonar inmediatamente por debajo de la válvula pulmonar (punta de flecha). Por Doppler color se delimita mejor el trayecto fistuloso originado en la arteria coronaria derecha, al observarse un flujo codificado en rojo (porción inicial) y azul (resto del trayecto). Ao: raíz aórtica.
DISCUSIÓN
La técnica de Doppler ha incrementado de manera considerable la posibilidad de detectar fístulas coronarias que previamente pasaban desapercibidas y que sólo se podían diagnosticar mediante un estudio angiográfico, indicado por un alto índice de sospecha o por otra causa distinta a la propia fístula 3.
Habitualmente las fístulas coronarias congénitas detectadas por ecocardiografía-Doppler en sujetos asintomáticos pueden ser objeto de seguimiento periódico sin conductas invasivas. Una de las evidencias que apoyan este tipo de estrategia es la proporción no despreciable de cierre espontáneo de las mismas 4-6. En este sentido, Sherwood et al 4, en su estudio sobre la significación clínica de las fístulas coronarias silentes halladas de forma casual mediante ecocardiografía-Doppler, objetivaron su cierre espontáneo en 7 de los 31 pacientes incluidos (23%), uno de los cuales presentaba una fístula bilateral y una relación de flujo pulmonar-sistémico de 1,7. Otros 23 enfermos permanecían asintomáticos, sin ningún tipo de intervención, al final del seguimiento. Según estos datos, se recomienda realizar un seguimiento periódico de las fístulas coronarias congénitas asintomáticas, ya que cualquier intervención para su cierre no está exenta de un incremento en el riesgo de morbilidad y no se ha demostrado un claro beneficio con este proceder 4-6.
Estos hallazgos están en la línea de los obtenidos por Hobbs et al 5, quienes no encontraron nuevos efectos adversos entre los 101 pacientes adultos con fístulas coronarias detectadas en la angiografía y que fueron objeto de seguimiento clínico durante 11 años.
En algunos trabajos 7,8, uno de los hallazgos que distinguió a los pacientes asintomáticos de los sintomáticos fue el origen del trayecto fistuloso, de forma que la mayoría de los casos sintomáticos se originaban de la coronaria derecha y más del 90% drenaban en las cavidades derechas, siendo el ventrículo derecho el destino más frecuente, seguido por la aurícula derecha y el tronco de la arteria pulmonar. Por el contrario, entre los pacientes asintomáticos se ha encontrado una mayor incidencia de fístulas originadas en la arteria coronaria izquierda 4,7,8.
En los enfermos sintomáticos se recomienda generalmente la intervención quirúrgica mediante ligadura epicárdica o endocárdica del vaso anómalo 1,2. No obstante, diversos estudios ponen de manifiesto que es posible efectuar un tratamiento corrector mediante la embolización con coil transcatéter percutáneo 9-13.
El caso que presentamos constituye uno de los raros ejemplos de fístula coronaria bilateral. Igualmente infrecuente es su drenaje, que demostró múltiples orificios de abocadura al ventrículo derecho para las fístulas procedentes de la arteria coronaria izquierda y un orificio de drenaje único en el tronco de la arteria pulmonar para la originada en la coronaria derecha.
Un análisis exhaustivo de la literatura científica, que comprende 119 casos de fístula coronaria congénita, indica que 64 (54%) tenían su origen en la coronaria izquierda, 45 (38%) en la coronaria derecha y 10 (8%), en ambas. Por lo que respecta al drenaje, 42 (35%) abocaban al ventrículo derecho, 27 (23%) lo hacían a la aurícula derecha, 37 (31%) drenaban en la arteria pulmonar y 11 (8%) en el ventrículo izquierdo 2,4,9,14-16.
En la actualidad nuestro paciente es objeto de seguimiento periódico y se encuentra clínicamente asintomático. Debido al potencial riesgo de endocarditis infecciosa 17, se le recomendó la conveniencia de efectuar profilaxis antibiótica.
La fístula coronaria congénita es una anomalía relativamente inusual consistente en la comunicación entre una o ambas arterias coronarias y uno de los vasos (arterias o venas) o bien una cámara cardíaca. La mayoría drenan al ventrículo derecho, aurícula derecha, arteria pulmonar o seno coronario, siendo menos frecuente que lo hagan al ventrículo izquierdo y la aurícula izquierda.
Estos enfermos pueden presentar isquemia miocárdica provocada por el efecto de robo o bien desarrollar hipertensión pulmonar e insuficiencia cardíaca congestiva si se produce un cortocircuito de considerable magnitud, rotura o trombosis de la fístula, aneurisma de la misma y endocarditis infecciosa.
La gran mayoría de los pacientes con esta malformación suelen estar asintomáticos y habitualmente son motivo de estudio por soplo cardíaco. El electrocardiograma y la radiografía de tórax suelen ser normales aunque, en ocasiones, se observan signos de isquemia miocárdica o agrandamiento de alguna cavidad cardíaca. El estudio ecocardiográfico pone de manifiesto a menudo arterias coronarias aumentadas de tamaño, y el Doppler color ayuda a localizar el punto de entrada y salida de la fístula, además de su trayecto. La angiografía practicada con balón de oclusión en la raíz aórtica, con el fin de visualizar las coronarias, permite identificar las características anatómicas del trayecto fistuloso y puede incluso proporcionar el tratamiento si el mismo es susceptible de cierre por embolización percutánea 1,2.
CASO CLÍNICO
Varón de 10 años de edad remitido por el servicio de pediatría para estudio de soplo cardíaco. Éste ya se conocía desde los 4-5 años de edad y era continuo, de intensidad III/VI y más audible en el borde esternal izquierdo bajo. En el electrocardiograma no se apreciaban alteraciones y el niño, por lo demás, se encontraba asintomático e incluso practicaba actividades deportivas de una forma semicompetitiva. El estudio ecocardiográfico puso de manifiesto un ventrículo izquierdo de tamaño normal (43 mm de diámetro telediastólico), con fracción de acortamiento de 38%, grosor de paredes normales, ventrículo derecho de tamaño (20 mm de diámetro telediastólico) y función normales, tamaños de aurícula izquierda y de raíz aórtica también normales. Las válvulas cardíacas tenían una estructura y una movilidad normales y no se detectaban regurgitaciones valvulares patológicas. Tanto la coronaria derecha proximal como el tronco común de la coronaria izquierda se encontraban dilatados (9 y 8 mm, respectivamente) (fig. 2A). De la coronaria derecha se originaba un trayecto fistuloso de 7 mm de diámetro que discurría de manera transversal por delante de la aorta ascendente, hasta abocar al tronco de la arteria pulmonar, inmediatamente por debajo de la válvula pulmonar (figs. 1A y B). La técnica de Doppler color detectaba un flujo predominantemente diastólico a lo largo de toda la fístula, facilitando la delimitación de la misma (fig. 1C). Desde la arteria coronaria izquierda se originaban dos trayectos fistulosos, de 7 mm de diámetro máximo cada uno, con múltiples ramificaciones que drenaban al ventrículo derecho (figs. 2A y B y 3A y B), siendo también fundamental el Doppler color para su diagnóstico definitivo.
Fig. 3. A: ecocardiograma bidimensional, plano paraesternal transversal alto congelado en diástole, ligeramente modificado para apreciar un trayecto fistuloso (asterisco) también originado en la arteria coronaria izquierda, que discurre paralelo al lado derecho del tronco de la arteria pulmonar para abocar al tracto de salida del ventrículo derecho. B: por Doppler color se delimita mejor la fístula y sus abocaduras múltiples (flechas) por delante de la válvula pulmonar. Se aprecia también el flujo de regurgitación pulmonar ligera fisiológica (estrella).
Fig. 2. A: ecocardiograma bidimensional, plano paraesternal transversal alto congelado en diástole, ligeramente modificado para observar el trayecto fistuloso (asterisco) originado en una arteria coronaria izquierda dilatada (estrella) y dirigido hacia adelante para abocar al tracto de salida del ventrículo derecho. B: por Doppler color se aprecia el flujo de la fístula codificado en rojo y sus abocaduras múltiples (flechas) inmediatamente por delante de la válvula pulmonar (punta de flecha). Ao: raíz aórtica.
Fig. 1. Ecocardiograma bidimensional. A: plano paraesternal longitudinal en el que se detecta un trayecto fistuloso circular inmediatamente por delante de la aorta ascendente (asterisco), con flujo codificado en color en su interior. B y C: plano paraesternal transversal alto congelado en diástole, en el que se observa la fístula (asterisco) abocando al tronco de la arteria pulmonar inmediatamente por debajo de la válvula pulmonar (punta de flecha). Por Doppler color se delimita mejor el trayecto fistuloso originado en la arteria coronaria derecha, al observarse un flujo codificado en rojo (porción inicial) y azul (resto del trayecto). Ao: raíz aórtica.
DISCUSIÓN
La técnica de Doppler ha incrementado de manera considerable la posibilidad de detectar fístulas coronarias que previamente pasaban desapercibidas y que sólo se podían diagnosticar mediante un estudio angiográfico, indicado por un alto índice de sospecha o por otra causa distinta a la propia fístula 3.
Habitualmente las fístulas coronarias congénitas detectadas por ecocardiografía-Doppler en sujetos asintomáticos pueden ser objeto de seguimiento periódico sin conductas invasivas. Una de las evidencias que apoyan este tipo de estrategia es la proporción no despreciable de cierre espontáneo de las mismas 4-6. En este sentido, Sherwood et al 4, en su estudio sobre la significación clínica de las fístulas coronarias silentes halladas de forma casual mediante ecocardiografía-Doppler, objetivaron su cierre espontáneo en 7 de los 31 pacientes incluidos (23%), uno de los cuales presentaba una fístula bilateral y una relación de flujo pulmonar-sistémico de 1,7. Otros 23 enfermos permanecían asintomáticos, sin ningún tipo de intervención, al final del seguimiento. Según estos datos, se recomienda realizar un seguimiento periódico de las fístulas coronarias congénitas asintomáticas, ya que cualquier intervención para su cierre no está exenta de un incremento en el riesgo de morbilidad y no se ha demostrado un claro beneficio con este proceder 4-6.
Estos hallazgos están en la línea de los obtenidos por Hobbs et al 5, quienes no encontraron nuevos efectos adversos entre los 101 pacientes adultos con fístulas coronarias detectadas en la angiografía y que fueron objeto de seguimiento clínico durante 11 años.
En algunos trabajos 7,8, uno de los hallazgos que distinguió a los pacientes asintomáticos de los sintomáticos fue el origen del trayecto fistuloso, de forma que la mayoría de los casos sintomáticos se originaban de la coronaria derecha y más del 90% drenaban en las cavidades derechas, siendo el ventrículo derecho el destino más frecuente, seguido por la aurícula derecha y el tronco de la arteria pulmonar. Por el contrario, entre los pacientes asintomáticos se ha encontrado una mayor incidencia de fístulas originadas en la arteria coronaria izquierda 4,7,8.
En los enfermos sintomáticos se recomienda generalmente la intervención quirúrgica mediante ligadura epicárdica o endocárdica del vaso anómalo 1,2. No obstante, diversos estudios ponen de manifiesto que es posible efectuar un tratamiento corrector mediante la embolización con coil transcatéter percutáneo 9-13.
El caso que presentamos constituye uno de los raros ejemplos de fístula coronaria bilateral. Igualmente infrecuente es su drenaje, que demostró múltiples orificios de abocadura al ventrículo derecho para las fístulas procedentes de la arteria coronaria izquierda y un orificio de drenaje único en el tronco de la arteria pulmonar para la originada en la coronaria derecha.
Un análisis exhaustivo de la literatura científica, que comprende 119 casos de fístula coronaria congénita, indica que 64 (54%) tenían su origen en la coronaria izquierda, 45 (38%) en la coronaria derecha y 10 (8%), en ambas. Por lo que respecta al drenaje, 42 (35%) abocaban al ventrículo derecho, 27 (23%) lo hacían a la aurícula derecha, 37 (31%) drenaban en la arteria pulmonar y 11 (8%) en el ventrículo izquierdo 2,4,9,14-16.
En la actualidad nuestro paciente es objeto de seguimiento periódico y se encuentra clínicamente asintomático. Debido al potencial riesgo de endocarditis infecciosa 17, se le recomendó la conveniencia de efectuar profilaxis antibiótica.
Bibliografía
[1]
Congenital heart disease in infancy and childhood. En: Braunwald E, editor. Heart disease. Filadelfia: WB Saunders Company, 1997; 908-909.
[2]
Congenital coronary artery fistula in infancy and childhood: diagnostic and therapeutic aspects. Thorac Cardiovasc Surg 1997; 45: 287-294.
[3]
Congenital coronary artery fistula: diagnosis by two-dimensional Doppler echocardiography. Am Heart J 1990; 120: 1244-1248.
[4]
Prognostic significance of clinically silent coronary artery fistulas. Am J Cardiol 1999; 83: 407-411.
[5]
Coronary artery fistulae: a ten-year review. Clev Clin Q 1982; 49: 191-197.
[6]
Spontaneous near closure artery fistula: Doppler echocardiographic findings. Acta Paediatr Jpn 1991; 22: 389-393.
[7]
Coronary artery fistula: an abnormality affecting all age groups. Medicine 1990; 69: 101-113.
[8]
Congenital coronary artery fistulae: six new cases with a collective review. Clin Radiol 1980; 31: 301-311.
[9]
Coronary artery fistulas in infants and children: a surgical review and discussion of coil embolization. Ann Thorac Surg 1997; 63: 1235-1242.
[10]
Congenital coronary fistulas in children and adults: diagnosis, surgical technique and results. Cardiology 1996; 87: 325-330.
[11]
Succesful embolization of coronary arteriovenous fistula using an interlocking detachable coil. Pediatr Cardiol 1997; 18: 152-155.
[12]
Transcatheter embolization of coronary artery fistula with controlled release coils. J Paediatr Child Health 1996; 32: 542-544.
[13]
Fístula coronaria congénita a ventrículo derecho. Tratamiento mediante embolización transcatéter con coils. Rev Esp Cardiol 1999; 52: 526-528.
[14]
Congenital coronary artery fistula: a report of 24 patients. J Med Assoc Thai 1996; 79: 630-634.
[15]
Doppler echocardiographic features of coronary artery fistula: report of 8 cases. J Am Soc Echocardiogr 1999; 12: 149-154.
[16]
Coronary artery fistula in children and adults: a review of 25 cases with long-term observations. Int J Cardiol 1997; 58: 47-53.
[17]
Endocarditis of the tricuspid valve associated with congenital coronary arteriovenous fistula. Br Heart J 1993; 70: 276-278.