La cardio-oncología es un campo en crecimiento que abarca el diagnóstico y el tratamiento de las enfermedades cardiovasculares (ECV) de los pacientes con cáncer y se centra en especial en la toxicidad cardiovascular relacionada con el tratamiento del cáncer (TCV-RTC). La Sociedad Europea de Cardiología (ESC) ha presentado recientemente su primera guía sobre cardio-oncología1. Toda la información contenida en esta nueva guía es muy esperada y pertinente: es útil, está presentada de una forma excelente y tendrá una repercusión importante en el tratamiento de los pacientes oncohematológicos en los que se utilizan tratamientos antitumorales de posible toxicidad cardiaca.
En consonancia con todas las guías de la ESC, el documento se elaboró en colaboración con otras sociedades internacionales relacionadas con el tema y siguiendo un protocolo estricto para la revisión de la literatura, las recomendaciones y la evidencia que las respalda. Se llevó a cabo una revisión rigurosa de cada uno de los temas, si bien, dada la escasez de evidencia publicada en el campo de la cardio-oncología, el 76% de las recomendaciones tienen un nivel de evidencia C, lo cual resalta la necesidad de una investigación continua. Es de destacar que el documento es largo, con 133 páginas y 272 nuevas recomendaciones que implican una colaboración multidisciplinaria y la disponibilidad de recursos, lo cual hace que puedan ser difíciles de aplicar, en especial en centros que están iniciando su actividad clínica en cardio-oncología. En consecuencia, es importante examinar cuidadosamente la guía e identificar las recomendaciones que pueden aplicarse de manera realista en España y proporcionarán el máximo beneficio a nuestros pacientes con cáncer.
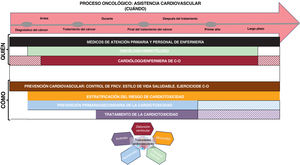
Este comentario tiene como finalidad aportar un análisis detallado de cada uno de los apartados de la guía ESC 2022 sobre cardio-oncología y profundizar en las posibles estrategias para aplicar las recomendaciones en nuestro sistema sanitario. En la tabla 1 se resumen los principales aspectos positivos, los controvertidos y las consideraciones locales, mientras que en la figura 1 se presenta el enfoque general en todo el espectro de la asistencia cardiovascular a esos pacientes.
Principales aspectos positivos y controvertidos y consideraciones locales
| Positivos | Controvertidos | Consideraciones locales | |
|---|---|---|---|
| Definiciones de la toxicidad cardiovascular relacionada con el tratamiento del cáncer | Criterios universales y unificados de toxicidad cardiovascular basados en las definiciones de la IC-OS | Diferencias probables (desconocidas) con la clasificación CTCAE (versión 6.0, de próxima aparición), comúnmente utilizada en oncología | Debe fomentarse la formación básica en cardio-oncología en todos los niveles d asistenciales |
| Estratificación del riesgo de toxicidad cardiovascular antes del tratamiento oncológico | Estratificación del riesgo basada en los trastornos del paciente y el tratamiento oncológico (proformas de HFA-IC-OS)La aplicación online lo facilita | Algunas exploraciones recomendadas (ecocardiografía tridimensional, RMC, PECP) no son una práctica clínica habitual | Modificación sustancial de los protocolos de monitorización actualmente utilizados en los hospitales españoles |
| Prevención y monitorización de las complicaciones cardiovasculares durante el tratamiento del cáncer | Las pautas de monitorización que incluyen técnicas de imagen cardiacas y biomarcadores cardiacos se proporcionan en función del riesgo inicial y de los tratamientos específicosRecomendaciones para la prevención primaria (aceptando una evidencia menor) y secundaria | La mayoría de los centros no disponen de recursos suficientes para aplicar todas las recomendacionesEl examen de detección sistemática inicial de la EC en los pacientes asintomáticos es una medida controvertidaDiscrepancias en los resultados obtenidos con las estatinas como prevención primaria | El dexrazoxano no está disponible en la mayoría de los centros de EspañaEs necesario aumentar los recursos humanos y materiales en cada centro para garantizar una asistencia cardiovascular rápida y de alta calidad |
| Diagnóstico y tratamiento de la toxicidad aguda y subaguda de los pacientes en tratamiento oncológico | Tratamiento de las principales complicaciones cardiovascularesAlgunas nuevas recomendaciones específicas, como en el caso de la miocarditis relacionada con los ICIOrganizar un EMD para la toma de las decisiones clave, como interrumpir el tratamiento o continuarlo | Hay umbrales diferentes (y numerosos) para el tratamiento de la hipertensiónIncidencia muy baja con la reexposición a determinados fármacos después de la cardiotoxicidad | Proponer la inclusión de la cardio-oncología en los comités de tumoresEMD para el tratamiento de la cardiotoxicidad y otras toxicidades también en el contexto agudo, es decir, miocarditis por ICI |
| Evaluación del riesgo cardiovascular al final del tratamiento del cáncer | En el primer año después del final del tratamiento, revaluar el riesgo de complicaciones futurasEvaluar la FCR y recomendar el ejercicio para mantener la mejor capacidad funcional posible | Carencia de enfermería en cardio-oncología para la formación sanitaria y la atención al estilo de vida saludableSuspensión de los fármacos para la IC al final del tratamiento oncológico de los pacientes que hayan tenido una cardiotoxicidad leve o moderada en el seguimiento y se hayan recuperado por completoEn muchos centros no se dispone de PECP para evaluar la FCR | La coordinación con atención primaria puede facilitar la evaluación, realizando en el hospital solo la ecocardiografía cuando esté indicadaVigilancia estricta coordinada con atención primaria si se suspende el tratamientoLa FCR podría evaluarse con actividades más sencillas cuando no se disponga de PECP |
| Seguimiento a largo plazo y complicaciones cardiovasculares crónicas de los pacientes que sobreviven al cáncer | Clasificación del riesgo específica para los pacientes que han presentado un proceso oncohematológico durante su infancia o juventud (riesgo de DCRTC) o en la edad adulta (principalmente ateroesclerosis) | Los supervivientes a largo plazo actuales pueden diferir de los que habrá en el futuro, con nuevos fármacos y nuevos equipos de radioterapia | El control de los factores de riesgo cardiovascular puede llevarse a cabo correctamente con el programa SEC-PrimariaLa cardiología debería aplicar las técnicas de imagen recomendadas para la detección sistemática como mínimo en los pacientes de alto riesgo |
| Grupos de población especiales | En este apartado se incluyen los tumores cardiacos, los carcinoides y la amiloidosis AL cardiacaLa inclusión de un apartado sobre el embarazo es algo muy positivo, dada la complejidad del problema | Es importante definir el seguimiento compartido de estas entidades, sin limitarse a la cardiotoxicidad | Una unidad de embarazos de alto riesgo debe incluir los antecedentes de cáncer y de su tratamiento para una evaluación cardiológica |
| Información al paciente, comunicación y autocuidado | La guía resalta la importancia del equipo multidisciplinario, la comunicación y la participación del paciente en la gestión del tratamiento | En este apartado, demasiado breve, no se especifica el papel fundamental de la enfermería en cardio-oncología | En el documento de consenso de la SEC de 2021, el personal de enfermería desempeña un papel fundamental en la prevención de la cardiotoxicidad y la formación sanitaria de los pacientes con cáncerLas intervenciones a distancia podrían ser un buen instrumento para la formación sanitaria y el seguimiento de estos pacientes |
| Función de las sociedades científicas en la promoción y el desarrollo de la cardio-oncología en la medicina moderna | El documento se ha elaborado en colaboración con otras sociedades internacionalesEl plan estratégico y la misión de ESC-CCO incluyen la mejora de la prevención, el diagnóstico y el tratamiento de la TCV-RTC y las mejoras de la calidad de la asistencia habitual de los pacientes con cáncer | Se echa en falta la participación de la ESMO como sociedad, si bien algunos de sus miembros destacados han colaborado en la redacción de la guía | Todas las sociedades de España (médicas, de enfermería y de la población general) que tienen interés en este campo han colaborado en la elaboración del documento de consenso de la SEC de 2021En la SEC hay un Grupo de Trabajo sobre Cardio-Oncología, muy activo, que organiza cursos de formación y ha publicado varios documentos en estrecha colaboración con otras sociedades |
| Mensajes clave | La mayor parte de las recomendaciones se resumen en 14 mensajes clave | No todos ellos son fáciles de llevar a la práctica | Los centros con pacientes con cáncer deben intentar organizar la asistencia de cardio-oncología adaptada a sus capacidades locales |
| Necesidades futuras | Hay 12 estrategias y áreas de investigación que se consideran prioritarias | Es posible que algunos de los aspectos controvertidos puedan esclarecerse si se resuelven estas necesidades | Los centros con experiencia y los de nueva creación deben colaborar en ensayos clínicos y encuestas y deben fomentar los avances en cardio-oncología |
| Lagunas en la evidencia | Las principales lagunas existentes se agrupan en 5 apartados que abordan aspectos de interés en los que es necesaria una mejora de la asistencia en cardio-oncología | Algunas de las lagunas ya se habían identificado como aspectos controvertidos anteriormente | Cada cual tiene la responsabilidad de intentar cubrir estas lagunas |
| Mensajes sobre «qué hacer» y «qué no» basados en la guía | El texto incluye más de 150 recomendaciones de clase I y solamente 5 de clase III para resolver las cuestiones principales | Solo 5 de estas recomendaciones tienen un nivel de evidencia A | La mayoría de los centros de España no podrán seguir todas las recomendaciones de clase I, debido a la falta de recursos y tiempo |
| Indicadores de la calidad en cardio-oncología | Hay una necesidad de medir y notificar la calidad y los resultados de la asistencia cardiovascular también en el ámbito de la cardio-oncologíaLos indicadores de calidad, junto con sus especificaciones de medición y el proceso de elaboración se publicarán por separado | En el momento de redactar este comentario, los indicadores de calidad no se han publicado todavía y no se puede determinar si son realistas | En España, el programa INCARDIO llevado a cabo por la SEC puede ayudar a definir indicadores de calidad específicos para la asistencia de cardio-oncología |
3D: tridimensional; CTCEA: criterios terminológicos comunes de eventos adversos; DCRTC: disfunción cardiaca relacionada con el tratamiento del cáncer; EC: enfermedad coronaria; EMD: equipo multidisciplinario; ESC-CCO: Sociedad Europea de Cardiología-Council of Cardio-Oncology; ESMO: European Society for Medical Oncology; FCR: forma física cardiorrespiratoria; HFA: ESC-Heart Failure Association; ICI: inhibidores del punto de control inmunitario; IC-OS: International Cardio-Oncology Society; PECP: prueba de estrés de ejercicio cardiorrespiratorio; RMC: resonancia magnética cardiaca; SEC: Sociedad Española de Cardiología; TCV-RTC: toxicidad cardiovascular relacionada con el tratamiento del cáncer.
Las complicaciones cardiovasculares secundarias a los tratamientos oncológicos pueden tener una forma de presentación clínica diferente de la que tiene la ECV en la población general, y su diagnóstico es crucial para reducir al mínimo las interrupciones de los tratamientos del cáncer. Por este motivo, se recomienda vivamente estandarizar las definiciones de los diferentes eventos adversos cardiovasculares. Entre ellos se encuentran la disfunción ventricular, la toxicidad vascular, la miocarditis, la hipertensión arterial o el intervalo QT prolongado, entre otros. El empleo de unos criterios diagnósticos universales para la TCV-RTC tendrá repercusiones importantes en el diagnóstico, el tratamiento y el seguimiento de estos pacientes, así como en la investigación futura y en los ensayos clínicos, que son esenciales en esta población. La nueva guía de la ESC sobre cardio-oncología confirma la nueva clasificación de la toxicidad cardiaca publicada en 2022 en forma de un documento de consenso de la International Cardio-Oncology Society (IC-OS)2.
En nuestra práctica clínica, estos criterios deberían aplicarse para el diagnóstico clínico, y también deberíamos utilizar estas definiciones en nuestros informes médicos. La guía sobre cardio-oncología fomenta el uso de esta clasificación y la pone a disposición de otros especialistas que también tratan a pacientes con cáncer.
ESTRATIFICACIÓN DEL RIESGO ANTES DEL TRATAMIENTO ONCOLÓGICOLa guía sobre cardio-oncología divide la asistencia cardiovascular de los pacientes con cáncer en función de la cronología: antes, durante y después del tratamiento del cáncer. En la primera etapa, los principales factores que deben tener en cuenta los oncólogos y los hematólogos antes del tratamiento son la estratificación del riesgo cardiovascular y la prevención de la cardiotoxicidad.
Se recomienda evaluar el riesgo de toxicidad cardiovascular y de cardiotoxicidad antes del tratamiento de todos los pacientes con cáncer utilizando las proformas de evaluación del riesgo inicial de HFA-ICOS3. Estas puntuaciones se adaptan para cada tipo de tratamiento del cáncer e incluyen la información sobre ECV previa, técnicas de imagen, biomarcadores, edad y factores de riesgo cardiovascular (FRCV) previos, para clasificar el riesgo de cardiotoxicidad como bajo, moderado, alto o muy alto. El texto nos recuerda las limitaciones que tienen las escalas de estratificación de riesgo previas. Las proformas de HFA-ICOS publicadas en 2020 se elaboraron mediante un consenso de expertos y no se validaron previamente. Sin embargo, durante el último congreso de la ESC, un estudio confirmó que esta herramienta permitía predecir satisfactoriamente la cardiotoxicidad por antraciclinas en la cohorte del registro CARDIOTOX4.
En el texto se resalta el papel de elementos básicos como la historia clínica y la electrocardiografía, que tienen un gran valor en la evaluación inicial. Por lo que respecta a los biomarcadores, se recomienda realizar una determinación basal de troponina o péptidos natriuréticos si se van a determinar durante el seguimiento para detectar la disfunción cardiaca relacionada con el tratamiento del cáncer (DCRTC). La técnica de diagnóstico por imagen cardiaca preferida es la ecocardiografía transtorácica (ETT): se recomienda determinar la fracción de eyección del ventrículo izquierdo (FEVI) y la deformación (strain) longitudinal global de todos los pacientes en riesgo alto o muy alto para evaluar la función cardiaca. La medición de la FEVI tridimensional sería la modalidad ideal, aunque su disponibilidad es escasa. Si la ventana acústica es desfavorable, deberá considerarse la posible conveniencia de utilizar la resonancia magnética cardiaca (RMC) para la evaluación de la FEVI y técnicas de imagen nuclear con adquisición sincronizada cuando la RMC no sea posible. No está indicado llevar a cabo de manera sistemática pruebas genéticas, pero este campo está abierto a una futura evaluación personalizada.
Un aspecto novedoso es la indicación de una evaluación de la forma física cardiorrespiratoria mediante una prueba de estrés de ejercicio cardiorrespiratorio (PECP), que es un buen predictor de la salud cardiovascular. No obstante, la evidencia que respalda la PECP antes del tratamiento se limita a la evaluación del riesgo preoperatorio de los pacientes con cáncer de pulmón, colon o recto. La evaluación del riesgo quirúrgico antes de la cirugía oncológica debe llevarse a cabo en función del tipo de tumor, los factores de riesgo, los tratamientos concomitantes y el riesgo quirúrgico en sí. Se recomienda una evaluación de cardio-oncología para los pacientes sintomáticos, los que ya tienen una ECV y los que presentan un riesgo alto o muy alto de cardiotoxicidad.
En resumen, la monitorización cardiovascular depende tanto del tratamiento oncológico como del riesgo basal de cardiotoxicidad. Este riesgo debe ser estimado por el oncólogo o el hematólogo. Para alcanzar este objetivo, deberá intensificarse la formación en cardio-oncología no solo de los cardiólogos, sino también hematólogos, oncólogos y radioterapeutas oncológicos. Por lo que respecta a la aplicabilidad de la evaluación previa al tratamiento en la práctica clínica cotidiana en España, la aplicación móvil (app) elaborada en la guía de bolsillo de cardio-oncología proporciona instrumentos interactivos de gran utilidad para una rápida evaluación del riesgo. Hasta hace unos pocos años, la única recomendación era una evaluación mediante ETT antes de tratamientos como antraciclinas o anti-HER2. La nueva guía recomienda ahora la ETT antes de emplear otras clases de medicamentos como los inhibidores del proteasoma o el osimertinib, incluso para pacientes en riesgo bajo (recomendación de clase I), lo cual podría ser difícil de abarcar en la actualidad teniendo en cuenta la elevada carga de trabajo que tienen las unidades de diagnóstico por imagen cardiaca.
PREVENCIÓN Y MONITORIZACIÓN DE LAS COMPLICACIONES CARDIOVASCULARESLa guía ESC 2022 sobre cardio-oncología resalta que el riesgo de TCV-RTC se incrementa en los pacientes con FRCV o con una ECV previa. Se hacen recomendaciones generales sobre estilo de vida saludable, ejercicio físico y corrección de los FRCV. Para facilitar la evaluación del riesgo cardiovascular y la optimización de los FRCV dentro del sistema de salud de España, varias sociedades científicas españolas elaboraron un documento de consenso previo en el que se especifican las diferentes escalas de evaluación y los objetivos terapéuticos para estos pacientes5.
Para la prevención primaria, la guía recomienda minimizar el uso de fármacos con potencial cardiotóxico si ello es posible. Se recomienda la prescripción de inhibidores de la enzima de conversión de la angiotensina (IECA) o antagonistas del receptor de la angiotensina II (ARA-II) y bloqueadores beta a los pacientes en riesgo alto o muy alto (recomendación IIa B para las antraciclinas y los tratamientos anti-HER2; recomendación IIa C para otros tratamientos que puedan causar insuficiencia cardiaca [IC]). También se ha propuesto prescribir estatinas a los pacientes con riesgo cardiovascular alto o muy alto en la evaluación inicial. Otras estrategias de prevención primaria son dexrazoxano antes de las antraciclinas y antraciclinas liposómicas para los pacientes adultos con cáncer que tengan un riesgo alto de toxicidad cardiovascular. La optimización del tratamiento cardioprotector y el uso de antraciclinas liposómicas son estrategias de fácil acceso en España, pero la indicación del dexrazonano está limitada al cáncer de mama avanzado, el cual requerirá una gran dosis acumulada de antraciclinas; además, su disponibilidad es escasa en la mayoría de los hospitales.
Para la prevención secundaria (pacientes con una ECV previa o con una TCV-RTC previa o de reciente aparición), se recomienda un abordaje mediante un equipo multidisciplinario (EMD). Se recomienda una evaluación cardiovascular durante el tratamiento oncológico en función del riesgo basal. Además de la DCRTC que generalmente se asocia con las antraciclinas y los tratamientos anti-HER2, se presentan recomendaciones detalladas en función del tratamiento indicado sobre la detección y la monitorización de la enfermedad coronaria (fluoropirimidinas o inhibidores del factor de crecimiento endotelial vascular), la hipertensión (p. ej., inhibidores del factor de crecimiento endotelial vascular o inhibidores de la tirosincinasa), la prolongación del intervalo QTc (inhibidores del factor de crecimiento endotelial vascular e inhibidores de la tirosincinasa como el nilotinib y el dasatinib), la hipertensión pulmonar (como dasatinib) y el examen de detección sistemática de la fibrilación auricular (FA) asociada con el ibrutinib (inhibidor de la tirosincinasa bruton), entre otras. Estas recomendaciones se resumen en figuras que tienen un diseño excelente. Como ya se ha mencionado, la mayoría de las recomendaciones se basan en la opinión de expertos (nivel de evidencia C), lo cual los propios autores reconocen al afirmar que hay una carencia importante de ensayos clínicos para orientar la toma de decisiones. Así, de todas las recomendaciones sobre la monitorización cardiovascular, solo 2 de clase I tienen un nivel de evidencia A: la heparina de bajo peso molecular (HBPM) para la profilaxis de la tromboembolia venosa (TEV) en pacientes con mieloma múltiple y factores de riesgo de TEV (excluida la TEV previa) y la monitorización del QTc en pacientes tratados con ribociclib.
Por lo que se refiere a la radioterapia, se recomienda utilizar la dosis cardiaca media en vez de la prescrita para clasificar con exactitud el riesgo de toxicidad cardiovascular, que además puede modificarse según las subestructuras cardiacas irradiadas y la distribución de la dosis. Esto requiere un cambio considerable en cómo se refleja la dosis de radiación en los informes clínicos en nuestros hospitales.
La aplicación de esta guía requiere una modificación profunda de la mayoría de los protocolos de monitorización actuales, así como el diseño de nuevos protocolos para la inclusión de todos los tratamientos antineoplásicos comentados en el documento. Ello implica un aumento significativo del número de determinaciones de biomarcadores cardiacos, electrocardiogramas y ETT y, por consiguiente, un mayor número de consultas específicas de cardio-oncología. Será preciso planificar nuevos recursos estructurales y humanos en cada centro para garantizar una asistencia cardiovascular rápida y de alta calidad, identificar las posibles complicaciones cardiovasculares lo antes posible y evitar interrupciones innecesarias de los tratamientos oncológicos. Mientras no se disponga de más recursos, cada centro deberá evaluar la carga de trabajo que puede aceptar y seleccionar a los pacientes que obtendrán el mayor beneficio de esta evaluación, es decir, los que tienen más riesgo de cardiotoxicidad. La guía no especifica unas recomendaciones básicas para las unidades de cardio-oncología de menor tamaño o que disponen de menos recursos, y nosotros damos por supuesto que deberán elaborarse protocolos locales individualizados.
TRATAMIENTO DE LA TOXICIDAD CARDIOVASCULARDisfunción ventricular e insuficiencia cardiacaLa guía actual proporciona recomendaciones específicas sobre la DCRTC debida a antraciclinas, tratamientos anti-HER2, linfocitos T con receptores antigénicos quiméricos, linfocitos infiltrantes de tumores, IC durante el trasplante de células madre hematopoyéticas, miocarditis por inhibidores del punto de control inmunitario y síndrome tako-tsubo relacionado con cáncer.
El tratamiento de la DCRTC por antraciclinas depende de si el paciente sufre una IC sintomática y de la gravedad de la disfunción ventricular. En general, los pacientes con una cardiotoxicidad sintomática grave suspenderán definitivamente el tratamiento con antraciclinas; los pacientes con una cardiotoxicidad moderada o asintomática con FEVI <50% deberán interrumpir transitoriamente el tratamiento con antraciclinas y el EMD deberá valorar si debe llevarse a cabo una reexposición con base en una evaluación de la relación entre riesgo y beneficio. Para los pacientes con una cardiotoxicidad sintomática leve, también el EMD deberá decidir si se mantiene o se interrumpe el tratamiento con antraciclinas. La guía sobre cardio-oncología tiene como finalidad abordar estas situaciones que difieren en los pacientes con cáncer, y el tratamiento médico de la disfunción ventricular y la IC sintomática debe seguir la guía de la ESC sobre IC6,7. Además, se proponen 3 estrategias de cardioprotección para los pacientes con DCRTC que reinician el tratamiento con antraciclinas, a lo largo del tratamiento de la IC y después de una recuperación de la FEVI: reducción de la dosis, antraciclinas liposómicas y dexrazoxano.
La DCRTC asintomática leve es una situación clínica frecuente en cardio-oncología, que se define como una nueva disminución del strain longitudinal global >15% y/o un aumento de los biomarcadores cardiacos (ya sea la troponina o los péptidos natriuréticos) con FEVI normal y sin signos ni síntomas de IC. Aunque la evidencia clínica correspondiente a este contexto se basa en estudios de pequeño tamaño y los resultados son heterogéneos, la guía recomienda iniciar la administración de IECA o bloqueadores beta a estos pacientes con objeto de evitar la progresión de la cardiotoxicidad (recomendación de clase IIa B para los pacientes con elevación de troponinas o deterioro del strain longitudinal global; clase IIb C para los pacientes con elevación de los péptidos natriuréticos).
Las recomendaciones son similares para la DCRTC que se origina por tratamientos anti-HER2, pero dado que su toxicidad es menos grave y con frecuencia es un efecto reversible, el umbral para suspender su administración es más alto. Este mensaje es importante, dado el temor existente a que la DCRTC conduzca a una interrupción innecesaria del tratamiento anti-HER2 y su posible beneficio oncológico, a pesar de una cardiotoxicidad moderada que puede tolerarse bien8. Creemos que, para aplicar todas estas recomendaciones, el trabajo de las unidades de cardio-oncología tendrá que integrarse con el de las unidades de IC.
Se revisa claramente la miocarditis relacionada con los inhibidores del punto de control inmunitario. Los 3 pilares del tratamiento son: a) suspender la administración de los inhibidores del punto de control inmunitario cuando se sospeche; b) confirmar el diagnóstico con rapidez: troponinas elevadas, electrocardiograma, exploraciones de imagen cardiacas (con un papel predominante de la RMC), descartar otras causas de lesión miocárdica como el síndrome coronario agudo (SCA) o la miocarditis vírica, y c) iniciar la administración de dosis altas de metilprednisolona en bolos para todos los pacientes en quienes se sospeche, sobre todo en casos fulminantes, en los que no puede retrasarse un diagnóstico diferencial emergente (incluida la biopsia endomiocárdica, IIa B). A pesar de que no hay una recomendación basada en la evidencia, conviene tener una guía clara respecto a cómo llevar a cabo la retirada progresiva de los corticoides, cuándo utilizar un inmunosupresor de segunda línea y cuándo realizar una reexposición (siempre acordada por el EMD) en esta complicación muy infrecuente.
Se informa a los lectores sobre otras complicaciones de la IC específicas de los pacientes con síndrome de liberación de citocinas en los tratamientos con linfocitos T con receptor antigénico quimérico y con linfocitos infiltrantes de tumores, así como los pacientes tratados con trasplante de células madre hematopoyéticas, en los que las toxicidades cardiovasculares incluyen arritmias, derrame pericárdico y taponamiento o IC que puede variar entre la congestión leve y el shock cardiogénico. Por último, se incluye también el tratamiento del síndrome de tako-tsubo en los pacientes con cáncer y se aportan unos mensajes esenciales para confirmar el diagnóstico descartando el SCA y la miocarditis (en lo cual la RMC desempeña nuevamente un papel importante). El documento resalta la conveniencia de evitar los fármacos que prolongan el intervalo QT durante la fase aguda y el riesgo de reiniciar un fármaco oncológico sospechoso de haber sido el causante después de un síndrome de tako-tsubo; debe precederse del análisis de un EMD.
Enfermedad coronariaLos pacientes con cáncer tienen un riesgo aumentado de enfermedad coronaria debido a que hay factores de riesgo comunes, pero también a causa del estado protrombótico y de la toxicidad de muchos de los tratamientos del cáncer. Los pacientes que son hospitalizados a causa de un SCA presentan tasas de mortalidad y de hemorragia más altas. El diagnóstico del SCA debe realizarse igual que en los pacientes sin cáncer. La revascularización percutánea es un tratamiento seguro y conduce a un mejor resultado clínico, por lo que se recomienda cuando la esperanza de vida sea ≥ 6 meses (I B). Es probable que el tratamiento antitrombótico deba ser menos agresivo en la mayor parte de los cánceres debido al aumento del riesgo de hemorragia. La duración del tratamiento antiagregante plaquetario doble debe individualizarse, y una duración corta de una estrategia de clopidogrel después de la ICP para un SCA podría ser una opción para los pacientes con cáncer y riesgo hemorrágico muy alto (IIa C).
Los tratamientos del cáncer deben suspenderse transitoriamente cuando se sospeche que el tratamiento oncológico es una causa contribuyente. La reexposición a fluoropirimidinas después de un vasoespasmo es una cuestión controvertida, pero podría intentarse, sobre todo combinando un tratamiento profiláctico con nitratos de acción prolongada y antagonistas del calcio. Los tratamientos no relacionados con isquemia pueden reanudarse una vez se ha estabilizado al paciente. En caso de angina estable de aparición reciente durante el tratamiento, el paciente debe pasar una evaluación clínica cuidadosa, modificar drásticamente los factores de riesgo e iniciar la toma de fármacos antiisquémicos.
ValvulopatíasLas valvulopatías aumentan el riesgo de toxicidad cardiaca. Una valvulopatía de aparición reciente o el agravamiento de una valvulopatía ya existente en los pacientes con cáncer pueden estar relacionados con otros trastornos coexistentes. La cirugía cardiaca se ve dificultada por las comorbilidades, la fragilidad o la fibrosis mediastínica debida a la radioterapia previa; por consiguiente, las intervenciones valvulares percutáneas pueden ser una opción para limitar el retraso en el inicio de los tratamientos del cáncer. En los pacientes con cáncer y sospecha de valvulopatía de reciente aparición o agravamiento de una valvulopatía ya existente, se debe llevar a cabo un examen de detección sistemática de endocarditis y tratarlos según las recomendaciones de la guía, pero dando prioridad al pronóstico correspondiente al cáncer.
Arritmias cardiacasTodos los tipos de cáncer conllevan un aumento del riesgo de FA y se asocian con un aumento al doble del riesgo de tromboembolia sistémica/ictus y un incremento de 6 veces en el riesgo de IC. El tratamiento de la FA de los pacientes con cáncer debe seguir inicialmente la «vía ABC» de la guía ESC 2020, pero podría diferir debido a sus peculiaridades clínicas y el tratamiento concomitante. El grupo español de cardio-oncología ya publicó anteriormente un documento de consenso sobre este tema para orientar el tratamiento en nuestro contexto9.
El inicio de la anticoagulación en los casos de FA de aparición reciente debe basarse en las puntuaciones CHA2DS2-VASC y HAS-BLED; se recomienda para los pacientes adultos con una puntuación CHA2DS2-VASC ≥ 2 (varones) o ≥ 3 (mujeres) y debe considerarse también su posible conveniencia cuando la puntuación sea 1 (varones) o 2 (mujeres). Sin embargo, es preciso tener en cuenta los factores que pueden modificar los riesgos embólico y hemorrágico de los pacientes con cáncer. Deben preferirse los anticoagulantes orales directos (ACOD) a los antagonistas de la vitamina K en la FA no valvular. Con objeto de evaluar con mayor detalle estos riesgos y las situaciones clínicas complejas, en 2020 el grupo de cardio-oncología de la Sociedad Española de Cardiología (SEC) elaboró unos algoritmos de anticoagulación que facilitan la evaluación10 y el Grupo Español de Trombosis creó una aplicación móvil para simplificar la indicación del tratamiento anticoagulante11.
HipertensiónLa guía incluye recomendaciones detalladas sobre el tratamiento de la hipertensión de los pacientes con cáncer, incluidos umbrales claros de presión arterial (PA) sistólica ≥ 180mmHg o PA diastólica ≥ 110mmHg en que debe posponerse o suspenderse la medicación para el cáncer hasta que se alcance un control suficiente de la PA. Se reconoce que la hipertensión no controlada es un factor impulsor de la toxicidad cardiaca y la IC durante el tratamiento con antraciclinas, ibrutinib o inhibidores del factor de crecimiento endotelial vascular. El nuevo algoritmo resalta los IECA o ARA-II como primera opción, en monoterapia o en combinación con antagonistas del calcio dihidropiridínicos. Este algoritmo es de suma utilidad en la práctica clínica tanto de cardiología como de oncología/hematología. La nueva recomendación sobre el empleo de umbrales de PA diferentes en función del pronóstico del cáncer se basa en la opinión de expertos.
Eventos tromboembólicosSe presenta un nuevo algoritmo para buscar un equilibrio entre los riesgos tromboembólico y hemorrágico con objeto de respaldar decisiones difíciles en la práctica clínica diaria.
Para la prevención secundaria de la TEV, el primer paso (como en la FA) es evaluar el riesgo tromboembólico, el riesgo hemorrágico, las interacciones del tratamiento y las preferencias del paciente. Cuando no haya ninguna contraindicación para iniciar la anticoagulación, la guía sobre cardio-oncología recomienda la HBPM o un ACOD (indicación I A en ambos casos). La HBPM será la primera opción en los casos de cáncer gastrointestinal (GI) o genitourinario no operado, comorbilidades o toxicidad GI, disfunción renal grave (aclaramiento de creatinina ≤ 15ml/min), interacciones farmacológicas importantes de los ACOD o recuento plaquetario <50.000/μl. En las demás situaciones, se recomienda la HBPM o un ACOD con la misma clase de recomendación, y debe tenerse en cuenta la preferencia del paciente.
Se asigna a la prescripción de HBPM a mitad de dosis una indicación de clase IIb si el recuento de plaquetas es de entre 25.000 y 50.000/μl. En los pacientes con un riesgo hemorrágico muy alto determinado por la presencia de una hemorragia mayor activa o reciente, lesiones intracraneales recientes o en evolución o un recuento de plaquetas < 25.000/μl, debe suspenderse la anticoagulación incluso en caso de TEV.
Para la prevención primaria de la TEV, se recomienda la HBPM profiláctica para los pacientes hospitalizados (indicación I B). En los pacientes ambulatorios con alto riesgo de TEV, puede usarse HBPM, apixabán o rivaroxabán si no hay contraindicaciones para ello (IIb B).
A pesar de la evidencia publicada sobre el uso de ACOD en los pacientes con cáncer y que son un tratamiento más eficaz y mejor tolerado que la HBPM, la falta de reembolso de estos fármacos por el sistema de salud de España es la principal limitación para su uso en la TEV o la trombosis relacionada con el cáncer.
Otras complicacionesAunque hay pocas novedades por lo que respecta a la enfermedad arterial periférica, se presentan nuevas recomendaciones sobre la forma de monitorizar la hipertensión pulmonar relacionada con el dasatinib y sobre cuándo suspender este tratamiento (nivel de evidencia C). Las novedades en cuanto a la enfermedad pericárdica incluyen recomendaciones sobre el tratamiento de la pericarditis relacionada con los inhibidores del punto de control inmunitario y de los derrames pericárdicos recurrentes, con una ventana quirúrgica pericárdica o la infusión intrapericárdica de fármacos esclerosantes.
Evaluación al final del tratamiento del cáncerLa guía de cardio-oncología recomienda una evaluación cardiovascular después del tratamiento del cáncer. Al final del tratamiento del cáncer, la evaluación del riesgo cardiovascular se circunscribe a los 12 meses posteriores al último tratamiento potencialmente cardiotóxico. Como novedad, el documento proporciona una clasificación del riesgo y el correspondiente enfoque clínico. El objetivo principal del seguimiento es descartar una DCRTC mediante biomarcadores y ETT, y la frecuencia del seguimiento variará en función de cuál sea el riesgo estimado. En nuestro contexto clínico, este seguimiento puede verse facilitado por el programa SEC-Primaria junto con un sistema de consulta electrónica que limita a la realización de la ETT las visitas presenciales en los hospitales12,13.
Dado que los pacientes en baja forma física cardiorrespiratoria tienen un pronóstico desfavorable, es crucial fomentar la actividad física. Se recomienda una PECP para evaluar la forma física cardiorrespiratoria para todos los pacientes y se aconseja el ejercicio físico a todos los que están en programas de rehabilitación cardiaca. En nuestro entorno puede resultar difícil realizar una PECP a todos los pacientes, pero puede ofrecerse un programa de rehabilitación específico a pacientes seleccionados. Cuando no se disponga de PECP, puede utilizarse un enfoque más sencillo, como una prueba de sentarse y ponerse de pie en 30 s o una prueba de 6 min de marcha como alternativa para estimar la capacidad funcional14.
Por último, se asigna una recomendación IIa C a la suspensión de los fármacos para la IC al final del tratamiento antitumoral de los pacientes que hayan sufrido una cardiotoxicidad leve o moderada asintomática y se hayan recuperado por completo (FEVI y biomarcadores normalizados). Esto podría ser controvertido en el caso de pacientes que hayan tenido una disminución importante de la FEVI. Es cierto que esta recomendación se limita a pacientes seleccionados con riesgo bajo, pero no está claro que la respuesta de estos pacientes pueda ser similar a la de aquellos con IC y FEVI recuperada, para quienes la guía de la ESC sobre IC recomienda mantener el tratamiento de la IC a causa del riesgo de recurrencia de la miocardiopatía6,15. Si se suspende el tratamiento de la IC, la guía sobre cardio-oncología resalta la importancia de una monitorización ulterior mediante biomarcadores y ETT.
Seguimiento de los supervivientes a largo plazoLa guía proporciona una clasificación del riesgo específica para los pacientes que han tenido un proceso oncohematológico durante su infancia o en la edad adulta. El seguimiento de estos pacientes gira en torno a descartar la DCRTC en el primer grupo y abarca la ateroesclerosis prematura en el segundo. Para ambos grupos, la guía recomienda una detección sistemática con técnicas de imagen complejas que intentaríamos implementar como mínimo para los pacientes en alto riesgo.
Es importante resaltar el control de los FRCV, que puede alcanzarse con el programa SEC-Primaria5,12,13. Es de destacar que los supervivientes a largo plazo actuales a los que se refiere este apartado no son los que recibirán los nuevos fármacos o se someterán a técnicas de radioterapia más modernas; por consiguiente, es muy posible que las recomendaciones cambien en futuras versiones de la guía.
Grupos de población especialesEl documento incluye una interesante figura en la que se muestran las localizaciones más frecuentes de los tumores cardiacos primarios y secundarios, y que recuerda a los lectores con una simple mirada lo que se debe descartar en las diferentes cámaras cardiacas.
Hay un apartado específico dedicado al embarazo, que abarca un campo sumamente complejo. Aunque no haya estudios específicos pertinentes en supervivientes al cáncer de alto riesgo, el asesoramiento previo al embarazo y el tratamiento durante este y el parto por un EMD cardiaco del embarazo tiene asignada una recomendación de clase I.
En este apartado se comentan también enfermedades minoritarias, como el carcinoide o la amiloidosis AL cardiaca. Se recomienda la ETT para la detección cuando haya altas concentraciones de péptidos natriuréticos o signos clínicos de cardiopatía carcinoide, y seguimiento cada 3 o 6 meses en función de la gravedad de la afección cardiaca y el estado clínico. La amiloidosis cardiaca tiene repercusiones aún mayores en la práctica clínica debido al progreso terapéutico reciente. Se recomiendan ETT y RMC, así como la determinación de péptidos natriuréticos y troponinas para el diagnóstico de la amiloidosis cardiaca por cadenas ligeras en los pacientes con discrasia de células plasmáticas (clase I C). Se asigna a la biopsia endomiocárdica una recomendación de clase IIa.
Este apartado termina con una recomendación muy práctica sobre el tratamiento de los pacientes con un dispositivo electrónico cardiaco implantable situado en el haz del tratamiento de radioterapia o fuera del volumen de radioterapia.
Enfermería en cardio-oncologíaProbablemente este sea el único apartado que los autores del presente documento consideran deficitario. Aunque hay algunos apartados que abordan los hábitos de estilo de vida, el ejercicio físico, la alimentación, etc., y a pesar de que la «especificación de las funciones de los diferentes profesionales de la asistencia sanitaria, incluido el personal de enfermería y de farmacia», se considera una laguna en la evidencia existente, nos habría gustado encontrar un apartado explícito sobre enfermería en cardio-oncología. La guía resalta la importancia del EMD y la comunicación con los pacientes y promueve que se involucren y participen en el tratamiento, tarea que el personal de enfermería debe dirigir. Los estilos de vida poco saludables y la mala adherencia al tratamiento fomentan los FRCV, la ECV y la cardiotoxicidad. Los programas integrados de apoyo al autocuidado general y específico en diferentes procesos oncológicos han mostrado una notable mejora en la calidad de vida percibida y el nivel de autocuidado de las personas afectadas y han mejorado su grado de autonomía y los resultados en general. Debe proporcionarse un asesoramiento estructurado para fomentar comportamientos saludables y la identificación y control estricto de los FRCV (alimentación saludable, dejar de fumar, ejercicio regular y control del peso) antes, durante y después del tratamiento, el uso adecuado de los recursos disponibles y un seguimiento clínico para descartar signos y síntomas que indiquen cardiotoxicidad16.
En el documento de consenso de la SEC sobre la evaluación del riesgo cardiovascular5, el personal de enfermería desempeña una función fundamental en la prevención de la cardiotoxicidad, con estrategias que tienen una relación de coste-eficacia favorable, como identificar, controlar y monitorizar los FRCV antes, durante y después del tratamiento, la detección precoz de signos y/o síntomas de alarma y el fomento de un estilo de vida saludable.
Indicadores de la calidad en cardio-oncologíaLa calidad mejora cuando se supervisa; sin embargo, las prácticas óptimas deben basarse en las medidas que proporcionan el máximo beneficio, y en la actualidad la escasa evidencia clínica existente en cardio-oncología dificulta establecer estrictamente indicadores de la calidad en este campo.
La guía reconoce la importancia de elaborar instrumentos para medir la calidad, y otro grupo de trabajo está preparando un documento específico al respecto que se publicará en breve. Hay muchos parámetros que pueden usarse para definir la calidad en diferentes dominios y todos ellos deben ser, cuando menos, visibles; sin embargo, teniendo en cuenta el nivel de evidencia existente, sería mejor resaltar al menos unos pocos parámetros realmente relevantes y evaluables para facilitar las auditorías y las comparaciones.
Nosotros preveríamos la inclusión de datos sencillos, como a) una unidad/equipo de cardio-oncología formalmente estructurado, organizado y reconocido en cada hospital/centro sanitario; b) el número de casos con al menos 1 visita (basal) de entre el número total de pacientes con un nuevo diagnóstico de cáncer a los que se prescriben tratamientos que pueden ser cardiotóxicos, y c) el número de pacientes con IC u otro evento cardiovascular mayor por año con y sin una visita previa del EMD registrada.
En cuanto a la calidad, las sociedades de cardiología nacionales e internacionales pueden aportar una guía y auditorías locales. La SEC está elaborando actualmente un programa para facilitar la organización y certificación de las unidades de cardio-oncología.
CONCLUSIONESLa guía ESC 2022 sobre cardio-oncología es una referencia excelente para respaldar a todos los profesionales que participan en la evaluación y el tratamiento de los pacientes con cáncer. Sin embargo, muchos centros no podrán aplicar el enorme número de nuevas recomendaciones, por lo que probablemente deberíamos centrarnos en los pacientes con riesgo alto o muy alto hasta que se incrementen los recursos para las unidades de cardio-oncología. Dado el escaso número de ensayos clínicos y metanálisis publicados en este campo, la mayor parte de las recomendaciones tienen un nivel de evidencia C. Debemos estimular la investigación en cardio-oncología para mejorar la evidencia disponible para guías futuras. El Grupo de Cardio-Oncología de la SEC y el Grupo de Trabajo de la SEC para la guía ESC 2022 de cardio-oncología fomentan también el uso de nuestros instrumentos previos y documentos de consenso locales para aplicar las nuevas recomendaciones y mejorar la asistencia cardiovascular de los pacientes con cáncer. Por último, agradecemos a los autores de la guía sobre cardio-oncología de la ESC la elaboración de un excelente documento y los materiales acompañantes para facilitar su uso y aplicación.
FINANCIACIÓNNinguna.
CONFLICTO DE INTERESESLos documentos de declaración de conflicto de intereses de los autores se pueden consultar en el material adicional.
Grupo de trabajo de la SEC para la guía ESC 2022 sobre cardio-oncología: Pedro Moliner (coordinador), Pilar Mazón (coordinadora), Alberto Cordero, Concepción Fernández, José Luis López Sendón, Ana Martín García, Amparo Martínez-Monzonís, Cristina Mitroi, Milagros Pedreira, Nuria Vallejo, José Luis Zamorano, Eduardo Zatarain-Nicolás.
Comité de guías de la SEC: Rut Andrea, Pablo Avanzas, Gemma Berga, Araceli Boraita, David Calvo, Raquel Campuzano, Victoria Delgado, Laura Dos Subirá, Juan José Gómez Doblas, Pilar Mazón, Domingo Pascual, Juan Sanchis, José M. de la Torre, David Vivas, José L. Ferreiro (presidente).
Véase contenido relacionado: https://secardiologia.es/cientifico/guias-clinicas/cardio-oncologia/13910-2022-esc-guidelines-on-cardio-oncology-developed-in-collaboration-with-eha-estro-and-ic-os.
Los nombres de todos los autores se indican por orden alfabético en el anexo.
Autor para correspondencia.
Correos electrónicos: pilarmazon@yahoo.es (P. Mazón); pmolinerborja@gmail.com (P. Moliner).