Presentamos 2 casos en los que la estimulación en el ventrículo derecho produjo un deterioro hemodinámico muy importante y en los que de forma aguda el cambio del sitio de estimulación del ventrículo derecho al ventrículo izquierdo corrigió estas alteraciones, mientras que no lo hacía la estimulación biventricular simultánea. La estimulación crónica del ventrículo izquierdo puede ser capaz de resolver las alteraciones hemodinámicas de los síndromes de marcapasos graves y puede evitar la necesidad de implantación de una prótesis mitral en algunos casos. La aplicación en el momento actual debe hacerse de forma individualizada, incluyendo estudio hemodinámico y ecocardiográfico agudo, ya que la anchura del complejo QRS durante la estimulación no es un índice significativo de eficacia hemodinámica.
Palabras clave
Estimulación eléctrica
Insuficiencia mitral
Marcapasos
INTRODUCCIÓN
La estimulación cardíaca eléctrica crónica puede producir ocasionalmente efectos adversos sobre la función cardíaca, que son generalmente secundarios a una selección de modo de estimulación o programación inadecuadas 1. Los síntomas más prominentes son atribuibles a un descenso del gasto cardíaco y la presión arterial o debidos a congestión venosa pulmonar. La incidencia del conjunto de síntomas y signos conocido como síndrome de marcapasos es variable según la rigidez en su definición 2 y son más fácilmente reconocibles los pacientes que presentan síntomas graves.
Los avances en el conocimiento de la fisiopatología de la estimulación cardíaca han permitido el desarrollo de modos especiales de estimulación dirigidos a la mejoría de la función ventricular en pacientes con insuficiencia cardíaca. Inicialmente se ha buscado la optimización del llenado ventricular y la reducción de la regurgitación mitral manipulando el intervalo auriculoventricular (AV) 3, pero las limitaciones de este procedimiento 4 han llevado a intentar mejorar la función ventricular, alterada por la estimulación del ápex del ventrículo derecho (VD) mediante la estimulación septal en VD 5 y la estimulación biventricular 6-9. Algunos datos clínicos 7,8,10 y experimentales 11,12 incluso sugerirían ventajas con la estimulación única en ventrículo izquierdo (VI).
A continuación presentamos los casos de 2 pacientes con síndrome grave de marcapasos, incluyendo insuficiencia cardíaca refractaria, durante la estimulación en ápex de VD, en los que un estudio hemodinámico y ecocardiográfico demostró una mejoría significativa con la estimulación del VI. En un caso la estimulación crónica del VI resolvió completamente el cuadro clínico.
CASOS CLÍNICOS
Caso 1
Mujer de 54 años con historia de hipertensión arterial y fibrilación auricular (FA) incontrolable a pesar de varias cardioversiones y fármacos. Se implantó marcapasos VVIR en el ápex del VD tras ablación de la conducción AV con radiofrecuencia. En el ecocardiograma antes de la ablación se observó función sistólica de VI normal con diámetro diastólico de 4,8 cm y volumen diastólico de 108 ml, así como regurgitación mitral ligera.
Dos semanas después de la implantación presentó disnea progresiva hasta hacerse de mínimos esfuerzos, ortopnea y disnea paroxística nocturna. Se auscultó un nuevo soplo de insuficiencia mitral (IM) y en el ecocardiograma transtorácico y transesofágico se detectó un importante aumento de la IM, que se consideró severa. No había cambios en el volumen y función del VI ni en las dimensiones de la aurícula izquierda.
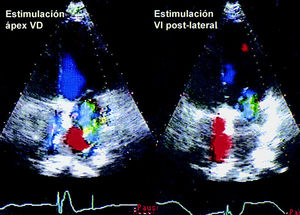
Dada la ausencia de respuesta terapéutica se estudió la respuesta a diferentes formas de estimulación ventricular mediante estudio hemodinámico con catéter de Swan-Ganz y ecocardiograma transtorácico y transesofágico. Los resultados se exponen en la tabla 1. La estimulación en VI, a pesar de producir el complejo QRS más ancho, corregía la IM grave secundaria a la estimulación en ápex de VD (fig. 1), con disminución significativa de la onda V, del área y del tiempo de regurgitación durante la sístole y desapareciendo la inversión sistólica del flujo de venas pulmonares que se observaba en el estudio transesofágico.
Fig. 1. Ecocardiograma transtorácico en modo 2D con Doppler color durante el estudio agudo con diferentes modos de estimulación, en proyección apical 4 cámaras. Nótese la llamativa disminución del área de regurgitación mitral cuando se estimula en VI.
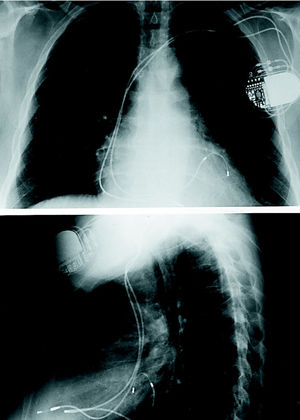
Se implantó un nuevo electrodo definitivo para estimulación en epicardio posterolateral de VI a través del seno coronario (vena marginal) (fig. 2). El electrodo del VI se conectó a la salida auricular de un marcapasos DDD y el de VD a la salida ventricular, con el objeto de garantizar la estimulación en caso de evolución desfavorable del umbral o desplazamiento del electrodo de VI, pero con una programación que conseguía estimulación exclusiva de VI. La paciente mejoró significativamente y sigue en clase funcional II de la NYHA tras un año de seguimiento. En controles ecocardiográficos posteriores, se ha podido comprobar el empeoramiento agudo de la IM cuando la estimulación se realiza desde el VD por cambio de programación del marcapasos.
Fig. 2. Radiografías de tórax posteroanterior y lateral en las que se observa la localización del electrodo de estimulación en epicardio posterolateral de VI, implantado a través de seno coronario.
Caso 2
Varón de 65 años con antecedentes de cardiopatía isquémica avanzada, con infartos antiguos inferoposterior y anterolateral, obstrucción de 3 vasos no revascularizable y ablación con éxito de taquicardias ventriculares. Presentaba episodios recurrentes de taquicardia y FA tratados con 200 mg diarios de amiodarona. Función sistólica de VI severamente deprimida e IM moderada (6 cm 2 en el ecocardiograma transtorácico). Electrocardiograma con PR de 320 ms y trastorno de la conducción intraventricular inespecífico con QRS de 155 ms. Disnea de ligeros esfuerzos bajo tratamiento con inhibidores de la enzima de conversión de la angiotensina y furosemida a dosis altas, con ingresos repetidos por insuficiencia cardíaca.
Se implantó marcapasos DDD para intentar estabilizar el ritmo auricular y optimizar el llenado ventricular acortando el intervalo AV. Tras la implantación se observó que la estimulación DDD producía inmediatamente hipotensión y astenia profunda, por lo que fue dado de alta con estimulación AAI. Tras un episodio de síncope se reprogramó en modo DDD (intervalo AV 150 ms) pero desarrolló hipotensión e intolerancia al mínimo esfuerzo. En el ecocardiograma se detectó IM severa (área 13,5 cm 2).
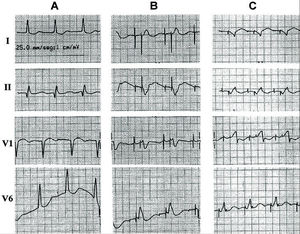
Se decidió realizar un estudio hemodinámico (catéter de Swan-Ganz) y ecocardiográfico (transtorácico) para valorar el efecto de la estimulación ventricular izquierda y biventricular. Todas las mediciones fueron realizadas a 70 lat/min. Los resultados se exponen en la tabla 2. A pesar del PR largo con estimulación AAI, la estimulación DDD en el ápex de VD producía un franco deterioro hemodinámico con aumento de la IM y de la presión capilar pulmonar y ligero descenso del gasto cardíaco. La estimulación DDD en VI (basal posterolateral, en el seno coronario distal), con intervalo AV 150 ms, producía una mejoría importante con respecto a DDD en VD con el mismo intervalo AV, con aumento del gasto cardíaco, retorno de la presión capilar pulmonar a valores basales (AAI) y el mínimo grado de IM conseguido con todos los modos de estimulación. La estimulación DDD biventricular no ofrecía ventajas respecto a la estimulación DDD en VD. La mejoría con estimulación en VI se producía a pesar de un mayor ensanchamiento del QRS si se comparaba con el ritmo propio y con la estimulación biventricular (fig. 3 y tabla 2).
Fig. 3. Derivaciones I, II, V1 y V6 del electrocardiograma de nuestro segundo paciente cuando está en ritmo propio (A), en ritmo de marcapaso DDD con estimulación en VD (B) y con estimulación en VI (C), que muestra claramente las diferencias en la duración del complejo QRS.
Se implantó un marcapasos permanente DDD con electrodo ventricular en VI inferoposterior, a medio camino entre ápex y base, aunque no pudo reproducirse la posición usada durante el estudio agudo. No se observaron los síntomas de bajo gasto con estimulación DDD en VD, pero el seguimiento ha sido complicado por nuevas recidivas de FA que terminó por instaurarse de manera crónica, lo que obligó a un cambio de modo en VVI, con recaídas en insuficiencia cardíaca intratable que llevó a su fallecimiento a los 6 meses. DISCUSIÓN
Aunque con contextos clínicos muy diferentes, los 2 casos presentados tienen en común ser ejemplos de síndrome de marcapasos en su forma más grave: deterioro hemodinámico con insuficiencia cardíaca refractaria, asociados en los dos con IM grave. Además, en ambos se pudo demostrar una mejoría hemodinámica significativa, incluyendo reducción importante de la IM, con estimulación de VI y no con estimulación biventricular, a pesar de que el complejo QRS resultante fuese mucho más estrecho con la estimulación biventricular.
La IM es una rara complicación de la estimulación de VD, que puede tener consecuencias catastróficas y llevar al reemplazo valvular mitral. Los mecanismos de aparición de IM durante la estimulación de VD son complejos. El cierre sistólico mitral depende no sólo de la integridad del anillo mitral, las cuerdas tendinosas, las valvas y los músculos papilares, sino también de la función auricular y ventricular. La pérdida de la sincronía AV con estimulación VVI puede producir IM al impedir que la contracción auricular precedente a la ventricular ayude al cierre valvular mitral 13. La longitud del intervalo AV también puede ser importante en este sentido 3,7,14. No sólo la reducción presistólica de tamaño del anillo mitral desempeñaría un papel, sino que el mejor llenado ventricular potenciaría la generación rápida de un gradiente entre VI y aurícula que cerraría la válvula mitral. Pero la sincronización AV no podía tener ningún papel en el caso 1, en fibrilación auricular, aunque podría tener un papel significativo en el caso 2, donde se apreciaba mejoría significativa con estimulación DDD en VI con intervalo de 150 ms, con respecto a intervalos AV más cortos o más largos.
Otro mecanismo de producción de IM que podría haber afectado a los 2 casos es la alteración de la función sistólica por el cambio en la secuencia de activación ventricular izquierda 15 que a largo plazo puede llegar a alteraciones importantes de la función sistólica de VI con remodelado ventricular 16. La generación rápida de presión intraventricular se ha descrito recientemente como un factor importante para el cierre efectivo de la válvula 17. La depresión aguda de la función sistólica al estimular VD podría ser un factor en la producción de IM en nuestros casos, pero, además, se puede producir un cambio de alineación o grado de tensión de los músculos papilares que interfiera con el cierre mitral 18. Estudios experimentales recientes refieren la importancia de una tensión equilibrada de los componentes del aparato subvalvular, en interacción con las valvas y el anillo mitral, para el cierre correcto de la válvula. La alteración de la secuencia y sincronía de contracción de VI producida por la estimulación de VD podría fácilmente alterar este equilibrio 12,19. Es interesante que se haya descrito insuficiencia mitral aguda con edema de pulmón relacionada con bloqueo de rama izquierda intermitente, ya que en esta situación se produciría una activación de VI similar a la producida con estimulación de VD 20.
En los 2 casos se hace evidente que es la estimulación de VI, y no la «sincronización» de VD y VI, lo que produce la mejoría, lo que concordaría con hallazgos de otros autores. La estimulación de VI ha de-mostrado ser capaz de corregir, al menos en parte, las alteraciones de la contracción producidas por la estimulación de VD 7,8,10,11 y también de mejorar la función ventricular en pacientes con retrasos importantes de conducción intraventricular 8. Estudios detallados han referido que no todos los puntos de estimulación son de la misma efectividad en este sentido 21. En nuestros casos sólo se probó agudamente la estimulación en el seno coronario distal, que fue eficaz en ambos. Sin embargo, la estimulación crónica sólo se llevo a cabo en la misma zona de VI en el primer caso, mientras que en el segundo sólo fue posible estabilizar el electrodo de estimulación permanente en una zona más inferior y más cerca del ápex. Esta diferencia entre la posición de estimulación en el estudio agudo y el crónico pueden explicar en parte la falta de eficacia aparente de la estimulación permanente de VI en el segundo caso, pero también hay que considerar que éste se trataba de un paciente con enfermedad coronaria en fase terminal, con función ventricular izquierda muy deprimida y arritmias auriculares recurrentes, por lo que no es de extrañar una mala evolución final.
En el caso 1, por contra, la estimulación de VI corrigió por completo la IM y el cuadro clínico de insuficiencia cardíaca inducidos por la estimulación de VD, demostrando la estrecha relación causal entre la secuencia de estimulación y función mitral y de VI. Creemos que se trata del primer paciente de estas características descrito en la bibliografía y sienta un antecedente importante, porque de no haberse solucionado de esta forma, hubiera sido preciso un reemplazo valvular mitral.
La estimulación cardíaca eléctrica crónica puede producir ocasionalmente efectos adversos sobre la función cardíaca, que son generalmente secundarios a una selección de modo de estimulación o programación inadecuadas 1. Los síntomas más prominentes son atribuibles a un descenso del gasto cardíaco y la presión arterial o debidos a congestión venosa pulmonar. La incidencia del conjunto de síntomas y signos conocido como síndrome de marcapasos es variable según la rigidez en su definición 2 y son más fácilmente reconocibles los pacientes que presentan síntomas graves.
Los avances en el conocimiento de la fisiopatología de la estimulación cardíaca han permitido el desarrollo de modos especiales de estimulación dirigidos a la mejoría de la función ventricular en pacientes con insuficiencia cardíaca. Inicialmente se ha buscado la optimización del llenado ventricular y la reducción de la regurgitación mitral manipulando el intervalo auriculoventricular (AV) 3, pero las limitaciones de este procedimiento 4 han llevado a intentar mejorar la función ventricular, alterada por la estimulación del ápex del ventrículo derecho (VD) mediante la estimulación septal en VD 5 y la estimulación biventricular 6-9. Algunos datos clínicos 7,8,10 y experimentales 11,12 incluso sugerirían ventajas con la estimulación única en ventrículo izquierdo (VI).
A continuación presentamos los casos de 2 pacientes con síndrome grave de marcapasos, incluyendo insuficiencia cardíaca refractaria, durante la estimulación en ápex de VD, en los que un estudio hemodinámico y ecocardiográfico demostró una mejoría significativa con la estimulación del VI. En un caso la estimulación crónica del VI resolvió completamente el cuadro clínico.
CASOS CLÍNICOS
Caso 1
Mujer de 54 años con historia de hipertensión arterial y fibrilación auricular (FA) incontrolable a pesar de varias cardioversiones y fármacos. Se implantó marcapasos VVIR en el ápex del VD tras ablación de la conducción AV con radiofrecuencia. En el ecocardiograma antes de la ablación se observó función sistólica de VI normal con diámetro diastólico de 4,8 cm y volumen diastólico de 108 ml, así como regurgitación mitral ligera.
Dos semanas después de la implantación presentó disnea progresiva hasta hacerse de mínimos esfuerzos, ortopnea y disnea paroxística nocturna. Se auscultó un nuevo soplo de insuficiencia mitral (IM) y en el ecocardiograma transtorácico y transesofágico se detectó un importante aumento de la IM, que se consideró severa. No había cambios en el volumen y función del VI ni en las dimensiones de la aurícula izquierda.
Dada la ausencia de respuesta terapéutica se estudió la respuesta a diferentes formas de estimulación ventricular mediante estudio hemodinámico con catéter de Swan-Ganz y ecocardiograma transtorácico y transesofágico. Los resultados se exponen en la tabla 1. La estimulación en VI, a pesar de producir el complejo QRS más ancho, corregía la IM grave secundaria a la estimulación en ápex de VD (fig. 1), con disminución significativa de la onda V, del área y del tiempo de regurgitación durante la sístole y desapareciendo la inversión sistólica del flujo de venas pulmonares que se observaba en el estudio transesofágico.
Fig. 1. Ecocardiograma transtorácico en modo 2D con Doppler color durante el estudio agudo con diferentes modos de estimulación, en proyección apical 4 cámaras. Nótese la llamativa disminución del área de regurgitación mitral cuando se estimula en VI.
Se implantó un nuevo electrodo definitivo para estimulación en epicardio posterolateral de VI a través del seno coronario (vena marginal) (fig. 2). El electrodo del VI se conectó a la salida auricular de un marcapasos DDD y el de VD a la salida ventricular, con el objeto de garantizar la estimulación en caso de evolución desfavorable del umbral o desplazamiento del electrodo de VI, pero con una programación que conseguía estimulación exclusiva de VI. La paciente mejoró significativamente y sigue en clase funcional II de la NYHA tras un año de seguimiento. En controles ecocardiográficos posteriores, se ha podido comprobar el empeoramiento agudo de la IM cuando la estimulación se realiza desde el VD por cambio de programación del marcapasos.
Fig. 2. Radiografías de tórax posteroanterior y lateral en las que se observa la localización del electrodo de estimulación en epicardio posterolateral de VI, implantado a través de seno coronario.
Caso 2
Varón de 65 años con antecedentes de cardiopatía isquémica avanzada, con infartos antiguos inferoposterior y anterolateral, obstrucción de 3 vasos no revascularizable y ablación con éxito de taquicardias ventriculares. Presentaba episodios recurrentes de taquicardia y FA tratados con 200 mg diarios de amiodarona. Función sistólica de VI severamente deprimida e IM moderada (6 cm 2 en el ecocardiograma transtorácico). Electrocardiograma con PR de 320 ms y trastorno de la conducción intraventricular inespecífico con QRS de 155 ms. Disnea de ligeros esfuerzos bajo tratamiento con inhibidores de la enzima de conversión de la angiotensina y furosemida a dosis altas, con ingresos repetidos por insuficiencia cardíaca.
Se implantó marcapasos DDD para intentar estabilizar el ritmo auricular y optimizar el llenado ventricular acortando el intervalo AV. Tras la implantación se observó que la estimulación DDD producía inmediatamente hipotensión y astenia profunda, por lo que fue dado de alta con estimulación AAI. Tras un episodio de síncope se reprogramó en modo DDD (intervalo AV 150 ms) pero desarrolló hipotensión e intolerancia al mínimo esfuerzo. En el ecocardiograma se detectó IM severa (área 13,5 cm 2).
Se decidió realizar un estudio hemodinámico (catéter de Swan-Ganz) y ecocardiográfico (transtorácico) para valorar el efecto de la estimulación ventricular izquierda y biventricular. Todas las mediciones fueron realizadas a 70 lat/min. Los resultados se exponen en la tabla 2. A pesar del PR largo con estimulación AAI, la estimulación DDD en el ápex de VD producía un franco deterioro hemodinámico con aumento de la IM y de la presión capilar pulmonar y ligero descenso del gasto cardíaco. La estimulación DDD en VI (basal posterolateral, en el seno coronario distal), con intervalo AV 150 ms, producía una mejoría importante con respecto a DDD en VD con el mismo intervalo AV, con aumento del gasto cardíaco, retorno de la presión capilar pulmonar a valores basales (AAI) y el mínimo grado de IM conseguido con todos los modos de estimulación. La estimulación DDD biventricular no ofrecía ventajas respecto a la estimulación DDD en VD. La mejoría con estimulación en VI se producía a pesar de un mayor ensanchamiento del QRS si se comparaba con el ritmo propio y con la estimulación biventricular (fig. 3 y tabla 2).
Fig. 3. Derivaciones I, II, V1 y V6 del electrocardiograma de nuestro segundo paciente cuando está en ritmo propio (A), en ritmo de marcapaso DDD con estimulación en VD (B) y con estimulación en VI (C), que muestra claramente las diferencias en la duración del complejo QRS.
Se implantó un marcapasos permanente DDD con electrodo ventricular en VI inferoposterior, a medio camino entre ápex y base, aunque no pudo reproducirse la posición usada durante el estudio agudo. No se observaron los síntomas de bajo gasto con estimulación DDD en VD, pero el seguimiento ha sido complicado por nuevas recidivas de FA que terminó por instaurarse de manera crónica, lo que obligó a un cambio de modo en VVI, con recaídas en insuficiencia cardíaca intratable que llevó a su fallecimiento a los 6 meses. DISCUSIÓN
Aunque con contextos clínicos muy diferentes, los 2 casos presentados tienen en común ser ejemplos de síndrome de marcapasos en su forma más grave: deterioro hemodinámico con insuficiencia cardíaca refractaria, asociados en los dos con IM grave. Además, en ambos se pudo demostrar una mejoría hemodinámica significativa, incluyendo reducción importante de la IM, con estimulación de VI y no con estimulación biventricular, a pesar de que el complejo QRS resultante fuese mucho más estrecho con la estimulación biventricular.
La IM es una rara complicación de la estimulación de VD, que puede tener consecuencias catastróficas y llevar al reemplazo valvular mitral. Los mecanismos de aparición de IM durante la estimulación de VD son complejos. El cierre sistólico mitral depende no sólo de la integridad del anillo mitral, las cuerdas tendinosas, las valvas y los músculos papilares, sino también de la función auricular y ventricular. La pérdida de la sincronía AV con estimulación VVI puede producir IM al impedir que la contracción auricular precedente a la ventricular ayude al cierre valvular mitral 13. La longitud del intervalo AV también puede ser importante en este sentido 3,7,14. No sólo la reducción presistólica de tamaño del anillo mitral desempeñaría un papel, sino que el mejor llenado ventricular potenciaría la generación rápida de un gradiente entre VI y aurícula que cerraría la válvula mitral. Pero la sincronización AV no podía tener ningún papel en el caso 1, en fibrilación auricular, aunque podría tener un papel significativo en el caso 2, donde se apreciaba mejoría significativa con estimulación DDD en VI con intervalo de 150 ms, con respecto a intervalos AV más cortos o más largos.
Otro mecanismo de producción de IM que podría haber afectado a los 2 casos es la alteración de la función sistólica por el cambio en la secuencia de activación ventricular izquierda 15 que a largo plazo puede llegar a alteraciones importantes de la función sistólica de VI con remodelado ventricular 16. La generación rápida de presión intraventricular se ha descrito recientemente como un factor importante para el cierre efectivo de la válvula 17. La depresión aguda de la función sistólica al estimular VD podría ser un factor en la producción de IM en nuestros casos, pero, además, se puede producir un cambio de alineación o grado de tensión de los músculos papilares que interfiera con el cierre mitral 18. Estudios experimentales recientes refieren la importancia de una tensión equilibrada de los componentes del aparato subvalvular, en interacción con las valvas y el anillo mitral, para el cierre correcto de la válvula. La alteración de la secuencia y sincronía de contracción de VI producida por la estimulación de VD podría fácilmente alterar este equilibrio 12,19. Es interesante que se haya descrito insuficiencia mitral aguda con edema de pulmón relacionada con bloqueo de rama izquierda intermitente, ya que en esta situación se produciría una activación de VI similar a la producida con estimulación de VD 20.
En los 2 casos se hace evidente que es la estimulación de VI, y no la «sincronización» de VD y VI, lo que produce la mejoría, lo que concordaría con hallazgos de otros autores. La estimulación de VI ha de-mostrado ser capaz de corregir, al menos en parte, las alteraciones de la contracción producidas por la estimulación de VD 7,8,10,11 y también de mejorar la función ventricular en pacientes con retrasos importantes de conducción intraventricular 8. Estudios detallados han referido que no todos los puntos de estimulación son de la misma efectividad en este sentido 21. En nuestros casos sólo se probó agudamente la estimulación en el seno coronario distal, que fue eficaz en ambos. Sin embargo, la estimulación crónica sólo se llevo a cabo en la misma zona de VI en el primer caso, mientras que en el segundo sólo fue posible estabilizar el electrodo de estimulación permanente en una zona más inferior y más cerca del ápex. Esta diferencia entre la posición de estimulación en el estudio agudo y el crónico pueden explicar en parte la falta de eficacia aparente de la estimulación permanente de VI en el segundo caso, pero también hay que considerar que éste se trataba de un paciente con enfermedad coronaria en fase terminal, con función ventricular izquierda muy deprimida y arritmias auriculares recurrentes, por lo que no es de extrañar una mala evolución final.
En el caso 1, por contra, la estimulación de VI corrigió por completo la IM y el cuadro clínico de insuficiencia cardíaca inducidos por la estimulación de VD, demostrando la estrecha relación causal entre la secuencia de estimulación y función mitral y de VI. Creemos que se trata del primer paciente de estas características descrito en la bibliografía y sienta un antecedente importante, porque de no haberse solucionado de esta forma, hubiera sido preciso un reemplazo valvular mitral.
Bibliografía
[1]
The pacemaker syndrome. Ann Intern Med 1985; 103: 420-429.
[2]
True incidence of pacemaker syndrome. PACE 1990; 13: 1742-1750.
[3]
Effects of dual-chamber pacing with short atrioventricular delay in dilated cardiomyopathy. Lancet 1992; 340: 1308-1312.
[4]
VDD pacing at short atrioventricular intervals does nor improve cardiac output in patients with dilated heart failure. Pacing Clin Electrophysiol 1994; 17: 959-965.
[5]
Septal short atrioventricular delay pacing: additional hemodynamic improvements in heart failure. Pacing Clin Electrophysiol 1994; 17: 1980-1983.
[6]
Four chamber pacing in dilated cardiomyophathy. Pacing Clin Electrophysiol 1994; 17: 1974-1979.
[7]
Evaluation of different ventricular pacing sites in patients with severe heart failure: results of an acute hemodynamic study. Circulation 1997; 96: 3273-3277.
[8]
Improved left ventricular mechanics from acute VDD pacing in patients with dilated cardiomyopathy and ventricular conduction delay. Circulation 1999; 99: 1567-1573.
[9]
Acute hemodynamic effects of biventricular DDD pacing in patients with end-stage heart failure. J Am Coll Cardiol 1998; 32: 1825-1831.
[10]
Effect of pacing chamber and atrioventricular delay on acute systolic function of paced patients with congestive heart failure. Circulation 1999; 99: 2993-3001.
[11]
Optimal sequence rather minimal asynchrony of activation improves ventricular function during ventricular pacing [resumen]. Eur Heart J 1999; 20; 2444.
[12]
Two-dimensional echocardiographic contrast assessment of pacing-induced mitral regurgitation: relation of altered regional left ventricular function. J Am Coll Cardiol 1984; 3: 986-991.
[13]
Ventricular pacing: a cause of reversible severe mitral regurgitation. Am Heart J 1996; 131: 1035-1037.
[14]
Short atrioventricular delay reduces the degree of mitral regurgitation in patients with a sequencial dual-chamber pacemaker. Am J Cardiol 1997; 80: 901-905.
[15]
Pacemaker induced mitral regurgitation: an alternative form of pacemmaker syndrome. PACE 1997; 20: 735-738.
[16]
Effects of long-term right ventricular apical pacing on left ventricular perfusion, innervation, function and histology. J Am Coll Cardiol 1994; 24: 225-232.
[17]
Mechanism of dynamic regurgitant orifice area variation in funcional mitral regurgitation. J Am Coll Cardiol 1999; 33: 538-545.
[18]
Insuficiencia mitral funcional. Fisiopatología e impacto del tratamiento médico y de las técnicas quirúrgicas de reducción ventricular izquierda. Rev Esp Cardiol 1999; 52: 512-520.
[19]
Chordal force distribution determines systolic mitral leafflet configuration and severity of functional mitral regurgitation. J Am Coll Cardiol 1999; 33: 843-853.
[20]
Acute pulmonary edema induced by left bundle branch block. Am J Cardiol 1983; 52: 648-649.
[21]
Transvenous biventricular pacing for heart failure: Can the obstacles be overcome? Am J Cardiol 1999; 83: 136D-142D.